JNB︱脑瘤治疗新范式!苏州大学朱然团队设计131I/MTX共载工程化细菌外膜囊泡介导脑胶质瘤序贯放射-代谢-免疫协同治疗
撰文︱梁茂林
审阅︱朱 然
责编︱王思珍
脑胶质瘤因位置深、血脑屏障坚固且免疫环境高度抑制,导致治疗效果差、复发快。现有方案中,单纯放疗易因肿瘤细胞损伤修复而失效;甲氨蝶呤(MTX)虽能干扰DNA合成,却难以精准入脑且易损伤正常组织;免疫疗法则因脑内缺乏有效免疫激活信号而响应微弱。细菌外膜囊泡(OMVs)作为源自微生物的纳米级载体,天然具备免疫激发潜能,且可安全递送药物进入复杂组织,在脑部疾病治疗中具有潜在适用性。然而,天然囊泡存在脑瘤靶向效率低、无法同步负载放射性物质与化疗药的缺陷,导致治疗碎片化、效应不同步。因此,如何让放射杀伤、代谢抑制与免疫唤醒在同一时空维度精准接力,成为突破脑胶质瘤治疗瓶颈的关键矛盾。
2025年12月,苏州大学朱然教授团队在Journal of Nanobiotechnology在线发表论文“131I/MTX-loaded engineered outer membrane vesicles for sequentially coordinated radio-metabolic-immunotherapy of glioma”,该研究设计了一种搭载放射性碘-131和抗癌药物甲氨蝶呤的细菌外膜囊泡,攻克了脑胶质瘤放疗易耐受、免疫微环境“冷”且难激活的关键难题。通过基因工程改造囊泡表面蛋白并实现双药精准共载,实现了放射杀伤、代谢阻断与免疫唤醒三步协同。显著抑制了肿瘤生长并延长小鼠生存期,为脑瘤综合治疗提供了新范式。

1. 131I-O/M-P的构建和表征
作者通过基因工程技术将富含酪氨酸和脯氨酸的唾液酸蛋白statherin(STATH)整合到减毒沙门氏菌VNP20009的外膜上,使STATH在囊泡表面成功表达。随后利用探头超声法和及挤出法进行OMVs的MTX负载和PEG表面修饰,并通过透射电镜(TEM)、DLS与Zeta电位测试等证实了O/M-P的成功合成。此外,OMVs表面表达含有多个酪氨酸残基的STATH,使O/M-P的放射性碘(131I/125I)标记成为可能,并获得了具有较高放射性标记效率和良好体外放射化学稳定性的131I/125I-O/M-P(图1)。这些发现表明多功能纳米平台(131I-O/M-P)的成功构建,为后续实现肿瘤细胞代谢干扰、放疗增敏和免疫激活的协同治疗提供了坚实的材料基础。
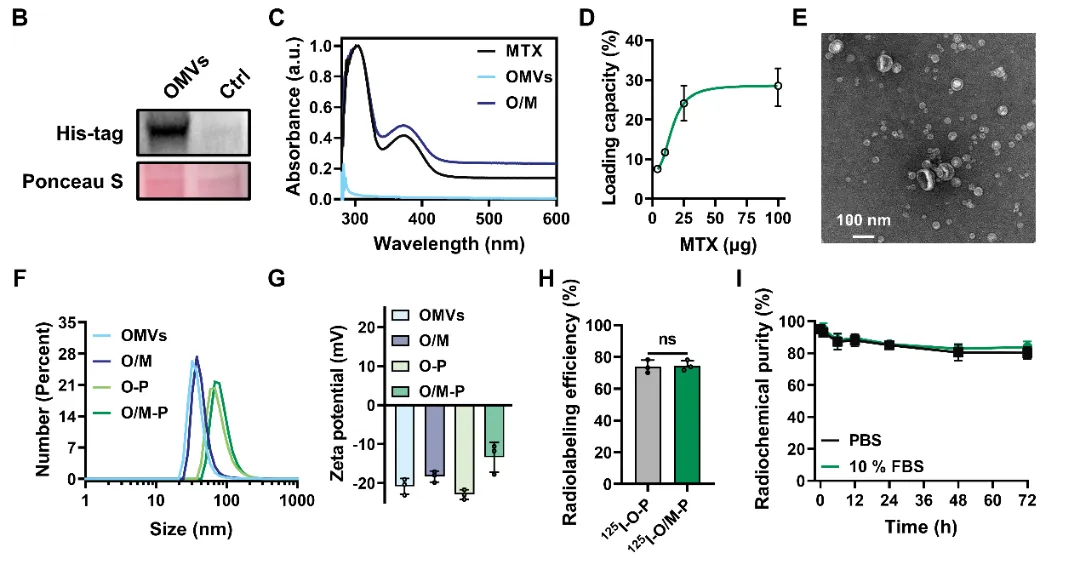
图1 131I-O/M-P的构建和表征
2. 131I-O/M-P抑制肿瘤细胞周期和代谢,增强放射敏感性
在完成O/M-P的理化性质评估后,进一步在细胞水平系统验证其代谢干扰与放疗增敏效应。细胞水平验证显示其具备良好的细胞相容性,能够高效进入肿瘤细胞;抑制肿瘤细胞周期G1/S转换,下调细胞周期/复制相关蛋白Cyclin A2与PCNA的表达,同时降低DHFR蛋白水平发挥代谢干扰作用。在此基础上构建的131I-O/M-P可以直接造成DNA双链断裂(DSBs),从而杀死肿瘤细胞,使凋亡增加。同时其可显著升高p-STING及p-IRF3水平,激活cGAS-STING通路以奠定体内免疫相关过程的分子基础(图2)。因此,131I-O/M-P在细胞层面实现了由代谢抑制与周期调控出发,叠加131I诱导的DNA损伤并伴随cGAS-STING轴激活,进而转化为增强的细胞抑制与凋亡的顺序协同过程,与后续体内放射-代谢-免疫治疗提供基础。
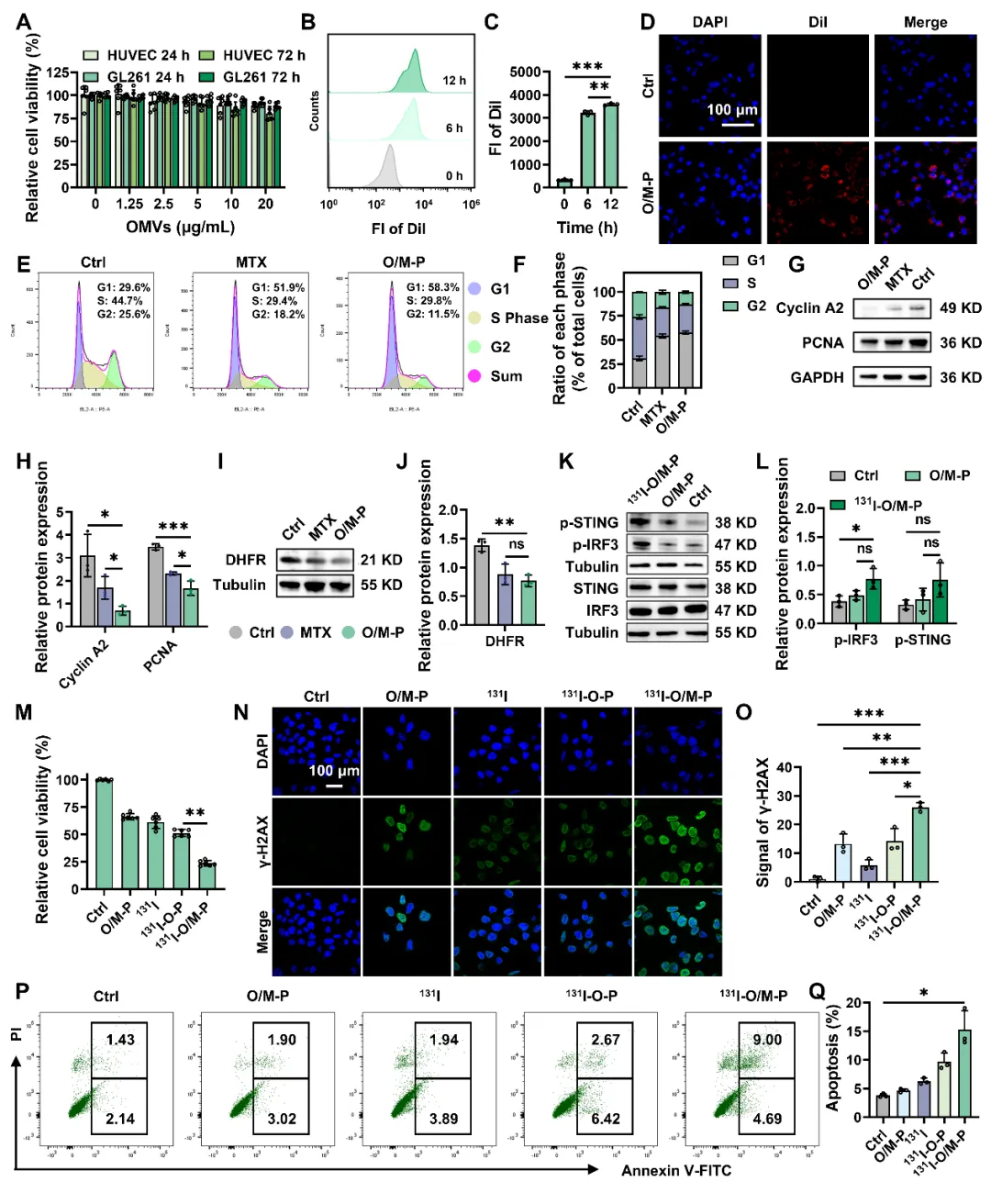
图2131I-O/M-P抑制肿瘤细胞周期和代谢,增强放射敏感性
3. 131I-O/M-P的生物分布、安全性及抗肿瘤免疫激活。
鉴于131I-O/M-P在细胞水平表现出明确的代谢-免疫调节能力与肿瘤杀伤效应,我们进一步开展体内研究。采用化学性质等同且辐射更安全的125I-O/M-P探究其体内行为的实验结果表明,其尾静脉注射后肿瘤部位高放射性摄取值,未见显著毒性反应,证实具有良好生物相容性与体内稳定性,并具备肿瘤靶向递送潜力。体内抗肿瘤及免疫激活验证结果显示,131I-O/M-P处理使肿瘤细胞凋亡显著增加、γ-H2AX信号升高,提示131I诱导的DNA双链断裂(DSBs)有效放大并转化为凋亡效应;同时肿瘤组织p-STING水平升高,淋巴结内CD80+ CD86+成熟树突状细胞(DC)比例上调,肿瘤组织中F4/80+ CD86+ M1型巨噬细胞极化增加(图3)。因此,131I-O/M-P在体内实现了放射损伤、先天免疫感知和适应性免疫激活的链式联动。
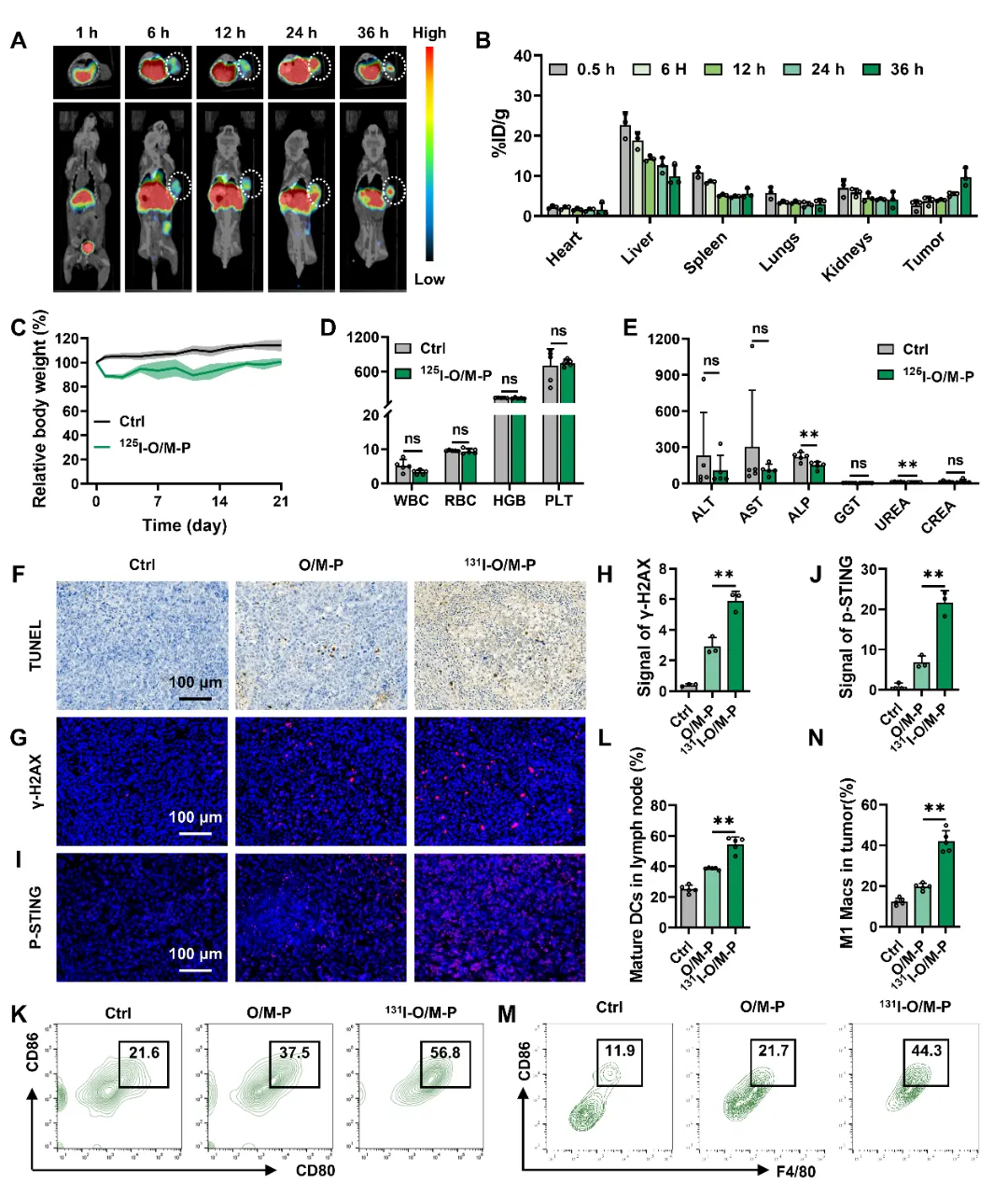
图3 131I-O/M-P的生物分布、安全性和抗肿瘤免疫激活
4. 131I-O/M-P介导的放射代谢免疫治疗抑制胶质瘤进展
基于前述体内行为与免疫激活结果,我们进一步在GL261皮下肿瘤模型中评估131I-O/M-P的综合治疗能力。结果显示,131I-O/M-P具有最显著的肿瘤抑制作用,肿瘤生长几乎被完全阻断,肿瘤组织结构破坏,Ki67与PCNA免疫荧光显著下调,提示肿瘤细胞增殖被有效限制。进一步的免疫分析显示,131I-O/M-P治疗后肿瘤组织内CD3+CD8+GranzymeB+细胞毒性T细胞(CTL)比例显著上升,CD3+CD8+PD-1+T细胞比例下降,表明在获得性免疫被激活的同时,T细胞功能抑制状态亦得到改善,有利于持续的效应阶段。此外,肿瘤组织内CD45+NK1.1+自然杀伤(NK)细胞浸润比例增加,提示先天杀伤通路被并行增强,可与CTL形成互补杀伤网络(图4)。因此,131I-O/M-P在皮下胶质瘤模型中实现了放射-代谢-免疫治疗。一方面,131I的持续辐射与MTX介导的代谢抑制共同放大DNA损伤并限制修复,从而抑制肿瘤增殖;另一方面,ICD标志上调、STING轴激活、DC成熟与 M1极化推动了CTL与NK的有效募集与功能维持,进一步重塑免疫微环境并放大抗肿瘤效应,为后续在原位脑瘤模型中的验证与机制精细化研究提供了坚实依据。
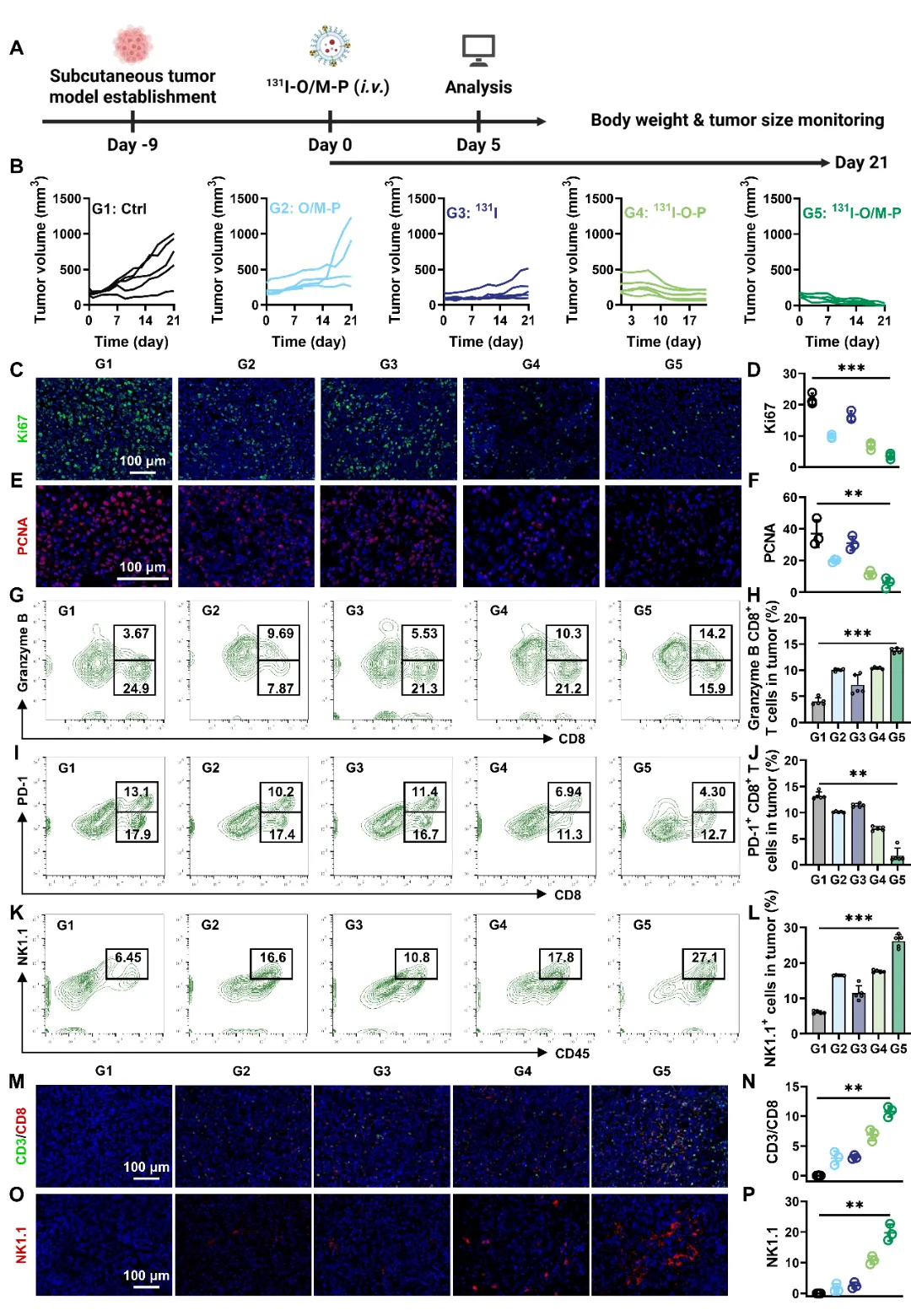
图4 131I-O/M-P介导的放射代谢免疫治疗抑制胶质瘤进展
5. 131I-O/M-P抑制原位胶质瘤,增强免疫调节
在确认131I-O/M-P对皮下肿瘤具有显著治疗作用后,我们进一步评估其在原位脑胶质瘤模型中的抗肿瘤效果。采用125I-O/M-P表征体内行为,结果证实其脑内给药后具有良好局部滞留与肿瘤指向性,为后续疗效奠定药代基础。系统疗效评估结果显示,131I-O/M-P显著抑制肿瘤生长,中位生存期达22.5d。组织学层面评估结果显示,TUNEL染色显著阳性,Ki67免疫荧光下调,GFAP染色减弱,MMP-9表达受抑,提示肿瘤凋亡发生明显,肿瘤细胞增殖受限。进一步的免疫评估表明, 131I-O/M-P治疗后肿瘤组织中CD3+ CD8+ GranzymeB+ CTL及CD45+ NK1.1+ NK细胞比例上升,表明131I-O/M-P有效募集并激活了CTL与NK两条杀伤轴线,与前述ICD信号与STING轴被激活的证据相呼应,并可能构成对放射损伤的免疫放大回路。体内生物安全性评估提示该方案在本给药方式与剂量下具有良好耐受性(图5)。综上,131I-O/M-P在原位脑胶质瘤模型中实现了放射增敏与免疫放大的效应。一方面,131I的持续β-辐射与MTX介导的代谢干预协同放大DNA损伤并限制修复,直接抑制肿瘤生长并带来生存获益;另一方面,ICD标志上调及STING通路活化促进CTLs与NK的募集与效应维持,并伴随M1极化与MMP-9下调,有助于降低侵袭性并改善肿瘤微环境。这些结果进一步证实131I-O/M-P在脑内环境中可以实现放射-代谢-免疫顺序协同与显著抗瘤潜力,为基于脑肿瘤的代谢免疫治疗提供了理论依据。
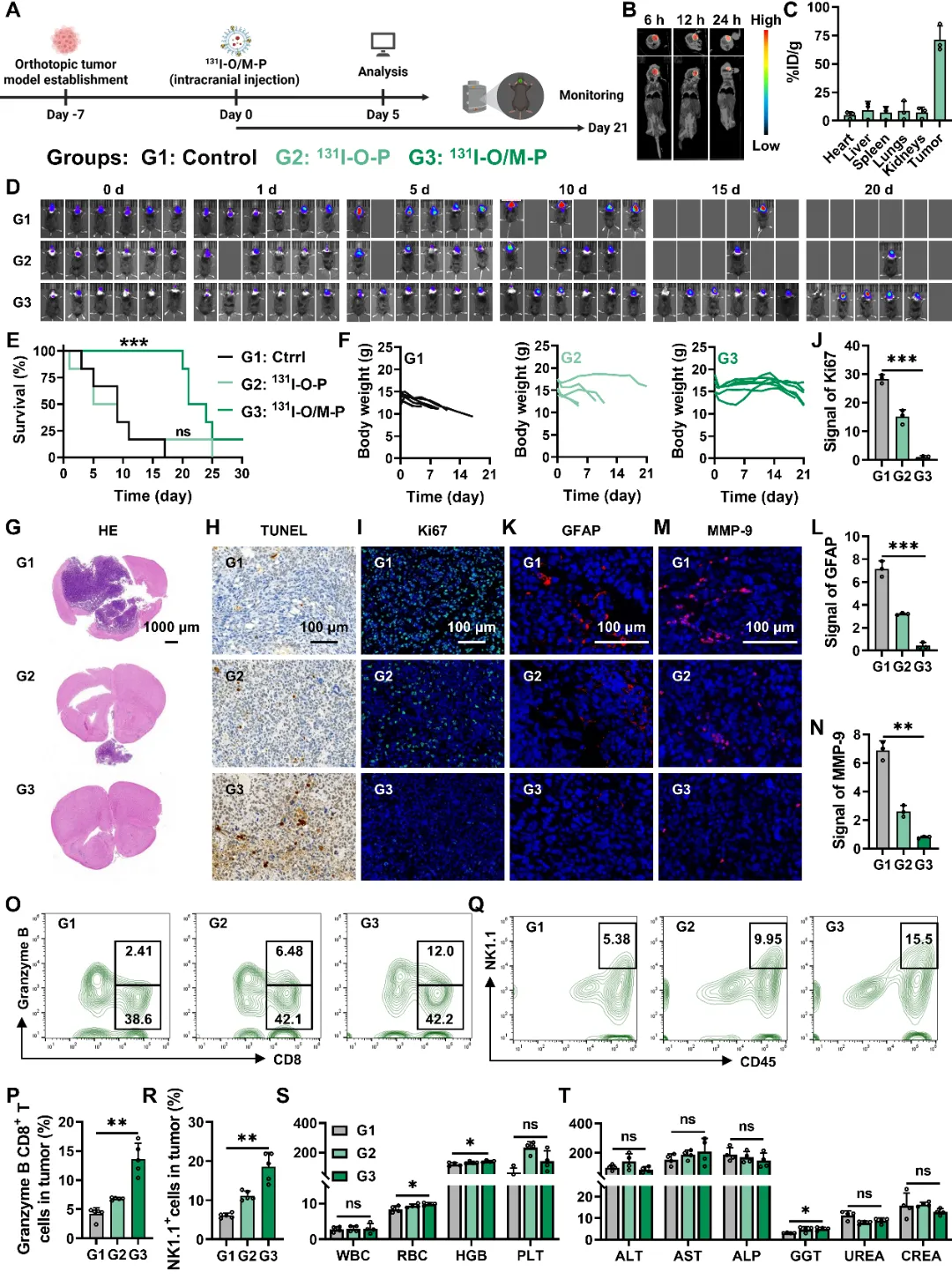
图5 131I-O/M-P抑制原位胶质瘤,增强免疫调节
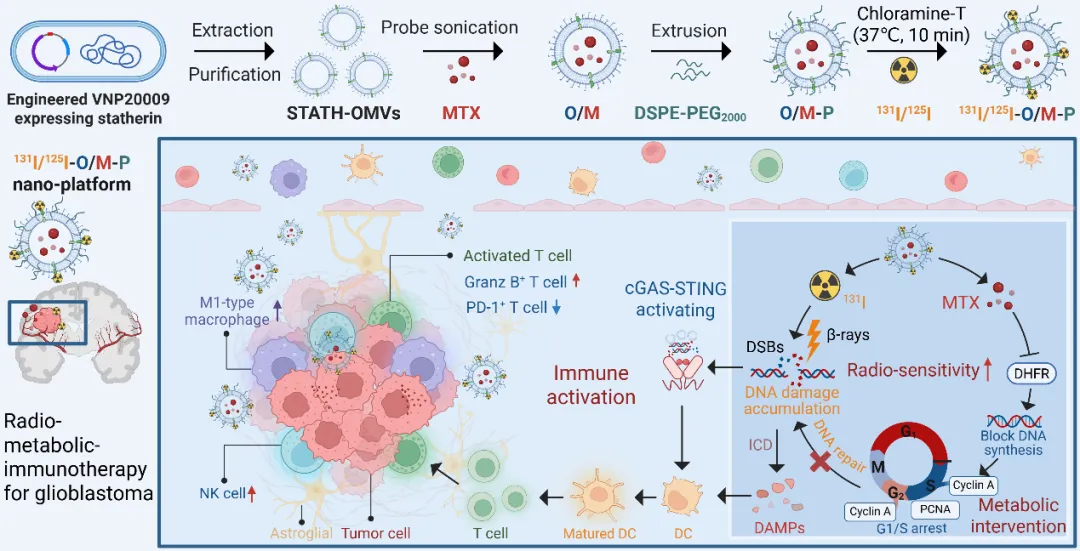 图6 文章总结图
图6 文章总结图
该研究基于工程化细菌外膜囊泡,通过“放射损伤→代谢阻断→免疫放大”的级联响应机制实现了脑胶质瘤三重协同治疗,该技术具备靶向性强+免疫原性高的双重优势。实验证明在侵袭性最强的原位脑瘤模型中获得67%小鼠20天存活率,在皮下瘤模型中实现肿瘤体积抑制率达92%。该研究不仅解决了脑瘤放疗易耐受、免疫难激活的行业痛点,更通过“生物源载体+时序功能编程”的方法论创新,为阿尔茨海默病靶向递药、术后抗复发疫苗等神经免疫交叉领域提供可迁移的技术路径。
原文链接:https://link.springer.com/article/10.1186/s12951-025-03936-4
苏州大学硕士研究生梁茂林、范龙飞、安徽医科大学硕士研究生张苏铭为论文共同第一作者,苏州大学放射医学与防护学院朱然教授、杨凯教授以及安徽医科大学裴佩副教授为通讯作者,苏州大学和中检核联(苏州)医药科技有限公司为该论文第一单位。该工作得到国家自然科学基金、安徽省杰出青年教师培养计划重点项目、安徽省自然科学基金、安徽省高等学校省级重点科研项目、江苏高校优势学科建设工程等资助。
转载须知:“逻辑神经科学”特邀稿件,且作者授权发布;本内容著作权归作者和“逻辑神经科学”共同所有;欢迎个人转发分享,未经授权禁止转载,违者必究。

“逻辑神经科学”微信群:文献学习
扫码添加微信,并备注:逻辑-文献-姓名-单位-研究领域-学位/职称