南京工业大学《Chem. Soc. Rev.》综述:有机光敏剂分子设计与光热诊疗
光动力疗法(PDT)近年来已成为肿瘤治疗领域中一种极具前景的创新性治疗手段。该疗法凭借其优异的时空选择性,能够精准作用于肿瘤组织而不损伤邻近健康组织;同时具有非侵入性特质,可显著减少手术干预带来的物理创伤,且相较于手术、放疗和化疗等传统癌症治疗方法,其副作用更小。PDT的作用机制通常依赖于三个核心要素:光敏剂、特定波长的光源以及分子氧(O₂)。其中光敏剂的合理设计与优化对PDT疗效起着决定性作用。在光激活过程中,光敏剂经历从单重态(S₁)向三重态(T₁)的系间窜越(ISC),进而通过II型机制将能量转移至周围环境中的氧分子,产生具有细胞毒性的活性氧化物(ROS),其中以单线态氧(¹O₂)为主要效应分子。相较而言,I型机制则涉及光敏剂三重态与生物底物间的光诱导电子转移,进而产生羟基自由基(˙OH)和超氧阴离子自由基(O₂⁻˙)等阳离子或阴离子自由基¹⁸⁻¹⁹。因此,促进ISC过程的策略通常能增强ROS生成,从而放大PDT的细胞毒性效应。尽管PDT在肿瘤治疗中展现出独特优势并已广泛应用于临床,但仍面临诸多技术挑战与临床局限性。传统有机光敏剂的临床转化仍受限于固有缺陷:光敏化效应低、乏氧肿瘤微环境(TME)中活性氧(ROS)生成不足、组织穿透深度有限及肿瘤靶向效率低。
针对这些挑战,来自南京工业大学的董晓臣等团队通过理性结构设计综述了分子工程策略,聚焦五大方向:(1)通过引入重原子、设计扭曲构象结构或聚合化光敏剂促进系间窜越(ISC)过程以增强ROS生成;(2)构建I型光敏剂、分步式光敏剂及其他自由基生成型光敏剂以克服肿瘤乏氧;(3)通过构建供体-受体(D-A)结构、制备J-聚集体或利用双光子激发实现近红外光激发以提升穿透深度;(4)通过偶联肿瘤特异性配体或基因编码片段实现肿瘤靶向治疗;(5)设计TME可激活型光敏剂以降低脱靶效应。此外,本文还重点探讨了在精准肿瘤治疗、抗菌治疗及余辉成像诊断等新兴领域的应用,并对有机光敏剂分子设计与光热诊疗一体化的前景与挑战进行展望,旨在架接基础研究与临床转化之间的桥梁,为发展新一代有机光敏剂提供战略思路。相关工作以题为“Organic photosensitizers: from molecular design to phototheranostics”的综述文章发表在2025年8月26日的期刊《Chemical Society Reviews》。

【研究内容】
本文总结了通过分子结构设计提升有机光敏剂在光动力治疗中性能的主要方法(图1)。首先概述光动力治疗的作用机制,重点阐释分子设计策略,进而介绍小分子光敏剂在肿瘤治疗、抗菌治疗及诊断成像领域的应用。最后,对有机光敏剂分子设计与光诊疗一体化面临的挑战和发展前景进行展望,以推动新一代有机光敏剂在光动力治疗中的发展。
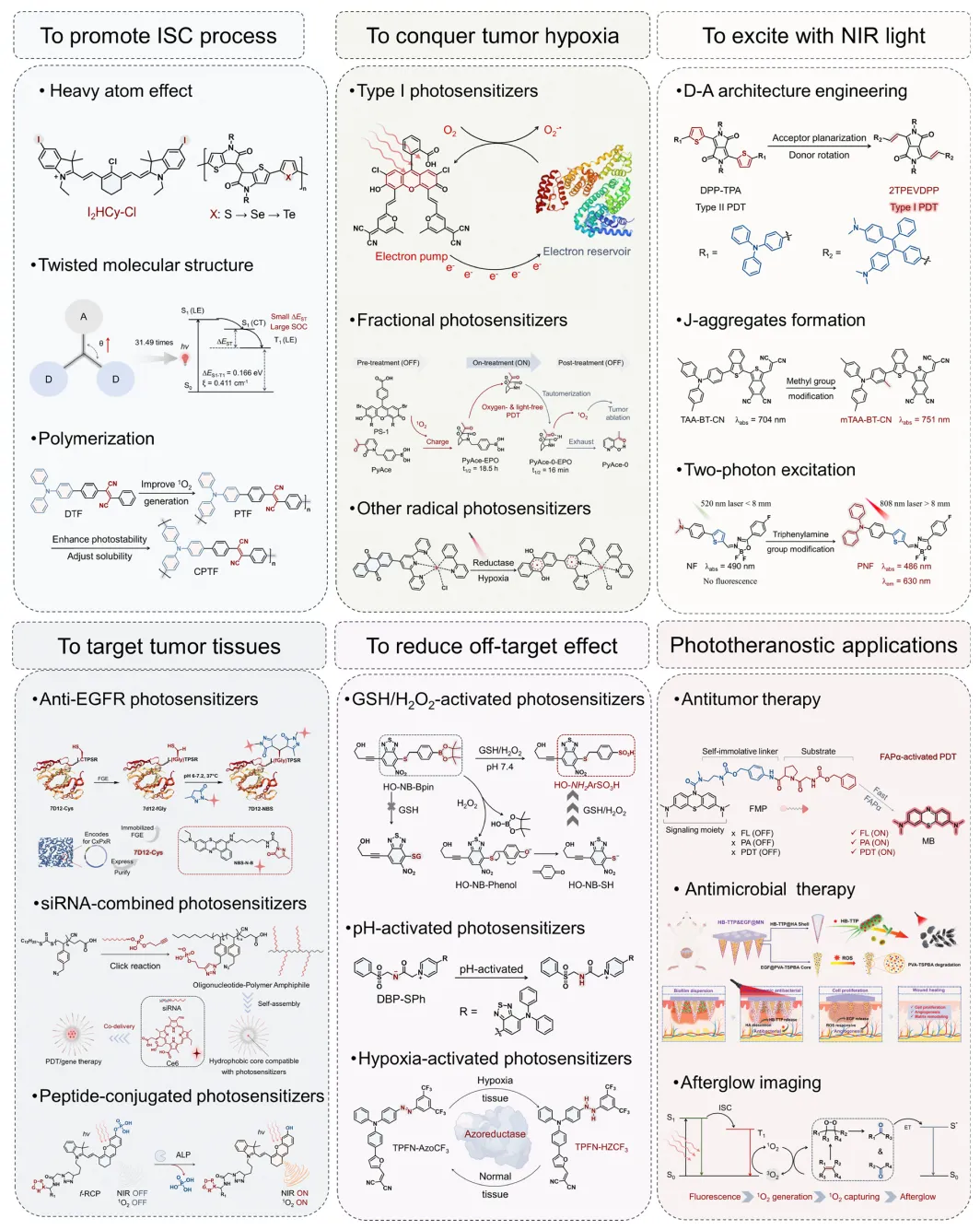
图1 有机光敏剂主要设计原理及光热诊疗应用示意图
【有机光敏剂的分子设计策略——促进活性氧生成的有效系间窜越过程】
以含硫族元素的杂环(噻吩、硒吩和碲吩)为供体、缺电子的硫代异靛蓝为受体,研究人员开发了一系列重原子取代的光敏剂(图2a)。通过逐步替换硫族原子(硫、硒、碲),利用重原子效应实现了对光物理性质的系统调控。特别值得注意的是,从硫到碲的原子序数递增使自旋轨道耦合矩阵元素呈现阶梯式增强。所得化合物PTS(硫)、PTSe(硒)和PTTe(碲)的自旋轨道耦合矩阵元素ξ(S1, T3)分别为0.04 cm⁻¹、0.06 cm⁻¹和0.12 cm⁻¹。这种近数量级的增长凸显了重原子取代在促进系间窜越方面的重要作用,为高效光动力活性奠定了坚实基础。
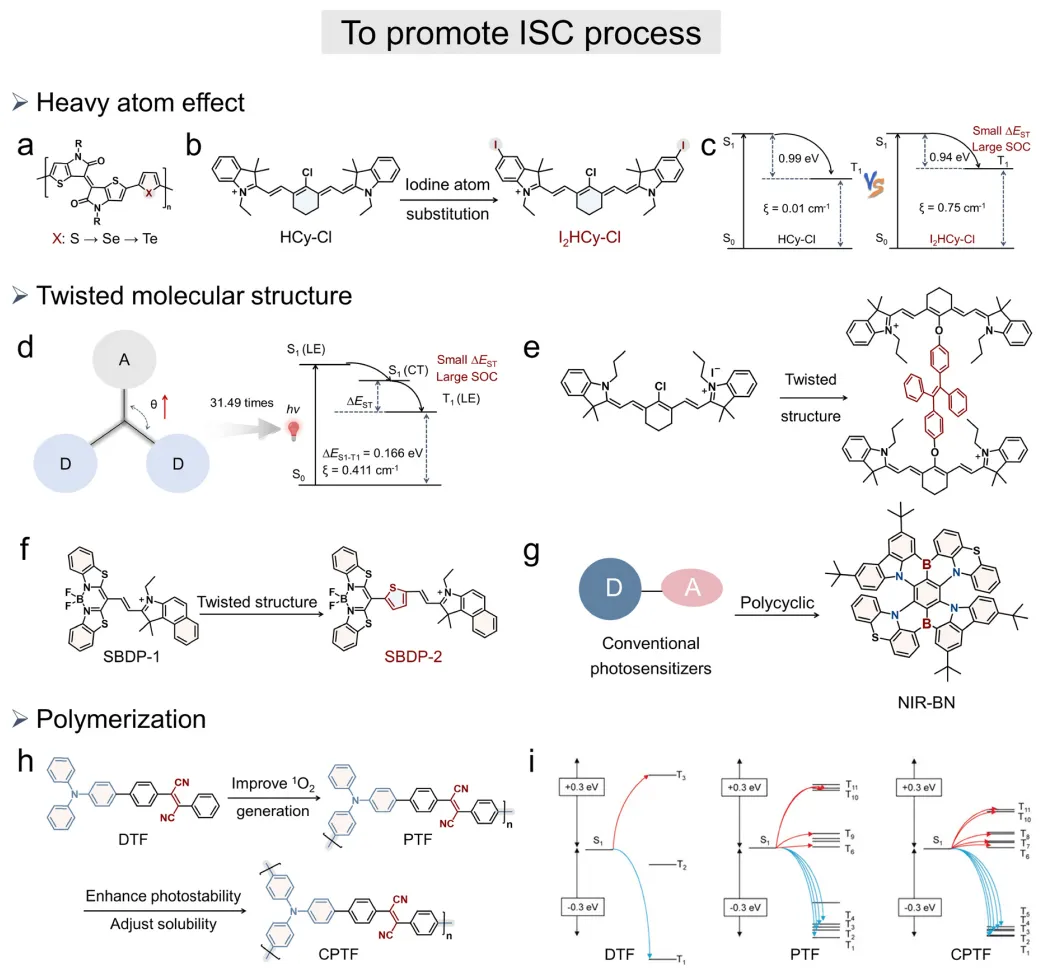
图2 PTS、PTSe与PTTe的重原子引入示意图
【有机光敏剂的分子设计策略——克服肿瘤缺氧的避缺氧途径】
当前的光动力治疗(PDT)主要依赖II型光敏剂通过能量转移机制产生细胞毒性单线态氧(¹O₂)。然而这种氧依赖性疗法的效果从根本上受限于肿瘤缺氧微环境(TME)。这种病理生理特征,加之快速耗氧和PDT诱导的血管损伤,显著削弱了治疗过程中¹O₂的生成,从而限制整体疗效。电荷驱动策略具有双重功能增强:(一)显著提升水溶性;(二)通过靶向负电荷细胞器(如线粒体膜和内质网)放大治疗效果。通过合理引入阳离子基团,分子电子密度将重新分布,促进系间窜越(ISC)和电子-空穴分离(图3a)。这些效应共同增强了超氧阴离子(O₂⁻˙)和羟基自由基(OH˙)的生成,即使在缺氧条件下也是如此。重要的是,所得阳离子光敏剂在线粒体中优先积累,从而提升PDT疗效。但尽管季铵盐或磺酸盐取代改善了溶解性,这些光敏剂相对较短的吸收波长仍限制其在深部组织中的应用。
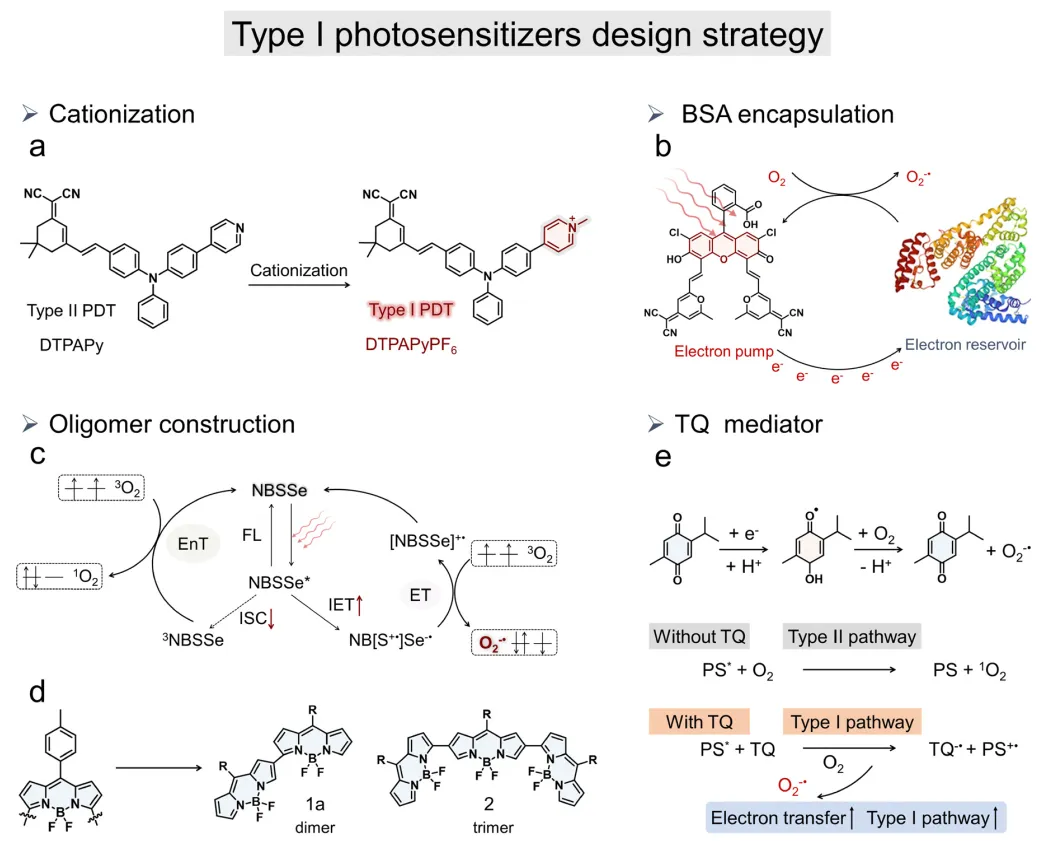
图3 阳离子化分子工程策略提升光动力疗法性能示意图
传统II型光动力疗法(PDT)的治疗效果从根本上受限于其对氧气的依赖性,导致其在缺氧肿瘤微环境(TME)中疗效不佳。为突破这一局限,暗可持续分次光动力疗法(fractional PDT)所用光敏剂的开发引起广泛关注——这类光敏剂能够在不依赖持续光照的条件下存储并释放单线态氧(¹O₂)。在此背景下,内过氧化物整合光敏剂作为一类新型智能分子构建体,通过将¹O₂捕获单元与光敏单元协同耦合,实现了¹O₂的可逆捕获和热触发释放,从而将细胞毒性效应延伸至光照窗口之外。进一步研究开发出具有内体逃逸能力的质子响应型可切换¹O₂纳米捕获系统(图4a)。基于蒽的分次光敏剂ANBDP在酸性细胞内区间发生质子化形成ANBDPH,该过程通过灭活电荷转移(CT)态显著增强¹O₂生成(图4b)。在730 nm光照下,ANBDPH高效产生¹O₂,随即被蒽单元捕获形成稳定的内过氧化物中间体(ANOBDPH)。值得注意的是,ANOBDPH通过热环逆反应释放耐缺氧¹O₂,实现了无需持续照明的暗可持续PDT,有效延长治疗时间窗口。
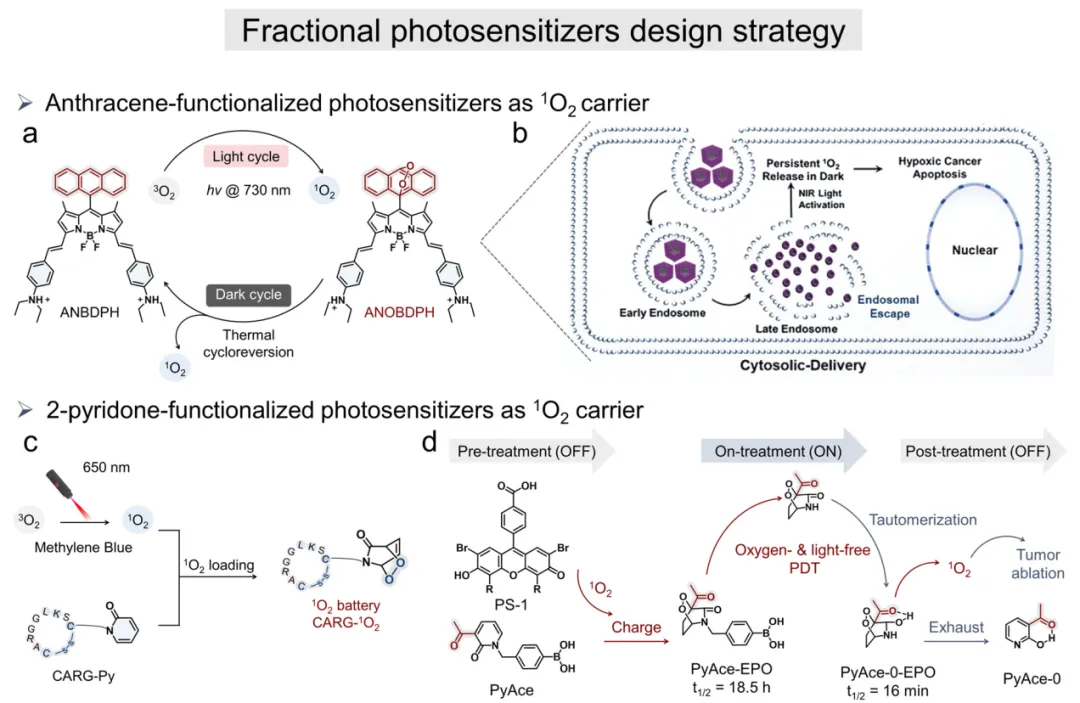
图4 ANBDPH在光照与黑暗条件下可逆捕获释放单线态氧的示意图
【有机光敏剂的分子设计策略——近红外光激发以增强组织穿透性】
引入供体-受体(D-A)框架是调控近红外二区(NIR-II)光敏剂吸收的成熟策略。通过共轭强给电子单元与强吸电子单元,可扩展π共轭体系并增强分子内电荷转移(ICT),从而实现吸收光谱红移(图5a)。例如,将强给电子基团三苯胺(TPA)与π桥噻吩及吡啶盐受体结合,可显著增强ICT效应。伴随的阳离子进一步富集局部电子密度,促进激发态光敏剂向分子氧或水转移电子,从而加速羟基自由基(OH˙)和超氧阴离子(O₂⁻˙)的生成。这种双活性氧生成能力与环境依赖性低的特性,使D-A体系在I/II型光化学反应中具有独特的多功能性。另一种D-A调控策略开发出兼具增强光动力疗效和本征NIR-II荧光发射的离子型光敏剂系列(图5b)。以二噻吩吡咯(DTP)作为强给体,吲哚嗪盐作为强受体构建的光敏剂DTP-In,其吸收和发射光谱均发生显著红移,光谱响应完全进入NIR-II区间。此外,在水相环境中DTP-In可自组装成带正电荷的纳米颗粒,其性能优于传统封装制剂,展现出卓越的细胞摄取效率和线粒体靶向能力。
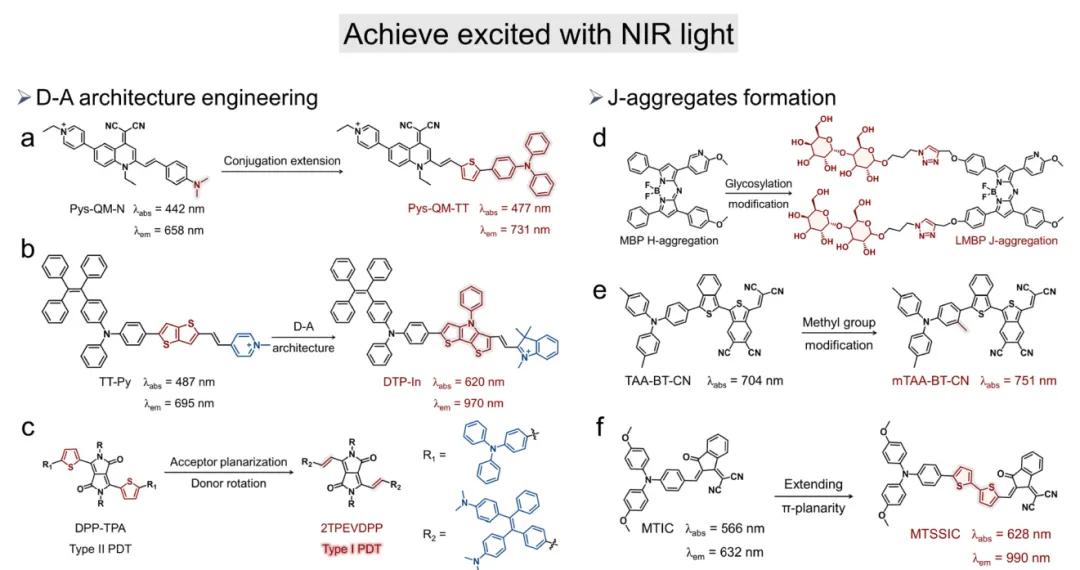
图5 Pys-QM-N、Pys-QM-T与Pys-QM-TT的分子结构
【有机光敏剂的分子设计策略——主动靶向肿瘤以提高治疗特异性】
基于上述理念,研究人员近期开发出一种活性氧激活型生物素靶向探针MB-PEG-Bio2(图6a)。该设计通过将生物素共价连接在活性氧敏感骨架上,增强受体-配体相互作用,从而提升肿瘤亲和性与选择性。该探针初始处于光学沉默状态,但能在肿瘤微环境高活性氧条件下被选择性激活,释放MB光敏剂并产生强近红外荧光及光声信号,实现精准肿瘤可视化。在多组小鼠模型中,MB-PEG-Bio2均展现出卓越的肿瘤靶向能力,可检测到直径小至3毫米的微小肿瘤。通过将抗EGFR纳米抗体(7D12)与苯并吩噻嗪类光敏剂NBS共价连接,研究人员构建了主动靶向肿瘤的光敏剂7D12-NBS(图6b),用于耐低氧光免疫治疗。该复合物能选择性靶向EGFR过表达的肿瘤细胞,在常氧和低氧条件下均表现出强细胞毒性,同时具有优良的药代动力学特性——通过EGFR介导的内吞作用实现快速全身清除和高肿瘤蓄积。
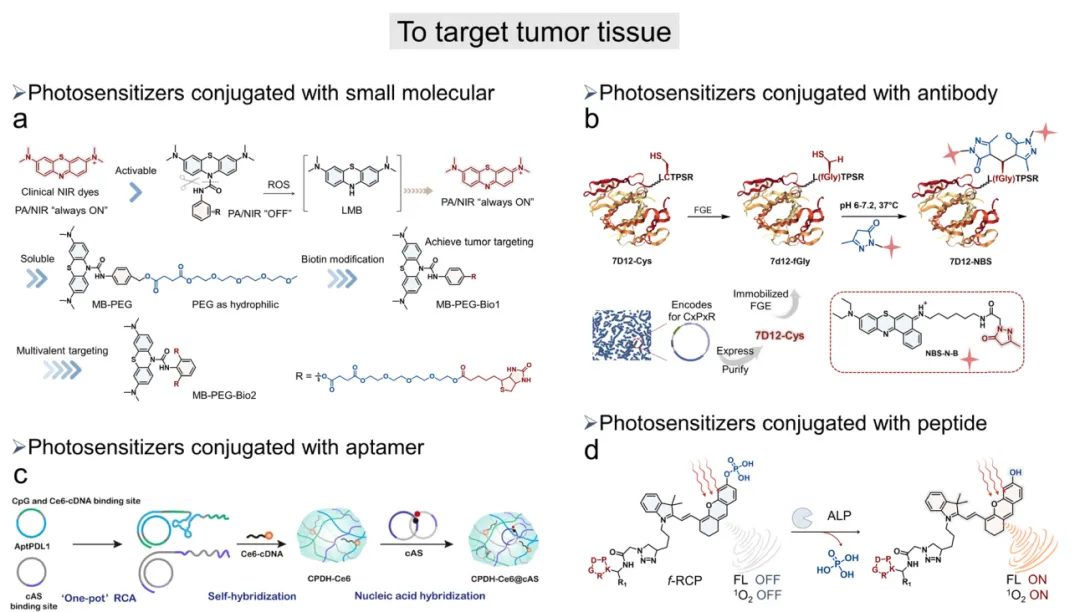
图6 靶向检测肿瘤组织的MB-PEG-Bio2探针设计策略
基因调控策略(尤其是小干扰RNA技术)因其能高特异性沉默疾病相关基因,已成为癌症治疗的重要工具。但未经修饰的siRNA存在细胞摄取率低、易被酶降解等问题。为突破这些局限,病毒载体、阳离子聚合物、脂质体及多孔纳米颗粒等多种纳米载体被用于提升递送效率和系统稳定性。典型代表PSNA@Ce6@siMCT1纳米平台将光敏剂Ce6封装于聚合物球形核酸疏水核内,表面杂交抗MCT1 siRNA(图7a),显著增强siRNA稳定性和摄取效率。在光照下,Ce6通过光化学内化效应引发溶酶体逃逸,促进siRNA转染并沉默MCT1表达,从而缓解肿瘤缺氧并增强Ce6的光动力疗效。为降低聚合物载体的生物安全性风险,研究人员开发出智能无载体siRNA递送系统:通过静电作用将阳离子硫代尼罗蓝光敏剂NB-Br与靶向PLK1的siRNA连接形成siPLK1-NB纳米颗粒(图7b)。该颗粒被肿瘤细胞溶酶体摄取后,光诱导产生的活性氧可破坏溶酶体膜,释放siRNA并有效沉默PLK1基因,最终诱导细胞凋亡。
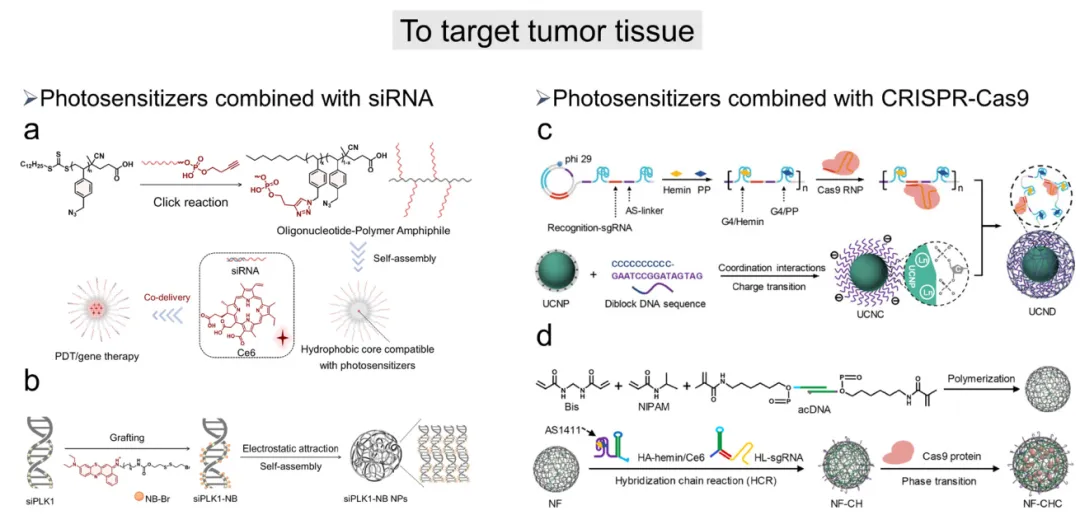
图7 包载siRNA与有机光敏剂Ce6的两亲性聚合物PSNA合成路线
【有机光敏剂的分子设计策略——刺激响应策略以最小化脱靶毒性】
PDT在癌症治疗领域前景广阔,但其临床应用常因脱靶效应损伤健康组织而受限。为解决这一难题,大量研究聚焦于开发肿瘤微环境(TME)激活型光敏剂。这类智能光敏剂在正常生理条件下保持惰性,从而显著降低系统毒性及对健康组织的非特异性损伤。当遇到肿瘤微环境特异性刺激(如升高的谷胱甘肽/活性氧水平、缺氧、酶过表达或低pH值)时,它们会被选择性激活并产生活性氧(图8a)。这种激活策略极大提升了PDT的治疗精准度和治疗指数,同时减少对周边健康组织的损害。通过将苯并噻二唑与频哪醇硼基团共轭连接,研究人员构建了线粒体靶向光敏剂HO-NB-Bpin。该化合物对升高的谷胱甘肽和过氧化氢水平具有双重响应特性,可在肿瘤微环境中选择性于线粒体内产生单线态氧和超氧阴离子自由基(图8b)。为增强过氧化氢选择性并调控光学特性,研究人员在设计中引入了硫醇响应性自消除机制:硼酸酯能稳定抵抗谷胱甘肽的亲核攻击,但可被过氧化氢特异性裂解,进而触发1,6-苄基消除反应,实现活性成分HO-NB-SH光敏剂的可控释放。
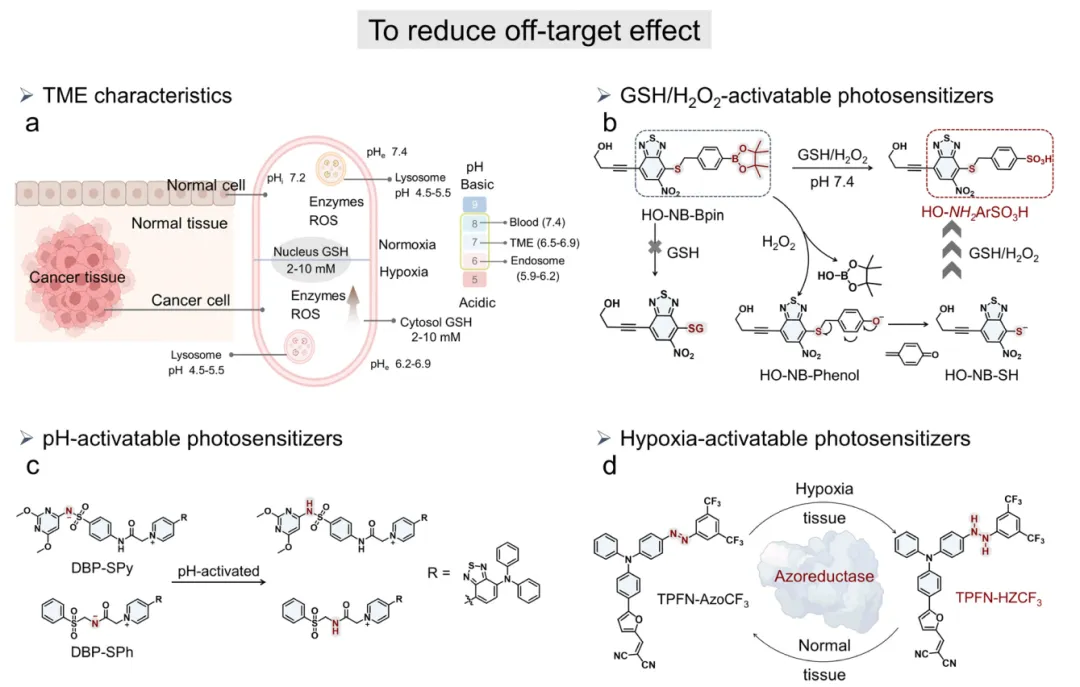
图8 可用于刺激响应癌症治疗的肿瘤微环境特征示意图
【有机光敏剂的治疗与诊断应用】
有机光敏剂在生物医学的治疗与诊断领域展现出卓越的多功能性。PDT作为一种非侵入性治疗方式,可与手术、化疗及放疗等传统策略协同应用(图9)。除治疗应用外,有机光敏剂还可利用辐射衰变过程作为荧光探针,在特定波长激发下实现实时成像。此外,通过非辐射衰变途径,某些有机光敏剂能将吸收的光能转化为局部热量,产生可用于光声成像的可检测超声信号。具有余辉发光特性的有机光敏剂能在照射后维持长时间信号持续,为实时及长期光热诊疗应用提供重要潜力。
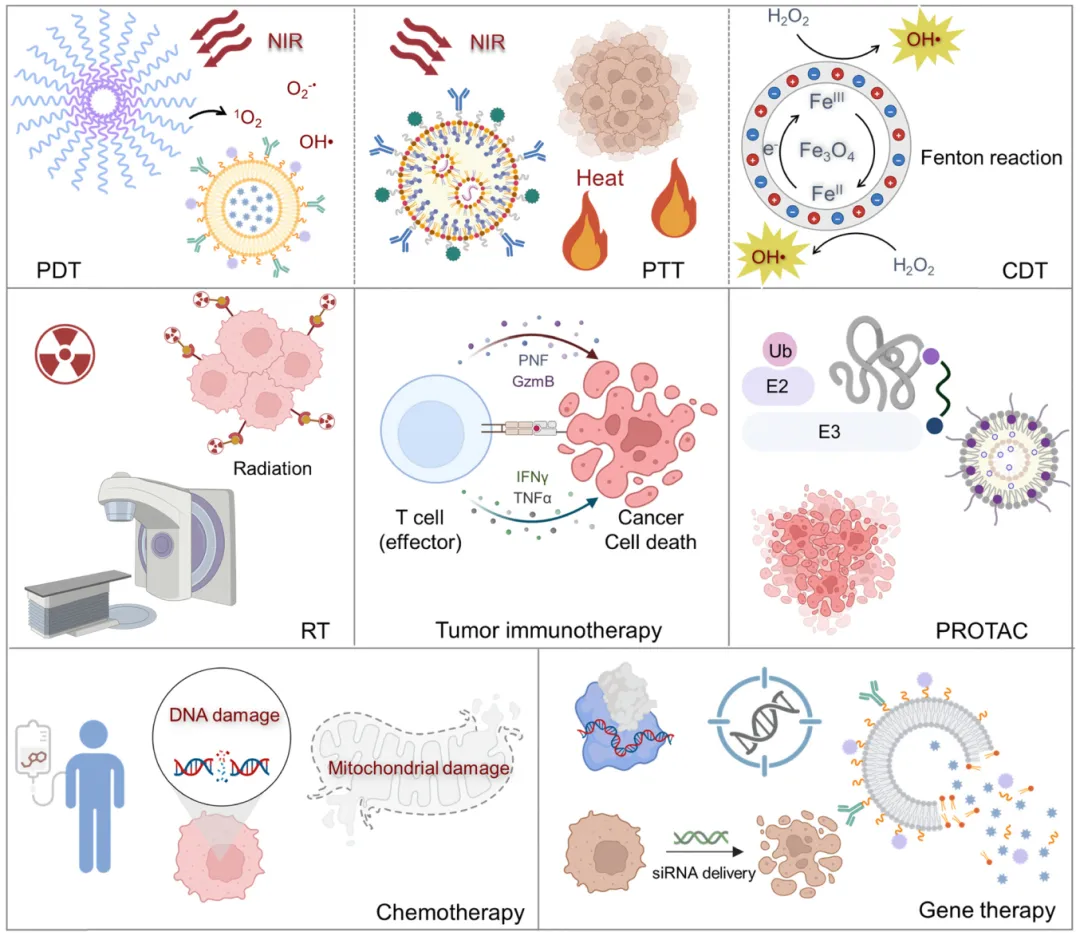
图9 有机光敏剂联合治疗示意图
目前,PDT与光热疗法(PTT)的结合是研究最广泛的策略之一。通过将四苯基乙烯(TPE)单元和亲水性磺酸基(SO3−)引入方酸菁染料(SQs),所得光敏剂TPE-SQ7在水介质中表现出显著的H-聚集和强自组装特性(图10a)。在亲水性SO3−基团作用下,TPE-SQ7转化为顺式构型并促使形成H型二聚体,这些二聚体通过分子间相互作用组装成一维纳米线,最终聚集成超分子H-聚集体。TPE-SQ7实现了超过50%的光热转换效率(PCE),并表现出聚集增强的I型活性氧(ROS)生成能力。体外和体内研究均证实其具有强大的抗肿瘤功效,甚至在缺氧条件下仍能有效作用。化学动力疗法(CDT)可生成高活性羟基自由基(OH˙),克服了PDT的局限性。发展PDT/CDT联合策略是提升肿瘤治疗效果的有效途径。研究人员开发了一种光激活光敏剂Cu-PCy JNPs,通过J-聚集调控实现从PDT向持续性CDT的转换(图10b)。有序的J-聚集体增强了花菁类光敏剂的光动力性能,同时抑制了铜-卟啉组分的化学动力学活性。在光照射下,花菁骨架的降解和J-聚集体的解组装触发级联CDT效应,表现为持续的OH˙生成和氧化应激,最终诱导肿瘤细胞凋亡。
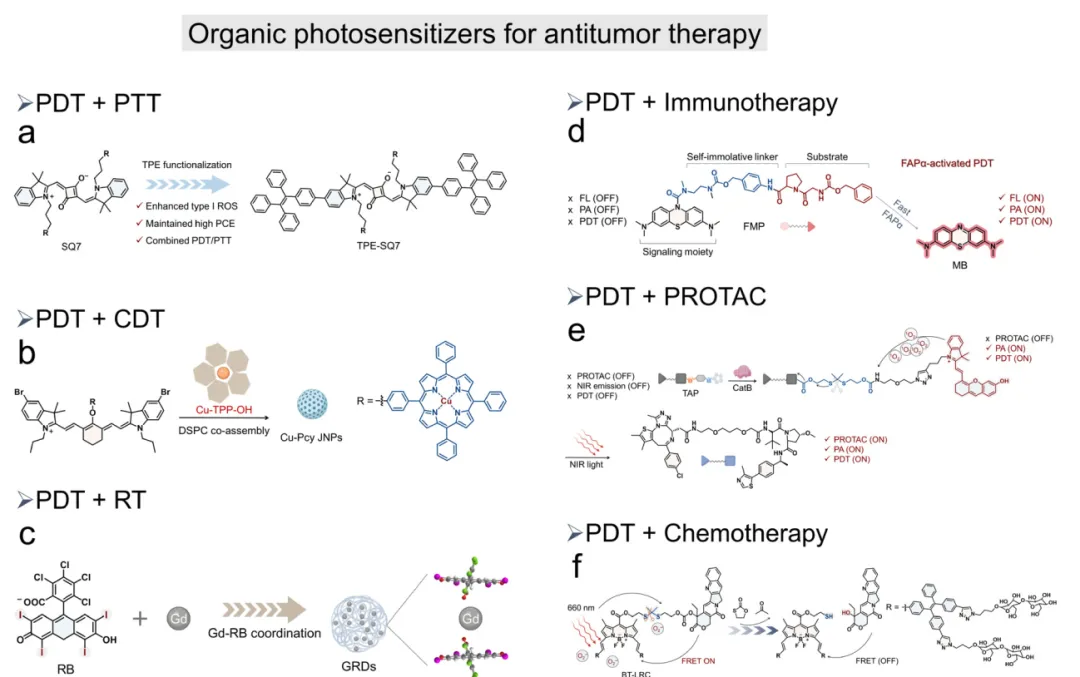
图10 基于SQ结构光敏剂的分子工程设计
【总结与展望】
本综述深入探讨了开发新一代有机光敏剂的分子工程策略,并重点介绍了其在光热诊疗应用中不断扩展的作用。本文系统总结了针对当前局限性的关键创新:(1) 为促进系间窜越过程,重原子引入、高度扭曲分子构象和共轭聚合等多种修饰方法已被证实有效;(2) 为克服肿瘤缺氧困境,通过开发I型光敏剂、分步激活光敏剂及其他自由基型光敏剂实现了耐缺氧工程化设计;(3) 为实现近红外光激发,通过给体-受体分子结构设计、J-聚集体形成及双光子激发技术实现了更深组织穿透;(4) 为靶向肿瘤组织,通过设计肿瘤特异性生物标志物触发型光敏剂和基因工程介导的靶向修饰增强了生物特异性;(5) 为降低脱靶效应,肿瘤微环境响应型有机光敏剂的开发显著提高了治疗选择性。
参考资料:
https://doi.org/10.1039/D5CS00599J
来源:EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!
