Cell Reports|南京大学华子春/徐运/吴乐阳开发一体化细胞创新疗法,实现溶瘤细菌与促炎因子可控释放、双相抗癌
- 2026-05-12 23:55:11
Cell Reports|南京大学华子春/徐运/吴乐阳开发一体化细胞创新疗法,实现溶瘤细菌与促炎因子可控释放、双相抗癌以巨噬细胞为基础的工程化疗法在癌症治疗领域展现出潜力,但仍面临若干关键限制:药物释放过程缓慢且难以控制,存在巨噬细胞被重编程为促癌表型的风险。此外,该类细胞的载药能力有限,为实现有效的抗肿瘤效果,常常需要输注大量工程化巨噬细胞(剂量可达108/kg)。这些因素共同制约了该疗法的进一步开发与临床转化。理想的细胞介导抗癌策略应具备可控性、易操作性以及持久疗效。与常规药物因时间推移而逐渐降解的特性不同,溶瘤细菌(如减毒鼠伤寒沙门氏菌)能够在肿瘤内部特异性增殖,并易于通过基因工程进行改造。同时,外源性细菌被认为可为巨噬细胞提供持续且强效的激活信号。因此,将巨噬细胞治疗与细菌疗法相结合,有望克服传统细胞疗法所面临的诸多挑战,为肿瘤治疗提供新的可行路径。 南京大学华子春/吴乐阳团队发现细菌 HtrA 蛋白是其抗癌关键效应蛋白,细菌可诱导瘤内巨噬细胞焦亡进行抗癌治疗。并开发出多个具有自主知识产权的溶瘤菌株,部分菌株已获准开展研究者发起的临床研究。团队进一步聚焦于细菌药物的智能精准递送新策略,基于溶瘤细菌与巨噬细胞的天然相互关系,开创“细胞-细菌-抗体”一体化的免疫细胞创新药物,实现对原位乳腺癌、黑色素瘤等肿瘤的精准瘤内药物释放。该策略有效避免了细菌药物大量暴露所带来的安全隐患。然而,如何实现巨噬细胞对装载细菌在瘤内的可控释放,以及阐明此类一体化细胞药物的抗癌机制,仍是当前面临的关键挑战。 近日,南京大学华子春教授、吴乐阳研究员联合南京大学附属鼓楼医院徐运教授,在 Cell Reports上发表了题为“Controlled pyroptosis of engineered macrophages enables biphasic antitumor via the release of oncolytic bacteria and inflammatory signals”的研究论文。该研究创新性地构建了一种热诱导巨噬细胞自溶解系统,并据此开发了用于肿瘤治疗的“巨噬细胞-微生物封装炸弹”(MME-Bomb)。MME-Bomb 是一种装载吲哚菁绿纳米颗粒与新型减毒沙门氏菌株的工程化巨噬细胞载体,能通过光控技术精确调控抗肿瘤反应,为临床精准免疫治疗的设计提供了新的技术路径。 
为构建热诱导自溶型巨噬细胞,研究团队首先设计了一套合成的热响应基因回路,该回路由热休克蛋白启动子(pHSP)与细胞焦亡效应蛋白 Gasdermin D 的 N 端结构域(GSDMD-N)组成。GSDMD-N 可诱导细胞膜穿孔,进而引起细胞焦亡性裂解与内容物释放。随后,研究人员在工程化巨噬细胞内共装载光敏剂吲哚菁绿(ICG)及耐热型减毒沙门氏菌株 DLV。在近红外光照射下,ICG 将光能转化为热能,触发巨噬细胞发生可控的焦亡并裂解,从而实现对其胞内细菌的精准、快速释放。 实验结果表明,基于该焦亡机制的细胞裂解使细菌释放效率提升8.3倍,同时伴随大量促炎细胞因子的迅速释放。瘤内释放的细菌能够快速增殖,并与急剧升高的促炎细胞因子协同作用,强力激活肿瘤局部免疫应答,最终实现了 MME-Bomb 的稳定、持久、精准抗癌。在多种临床前肿瘤模型中,MME-Bomb 均显著降低了小鼠的肿瘤负荷,并延长了荷瘤小鼠的生存周期。 总之,本研究成功开发了一种光热调控的一体化细胞抗癌(MME-Bomb)策略。单次注射 MME-Bomb 即可产生强大而持久的抗肿瘤疗效,有望突破传统细胞疗法的关键局限,为肿瘤治疗开辟具有转化潜力的新方向。 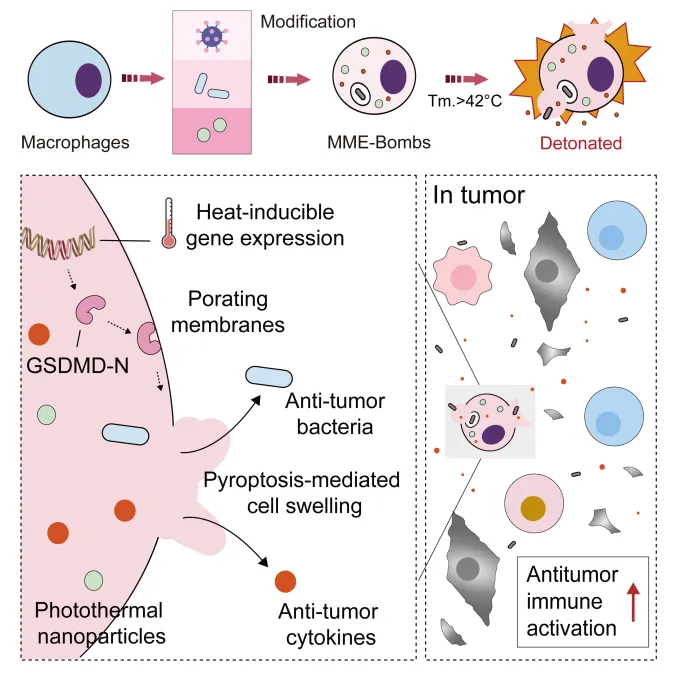
图1. 文章模式图
编辑丨Jesse
AutophagyAdvances


论文链接
https://www.sciencedirect.com/science/article/pii/S2211124725016900#abs0020
AutophagyAdvances
Autophagy Advances公众号是国内生命科学与自噬领域的高端学术公众号,集结了中科院、北大、清华、武大等众多高校学术骨干,旨在推广国内外生命科学及自噬领域学术交流与合作。
长按下方二维码,即可关注AutophagyAdvances
投稿邮箱:AutophagyAdv@163.com

本文来自网友投稿或网络内容,如有侵犯您的权益请联系我们删除,联系邮箱:wyl860211@qq.com 。
