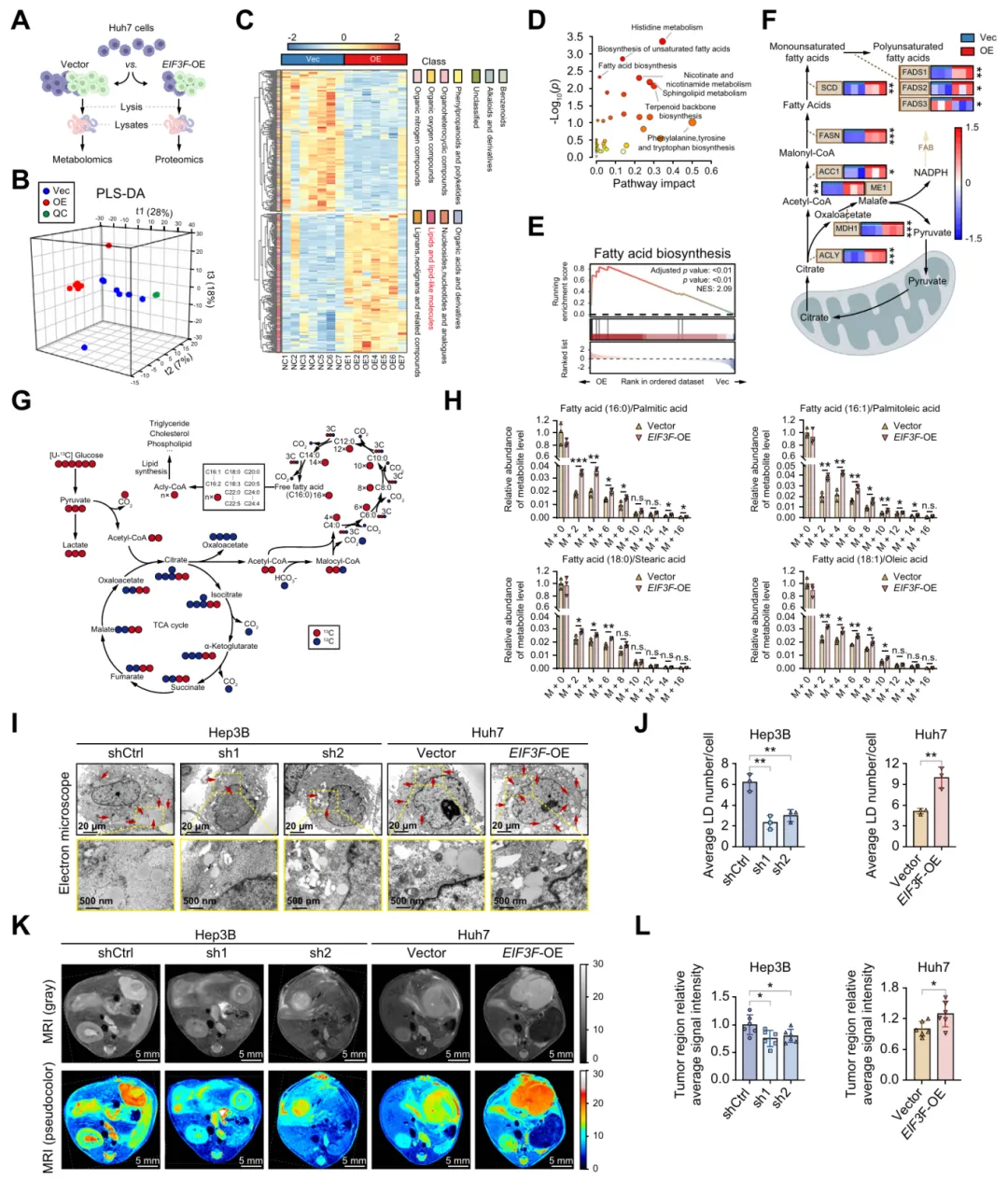
图3.eIF3f增强HCC中的脂肪酸合成和脂质积累
四、eIF3f特异性结合FAB关键因子——酰基辅酶A合成酶4(ACSL4)
通过多组学筛选证实 ACSL4 是 eIF3f 的关键靶蛋白,二者直接结合并定位于特定结构域,位点突变可破坏相互作用,介导 HCC 脂肪酸合成与恶性调控(图4)。
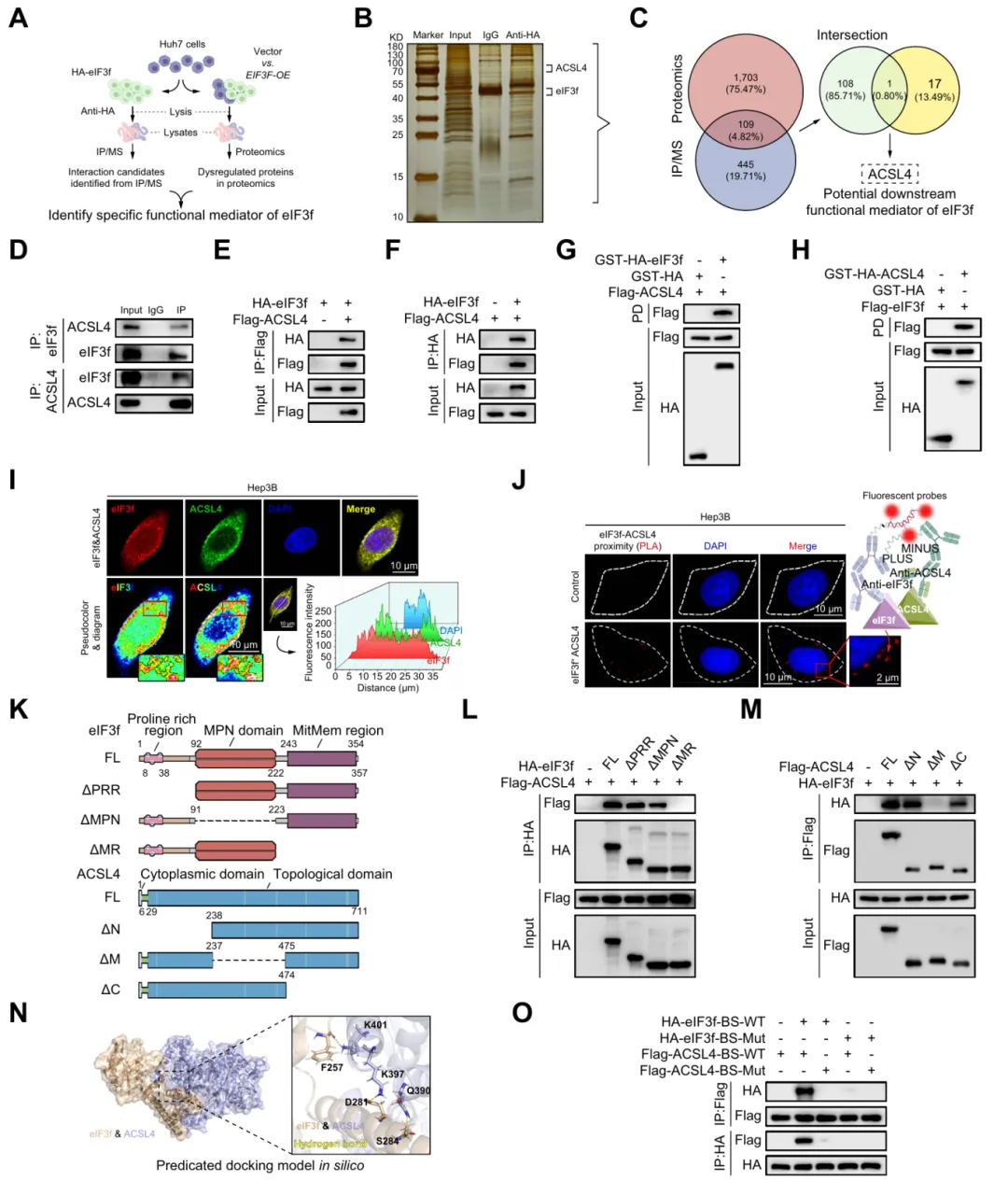
图4.eIF3f特异性结合脂肪酸合成关键因子ACSL4
五、eIF3f抑制K48连接的泛素介导的ACSL4蛋白酶体降解
研究证实 eIF3f 与 ACSL4 表达正相关,eIF3f 通过 MPN 结构域发挥去泛素化作用,在 K148 和 K536 位点稳定 ACSL4 蛋白,抑制其蛋白酶体降解(图5)。
图5.eIF3f抑制K48链接的泛素介导的ACSL4蛋白酶体降解
六、SRPK1介导的eIF3f Ser266磷酸化促进其与ACSL4的相互作用
实验证实 SRPK1 通过磷酸化 eIF3f 的 Ser266 位点,增强其与 ACSL4 的相互作用,该磷酸化修饰是二者结合的关键调控机制(图6)。
图6.SRPK1介导的eIF3f Ser266磷酸化促进其与ACSL4的相互作用
七、升高的eIF3f水平与HCC中CD8+ T细胞浸润减少相关
研究表明 eIF3f 可重塑 HCC 免疫微环境,敲低 eIF3f 能提升 CD8+ T 细胞浸润与杀伤功能,临床样本证实其与 ACSL4 正相关、与抗肿瘤免疫呈负相关(图7)。
图7.eIF3f水平升高与HCC中CD8+ T细胞浸润减少相关
八、靶向eIF3f可减少小鼠肿瘤负荷并增强抗PD-1活性
LNP‑siEif3f 联合抗 PD‑1 治疗肝癌,可显著抑制肿瘤生长、延长生存期,并增强 CD8+ T 细胞浸润与杀伤功能,为 HCC 免疫联合治疗提供新策略(图8)。
图8.靶向eIF3f可减轻小鼠肿瘤负荷并增强抗PD-1疗法的疗效