科研︱南京医科大学张展团队首次证实:长期日落黄暴露通过肠道微生物群促进小鼠对实验性结肠炎的易感性
- 2026-04-29 19:17:24
 点击蓝字“代谢组metabolome”,轻松关注不迷路
点击蓝字“代谢组metabolome”,轻松关注不迷路

生科云网址:https://www.bioincloud.tech/
编译:微科盟 Lili,编辑:微科盟X、江舜尧。
微科盟原创微文,欢迎转发转载。
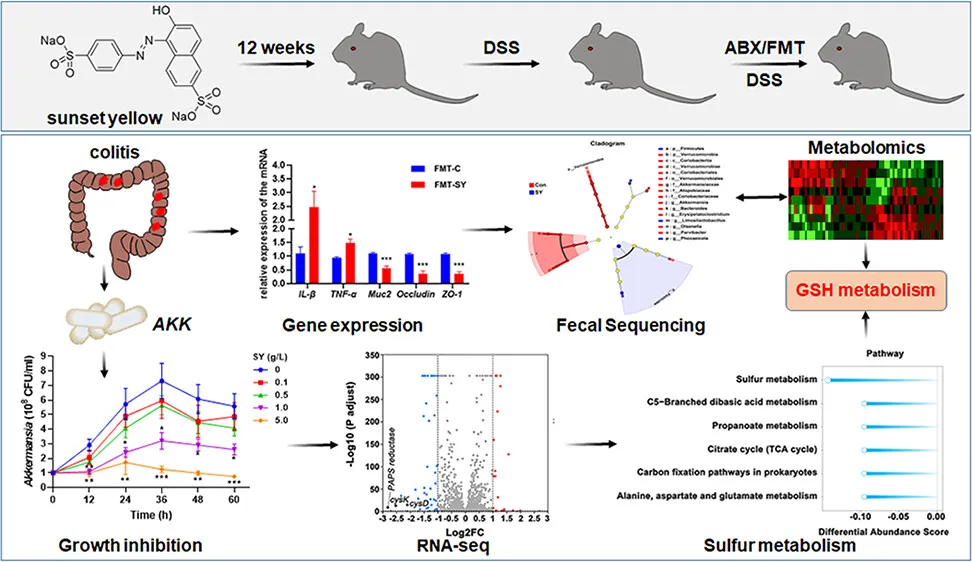
日落黄(Sunset Yellow, SY)是一种应用广泛的食品添加剂,但其对溃疡性结肠炎(UC)发生发展的影响尚不明确。本研究发现,SY暴露显著加重葡聚糖硫酸钠(DSS)诱导的小鼠UC表型,包括体重下降、疾病活动指数升高、组织学损伤、炎症反应增强、肠屏障功能受损、肠道菌群结构及硫代谢紊乱。粪便菌群移植实验进一步证实,SY暴露供体的菌群可重现性加剧受体小鼠的结肠炎程度。值得注意的是,SY在体内外均抑制嗜黏蛋白阿克曼菌(Akkermansia muciniphila, AKK)的生长。非靶向代谢组学显示,SY干扰谷胱甘肽(GSH)代谢,表现为正常及结肠炎小鼠体内GSH与氧化型谷胱甘肽(GSSG)水平同步降低。在AKK中,SY显著降低GSH含量,抑制谷胱甘肽S-转移酶活性,并扰乱硫代谢通路。补充GSH可显著逆转SY对AKK生长的抑制效应。综上,长期SY暴露通过依赖肠道菌群的GSH代谢失调促进小鼠实验性结肠炎的发生与发展。
论文ID
IF:6.2
DOI号:10.1021/acs.jafc.5c06410
实验设计
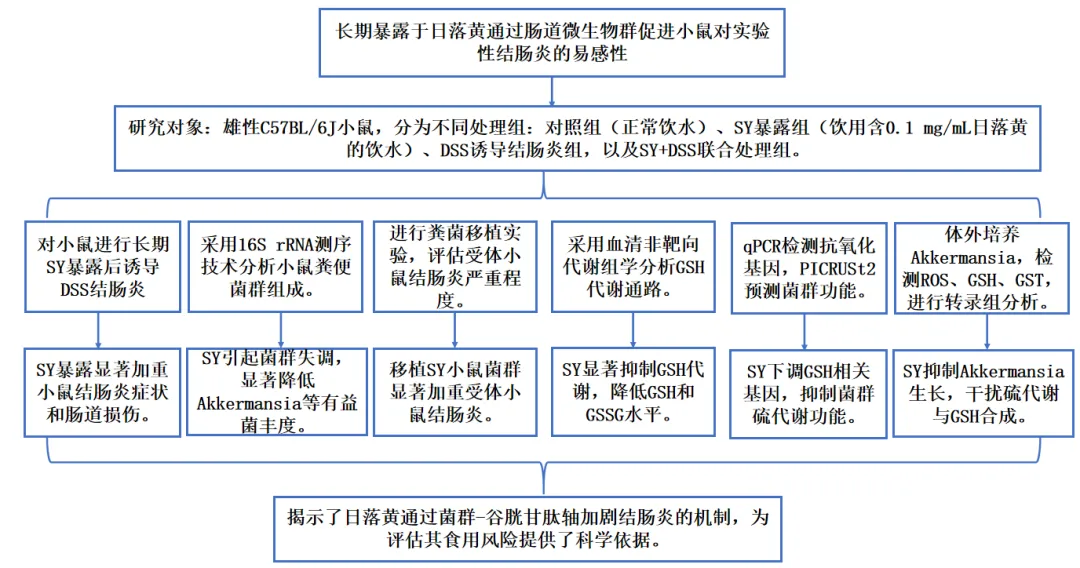
结果
1. SY暴露加重DSS诱导的小鼠结肠炎
为探究日落黄(SY)对结肠炎发展的影响,研究者对C57BL/6小鼠在整个实验期间持续饮用含SY(0.1 mg/mL)或不含SY的饮用水,并于最后一周给予2% DSS处理(图1A)。DSS组小鼠出现体重下降(P< 0.001),SY暴露组体重减轻更为显著(P< 0.001,图1B)。与单纯DSS组相比,SY+DSS组疾病活动指数(DAI)升高(P< 0.01),结肠长度显著缩短(P< 0.05,图1C、D)。组织学检查显示,SY+DSS组隐窝结构破坏加重,黏膜及黏膜下层免疫细胞浸润范围扩大,病理评分显著高于DSS组(P< 0.05,图1E)。此外,SY暴露显著抑制DSS结肠炎小鼠Muc2及ZO-1表达,进一步损害肠道黏液屏障(P< 0.05,图1F、G)。SY+DSS组结肠IL-1β和TNF-α水平显著升高(P< 0.01,图1H、I),且IL-1β、TNF-α表达均高于DSS组(P< 0.05,图1J、K),同时Muc2表达降低(P< 0.05,图1L)。
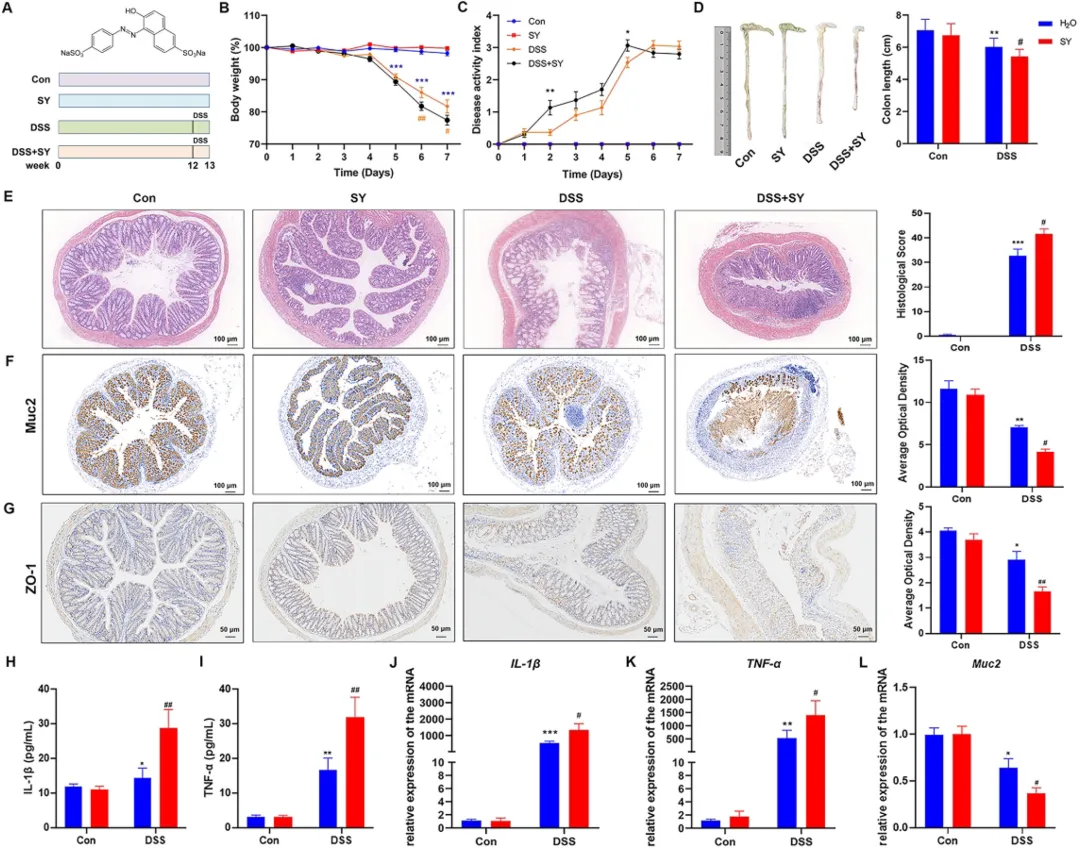
图1 SY暴露增加结肠炎易感性。(A) 实验设计示意图(n = 10)。(B) 体重变化以初始体重的均值变化表示。(C) 疾病活动指数(DAI)。(D) 结肠长度。(E) 结肠代表性HE染色及病理评分(n = 5),比例尺:100 μm。远端结肠组织免疫组化染色及平均光密度:(F)Muc2、(G)ZO-1,比例尺:100 μm(n = 5)。结肠组织中(H)IL-1β与(I)TNF-α水平。结肠组织中(J)IL-1β、(K)TNF-α及(L)MUC-2的mRNA表达(n = 10)。数据以均值±标准误表示,采用双因素方差分析结合Tukey多重比较。*P< 0.05,**P< 0.01,***P< 0.001 vs 对照组;#P< 0.05,##P< 0.01 vs 组内比较。
2. SY 改变肠道菌群结构并降低嗜黏蛋白阿克曼菌(AKK)丰度
随后,研究者探究肠道菌群是否介导SY 暴露加剧 C57BL/6 小鼠结肠炎易感性。与对照(Con)组相比,DSS 组(图 2A)与 SY 组(图 2B)的肠道健康指数(GMHI)均显著下降(P< 0.001),且 DSS+SY 组进一步降低(P< 0.001,图 2C)。同时,DSS 与 DSS+SY 组的微生物失调指数(MDI)显著升高(P< 0.001,图 2D),提示 SY 暴露负面影响了 UC 小鼠的肠道健康。尽管个体间差异显著,偏最小二乘判别分析(PLS-DA)显示四组粪便菌群明显分离(图 2E),表明菌群组成具有组间特异性。LEfSe 差异分析(图 2F、G)表明,SY 显著影响疣微菌门(Verrucomicrobia)、阿克曼菌科(Akkermansiaceae)及阿克曼菌属(Akkermansia)。值得注意的是,SY 组与 DSS 组中 AKK的相对丰度均显著低于对照组(图2H、I);DSS+SY 组肠杆菌属(Enterobacter)比例亦高于单纯 DSS 组(图 2J)。
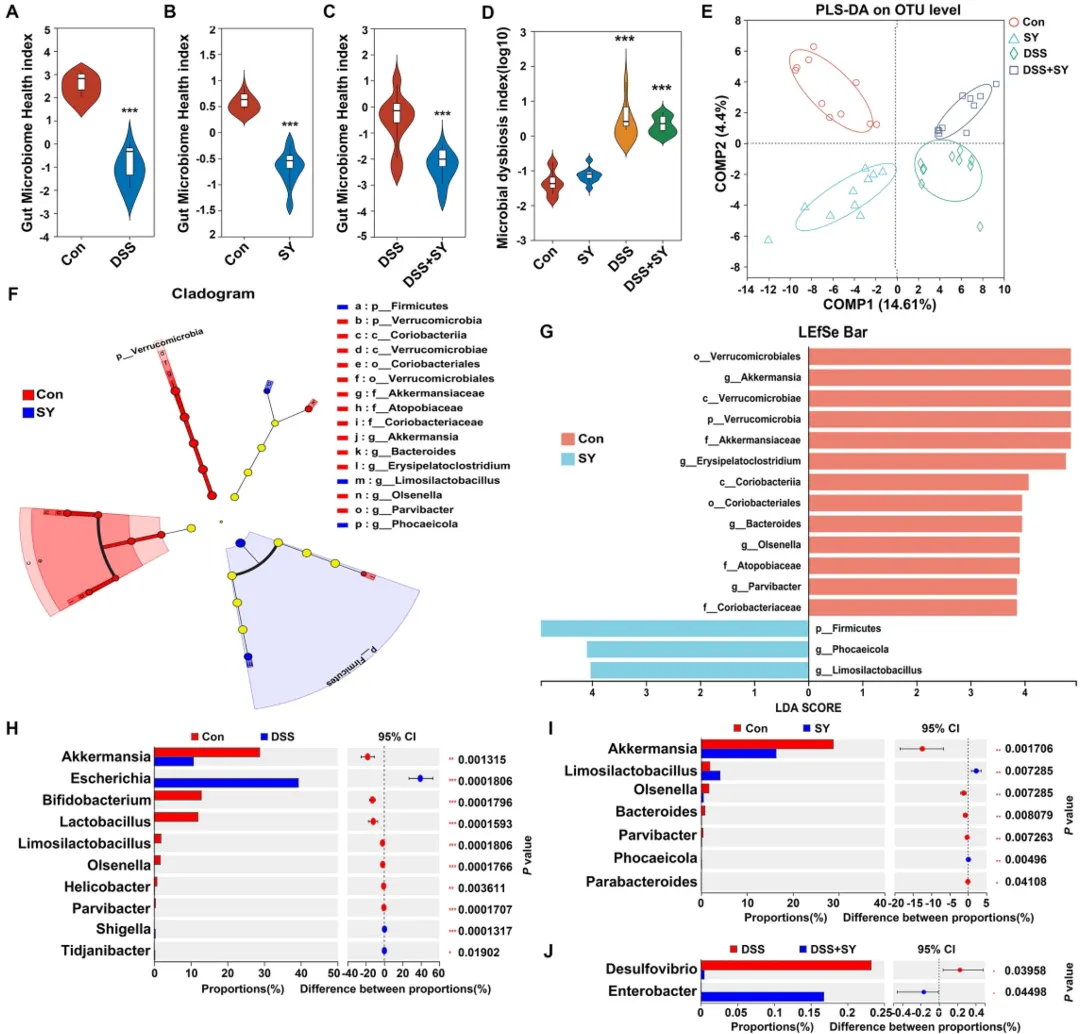
图2 日落黄暴露诱导肠道菌群组成与功能改变。(A) 正常小鼠经DSS处理后及(B) SY处理后肠道菌群健康指数(n=10)。(C) SY暴露的结肠炎小鼠肠道菌群健康指数。(D) 四组间微生物失调指数比较。(E) 基于OTU的偏最小二乘判别分析(PLS-DA)得分图。(F) LEfSe分析分支图展示肠道菌群群落结构。(G) 线性判别分析(LDA)显示各组在属水平显著富集的差异菌群。(H) 对照组与DSS组间属水平差异菌比较;SY暴露后(I)正常状态及(J)结肠炎小鼠属水平差异菌比较。数据以均值±标准误表示,采用Wilcoxon秩和检验分析;***P< 0.001 vs 对照组。
3. 肠道菌群介导日落黄暴露对小鼠结肠炎的加剧作用
菌群组成及代谢的改变已被证实可调控结肠炎易感性。因此,研究者推测日落黄(SY)诱导的肠道菌群失衡及其活性变化使SY处理小鼠更易患结肠炎。为验证肠道菌群的作用,开展了粪便菌群移植(FMT)实验(图3A)。与接受对照菌群(FMT-C)的小鼠相比,接受SY暴露供体菌群(FMT-SY)的小鼠结肠炎程度显著加重,表现为体重明显下降(P< 0.05)、疾病活动指数升高(P< 0.05)及结肠长度缩短(P< 0.05)(图3B–D)。组织学检查显示,FMT-SY组炎症细胞浸润增多、隐窝结构破坏加剧,病理评分显著升高(P< 0.05,图3E、F)。免疫组化染色表明,FMT-SY组Muc2表达较FMT-C组显著降低(P< 0.01,图3G、H)。FMT-SY组结肠组织IL-1β(P< 0.05)和TNF-α(P< 0.01)水平显著高于FMT-C组(图3I、J)。qPCR结果显示,FMT-SY组结肠IL-1β和TNF-αmRNA表达上调,而Muc2、Occludin及ZO-1 mRNA表达显著下调(P< 0.001,图3K)。蛋白水平亦证实,FMT-SY组Occludin和ZO-1表达降低,提示肠道屏障功能受损(图3L、M)。
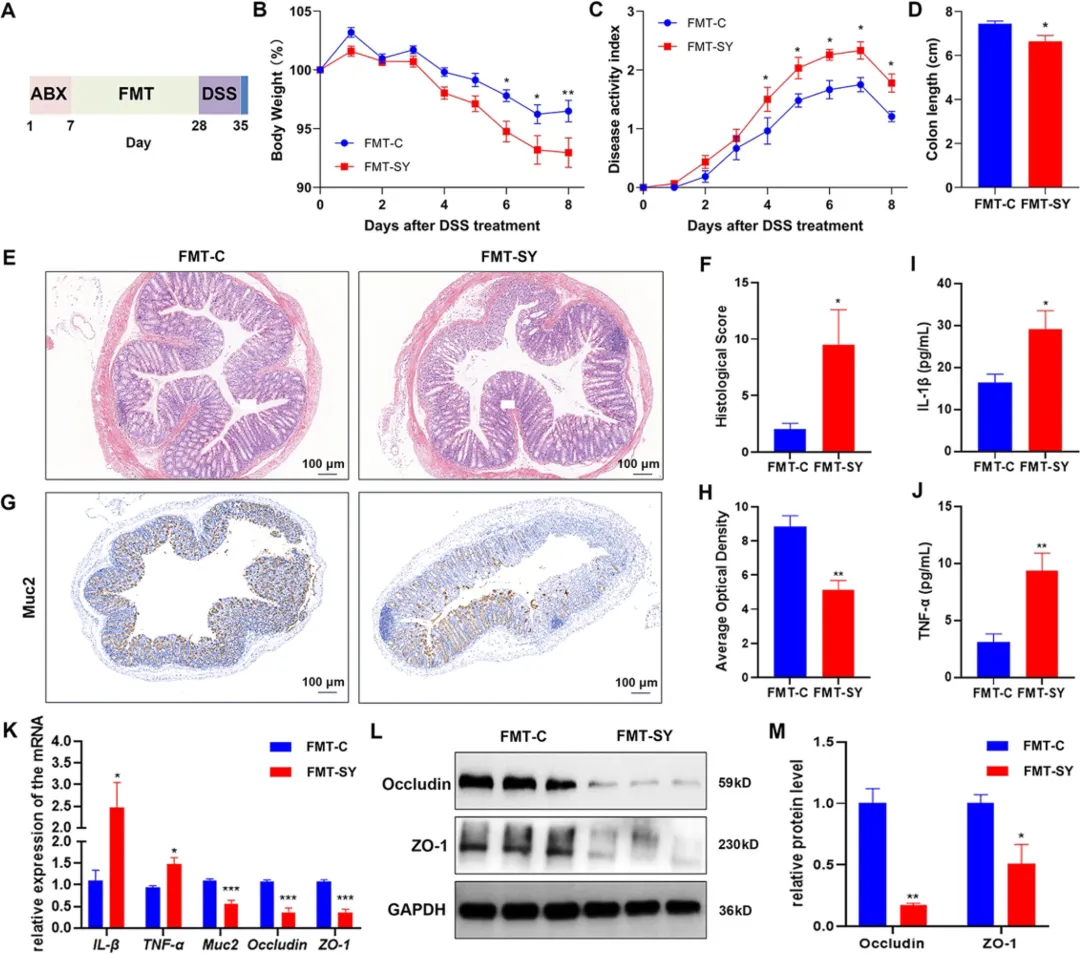
图3 肠道菌群介导日落黄处理小鼠结肠炎的加剧效应。(A) 实验设计示意图(n = 10)。(B) 体重变化:以初始体重为基线的体重改变。(C) 疾病活动指数。(D) 结肠长度。(E) 结肠代表性 HE 染色及 (F) 病理评分(n = 5),比例尺:100 μm。(G) 远端结肠 Muc2 免疫组化染色及 (H) 平均光密度,比例尺:100 μm。(I) 结肠组织 IL-1β 与 (J) TNF-α 含量。(K) 结肠组织中 IL-1β、TNF-α、MUC-2、Occludin及ZO-1的mRNA 表达水平。(L) Occludin、ZO-1 与 GAPDH 的 Western blot 代表性条带及 (M) 相对定量结果。数据以均值 ± 标准误表示,采用非配对双尾 t 检验进行分析;*P< 0.05,**P< 0.01,***P< 0.001 与对照组比较。
4. SY 暴露扰乱谷胱甘肽代谢
为阐明SY 暴露对相关分子机制的影响,研究者开展了血清代谢组学分析。PLS-DA 结果显示,无论是否给予 DSS 处理,小鼠血清代谢谱均出现显著分离(图 4A)。值得注意的是,SY 暴露小鼠的谷胱甘肽(GSH)代谢通路显著富集,该现象在 DSS 处理组(图 4C)与非 DSS 处理组(图 4B)中均可见。各组 GSH 及其氧化型谷胱甘肽(GSSG)水平均显著下调(P< 0.05,图 4D、E)。
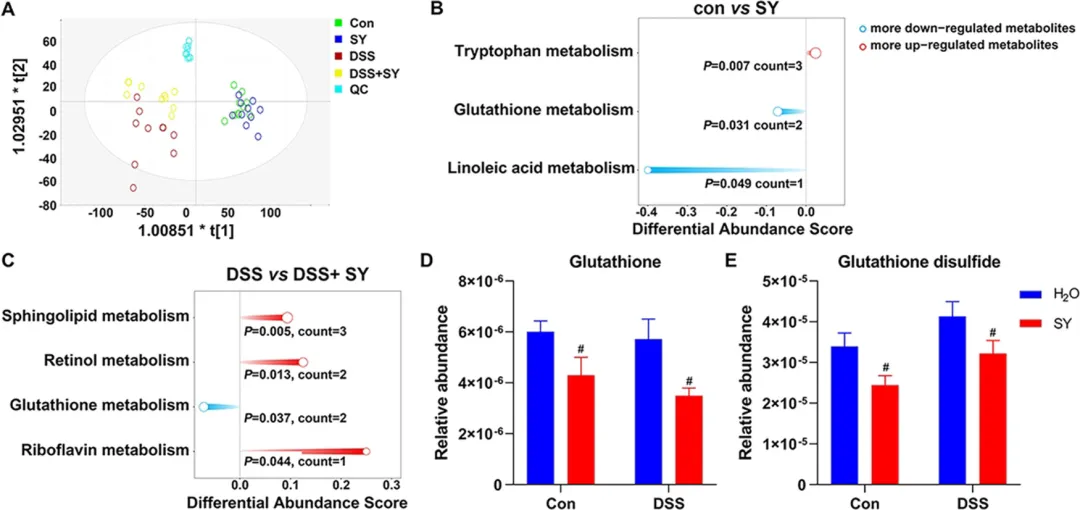
图4 日落黄暴露干扰谷胱甘肽代谢。(A) 各组血清代谢组学PLS-DA得分图(n = 10)。(B) 正常小鼠SY暴露与否的差异代谢物通路分析。(C) 结肠炎小鼠SY暴露与否的差异代谢物通路分析。血清中(D)谷胱甘肽(GSH)与(E)氧化型谷胱甘肽(GSSG)的相对丰度。数据以均值±标准误表示,采用双因素方差分析结合Tukey多重比较及非配对双尾t检验;#P< 0.05,与组内对照比较。
5. SY 暴露调控 GSH 相关基因及肠道菌群功能
结肠组织中谷胱甘肽过氧化物酶(GSH-Px)、谷胱甘肽 S-转移酶(GST)、过氧化氢酶(CAT)与环氧合酶-2(COX2)的蛋白表达在 SY 暴露后均显著下调(P< 0.05,图 5A–D)。粪菌移植实验进一步显示,接受SY 菌群(FMT-SY)的小鼠结肠内 GSH-Px、GST、CAT 和 COX2 的 mRNA 水平亦显著降低(P< 0.05,图 5E–H)。Mantel 检验表明,对照与 SY 组间差异菌属与差异代谢物显著相关,其中AKK 相对丰度与 GSH 水平呈正相关(图 5I)。PICRUSt2 功能预测分析显示,无论是否合并 DSS 处理,SY 暴露均显著抑制小鼠肠道菌群的硫代谢通路(P< 0.001,图 5J)。上述结果提示,SY 通过调控宿主 GSH 相关基因及干预肠道菌群功能,协同破坏机体谷胱甘肽代谢稳态。
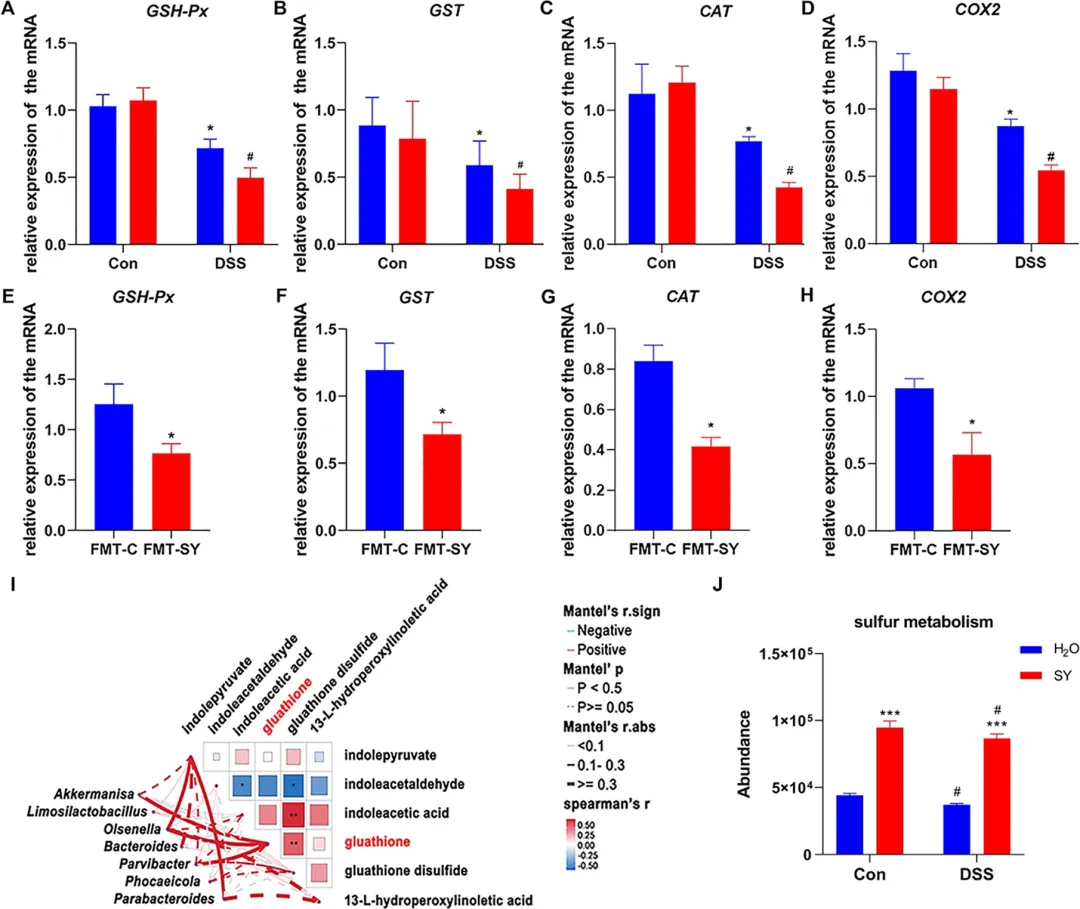
图5 日落黄暴露对GSH相关基因及肠道菌群功能的影响。(A–D) 慢性SY暴露小鼠结肠组织中GSH-px、GST、CAT与COX2的mRNA表达水平(n= 10)。(E–H) 粪便菌群移植处理后小鼠结肠组织中GSH-px、GST、CAT与COX2的mRNA表达水平(n= 10)。(I) 对照组与SY组间差异菌属与谷胱甘肽代谢通路差异代谢物的Mantel检验结果。(J) 基于PICRUSt 2.0预测的硫代谢通路丰度(n= 10)。数据以均值±标准误表示,采用非配对双尾t检验及双因素方差分析结合Tukey多重比较;*P< 0.05,***P< 0.001 vs 对照组;#P< 0.05 vs 组内对照。
6. SY 通过干扰谷胱甘肽代谢抑制 AKK 生长
体外培养实验进一步阐明SY 对嗜黏蛋白阿克曼菌(AKK)的影响。随SY 剂量升高,AKK 活菌数呈剂量依赖性下降(P< 0.05,图 6A);SY 暴露显著升高菌内活性氧(ROS)水平(P< 0.001,图 6B),降低 GSH 含量,并抑制谷胱甘肽 S-转移酶(GST)活性(P< 0.05,图 6C、D)。RNA-seq 分析显示,SY 处理共导致 64 个差异表达基因(DEGs),其中19 个上调、45 个下调(图 6E);3'-磷酸腺苷-5'-磷酰硫酸(PAPS)还原酶、半胱氨酸激酶(CysK)及半胱氨酸合酶(CysD)等硫代谢关键基因表达显著下调(图 6F)。GO 富集分析表明,DEGs 主要富集于硫及硫酸根相关生物过程(图 6G),硫代谢通路为 SY 干预后最显著富集的 KEGG 通路(图6H)。值得注意的是,外源补充 GSH 可显著逆转 SY 对 AKK 的生长抑制(P< 0.001,图 6I)。
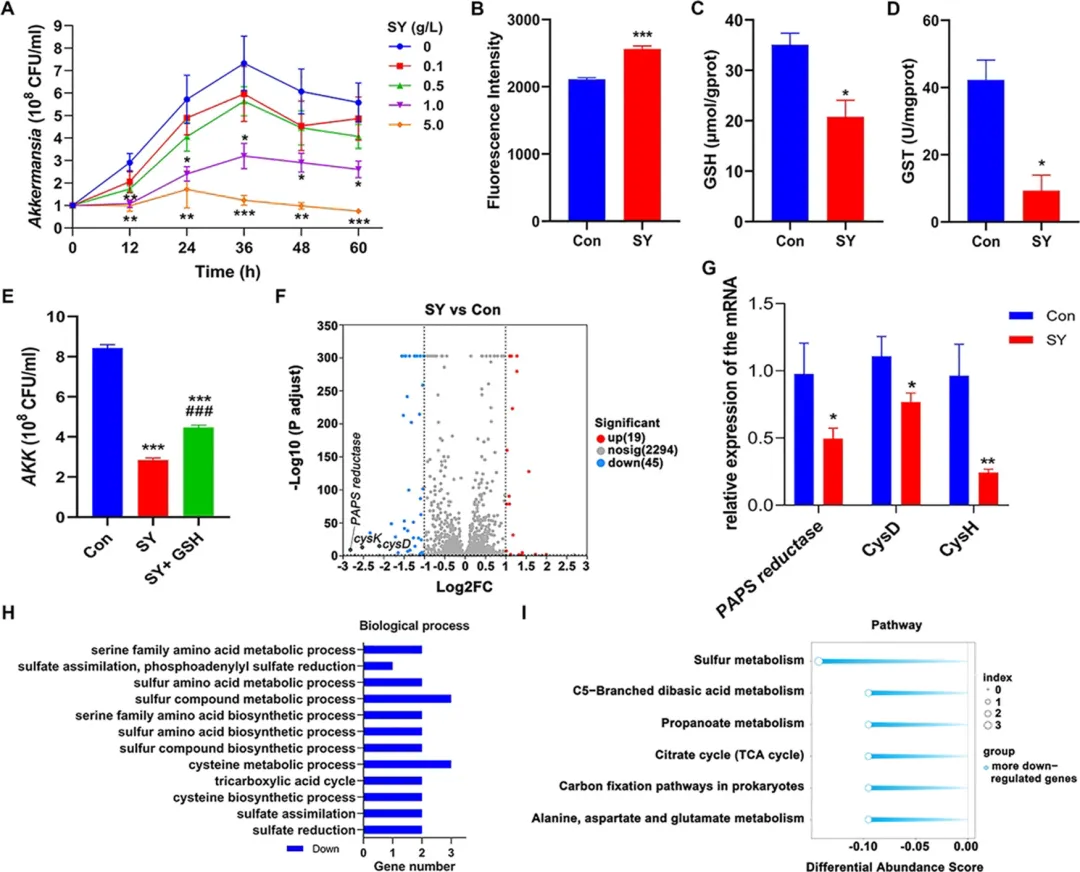
图6 日落黄通过干扰谷胱甘肽代谢抑制嗜黏蛋白阿克曼菌(AKK)生长。(A) SY对AKK生长的抑制效应(n = 5)。(B) SY暴露后AKK内活性氧(ROS)水平。(C) 谷胱甘肽(GSH)含量。(D) 谷胱甘肽S-转移酶(GST)活性。(E) 外源GSH补充逆转SY诱导的AKK生长抑制。(F) 差异表达基因(DEGs)数量统计。(G) AKK中3'-磷酸腺苷-5'-磷酰硫酸还原酶(PAPS reductase)、半胱氨酸激酶(CysK)及半胱氨酸合酶(CysD)的mRNA表达水平。(H) DEGs显著富集的Gene Ontology(GO)生物过程条目。(I) DEGs的KEGG通路富集分析。数据以均值±标准误表示,采用双因素方差分析结合Tukey多重比较或非配对双尾t检验;*P< 0.05,**P< 0.01,***P< 0.001 vs 对照组;###P< 0.001 vs 组内对照。
讨论
自19世纪以来,饮食结构与生活方式的转变推动加工食品消费量持续攀升,同期炎症性肠病(IBD)发病率亦呈上升趋势;至20世纪后期,IBD的患病率和发生率均已显著升高。人类每日经饮食暴露于多种化学物,而儿童膳食中尤为富含可提升食品视觉吸引力的合成色素。尽管与慢性疾病相关的饮食危险因素已被广泛识别,食用色素在IBD发病机制中的作用仍缺乏系统认知。本研究首次证实,在健康状态下,广泛应用的合成色素日落黄(SY)可通过改变肠道菌群组成与功能,显著提高小鼠对结肠炎的易感性。
虽然IBD的确切病因尚未阐明,但菌群组成及功能失衡已被公认为增加IBB易感性的关键因素。本研究显示,SY暴露不仅加重DSS诱导的结肠炎症,还导致菌群失调,表现为肠道菌群健康指数(GMHI)下降及菌群失调指数(MDI)升高。粪便菌群移植(FMT)是重建肠道菌群的有效手段;无菌小鼠接受经阿斯巴甜或甜菊糖处理的肥胖供体菌群后,体重、体脂增加且糖耐量受损。因此,研究者通过FMT实验验证菌群在SY触发溃疡性结肠炎(UC)中的介导作用:接受SY暴露供体菌群的小鼠DSS结肠炎进一步恶化,证实菌群介导了SY的促炎效应,与近期关于食品添加剂-菌群互作的研究结果一致。与既往报道相符,DSS诱导的结肠炎小鼠埃希氏-志贺菌属(Escherichia-Shigella)丰度显著升高;SY还提高肠杆菌属(Enterobacter)相对丰度,该菌属在结直肠癌患者中存在过度富集。尤为重要的是,SY与DSS均导致嗜黏蛋白阿克曼菌(AKK)显著耗竭,这一现象与常见食品添加剂报道的菌群失调效应相似。AKK作为定植于肠道黏液层的有益菌,已被确定为IBD治疗的潜在靶点。上述结果共同表明,肠道菌群介导了SY对DSS诱导结肠炎的加剧作用。
代谢组学技术为IBD患者代谢谱改变及代谢通路紊乱提供了充分证据。与既往研究一致,DSS诱导的结肠炎小鼠亦表现出与对照组显著不同的代谢特征。SY暴露分别于正常状态下干扰3条、于结肠炎状态下干扰4条代谢通路,其中谷胱甘肽(GSH)代谢为共同受累通路。GSH代谢在细胞氧化还原反应中发挥核心作用,不仅提供抗氧化防御,还参与调节人体及其他生物体的多种生理过程。本研究发现,SY暴露小鼠血清中GSH及其氧化型谷胱甘肽(GSSG)浓度均显著降低。作为细胞内最丰富的抗氧化剂,GSH可中和活性氧(ROS)并限制其蓄积。细胞内GSH水平通过GSH还原酶动态维持:该酶在氧化还原循环中将GSSG还原为GSH;而GSH-Px及谷氧还蛋白等抗氧化酶则在氧化解毒过程中促进GSSG生成。
高水平ROS可在氧化应激期间造成细胞损伤,并与UC病理过程密切相关。当GSH代谢受阻时,GSH不足无法有效抵御ROS损伤,导致肠道稳态失衡。为对抗ROS介导的组织损伤,机体内源性防御系统启用GSH-Px、GST、CAT及COX2等抗氧化酶。尽管食品添加剂通常被视为安全,且SY未表现出致突变或致癌作用,少数研究甚至报道其具有抗氧化及抗炎特性,本研究却发现SY暴露加剧上述抗氧化酶基因的上调,尤其在结肠炎小鼠中更为显著,提示SY可能增强氧化应激介导的结肠损伤。这种选择性调控提示,有必要在亚健康甚至病理状态下进一步评估食品添加剂的安全性。
嗜黏蛋白阿克曼菌(AKK)与肠道及代谢健康呈正相关;已有研究证实,AKK干预可缓解高脂高胆固醇饮食诱导的氧化应激,从而抑制肠道细胞凋亡。AKK还能通过增加褪黑素合成并清除活性氧(ROS),减轻镉所致肠黏膜损伤。本研究发现,SY暴露在体内外均抑制AKK生长,且SY处理后AKK相对丰度与血清GSH水平呈正相关。空间分辨代谢组学研究表明,口服AKK可显著改变小鼠GSH代谢并提高GSH浓度,进一步支持研究者的结果。SY显著干扰肠道菌群硫代谢,在AKK中尤为突出。
SY暴露可能大幅降低AKK胞内GSH含量,并下调参与硫代谢的3'-磷酸腺苷-5'-磷酰硫酸(PAPS)还原酶、半胱氨酸激酶(CysK)及半胱氨酸合酶(CysD)表达,提示硫同化过程受损。由于半胱氨酸的可利用性是GSH生物合成的主要限速因素,硫代谢受阻将直接限制GSH生成。值得注意的是,外源补充GSH可显著逆转SY对AKK生长的抑制作用,表明SY通过破坏硫代谢诱发氧化应激,进而抑制AKK增殖。
本研究首次证实,长期SY暴露增加小鼠对DSS诱导结肠炎的易感性。SY的不良效应由肠道菌群介导,具体表现为AKK丰度降低及硫代谢紊乱;其通过破坏GSH代谢加剧肠道炎症。然而,研究仍存在局限:所用剂量未必完全反映日常平均人群暴露水平,亟需开展基于人群的流行病学研究,包括IBD患者,以明确合成色素摄入与结肠炎发生的关联。鉴于膳食产品常含多种色素,探讨不同着色剂间相互作用对结肠炎易感性的影响亦具有重要意义。随着菌群失调与IBD关系研究的深入,饮食因素已成为公共卫生关注焦点;本研究为阐明SY在结肠炎中的作用奠定基础,并为评估其他食用色素对IBD发病机制的影响提供了新思路。
----------微科盟精彩文章----------
江苏省中医沈洪发文揭示白芷多糖通过降低肠道菌源咪唑丙酸从而激活PPAR-γ信号改善结肠炎
Int J Biol Macromol :山药多糖通过调节肠道微生态和代谢紊乱改善溃疡性结肠炎
如果需要原文pdf,请扫描文末二维码



获取此文献原文PDF、申请加入学术群,联系您所添加的任一微科盟组学老师即可,如未添加过微科盟组学老师,请联系微生态老师9,无需重复添加。
请关注下方名片,了解更多代谢组学知识
