科研 | 南京中医药大学:黄芩提取物通过调节脂质过氧化和GPX4/ACSL4抑制铁死亡从而改善结肠炎
- 2026-05-17 15:48:22
 点击蓝字“代谢组metabolome”轻松关注不迷路
点击蓝字“代谢组metabolome”轻松关注不迷路

生科云网址:https://www.bioincloud.tech/
编译:微科盟 草重木雪,编辑:微科盟X、江舜尧。
微科盟原创微文,欢迎转发转载。
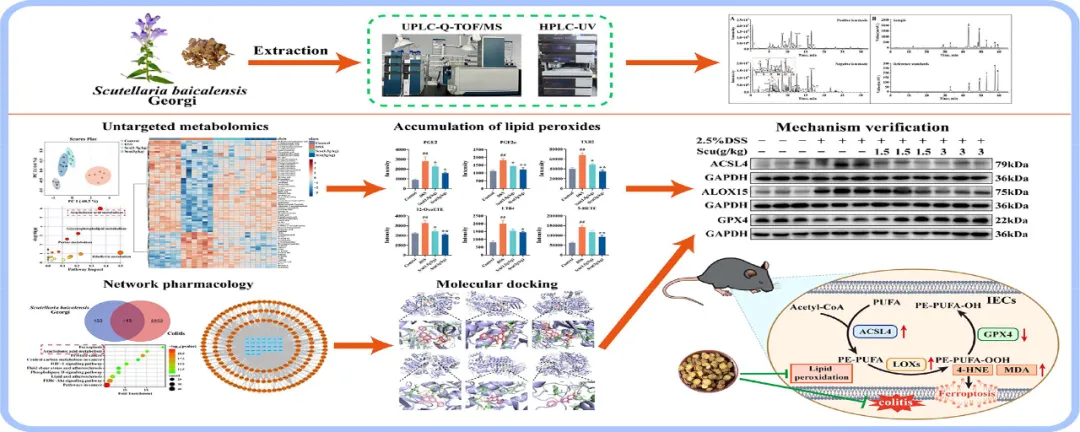
结肠上皮细胞铁死亡与溃疡性结肠炎(UC)的发展和随之而来的肠漏有关。黄芩(Scu)是一种广泛用于缓解UC的草药。本研究旨在阐明Scu通过抑制肠上皮细胞铁死亡对UC的治疗作用,并探讨其对脂质过氧化和GPX4/ACL4通路的调节机制。研究者采用UPLC-Q-TOF/MS分析草药提取物中的化学物质和Scu给药小鼠原型成分的结肠暴露情况;此外,研究者使用HPLC-UV对主要化合物进行了定量;在通过喂食右旋糖酐硫酸钠(DSS)建立的UC小鼠模型中全面探索了Scu的改善作用;基于HPLC-MS的代谢组学研究旨在鉴定Scu治疗UC小鼠结肠组织中的差异代谢物;网络药理学用于靶点预测和潜在通路分析。结合这些生物信息学分析,RT-qPCR、免疫荧光、免疫组织化学和免疫印迹用于阐明Scu在体内和体外模型中对铁死亡相关途径的调节机制。研究者对Scu中的78种化学成分进行了表征,其中42种在Scu小鼠的结肠组织中检测到。Scu可以缓解小鼠UC相关症状,包括结肠长度增加和病理评分降低。此外,Scu抑制了促炎细胞因子和介质,同时通过在mRNA和蛋白质水平上增加ZO-1和Occludin的表达来改善肠道屏障功能。基于代谢组学研究,共有71种差异代谢物在Scu给药后表现出逆转趋势。这些发现结合网络药理学的结果,表明花生四烯酸(AA)代谢和铁死亡可能是Scu干预UC的潜在途径。研究者进一步的实验表明,Scu对铁死亡的改善作用部分归因于其对脂质过氧化的调节及其对GPX4/ASCL4轴的调节作用,从而改善UC。当AA与Scu同时给药时,Scu对铁死亡、GPX4/ASCL4轴的调节作用及其对UC的保护作用显著降低。此外,当在体外敲除GPX4或过表达ACSL4时,Scu对铁死亡的抑制作用减弱。因此,Scu对UC的改善作用与调节脂质过氧化和GPX4/ASCL4介导的肠上皮铁死亡密切相关。
亮点:
1. 黄芩(Scu)对改善溃疡性结肠炎(UC)具有治疗作用;
2. 代谢组学和网络药理学研究表明,花生四烯酸代谢和铁死亡可能是Scu干预UC的潜在途径;
3. Scu通过调节多不饱和脂肪酸代谢和GPX4/ACL4轴来限制肠上皮铁死亡,从而发挥抗UC作用。
论文ID
实验设计
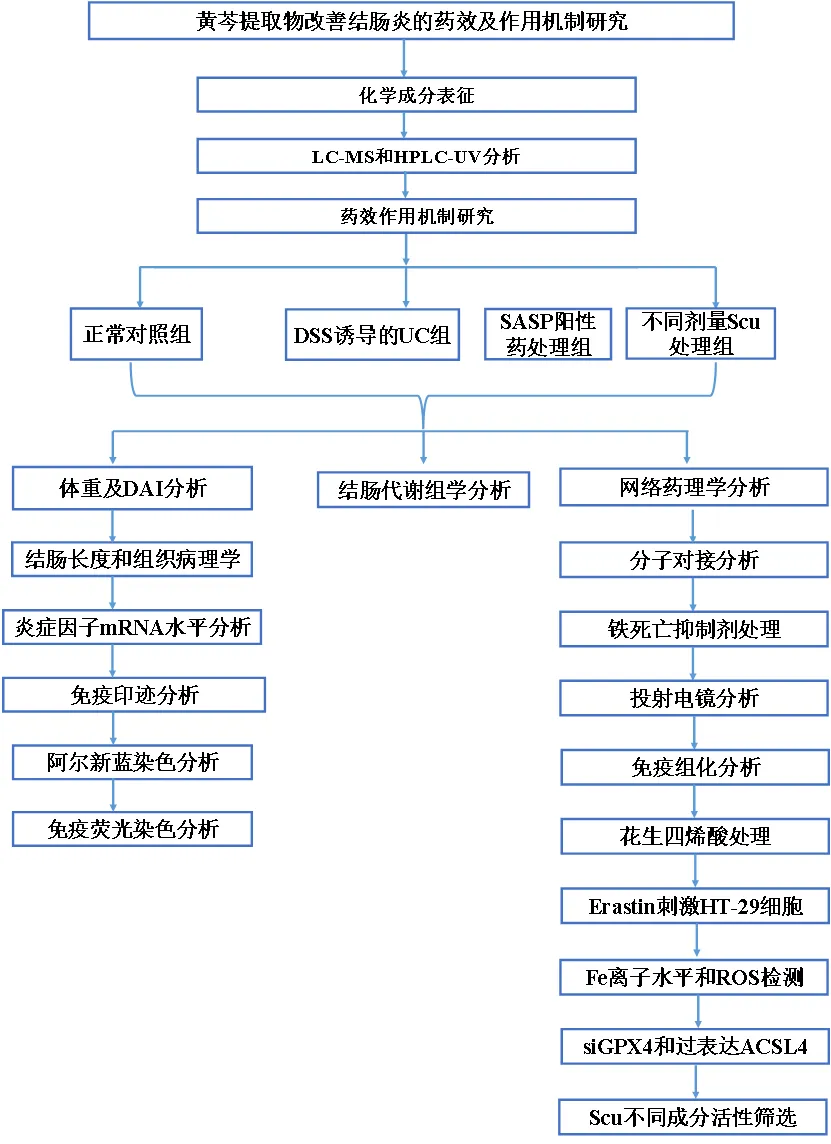
实验结果
1. 黄芩提取物的定性和定量分析
研究者通过高分辨率质谱对黄芩的化学成分进行了全面分析,最终,在黄芩提取物中鉴定出62种成分,主要由黄酮类和黄烷酮组成(图1A)。接下来,研究者通过验证的HPLC-UV方法对Scu的主要成分进行了定量分析。Scu提取物和标准品的色谱图见图1B,Scu提取物中这些成分的具体含量如表S2所示。野黄芩苷、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和木蝴蝶素A的含量分别为3.11、25.81、13.24、2.91、1.14和0.38mg/ml。
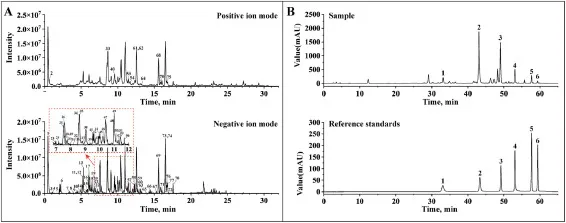
图1 Scu提取物的化学特征和主要成分的含量。(A)Scu提取物的总离子色谱图(TIC)。(B)Scu提取物和参考标准品的HPLC-UV色谱图。1,野黄芩苷;2,黄芩苷;3,汉黄芩苷;4,黄芩素;5,汉黄芩素;6,木蝴蝶素A。
2. Scu提取物改善溃疡性结肠炎相关症状
研究者建立UC模型和药物治疗概况的方法如图2A所示。同时,通过强饲法给予SASP(50mg/kg)和Scu(1.5g/kg、3g/kg)。数据表明,与DSS组相比,Scu显著逆转了小鼠的体重减轻(图2B),降低了DAI评分(图2C),增加了结肠长度(图2D,E)。在患有结肠炎的小鼠中,结肠组织表现出严重的病理损伤,其特征是绒毛结构畸形和隐窝破坏。然而,用Scu治疗后,这些症状明显缓解(图2F,G)。
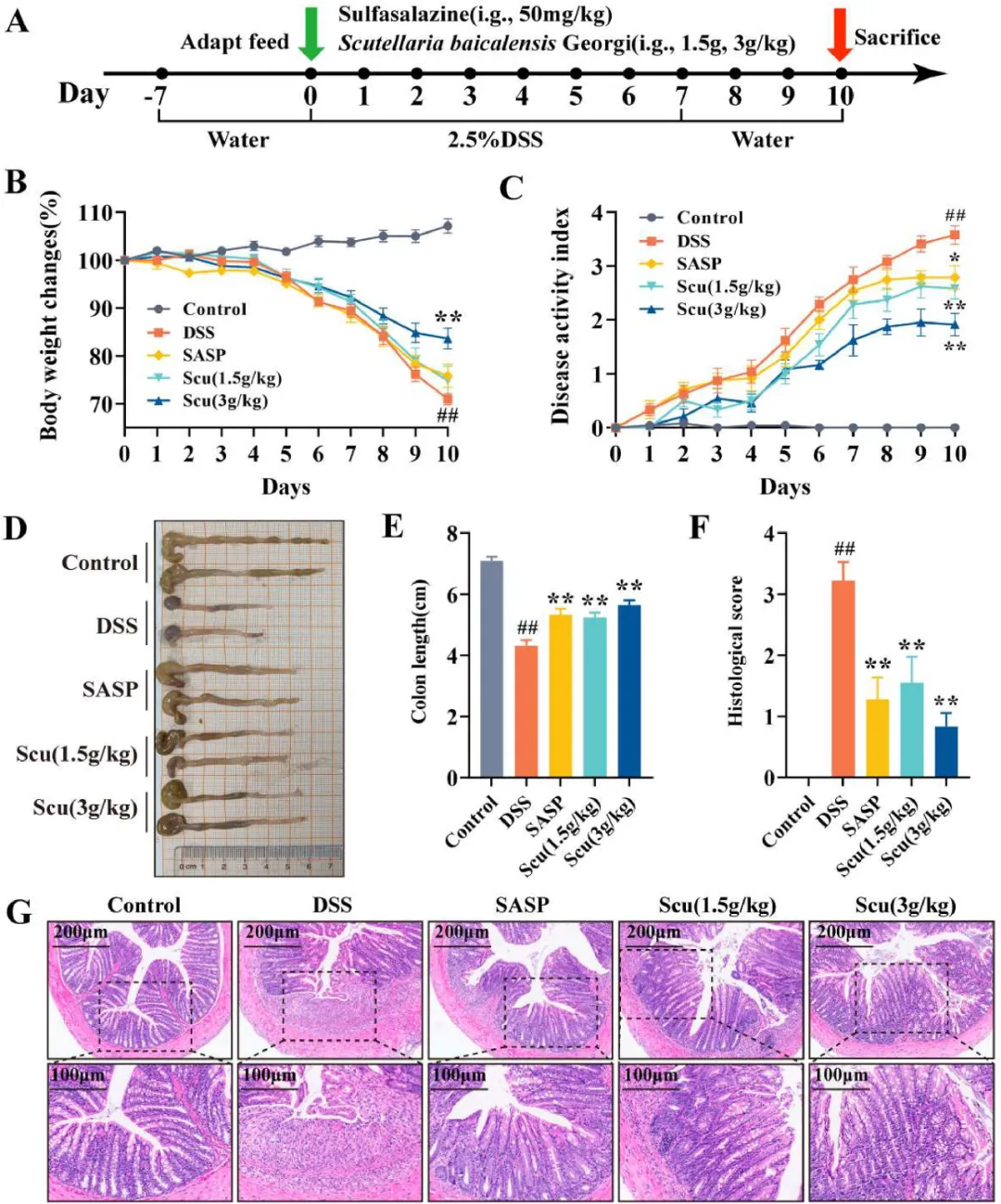
图2 改善DSS诱导的结肠炎小鼠的Scu(n=8)。(A)小鼠给予2.5%DSS 7天以建立UC模型,并分别用SASP(50mg/kg)和Scu(1.5g/kg,3g/kg)治疗。(B)小鼠体重的变化。(C)疾病活动指数(DAI)评分。(D)结肠组织的宏观图像。(E)结肠长度。(F)组织学评分。(G)结肠组织的典型H&E染色。结果以平均值±SEM表示。与对照组相比,##P<0.01;与DSS组相比,*P<0.05和**P<0.01。
此外,研究者还测定了IL-6、IL-1β和TNF-α的mRNA水平,以评估Scu的抗炎活性。在图3A-C中,与对照组相比,UC小鼠中这些细胞因子的mRNA水平明显升高。相比之下,这些细胞因子在Scu组中明显下调。研究者还评估了Scu对PTGS2和iNOS的蛋白表达和mRNA水平的影响(图3D-G)。DSS组PTGS2和iNOS的表达显著增加,经Scu处理后有所减少。总之,这些数据表明,Scu可以缓解UC的进展。
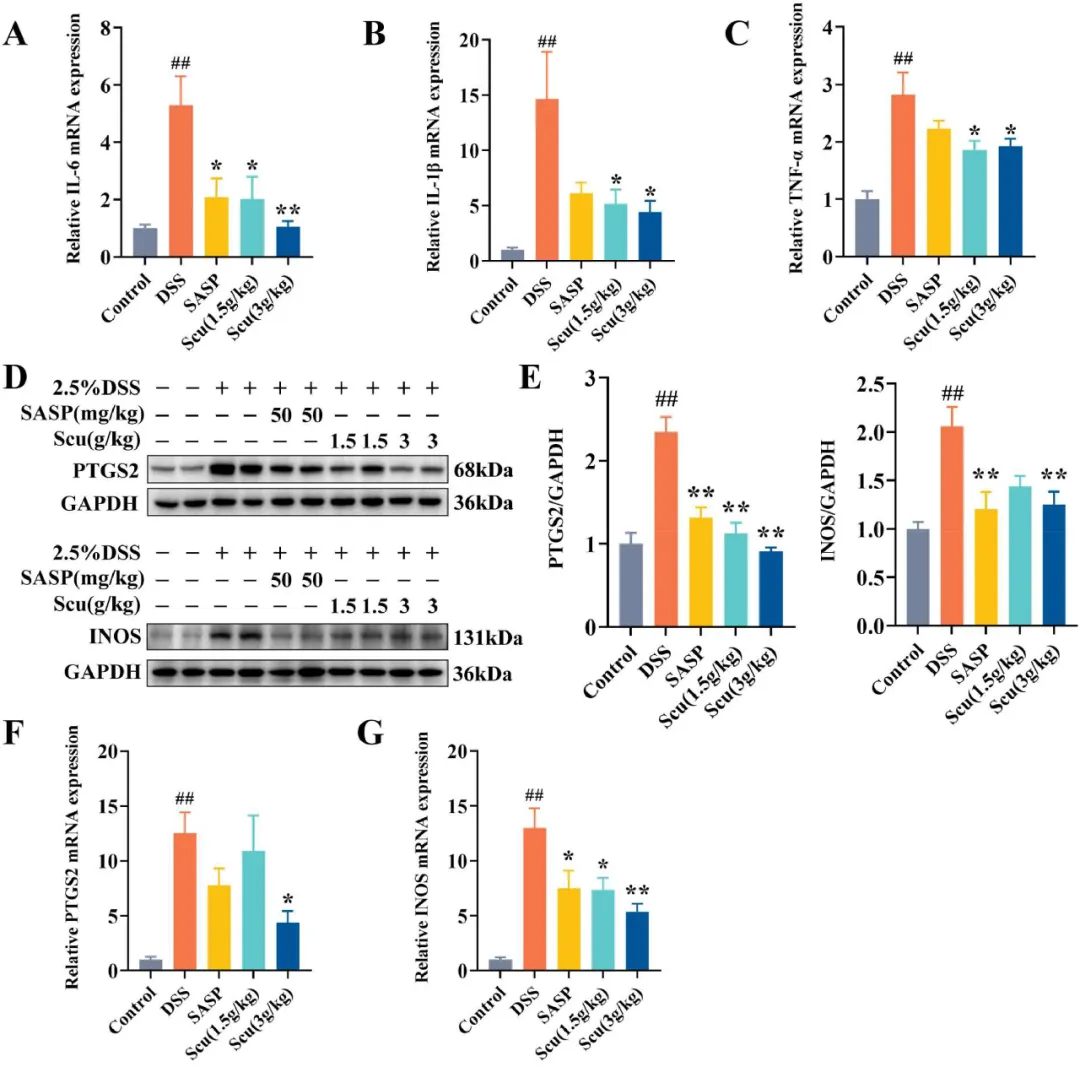
图3 Scu改善UC小鼠的结肠炎。(A-C)采用RT-qPCR检测结肠组织中IL-6、IL-1β和TNF-α的相对mRNA表达(n=6)。(D-E)免疫印迹检测结肠组织中iNOS和PTGS2的蛋白表达(n=3)。(F-G)采用RT-qPCR检测结肠组织中INOS和PTGS2的基因表达(n=6)。结果以平均值±SEM表示。与对照组相比,##P<0.01;与DSS组相比,*P<0.05和**P<0.01。
3. Scu提取物修复UC小鼠上皮损伤
由于Scu对UC小鼠结肠炎的改善潜力,研究者研究了Scu是否能有效恢复肠道屏障功能。研究者检测到UC小鼠中Occludin、ZO-1和MUC2的mRNA表达较低,Scu显著上调(图4A-C)。同样,Occludin的蛋白质表达也呈现出类似的趋势(图4D)。阿尔新蓝染色结果表明,UC小鼠杯状细胞显著减少,用Scu治疗后情况逆转(图4E)。此外,IF染色还证明DSS组中ZO-1和Occludin的表达降低,而Scu治疗组中这些蛋白质的表达基本得到改善(图4F)。总体而言,这些数据表明,Scu可以改善DSS受损的肠屏障完整性。
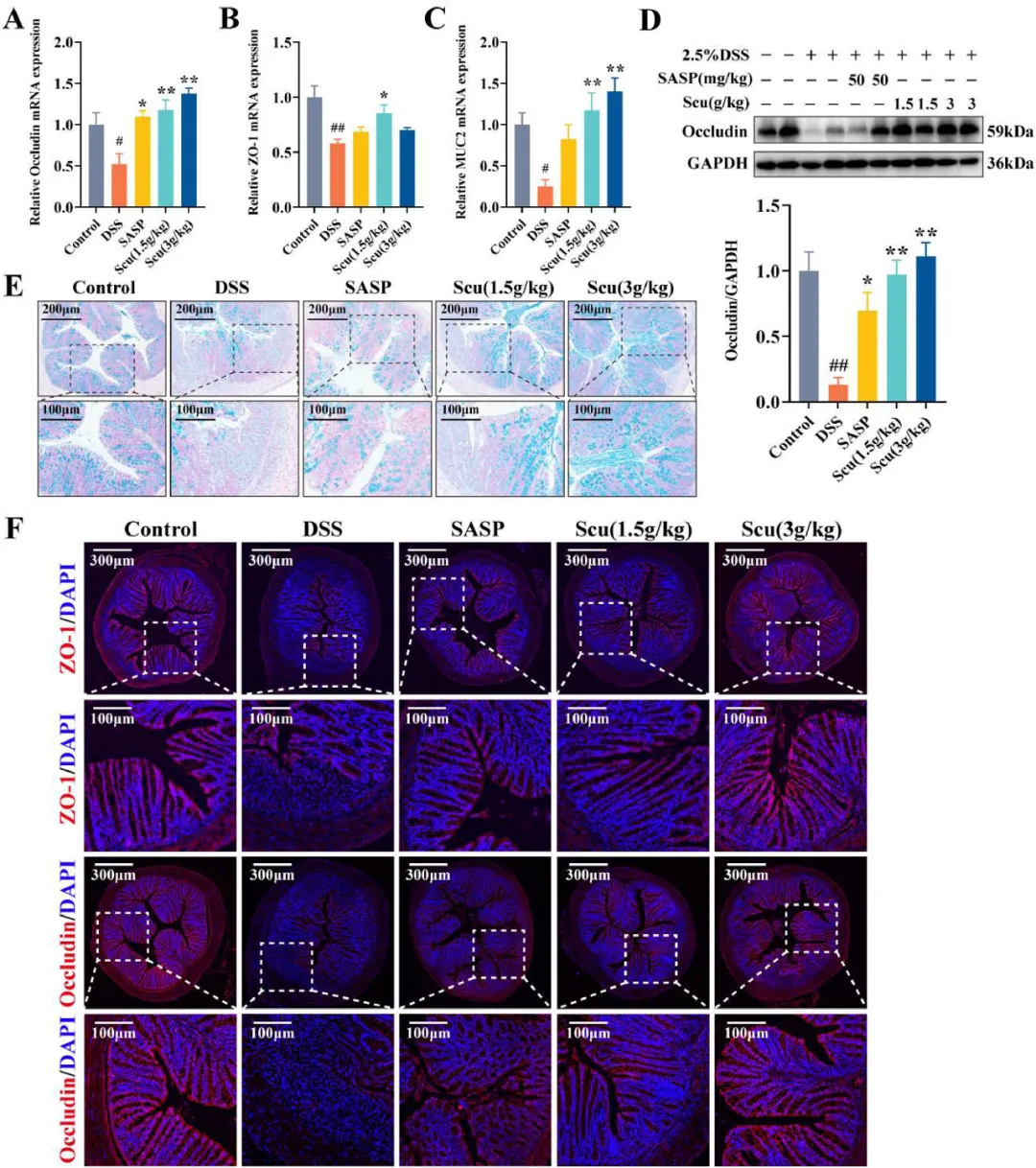
图4 Scu修复UC小鼠上皮损伤。(A-C)结肠组织中Occludin、ZO-1和MUC2的mRNA表达(n=6)。(D)不同组(n=3)结肠组织中Occludin的免疫印迹。(E)不同组别小鼠的结肠阿尔新蓝染色图像。(F)结肠组织切片中Occludin和ZO-1的免疫荧光组织化学染色。结果以平均值±SEM表示。与对照组相比,#P<0.05和##P<0.01;与DSS组相比,*P<0.05和**P<0.01。
4. Scu提取物调节UC小鼠PUFA代谢
为了进一步探索与UC相关的内源性代谢物的变化,研究者利用非靶向代谢组学技术来鉴定不同组中内源性代谢物的改变。研究者进行PCA以区分整体代谢物谱(图5A)。随后,热图分析提供了这些代谢物差异调节的直观表示,主要包括有机酸、氨基酸、核酸和脂质(图5B)。事实上,OPLS-DA模型中P值小于0.05和VIP值大于1被认为表明代谢生物标志物发生了显著变化。分析发现,对照组和DSS组中有38种代谢物发生了显著变化,其中大多数在Scu治疗后表现出显著的回归(表S4)。
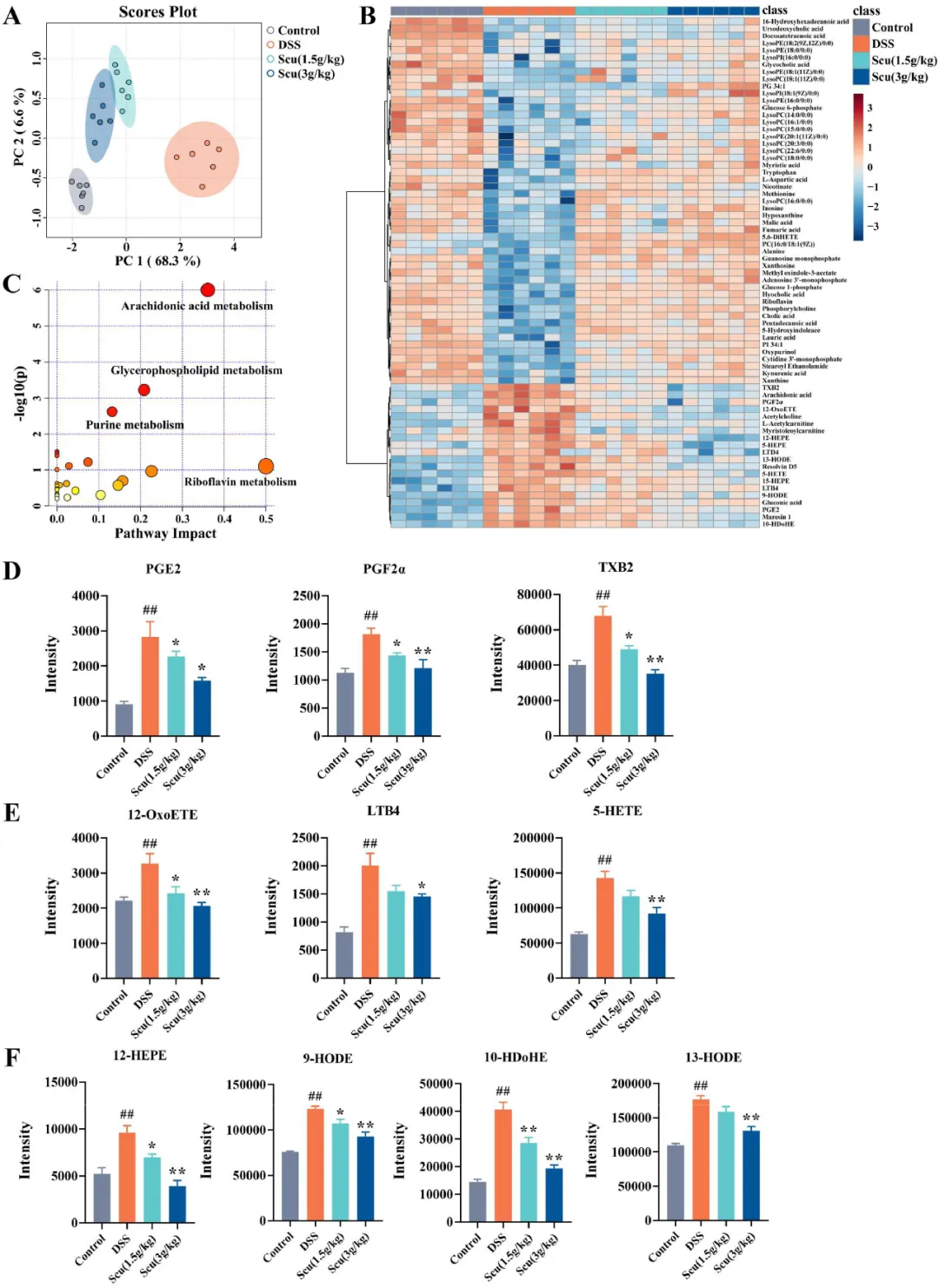
图5 小鼠结肠组织的代谢组学分析。(A)PCA分析。(B)代谢组学热图。(C)通路分析。(D)通过COX途径的AA代谢产物具有统计学意义。(E)通过LOX途径的AA代谢产物具有统计学意义。(F)其他脂质通过LOX途径的代谢产物具有统计学意义。结果以平均值±SEM表示。与对照组相比,##P<0.01;与DSS组相比,*P<0.05和**P<0.01。
研究者随后对上述代谢物进行了途径富集分析,以确定Scu调节的代谢途径。如图5C所示,花生四烯酸AA代谢和甘油磷脂代谢成为潜在的代谢途径。此外,PUFA代谢和甘油磷脂代谢紊乱,如AA代谢,被认为与脂质过氧化有关,而脂质过氧化与UC密切相关。
研究者分析了这些来源于AA的不同脂质过氧化物。与对照组相比,DSS组的PGE2、PGF2α和TXB2的EIC强度显著升高。在LOX途径的代谢产物中,DSS组的12-羟基二十碳四烯酸(12-OxoETE)、白三烯B4(LTB4)和5-羟过氧化二十碳四烯酸(5-HETE)的强度也显著升高。在Scu(1.5 g/kg,3 g/kg)组中,所有这些代谢物都显著降低(图5D,E)。此外,研究者通过LOX途径从其他脂质中提取的一些脂质过氧化物也表现出类似的趋势(图5F)。总之,研究者的研究表明,Scu主要通过调节UC小鼠结肠组织中PUFA的代谢来抑制脂质过氧化物的产生。
5. 网络药理学分析Scu与UC的潜在靶点和机制
网络药理学已被用于识别潜在的靶点和信号通路。因此,研究者利用这种方法来研究Scu是否可以调节UC中与脂质代谢和铁死亡相关的特定靶点。用Scu处理的小鼠结肠样本的BPC如图6A、6B所示。研究者在结肠组织中检测到42个原型成分(图6C),相关化学信息见表S5;从三个在线数据库中收集了276个与这些化合物相关的靶点和2395个与UC相关的靶点。Venn分析显示,143个潜在靶点与Scu对UC的改善作用有关(图6D)。在KEGG富集分析的前10条受显著影响的途径中,AA代谢与之前的代谢组学分析结果一致。通过AA代谢产生的脂质过氧化物最终会诱导细胞铁死亡(图6E)。在此之后,研究者使用Cytoscape 3.10.2软件将化合物靶点和与AA代谢或铁死亡相关的靶点转化成“化合物靶点”图,该图作为研究者分子对接分析的基础(图6F)。结合能低于-8千卡/摩尔通常被认为是强对接亲和力的指示。如图6G所示,小鼠结肠中来源于Scu的化合物与花生四烯酸代谢和铁死亡相关的蛋白质靶点表现出很强的亲和力,主要包括PTGS2、ACSL4、INOS2、AKR1C3和ALOX15。代表性化合物与蛋白质靶点分子对接的可视化结果如图6H所示。总的来说,这些发现与代谢组学结果的分析一致,表明Scu可能通过减少脂质过氧化来抑制铁死亡,从而改善UC。
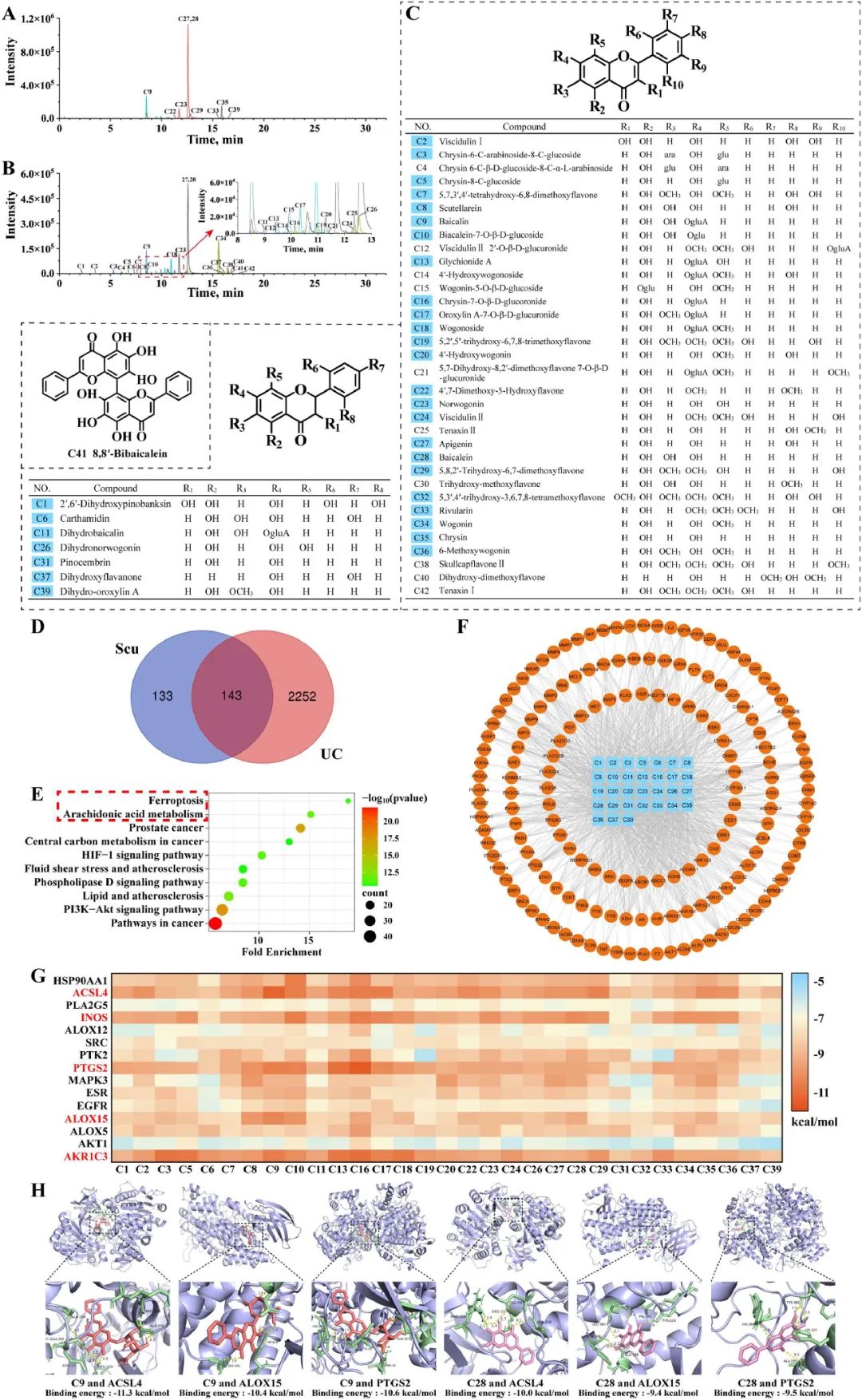
图6 可能分布在结肠组织中的Scu化合物的网络药理学分析。用Scu处理的小鼠结肠组织中原型化合物的正(A)和负(B)离子模式EIC。(C)已鉴定化合物的化学结构。(D)维恩图。(E)KEGG前10条通路的气泡图。(F)化合物靶向Scu网络。(G)结合能热图。(H)代表性化合物与蛋白质靶点的分子对接。
6.Scu抑制UC小鼠铁死亡并调节GPX4/ACL4轴
铁死亡的特征是铁诱导的脂质过氧化,与UC的发展有关。因此,研究者选择铁死亡抑制剂(Fer-1)作为阳性药物与Scu进行比较,进一步证实了Fer-1或Scu治疗可以缓解UC症状(图S1)。如图7A所示,与对照组相比,UC组的结肠SOD活性降低,但用Scu处理后,这一趋势明显逆转。MDA和4-HNE是两种主要的脂质过氧化类型,被认为是铁死亡的生物标志物。两者在UC小鼠中均显著增加,而在用Scu处理后呈下降趋势(图7B,C)。在透射电子显微镜下,DSS组的结肠上皮细胞显示线粒体体积减少和线粒体嵴消失,这被认为是细胞铁死亡的关键特征,这些线粒体损伤用Fer-1或Scu治疗修复(图7D)。此外,ACSL4和ALOX15的高表达水平增强了PUFA的氧化,可能导致与铁死亡相关的脂肪毒性。然而,研究发现Scu可以降低这些酶的表达。此外,蛋白质印迹分析和免疫组织化学显示,在对照处理的UC小鼠中,GPX4显著降低,而PTGS2显著增加(图7E、F)。用Scu处理后,上述实验中观察到的趋势显著逆转。总的来说,这些发现表明,Scu可能通过调节UC小鼠的脂质过氧化和GPX4/ACL4轴来限制肠上皮细胞铁死亡。
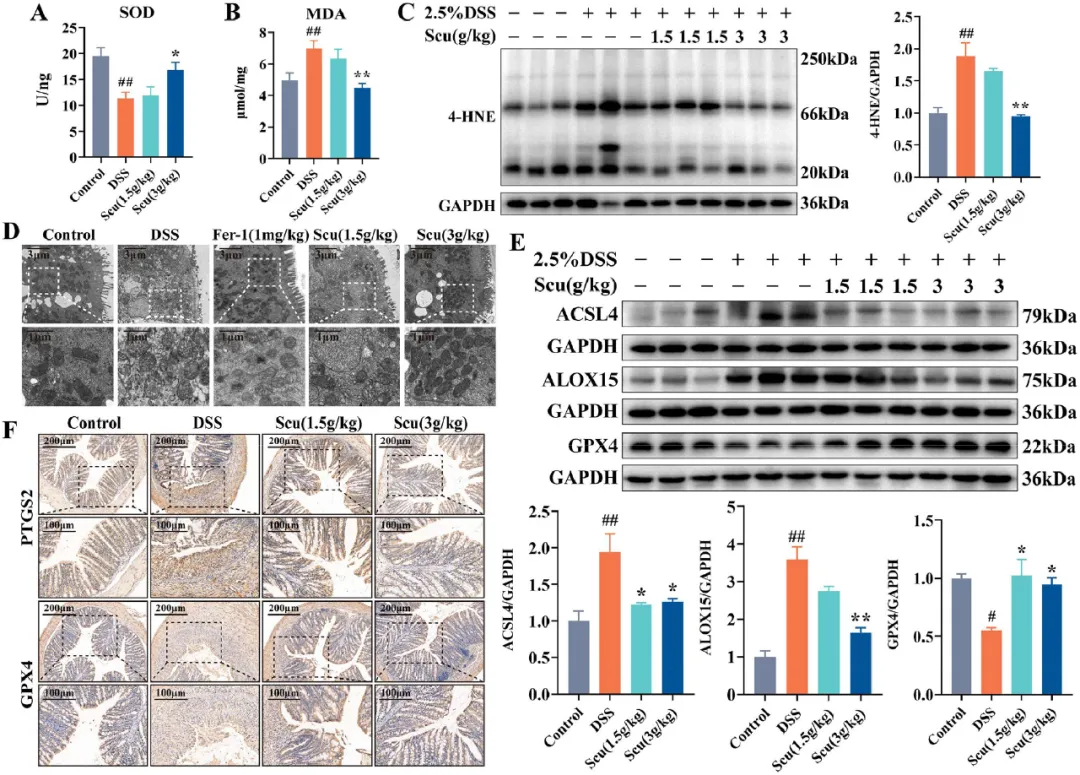
图7 Scu缓解DSS诱导的结肠炎小鼠结肠上皮细胞铁死亡,调节GPX4/ACL4轴。(A)SOD的水平。(B)MDA水平。(C)4-HNE修饰的蛋白质在不同UC治疗组中的分布。(D)结肠组织的代表性TEM图像。(E)ACSL4、ALOX15和GPX4的蛋白表达。(F)结肠中PTGS2和GPX4的代表性免疫组织化学图片。结果以平均值±SEM表示。与对照组相比,#P<0.05和##P<0.01;与DSS组相比,**P<0.05和**P<0.01。
7. 脂质过氧化物的增加削弱了Scu的疗效,加重了UC小鼠的铁死亡
研究者用AA、Scu或Scu+AA处理小鼠,以进一步研究补充AA的Scu对肠道炎症的影响(图8A)。结果显示,Scu+AA组的小鼠体重明显减轻(图8B),DAI评分较高(图8C)。同时,与仅用Scu处理相比,补充AA的结肠长度更短(图8D)。然后结肠的H&E染色显示Scu+AA组有严重的病理损伤,主要表现为绒毛结构畸形和炎性细胞浸润(图8E)。此外,与Scu组相比,Scu+AA组结肠组织中促炎细胞因子的表达增加(图8F)。然后,研究者对补充AA引起的铁死亡的易感性进行了研究。透射电镜观察到Scu+AA肠上皮细胞中存在完整的膜和线粒体嵴结构,这是铁死亡的典型特征(图8G)。随后,研究者检测了4-HNE和GPX4的蛋白表达,这两种蛋白是铁死亡相关的蛋白标志物。与Scu处理的小鼠相比,4-HNE偶联蛋白明显升高。Scu+AA组GPX4的表达显著降低(图8H,8I)。此外,与Scu组相比,免疫组织化学显示,Scu+AA组PTGS2呈上升趋势,GPX4呈下降趋势(图8J)。这些发现表明,脂质过氧化物的增加削弱了Scu的治疗效果,加重了UC小鼠的铁死亡。
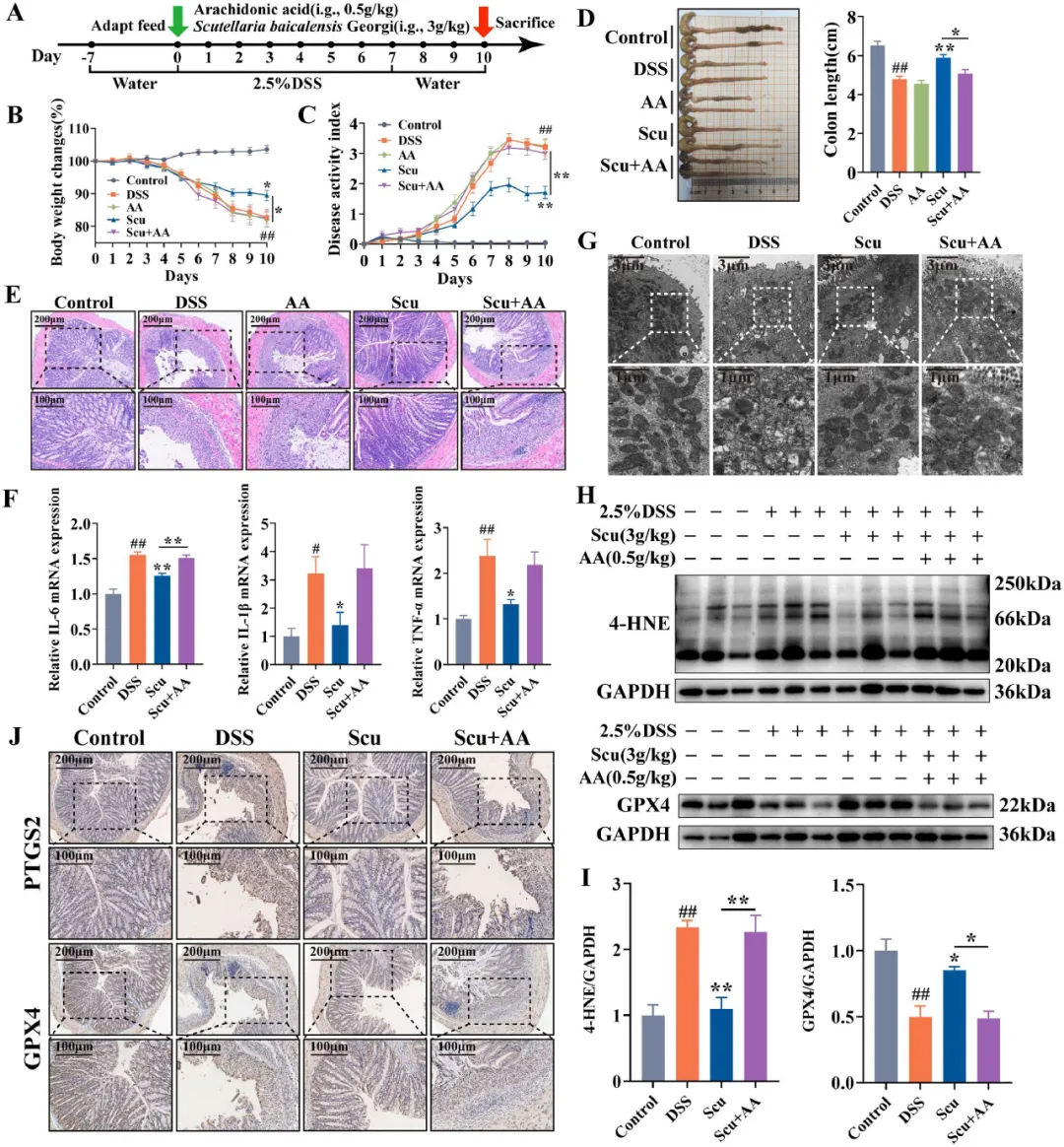
图8 脂质过氧化物的增加减弱了Scu的疗效,加重了UC小鼠的铁死亡。(A)建立UC模型和药物治疗的方法。(B)体重变化。(n=7-8)。(C)DAI得分。(D)结肠长度和结肠组织的宏观图片。(E)结肠的典型H&E图片。(F)通过RT-qPCR检测三种促炎细胞因子的相对mRNA表达。(G)结肠组织的代表性透射电子显微镜照片。(H-I)GPX4和4-HNE的蛋白表达。(J)结肠组织中PTGS2和GPX4的代表性免疫组织化学照片。结果以平均值±SEM表示。与对照组相比,#*P<0.05和**P<0.01;与DSS组相比,*P<0.05和**P<0.01。
8. Scu调节Erastin处理的HT-29细胞中GPX4/ACL4轴介导的铁死亡
最初,研究者在HT-29细胞中评估了不同浓度的Scu提取物和Scu衍生的一些成分,以确定最佳处理浓度(图S2)。随后,研究者用Erastin刺激HT-29细胞并用Scu处理,以研究其对铁死亡的影响。FerroOrange探针用于评估Erastin诱导的铁死亡细胞中显著升高的Fe2+水平。服用Scu后,Fe2+水平显著降低(图9A)。此外,研究者进行了MDA分析以评估脂质过氧化,这表明Scu处理显著逆转了Erastin诱导的MDA积累(图9B)。此外,经Erastin刺激后,GPX4的量显著减少,而ACSL4的量显著增加。然而,在Scu治疗后,蛋白质表达的这些趋势发生了实质性逆转(图9C、9D)。Erastin诱导的ROS水平升高被Scu处理抑制,绿色荧光减少证明了这一点(图9E)。随后,研究者对GPX4进行敲除和过表达ACSL4,以进一步研究。图S3和表S6详细展示了用于转染的实验试剂的效率,并选择了siGPX4-2进行后续实验。当GPX4被敲除并用Scu(100μg/mL)处理时,与仅用Erastin刺激的相比,Fe2+和ROS水平的相对含量没有显著差异。此外,研究者使用ACSL4过表达模型进行的类似研究显示了类似的趋势(图9F、9G)。研究者发现黄芩提取物中含量较高的成分,如黄芩苷、黄芩素、野黄芩苷和汉黄芩苷,可以降低Erastin引起的Fe2+含量升高(图9H)。因此,研究者提出这些黄酮类化合物是Scu中的关键生物活性化合物。总之,研究者的研究结果表明,Scu可能通过调节Erastin处理的HT-29细胞中的GPX4/ACL4轴来抑制铁死亡。
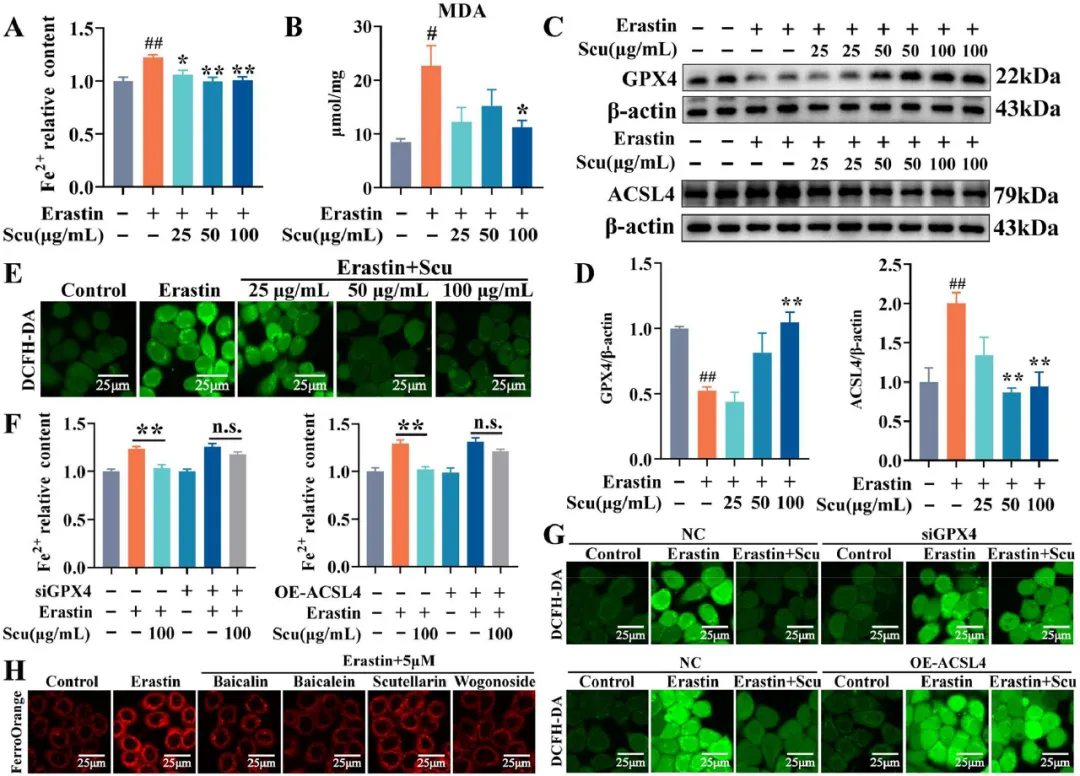
图9 Scu调节Erastin处理的HT-29细胞中GPX4/ACL4轴介导的铁死亡。Erastin(10μM)和不同浓度的药物在HT-29细胞中处理24小时。(A)Fe2+相对含量。(B)MDA水平。(C-D)免疫印迹检测GPX4和ACSL4的蛋白表达。(E)ROS的水平。HT-29细胞用siGPX4或ACSL4质粒转染24小时,然后用相应的药物再处理24小时。(F)Fe2+相对含量。(G)ROS的水平。(H)Scu提取物中主要成分的Fe2+荧光。结果以平均值±SEM表示。与对照组相比,#P<0.05和##P<0.01;与Erastin处理组相比,*P<0.05和**P<0.01;n.s.,无显著性。
讨论
近年来,UC的患病率在全球范围内有所上升,造成了巨大的医疗压力和经济负担。然而,其机制仍未得到充分理解。此外,目前的治疗药物面临着许多挑战,包括严重的不良反应、疾病复发和不一致的治疗效果。中草药治疗UC具有独特的优势,已成为一种替代治疗选择。
铁死亡,尤其是结肠上皮细胞中的铁死亡,已成为缓解UC的潜在调节靶点。同时,各种中草药提取物和天然化合物,包括华良姜素、香草酸、黄芪多糖和仙茅苷,已被证明可以通过调节铁死亡相关途径有效改善UC。Scu是一种含有大量天然黄酮类化合物的中草药,对UC具有治疗作用。然而,Scu通过抑制铁死亡途径对UC发挥改善作用的程度仍不完全清楚。为了探索这种相关性,本研究应用DSS诱导的溃疡性结肠炎小鼠模型,并用Scu治疗。通常,严重的病理损伤、肠屏障破坏和严重的炎症是UC的标志性特征。在UC发展过程中,IL-6、IL-1β和TNF-α的水平显著升高。肠黏膜的破坏通常伴随着ZO-1和Occludin的异常表达。研究者的研究证实,Scu可以改善UC,主要表现在其减轻病理损伤、降低促炎细胞因子水平和提高肠道完整性的能力上。此外,研究者观察到,UC小鼠结肠上皮细胞的线粒体体积减少,线粒体嵴减少或缺失,这与之前报道的铁死亡现象一致,通过TEM观察到。相比之下,Scu组的线粒体损伤得到了修复,这表明Scu可以通过调节铁死亡途径来改善UC。
脂质过氧化物的不受控制的积累是铁死亡的核心原因。PUFA必须首先被ACSL4激活为酰基辅酶A,然后通过溶血磷脂酰胆碱酰基转移酶3(LPCAT3)的作用与溶血磷脂酰基乙醇胺(LysoPE)或溶血磷脂胆碱(LysoPC)酯化产生磷脂酰乙醇胺(PE),最后被LOX直接氧化为脂质过氧化物,引发铁死亡。先前的研究表明,LysoPC和LysoPE的高表达有助于减轻UC的肠道损伤和挽救炎症损伤。同样,这项研究的结果也显示了类似的趋势。研究表明,AA是最容易受到脂质过氧化影响的PUFA,脂质过氧化会导致UC患者铁死亡和AA浓度显著增加。AA的代谢途径包括由COX、LOX和细胞色素P450(CYP450)调节的三种途径,它们在碳链的不同位置插入氧原子以产生各种脂质过氧化产物。然而,这些AA代谢物对肠道炎症和铁死亡的过程有不同的调节作用。研究表明,AA可以通过COX代谢为PGE2、PGF2α、TXB2,从而促进UC的炎症反应。AA可能通过LOX代谢为12-OxoETE、LTB4、5-HETE,其水平已被证实与炎症呈正相关。同时,据报道,由CYP450代谢的AA代谢产物,包括8,9-环氧二十碳三烯酸(8,9-EET)和5,6-二羟基二十碳四烯酸(5,6-DiHETE),具有抗炎活性,可以缓解UC。本研究中的代谢组学结果还显示,在DSS诱导的结肠炎动物模型中,PGE2、PGF2α、TXB2的含量通过COX途径增加,12-OxoETE、LTB4、5-HETE的含量通过LOX途径增加。此外,亚油酸、二十二碳六烯酸通过LOX途径的一些脂质过氧化物也显示出增加的趋势。相反,本研究中可以看到UC小鼠结肠组织中通过CYP450途径的5,6-DiHETE浓度降低。总体而言,这些受干扰的PUFA代谢,特别是AA相关代谢产物,可以通过Scu得到正向调节。总体而言,这些数据表明,Scu对UC的调节作用可能有助于其对PUFA的调节作用和脂质过氧化的积累。
Scu是一种被广泛认可的草药,含有多种黄酮类化合物。为了阐明其抗UC作用的物质基础及其独特的作用方式,了解其作用机制至关重要。研究者进一步分析了结肠组织中Scu的暴露化合物,并进行了网络药理学分析,以预测Scu对抗UC的潜在机制。结果表明,Scu可能通过调节铁死亡和AA代谢途径干预UC。此外,分子对接研究表明,Scu中的某些化合物对与脂质过氧化和铁死亡相关的蛋白质表现出很强的亲和力。
上述蛋白质,包括参与AA代谢和铁死亡的PTGS2、ACSL4和ALOX15,在许多疾病中高度表达,从而导致脂质过氧化物水平升高。这项研究还表明,这些蛋白质在UC小鼠中显著增加,并证实了Scu对它们的调节作用。此外,PTGS2不仅是一种脂质过氧化酶,也是炎症性疾病中氧化应激增加的指标。此外,研究表明,铁死亡是由过量ROS引起的。SOD可以催化超氧阴离子自由基的歧化产生ROS。而Scu增加了UC小鼠的SOD活性,表明其具有缓解氧化应激的潜力。脂质过氧化是评估铁死亡发生的最关键因素,MDA和4-HNE是通常用于评估脂质过氧化水平的脂质过氧化物的主要成分。此外,GPX4是一种抑制脂质过氧化的抗氧化酶。这项研究表明,Scu不仅降低了UC小鼠体内4-HNE结合蛋白和MDA的水平,还提高了GPX4的水平。最近的研究表明,桑色素与黄嘌呤氧化酶相互作用以发挥抗氧化作用,研究者的研究表明Scu通过铁死亡途径减轻了氧化应激。
由于DSS组中观察到AA及其相关代谢物的增加,以及Scu对PUFA代谢的调节作用,当UC小鼠用Scu治疗时,也给予了AA补充。这项研究可以帮助研究者确认Scu的抗UC作用是否与UC小鼠的PUFA代谢和细胞铁死亡有关。补充AA后,Scu组小鼠线粒体形态破坏,GPX4表达降低,4-HNE结合蛋白和PTGS2水平升高。此外,研究者观察到更严重的肠道损伤和炎症,表明Scu组补充AA会加剧脂质过氧化和铁死亡,最终导致UC加重。
此外,研究者使用Erastin诱导结肠上皮细胞系HT-29细胞铁死亡,结果具有上述趋势。然而,当研究者通过转染敲除GPX4或过表达的ACSL4时,Scu对铁死亡的抑制作用减弱。这些数据表明,Scu可以通过调节GPX4/ACL4轴来抑制铁死亡。之前的一项研究表明,载荷纳米颗粒的植物化合物对阿尔茨海默病具有抗炎作用。因此,研究者进一步研究了Scu中的主要黄酮类化合物,发现它们通过抑制铁死亡来发挥抗氧化作用。研究者的研究为Scu治疗UC的疗效和治疗潜力提供了证据,并证实了脂质过氧化和铁死亡在这种情况下的参与(图10)。目前,CRISPR-Cas系统被广泛用于识别植物化学物质干预的精确靶点。尽管研究者进行了分子对接研究和一些实验来验证,但还需要进一步的研究。此外,黄芩的主要成分,如黄芩苷、黄芩素、野黄芩苷和汉黄芩苷,需要在进一步的工作中进行进一步的实验研究,以验证它们调节铁死亡以改善UC的能力。
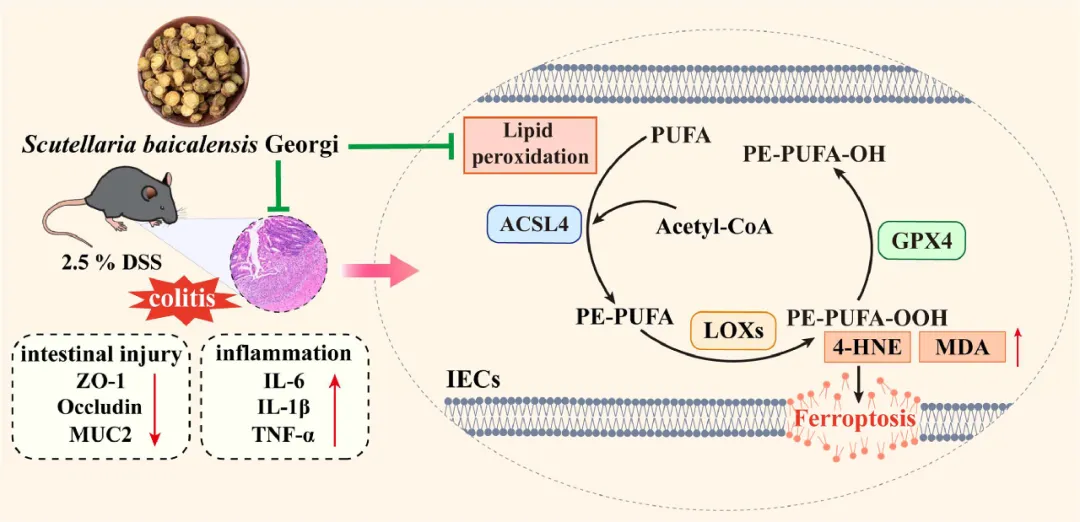
图10 Scu抗UC的拟议机制。
结论
总的来说,本研究表征了Scu中的成分,并证明了其对DSS诱导的结肠炎的治疗效果。通过代谢组学和网络药理学的联合分析,研究者提出其潜在机制可能涉及调节PUFA代谢和GPX4/ACL4轴,通过减轻肠上皮细胞中的脂质过氧化来抑制铁死亡,从而改善UC。
----------微科盟精彩文章----------
科研 | 安徽省二院:GAMG通过IRF1/SLC7A11信号通路诱导炎性巨噬细胞铁死亡从而减轻肝纤维化(国人佳作)
如果需要原文pdf,请扫描文末二维码



获取此文献原文PDF、申请加入学术群,联系您所添加的任一微科盟组学老师即可,如未添加过微科盟组学老师,请联系微生态老师9,无需重复添加。
请关注下方名片,了解更多代谢组学知识
