巨噬细胞早于炎症缺失:对比UC患者与健康人的结肠组织,研究者发现一个关键现象:在那些尚未发生炎症的区域,紧贴肠上皮下方的组织常驻巨噬细胞已出现显著减少【图1A-C】。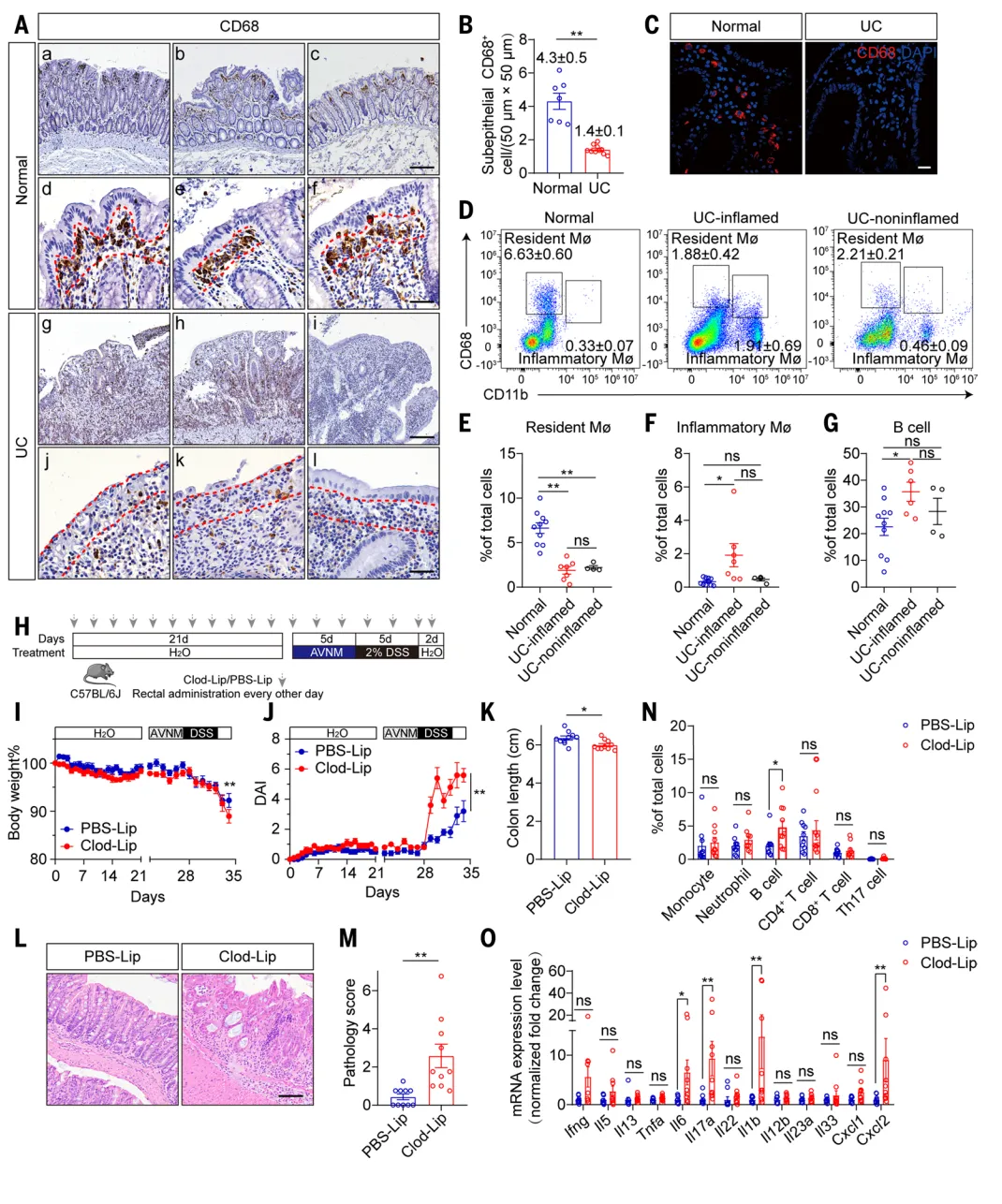 这种免疫 “哨兵”的缺失,发生于任何可见的上皮损伤和炎症细胞浸润之前【图1D-G】。这一现象提示,结肠炎的始动因素可能并非肠壁本身,而是其下方的免疫防线率先崩解。
这种免疫 “哨兵”的缺失,发生于任何可见的上皮损伤和炎症细胞浸润之前【图1D-G】。这一现象提示,结肠炎的始动因素可能并非肠壁本身,而是其下方的免疫防线率先崩解。
研究者据此推测,可能是肠道菌群中某种细菌分泌的毒素,直接导致了巨噬细胞的选择性死亡。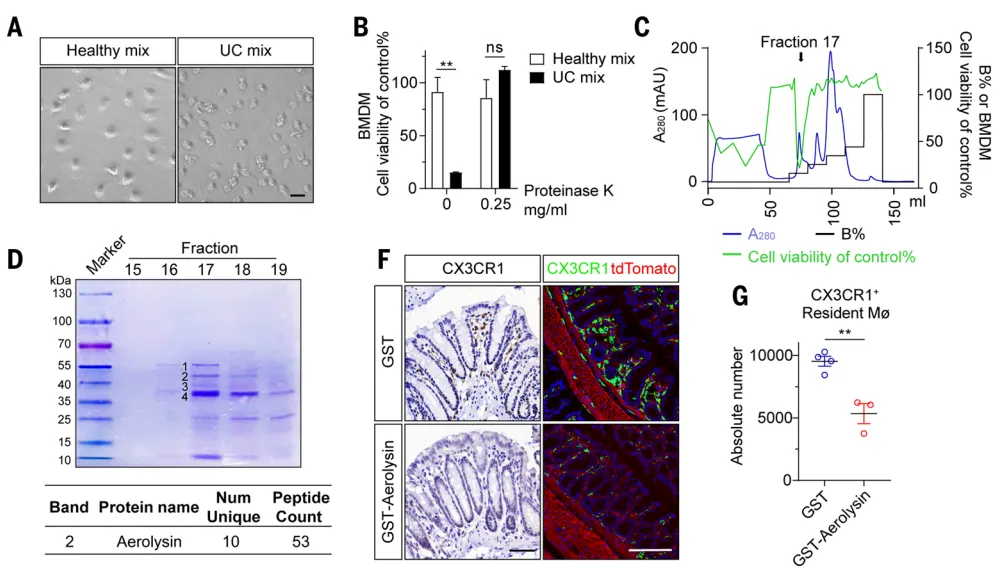
通过对大量粪便样本的系统筛查发现,近半数UC患者来源的细菌培养物能够高效杀伤巨噬细胞,而健康对照则无此作用。
质谱分析进一步精准锁定其毒性成分为气溶素——一种由气单胞菌属细菌分泌的成孔毒素【图2C-D】。
将纯化的气溶素作用于小鼠肠道后发现,它能够特异性清除上皮下层的巨噬细胞,而肠上皮细胞几乎不受影响【图2F-G】。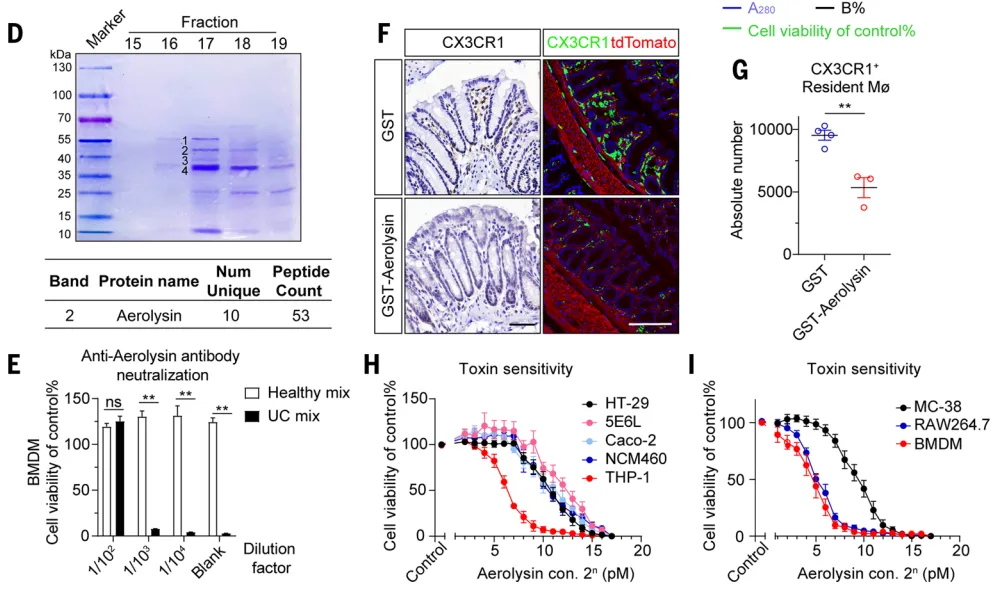 体外实验揭示了其靶向性的根源:巨噬细胞对气溶素的敏感性是肠道上皮细胞的20-80倍【图2H-I】。这种极高的选择性,使其能够精准破坏免疫屏障而不直接损伤肠道结构。
体外实验揭示了其靶向性的根源:巨噬细胞对气溶素的敏感性是肠道上皮细胞的20-80倍【图2H-I】。这种极高的选择性,使其能够精准破坏免疫屏障而不直接损伤肠道结构。
研究者成功分离出产毒菌株,命名为巨噬细胞毒性细菌。基因组分析显示,MTB是一种独特的气单胞菌变体,与常见的弗氏气单胞菌亲缘关系较近但存在明显差异【图2J-L】。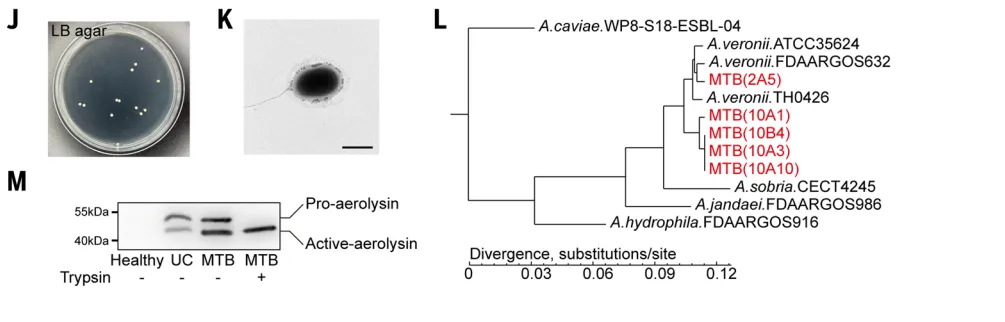 关键在于,普通气单胞菌难以在健康肠道中定植,而MTB却能在肠道屏障受损(如使用抗生素后)的环境下成功扎根并长期潜伏。
关键在于,普通气单胞菌难以在健康肠道中定植,而MTB却能在肠道屏障受损(如使用抗生素后)的环境下成功扎根并长期潜伏。
为验证气溶素在致病机制中的核心作用,研究者构建了毒素基因敲除的MTB突变株。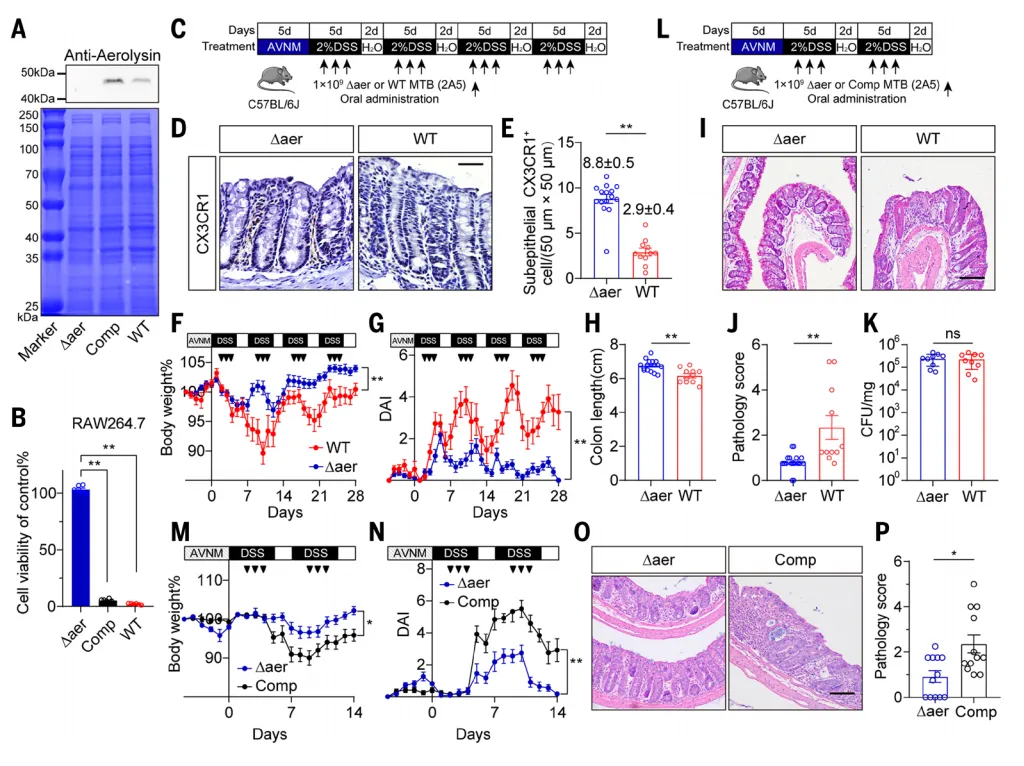 结果显示,失去毒素的MTB虽能正常定植,却完全丧失了引发结肠炎的能力【图4A-K】;而回补毒素基因后,其致病力立即恢复【图4L-P】。这一系列实验铁证如山:气溶素正是MTB致病的 “核心武器” 。
结果显示,失去毒素的MTB虽能正常定植,却完全丧失了引发结肠炎的能力【图4A-K】;而回补毒素基因后,其致病力立即恢复【图4L-P】。这一系列实验铁证如山:气溶素正是MTB致病的 “核心武器” 。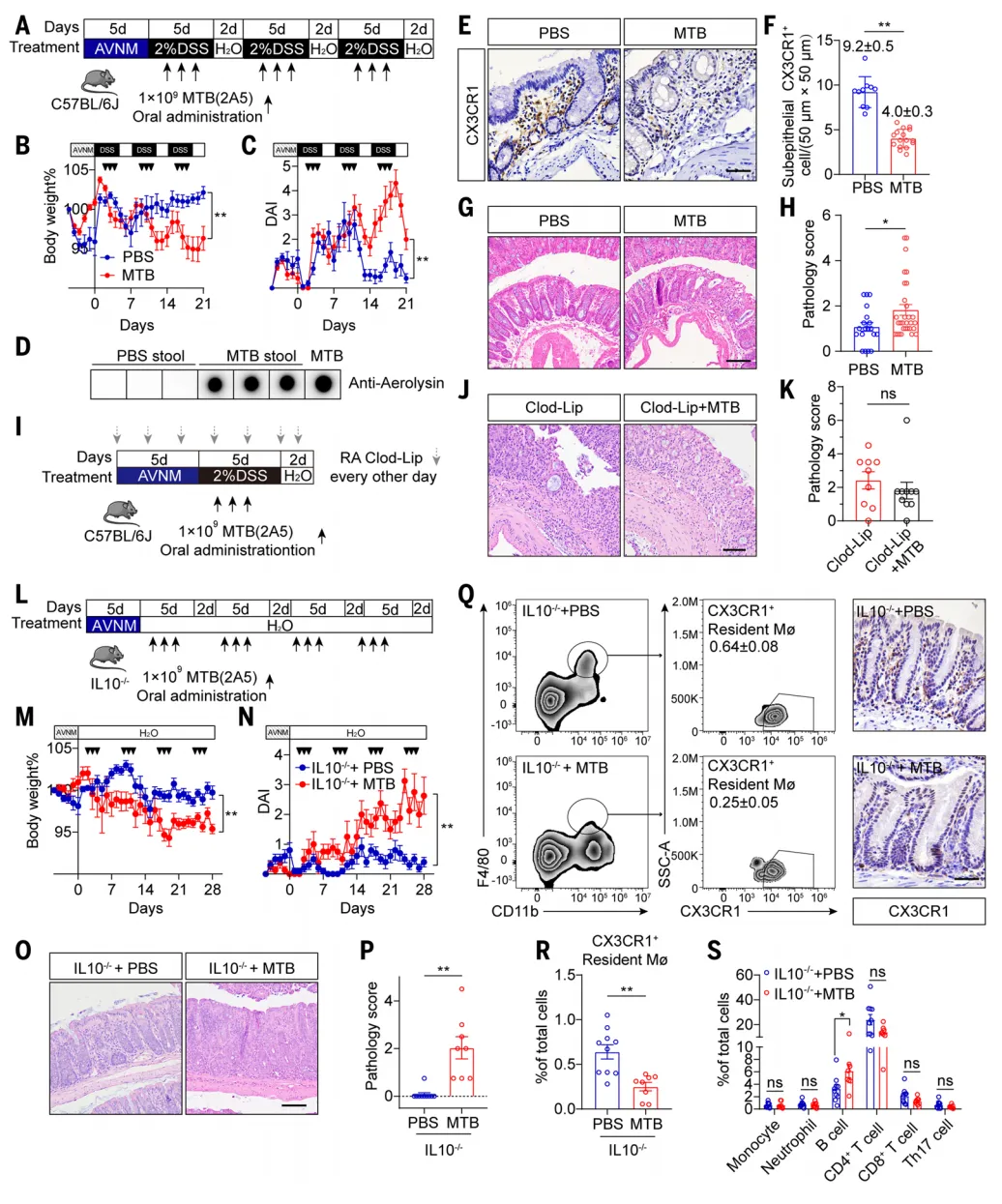 那么,巨噬细胞缺失是否是MTB致病的必需环节?当我们先用药物清除小鼠结肠巨噬细胞,再引入MTB时,MTB便无法加剧炎症【图3I-K】。这一结果明确表明,MTB的危害必须通过破坏巨噬细胞屏障这一 “枢纽步骤” 来实现。
那么,巨噬细胞缺失是否是MTB致病的必需环节?当我们先用药物清除小鼠结肠巨噬细胞,再引入MTB时,MTB便无法加剧炎症【图3I-K】。这一结果明确表明,MTB的危害必须通过破坏巨噬细胞屏障这一 “枢纽步骤” 来实现。
这一机制在患者群体中是否同样成立?流行病学数据给出了肯定的答案: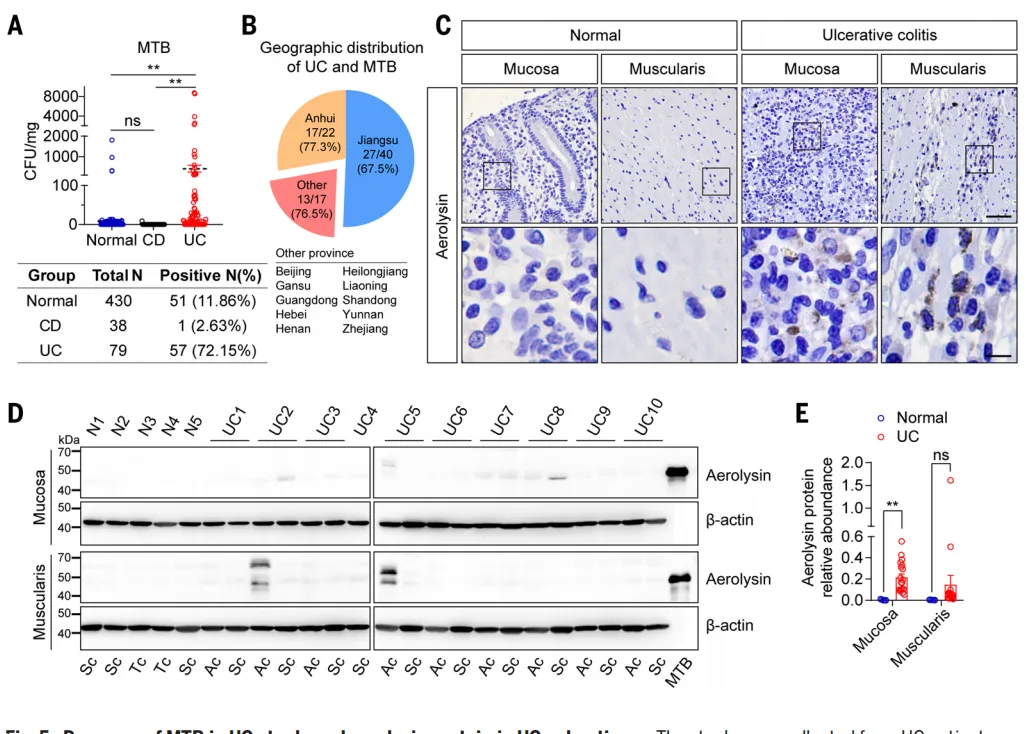
超过70%的UC患者粪便中可检出气单胞菌,阳性率远高于健康人群(约12%)和其他炎症性肠病患者(约2.6%)【图5A】。
更为关键的是,研究者利用特异性抗体,首次在UC患者的结肠病变组织内直接检测到气溶素蛋白【图5C-E】。
基于这一机制,研究者进一步测试了 “解毒”策略。无论是预防性还是治疗性给予抗气溶素中和抗体,均能在小鼠模型中有效阻止或显著缓解MTB诱导的结肠炎,并成功保护巨噬细胞屏障【图6】。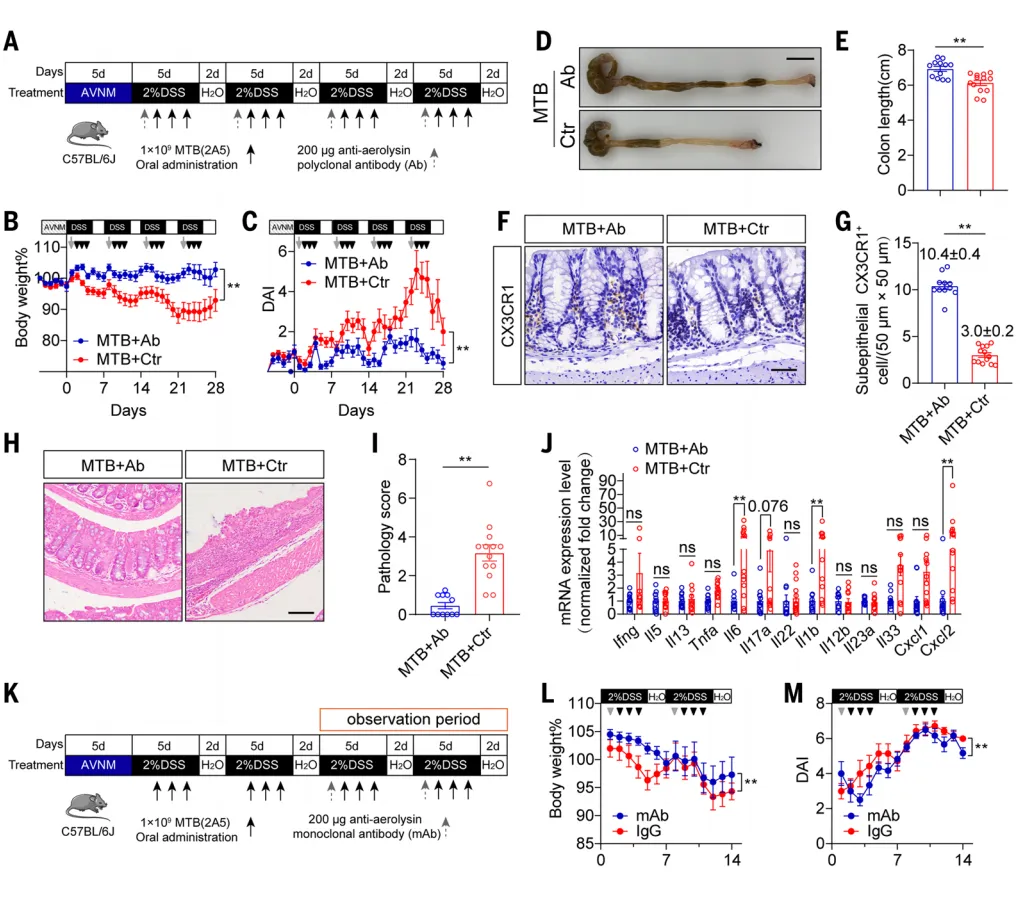
本研究系统揭示了溃疡性结肠炎发病的一条新途径——特定气单胞菌变体MTB在易感肠道定植 → 持续分泌气溶素 → 靶向清除上皮下巨噬细胞 → 免疫屏障崩溃 → 结肠炎发生。
这一发现不仅革新了对UC起病机制的传统认知,更指明了以气溶素为靶点进行诊断和治疗的崭新策略。