IF10.3!南京医科大学用“机器学习+SHAP”拿下二区!解析GRP75介导肝癌耐药机制及黄芩苷干预作用!
- 2026-05-22 12:53:56



🧬肝癌(HCC)治疗耐药的核心原因之一是肿瘤异质性,而葡萄糖调节蛋白75是驱动这一异质性的关键分子。如何精准识别GRP75相关的高危人群并进行靶向干预,是当前临床难点。
🔎本研究整合影像组学与人工智能,成功构建了一套术前影像无创识别系统,可准确筛选GRP75高表达且预后不良的HCC患者。这项研究为HCC的精准分层与个性化干预提供了从“识别”到“治疗”的完整解决方案。
📚如果你也想用“机器学习”发文的话,关注兔子生信,联系我们带你进一步了解~

文章标题:基于影像组学、机器学习和分子药理学的GRP75介导的耐药性肝细胞癌的智能识别与靶向干预研究
发表期刊:International Journal of Surgery
发表时间:2026年2月19日
影响因子:IF10.3/Q2


肝细胞癌(HCC)是癌症相关死亡的第三大原因,多数患者确诊时已失去手术机会,依赖TACE、索拉非尼等非手术治疗。然而,肿瘤异质性导致患者对相同治疗的反应差异巨大,耐药和复发是治疗失败的核心原因。因此,亟需开发非侵入性、可早期评估的GRP75识别方法,并探索靶向GRP75的逆转耐药策略。


本研究为多中心回顾性队列研究,纳入2018-2024年间接受TACE联合索拉非尼治疗的术后复发HCC患者。同时,利用TCMSP、ETCM等中药数据库筛选GRP75靶向单体,通过分子对接、分子动力学模拟和生物层干涉技术验证结合亲和力,并在GRP75过表达细胞系和裸鼠移植瘤模型中验证黄芩苷逆转耐药的效果及机制。

你是否也在寻找生信分析的最佳拍档?你是否也想拥有同款高分文章的漂亮图表?别再徘徊,速来联系兔子生信团队!我们提供从思路设计到数据挖掘的全流程服务,让你的科研之路轻松跳跃!
🌎肝癌治疗面临什么核心困境❓
🌟超70%患者初诊即失去手术机会,依赖TACE和靶向治疗。但肿瘤异质性导致耐药,最终治疗失败。如何早期识别耐药人群并精准干预,是临床关键难题。
🌎GRP75是什么❓
⌛️GRP75是驱动肝癌恶性进展和耐药的关键分子,但其检测依赖侵入性活检,且基因突变率极低,难以通过基因检测评估,亟需非侵入性识别方法。
🌎这篇研究发现了什么❓
🧠首次建立双模型AI影像组学系统,通过术前CT精准识别GRP75高表达、预后差的肝癌患者。同时,通过虚拟筛选和分子动力学,发现中药单体黄芩苷能特异性结合GRP75,破坏MAM结构,抑制钙离子/自噬轴,逆转肝癌耐药。这是首项从“精准识别”到“靶向干预”的肝癌耐药全链条研究!
GRP75在HCC中的临床意义及建模策略

在纳入的术后复发接受TACE联合索拉非尼治疗的患者中,BCLC-C期患者的GRP75水平显著高于BCLC-A期,且GRP75高表达预示不良预后。荟萃分析进一步确认GRP75过表达是HCC患者预后不良的危险因素(图1)。
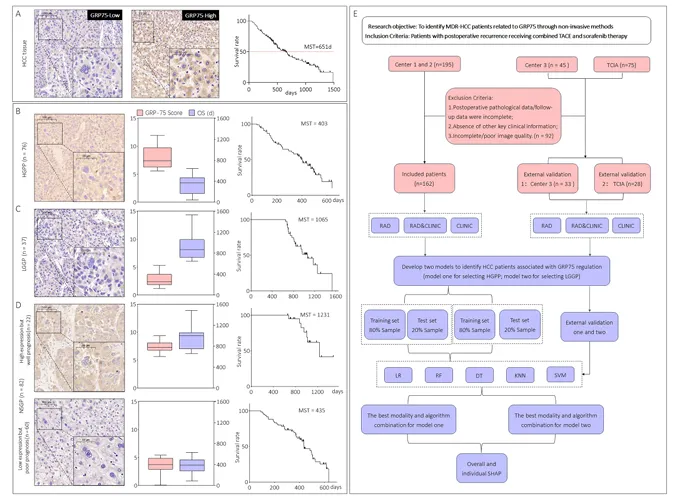
图1. 机器学习模型构建的工作流程
TCGA数据库显示GRP75基因在HCC中突变频率极低,提示遗传检测不适用。基于此,研究团队将患者分为HGPP、LGGP和NCGP三组,并建立了双模型分层识别系统:模型一用于从总人群中筛选HGPP组,模型二用于在剩余人群中筛选LGGP组。

从CT图像中共提取1688个影像组学特征,经ICC筛选保留1120个。经t检验、Spearman相关和LASSO回归四轮筛选后,模型一和模型二分别保留13个和11个关键影像组学特征(图2)。
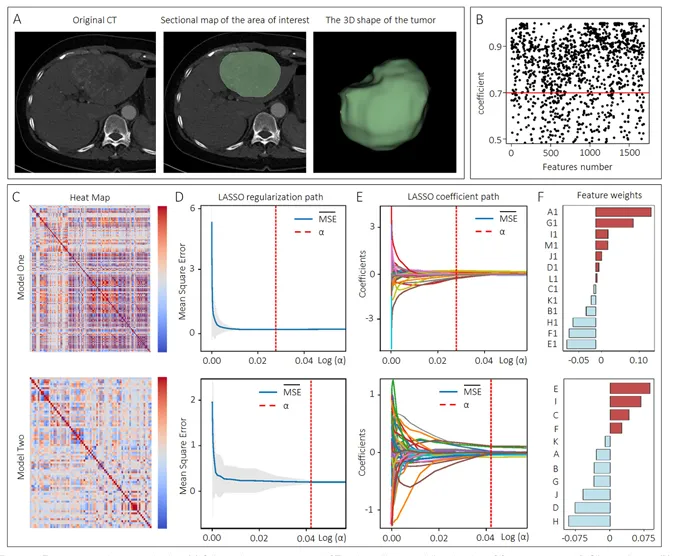
图2. 特征提取与选择过程
在五种机器学习算法中,随机森林(RF)在模型一表现最优,训练集、测试集和两个外部验证集的AUC分别达0.933、0.892、0.879和0.857(图3)
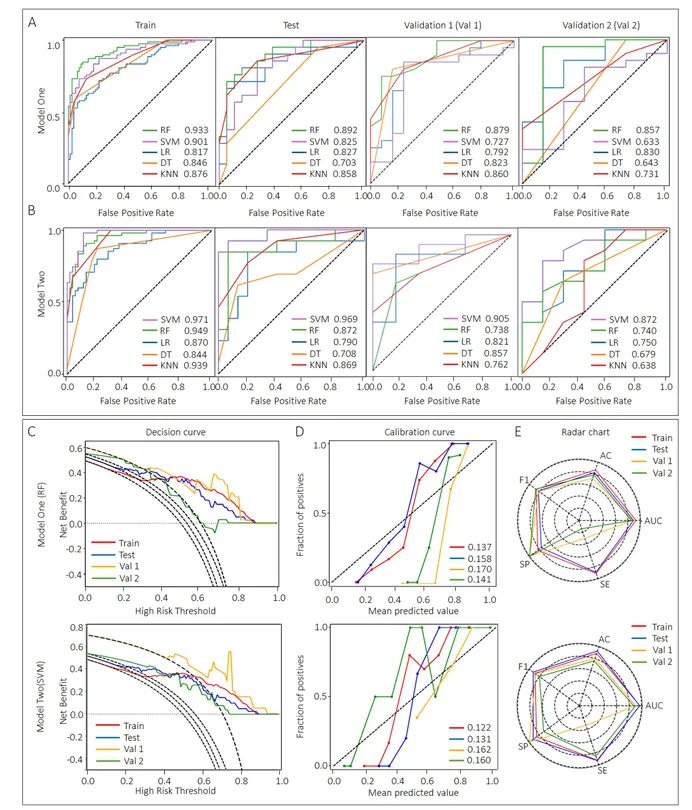
图3. 模型在训练集和验证集上的性能评估
支持向量机在模型二表现最优,AUC分别达0.971、0.969、0.905和0.872。决策曲线分析显示,两个模型在20%-80%阈值概率范围内均提供显著净获益,校准曲线Brier评分在0.122-0.170之间,表明模型具有良好的临床适用性和校准度。

SHAP分析揭示了关键影像组学特征的生物学意义:小波变换特征主要反映瘤内异质性,指数特征与增强特征相关。全局特征重要性图和蜂群图展示了各特征对预测概率的正负影响(图4)。
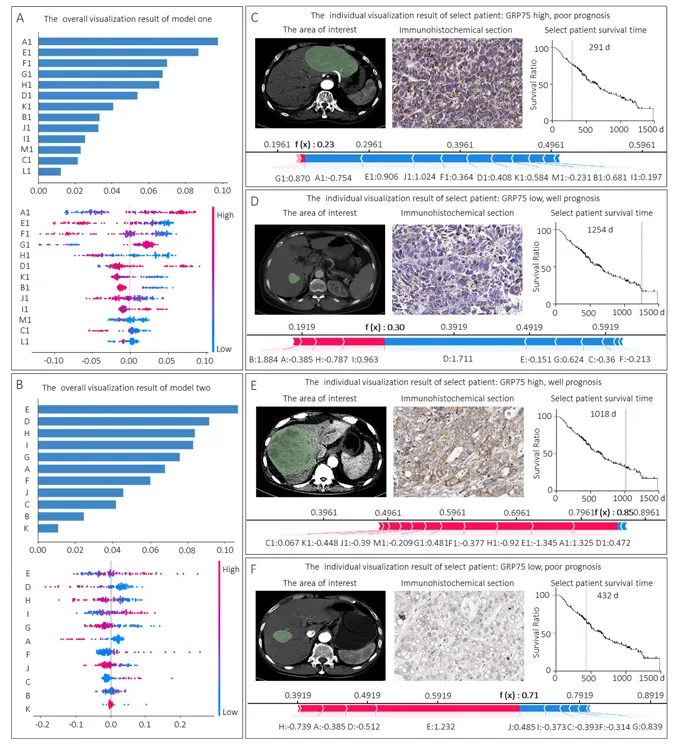
图4. 模型的SHAP分析
通过4例典型患者的个体化SHAP解释,清晰展示了模型如何基于影像特征做出最终预测,显著提升了AI模型在临床场景中的可解释性。

通过Coremine、TCMSP等数据库系统筛选,锁定丹参和柴胡两味具有抗HCC潜力的中药。从中筛选出黄芩苷、亚油酸和油酸三种候选单体。分子对接显示,黄芩苷与GRP75形成氢键结合,结合能最优(图5)。
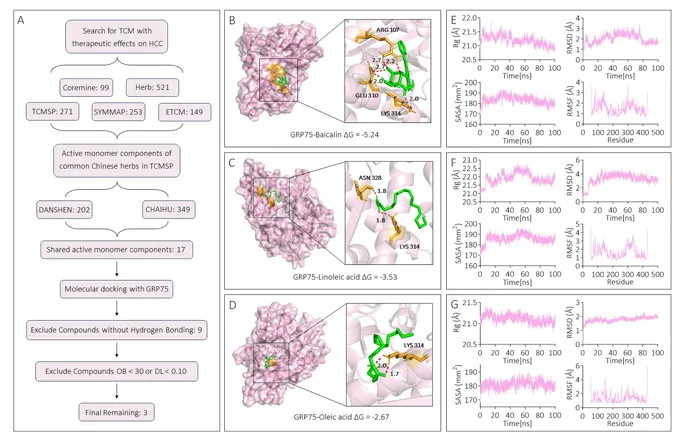
图5. 靶向GRP75的中药单体筛选
分子动力学模拟显示,黄芩苷-GRP75复合物的回转半径、均方根偏差和溶剂可及表面积在70 ns后均趋于稳定,表明复合物稳定性良好。综合药物相似性、结合能和模拟结果,选定黄芩苷进行后续研究。

分子对接显示,黄芩苷与GRP75的结合位点与VDAC1高度重叠,提示黄芩苷可能干扰IP3R-GRP75-VDAC1复合物形成。生物信息学分析表明,GRP75正相关基因主要富集于线粒体功能、钙转运和自噬通路(图6)。
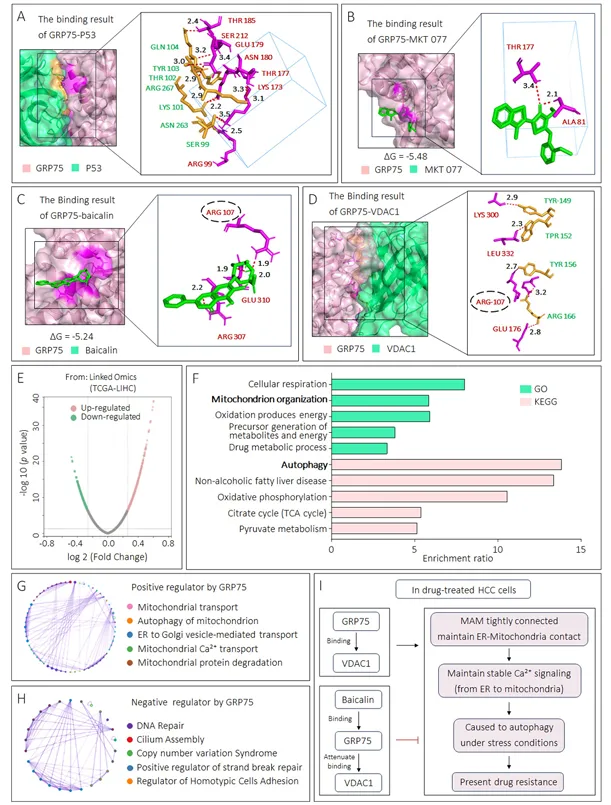
图6. 黄芩苷靶向GRP75的潜在机制探索
实验验证发现,黄芩苷处理可减弱GRP75与VDAC1的相互作用,增加线粒体与内质网间距,降低线粒体钙水平,并抑制自噬标志物LC3B表达、增加p62表达(图7)。
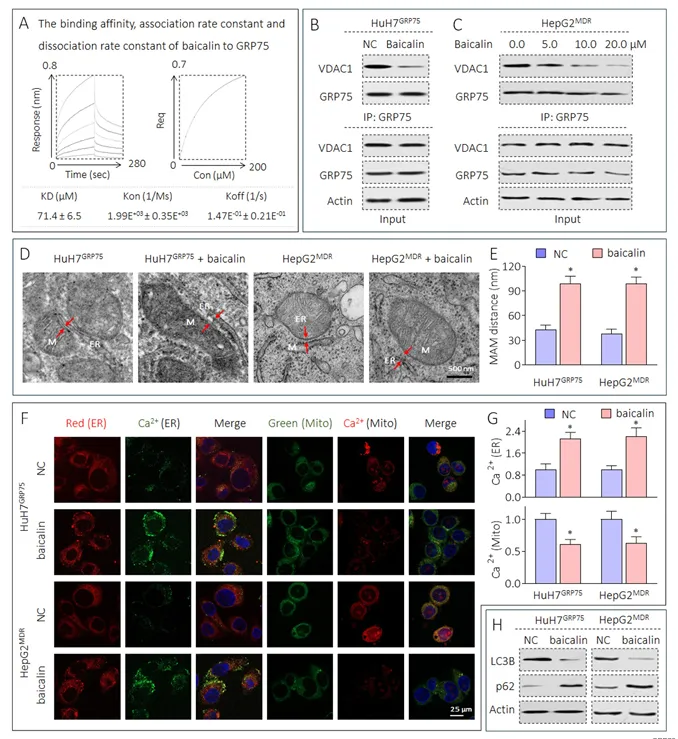
图7. 黄芩苷对GRP75及其下游生物学过程的影响
在p53突变型HuH7和p53野生型HepG2细胞中,黄芩苷的耐药逆转作用均依赖于GRP75,但不依赖于p53,与经典GRP75抑制剂MKT077机制不同。

在HuH7GRP75和HepG2MDR细胞中,黄芩苷处理显著增强细胞对顺铂和索拉非尼的敏感性,IC50值显著降低(图8)。
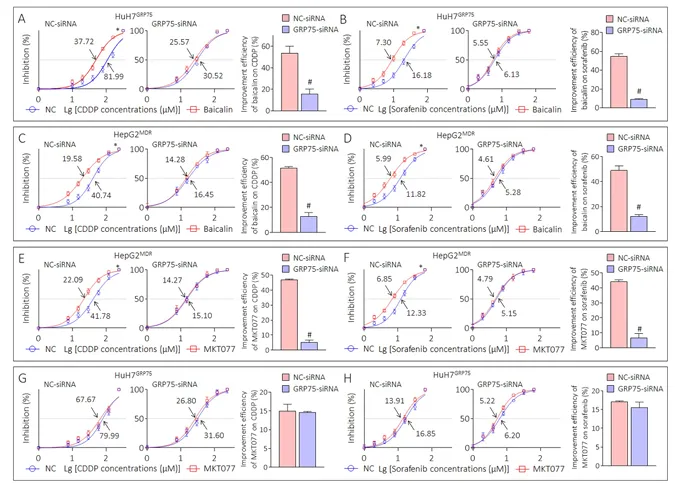
图8. 黄芩苷在体外逆转GRP75介导的多药耐药
当GRP75被敲低后,黄芩苷的增敏效应基本消失,证实其作用依赖GRP75。在裸鼠移植瘤模型中,黄芩苷联合顺铂或索拉非尼显著抑制肿瘤生长,降低GRP75和LC3B表达,增加p62表达(图9)。
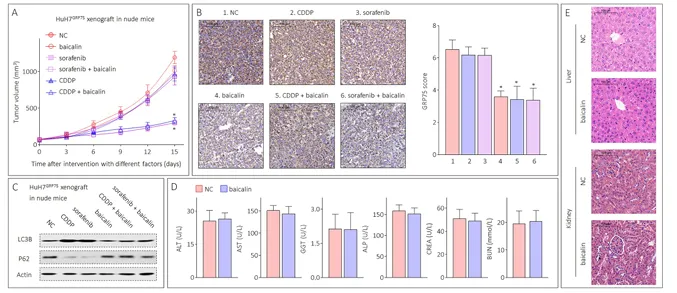
图9. 黄芩苷在体内逆转GRP75介导的多药耐药
安全性评估显示,黄芩苷单药治疗未引起明显的肝肾功能异常和肝肾组织病理损伤。
本研究首次构建了“影像组学-AI识别”与“中药单体靶向干预” 相整合的肝癌耐药精准诊疗框架。
开发了基于术前CT的GRP75相关耐药亚型双模型识别系统,实现非侵入性高危人群筛查;首次发现黄芩苷通过结合GRP75的Arg107位点,竞争性阻断VDAC1结合,破坏MAM结构,抑制线粒体钙/自噬轴,逆转肝癌多药耐药;验证了黄芩苷在p53突变型和野生型细胞中均有效,区别于传统GRP75抑制剂。
这一策略为肝癌精准分层和个性化治疗提供了新范式。
如果你也想用“机器学习”进行发文,思路复现,那就快来联系我们吧~




IF48.5!华中科技大学&武汉大学联手用“国自然”荣登《Nature》!揭示饮食脂质通过调控T细胞铁死亡影响免疫应答!




