南京大学王晓勇团队 | 缓解老年痴呆症中 Aꞵ 神经毒性的视黄酰胺合铂配合物
- 2026-05-27 04:31:02

01
研究背景
阿尔茨海默病 (Alzheimer’s disease, AD) 作为最常见的一种老年痴呆症影响全球数千万人的健康。随着人口老龄化进程的加速,AD 患者数量预计将持续攀升,而目前仍缺乏能够有效逆转或治疗该疾病的药物。AD 具有复杂的发病机制,其中 ꞵ-淀粉样蛋白 (Aꞵ) 的异常聚集及其引发的神经毒性是重要的病理特征之一。然而,针对 Aꞵ 单一靶点的治疗策略在临床实践中屡屡受挫,即使已经上市的 Aꞵ 单抗药物,其临床疗效也很有限,说明只靠清除 Aꞵ 或抑制其聚集不足以阻止疾病进程,因为 Aꞵ 的神经毒性涉及多个层面,既包括聚集过程本身,也包括聚集过程中产生的氧化应激及所引起的神经炎症等。因此,能同时干预 Aꞵ 聚集和缓解其下游多重损伤的多靶点药物被视为治疗 AD 的新希望。
02
研究内容
近日,南京大学王晓勇教授课题组设计合成了一种无细胞毒性的视黄酰胺合铂配合物 (图 1,简称 RP),它能同时抑制 Aꞵ 聚集和缓解其引发的神经毒性。该分子融合了两个功能单元,分别为可特异性结合 Aꞵ 链上组氨酸 (H) 或甲硫氨酸 (M) 残基的铂配合物结构,以及具有神经营养保护作用的视黄酸衍生物。RP 对 Aꞵ 具有很强的结合能力,可以竞争性抑制金属离子诱导的 Aꞵ 聚集,在细胞和动物模型中均表现出治疗 AD 的潜力。
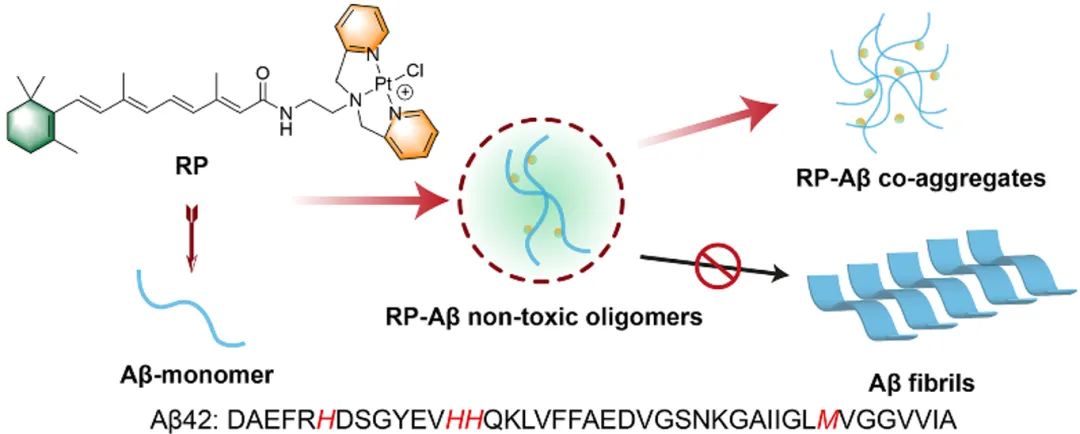
图1 RP 的化学结构及其与 Aꞵ42 的结合示意图,组氨酸和甲硫氨酸残基为潜在的铂结合位点。
研究发现,RP 能够有效抑制 Aꞵ 的自发聚集及金属离子诱导的聚集,透射电镜图像显示,经 RP 处理后,Aꞵ 形貌由长纤维转变为短碎片或无定形颗粒 (图 2)。蛋白免疫印迹实验进一步证明 RP 能减少毒性较强的小分子量 Aꞵ 寡聚体的含量。
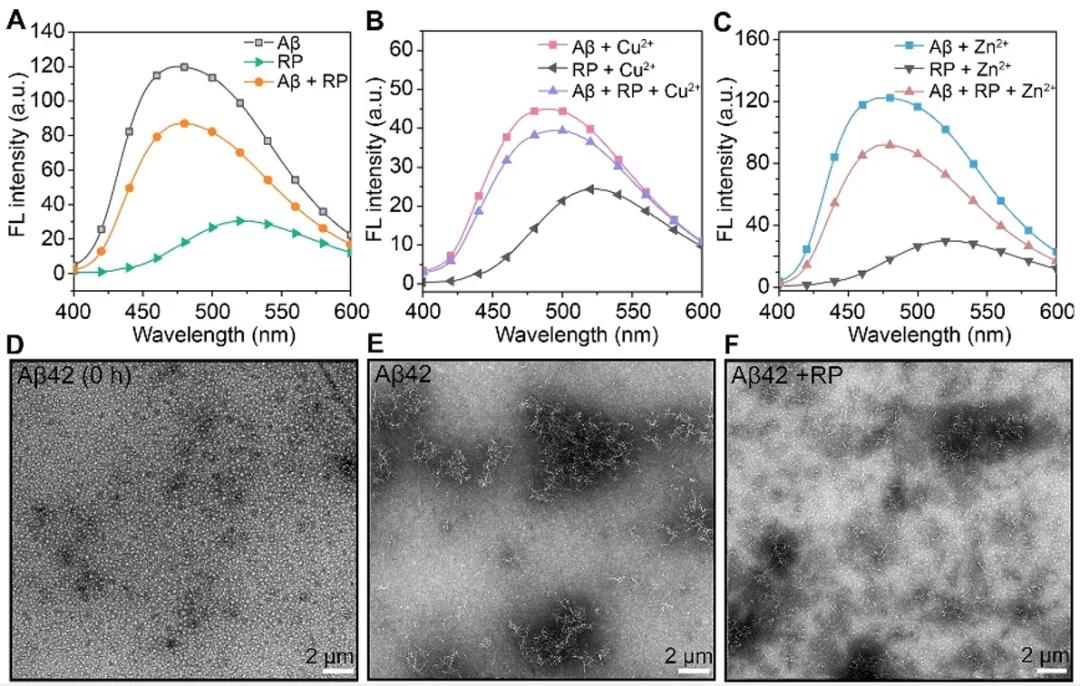
图2 RP 抑制 Aβ42 自聚集或金属离子诱导的聚集。在 37℃ 和 pH 7.4 条件下与 RP 共同孵育 24 小时后,无金属 (A) 或有Cu2+ (B) 和Zn2+ (C) 的 Aβ42 溶液中 ANS 的荧光强度;0 小时 (D) 及 24 小时后无 RP (E) 和有 RP (F) 的 Aβ42 透射电镜图像。[Aβ42] : [RP] = 1 : 1,[Aβ42] = 20 μM;[Aβ] : [金属离子] : [RP] = 1 : 1 : 1,λex = 380 nm。
在细胞层面,RP 无明显细胞毒性,能够显著缓解 Aꞵ 对 PC12 神经细胞的毒性,恢复细胞内抗氧化酶 (SOD) 的表达,并降低 Aꞵ 诱导产生的活性氧 (图 3)。同时,RP 与 Aꞵ 形成的共聚物对细胞膜的损伤相较于单独 Aꞵ 更小。此外,RP 还具有清除 Aꞵ 功能和减轻神经炎症作用,能减少炎症因子的分泌,在 BV-2 小胶质细胞中,RP 与 Aꞵ 形成的复合物更容易被细胞吞噬,并促进后续的溶酶体降解过程。
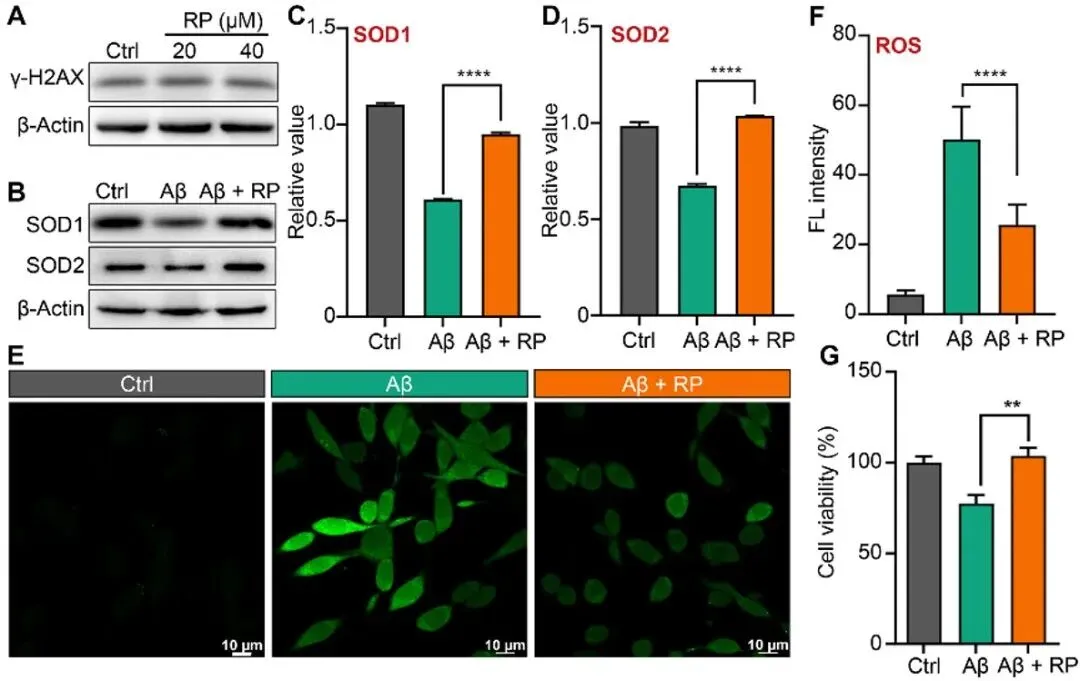
图3 RP 降低 Aβ42 的毒性。RP 存在下 PC12 细胞中 γ-H2AX 的表达 (A),Aβ42 处理过的 PC12 细胞中 SOD1 和 SOD2 的表达 (B) 及相应的蛋白质定量分析 (C 和 D),RP 对 Aβ42 诱导活性氧的影响 (E) 及定量荧光强度 (F),RP 对 Aβ42 诱导的 PC12 细胞毒性的影响 (G)。[Aβ] : [RP] = 1 : 1,[Aβ] = 20 μM。
以过度表达 Aꞵ 的 AD 线虫为动物模型,发现 RP 能显著延缓 Aꞵ 引起的运动障碍 (图 4)。与未经 RP 处理的 CL4176 线虫相比,RP 明显延迟了 Aβ 诱导瘫痪的作用。RP 对 CL4176 线虫的运动模式也产生了影响,在 25℃ 下生活 35 小时后,大多数未处理的线虫身体瘫痪,只有头部在运动,而许多投喂 RP 的线虫仍以弯曲方式移动,说明 RP 恢复了 CL4176 线虫的行为能力。RP 存在下,绿色 ThS 荧光强度显著降低,表明 CL4176 线虫的瘫痪延迟主要是由于 RP 抑制了 Aβ 诱导的毒性。
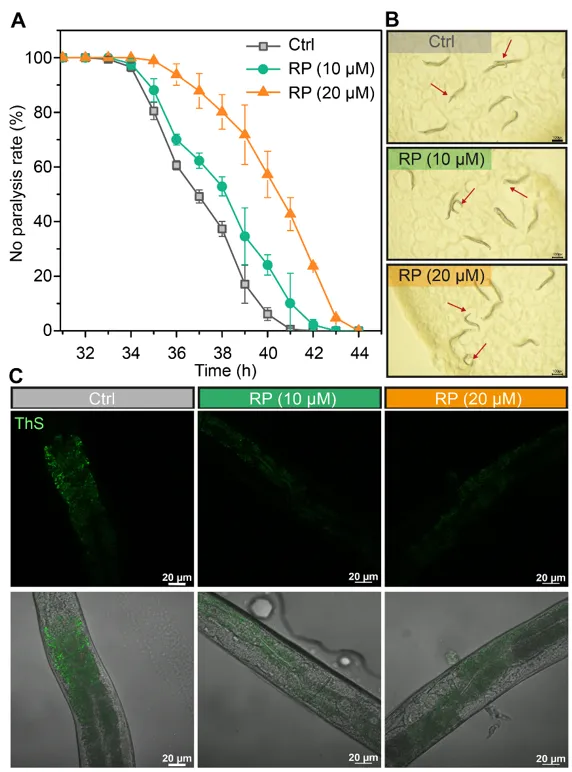
图4 RP 抑制 CL4176 线虫中 Aβ 的聚集和毒性。RP 在 25℃ 下对 CL4176 线虫瘫痪的影响 (A);RP 存在 35 小时对 CL4176 线虫运动模式的影响 (B);RP 存在下 ThS 染色的 CL4176 线虫中 Aβ42 物种的荧光变化 (C)。
03
总结展望
Aꞵ 聚集是 AD 发病机制中的关键事件,可导致多种神经障碍,包括活性氧产生、神经炎症和神经元死亡。本研究设计的视黄酰胺合铂配合物并非单纯地抑制 Aꞵ 聚集,而是通过形成低毒性 RP-Aꞵ 复合物改变 Aꞵ 的聚集途径与形态,同时增强机体对 Aꞵ 的清除能力,并抑制下游氧化应激与神经炎症反应发挥抗 AD 效应。这种将铂配合物的 Aꞵ 靶向能力与视黄酰胺神经保护活性相结合的策略不仅为开发多靶点抗阿尔茨海默病药物提供了新思路,也拓展了非毒性铂配合物在神经退行性疾病治疗中的应用潜力。
04
论文信息

Mitigation of Aβ neurotoxicity in Alzheimer's disease using a non-toxic platinum complex derived from retinamide
Chengyuan Qian, Yicun Shang, Linxiang Cai, Yunhua Zhang, Chengyan Chu, Zijian Guo and Xiaoyong Wang
Inorg. Chem. Front., 2026,13, 762-773
https://doi.org/10.1039/D5QI01746G
*文中图片皆来源上述文章
点击“阅读原文”直达上述文章
05
通讯作者简介

王晓勇
南京大学
王晓勇,南京大学医药生物技术全国重点实验室教授,博士生导师,从事无机药物化学和化学生物学基础研究,涉及生物无机化学、药物化学、生物化学、配位化学等多个学科,研究方向为抗阿尔兹海默症药物和抗肿瘤药物,擅长铂类抗肿瘤药物的设计和机制研究,近年来研究重点为金属化学免疫治疗剂的设计开发和靶点发掘,迄今为止,已经在 Chem. Rev.、Chem. Soc. Rev.、Acc. Chem. Res.、Angew Chem. Int. Ed.、Chem. Sci. 等期刊上发表论文 110 余篇。
推荐阅读
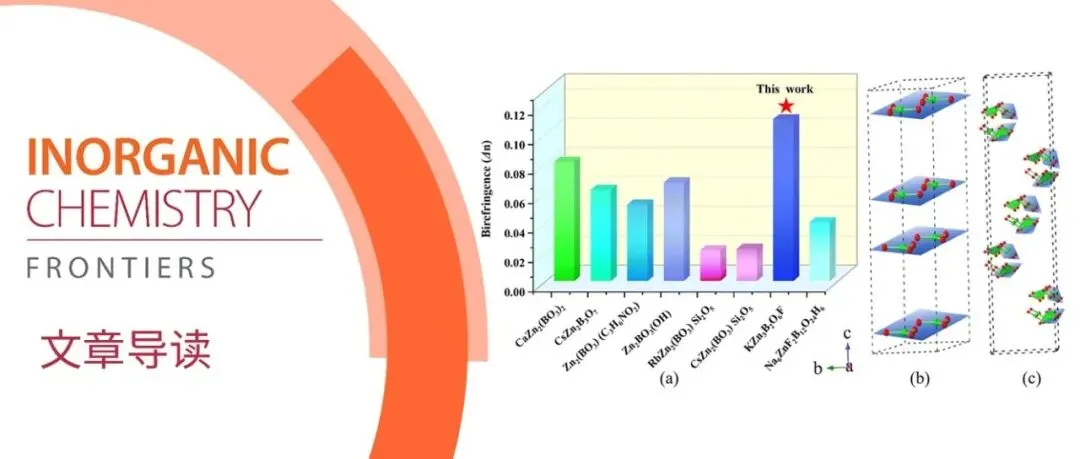
合肥大学郝玉成团队 | 通过 π 共轭 [BO₃] 单元的共面排列实现三维氟锌硼酸盐晶体材料中的高双折射
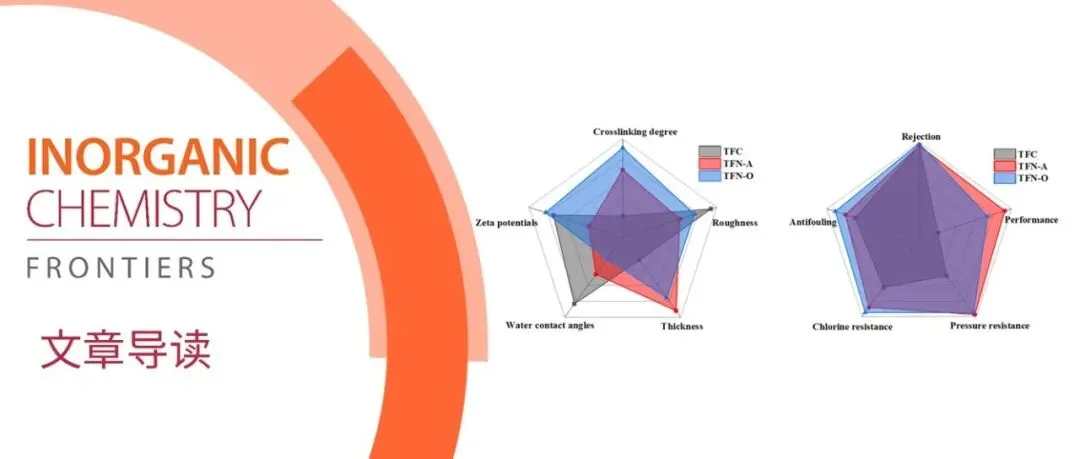
深圳大学牛青山/河北科技大学韩继龙团队 | FeOOH 纳米棒嵌入型 TFN 膜显著提升海水淡化性能

微信改版,公众号文章不再以时间轴排列啦!
将Frontiers Journals设为星标⭐ 不错过更多精彩内容!
喜欢今天的内容?
👇 就来分享、点赞、在看三连吧 👇
