南京工业大学黄维、卢晓梅等团队Biomaterials!!新型探针实现肿瘤免疫治疗高保真成像
- 2026-04-10 03:52:54
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

南京工业大学黄维院士、卢晓梅教授团队联合南京邮电大学及新加坡国立大学科研团队,成功开发出一种基于半导体聚合物链内给体-受体重构策略的新型NIR-II光声探针BDPNP。该探针通过精准识别巨噬细胞重编程关键生物标志物一氧化氮(NO),实现了肿瘤免疫治疗过程中M2型巨噬细胞向M1型极化的高保真动态监测。研究论文《Conjugated Polymer Intrachain Donor-Acceptor Reconfiguration-Tailored Off-On NIR-II Photoacoustic Probes with Ultralow Background for High-Fidelity Imaging of Immunotherapy-Associated Macrophage Reprogramming》发表于国际权威期刊《Biomaterials》,为肿瘤免疫治疗疗效评估提供了创新解决方案。
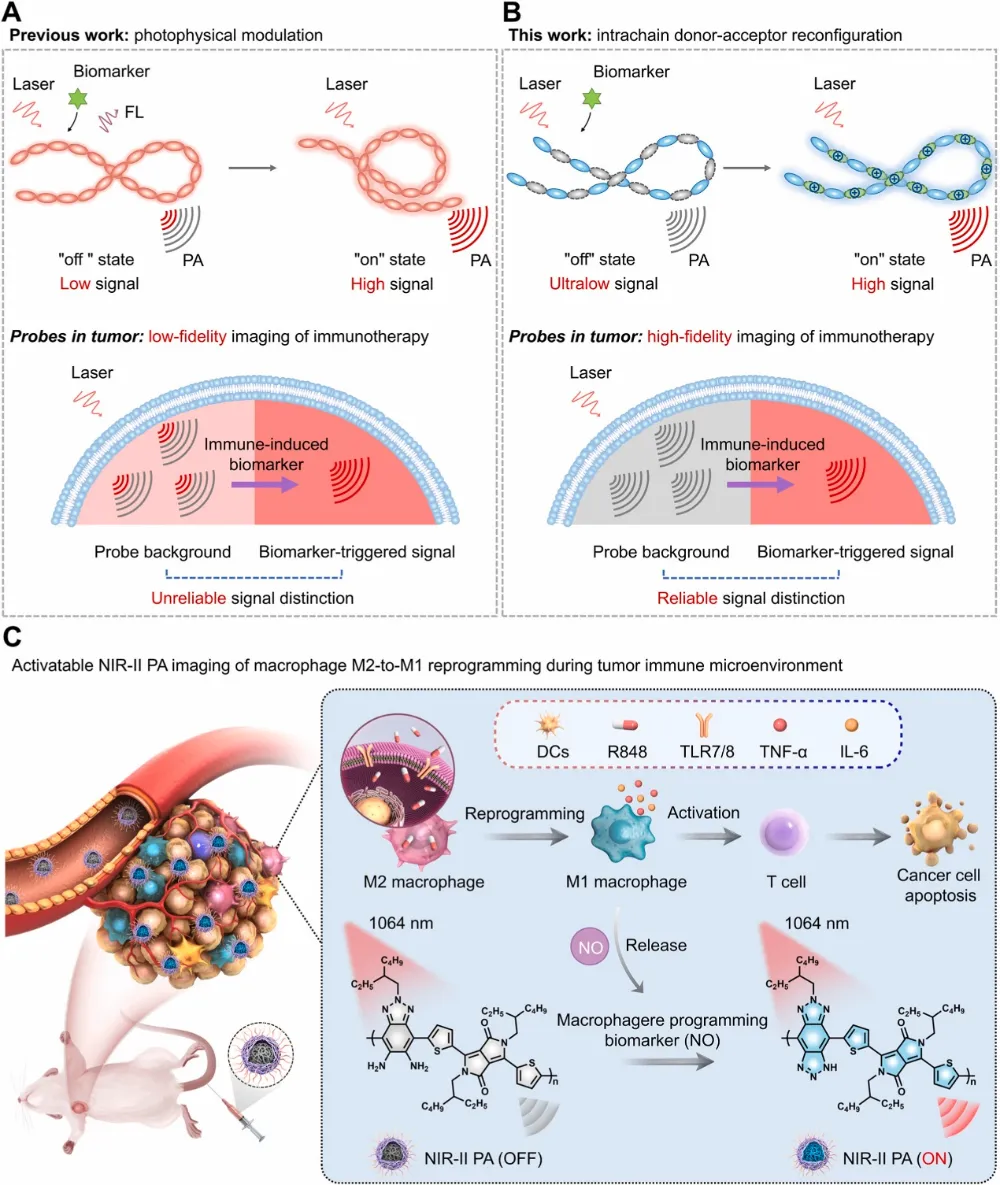
传统"关-开"型光声探针普遍存在本底信号干扰问题,即使未激活状态下仍会产生显著背景噪音,导致假阳性诊断。BDPNP探针通过独特的链内给体-受体重构机制破解了这一难题:在未激活状态下,BDPNP的邻苯二胺单元保持低电子亲和力构型,NIR-II吸收光谱位于700 nm附近,此时光声信号强度与生理盐水背景基本一致;当免疫治疗诱导巨噬细胞释放NO时,邻苯二胺迅速转化为苯并三唑衍生物,电子接受能力提升3个数量级,推动吸收光谱红移至1000 nm以上的NIR-IIb窗口,光声信号强度放大21.4倍。这种独特的开关机制使得探针在未激活时保持超低背景(信噪比>15),在激活后产生显著信号差异,有效区分生物标志物触发信号与探针本底。
研究团队通过纳米沉淀法制备的BDPNP探针粒径均一(~50 nm),展现出优异的被动靶向能力和光稳定性。在瑞喹莫德(R848)诱导的巨噬细胞重编程模型中,探针在注射后12小时即可清晰呈现肿瘤区域NO分布特征,较传统组织学分析提前48小时获得动态监测数据。该技术突破了传统成像手段的时空分辨率限制,为实时评估肿瘤免疫微环境重塑提供了新工具。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
