IF26.2!南京医科大学&南京大学联手用“多组学”荣登《Gut》顶刊!发现去泛素化酶JOSD1驱动肝癌代谢重编程!
- 2026-05-10 12:26:44


🧬肝细胞癌是全球第六大常见恶性肿瘤和第三大癌症死亡原因,代谢重编程是其核心特征之一。糖酵解增强不仅为肿瘤细胞提供能量和代谢中间产物,还通过乳酸积累重塑肿瘤微环境。
🔎本研究通过多组学分析结合大语言模型驱动的多智能体协作框架,鉴定出去泛素化酶JOSD1为HCC中糖酵解代谢的关键调控因子。靶向JOSD1可抑制肿瘤进展并与抗PD-1治疗协同增效。
文章标题:JOSD1通过调控PGAM1的泛素化-乳酸化开关驱动肝细胞癌恶性进展
发表期刊:Gut
发表时间:2026年4月28日
影响因子:IF26.2/Q1


肝细胞癌是全球第三大癌症死亡原因,代谢重编程是其核心特征。糖酵解增强不仅为肿瘤细胞提供能量,还通过乳酸积累重塑肿瘤微环境,抑制抗肿瘤免疫。揭示了JOSD1-AARS1轴通过协调PGAM1 K251位点的泛素化-乳酸化串扰驱动HCC恶性进展的机制。


本研究首先部署大语言模型驱动的多智能体协作框架,整合三个独立HCC队列的转录组数据和生存信息,筛选与糖酵解相关的预后基因。最后通过LNP-siJOSD1联合抗PD-1治疗评估靶向JOSD1的治疗潜力。
🌎S100A9抑制剂Paquinimod减轻SuHx诱导PH小鼠的症状❓
🌟通过去泛素化稳定PGAM1(K48连接泛素链去除,K251位点关键);通过促进AARS1介导的PGAM1 K251位点乳酰化增强酶活性;以及通过JOSD1-AARS1轴协调泛素化-乳酰化转换,形成上游分子开关。
🌎JOSD1高表达对免疫微环境有何影响❓
⌛️减少CD8⁺ T细胞浸润和GZMB/IFN-γ表达;增加MDSC和Treg比例;以及乳酸积累介导免疫抑制,与不良预后相关。
🌎这篇研究覆盖了什么❓
🧠从多组学筛选JOSD1为糖酵解相关预后基因,到体内外验证其促增殖、迁移和糖酵解表型;从IP-MS鉴定PGAM1为直接互作靶点,到K251位点去泛素化和AARS1介导乳酰化的双重修饰机制;以及LNP-siJOSD1联合抗PD-1协同抑制肿瘤并恢复CD8⁺ T细胞功能,确立JOSD1为代谢-免疫交叉调控的关键节点。
整合多组学分析鉴定JOSD1为HCC中糖酵解相关预后基因

通过大语言模型驱动的多智能体协作框架分析三个独立HCC队列,糖酵解通路在碳水化合物代谢中富集最强且预后相关性最显著。高糖酵解评分与临床晚期和病理T分期正相关(图1)。
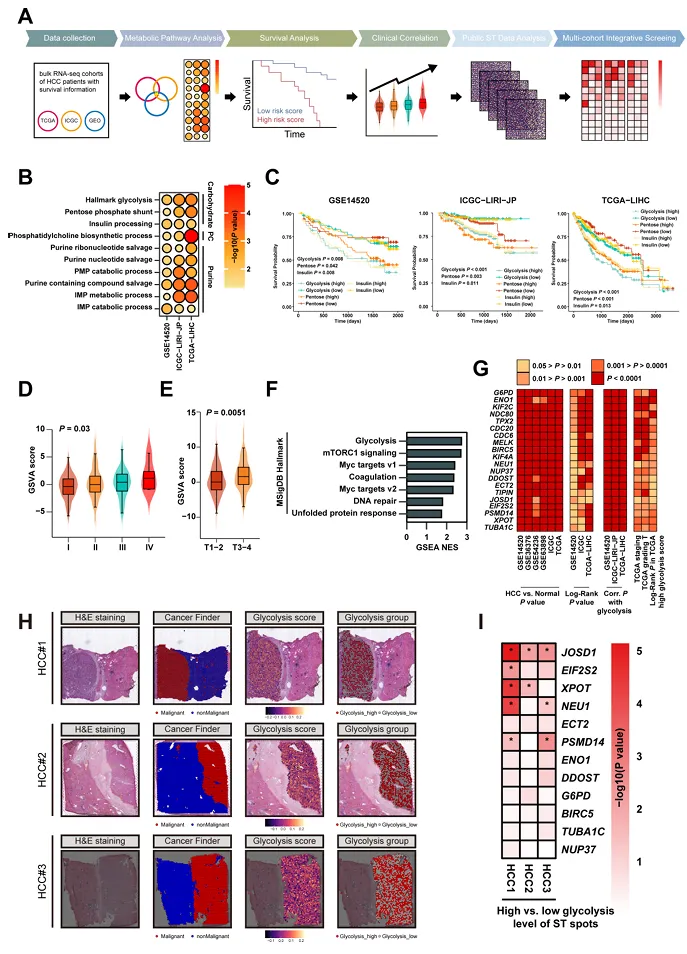
图1. 整合多组学分析鉴定糖酵解为HCC关键代谢通路并提名JOSD1为潜在调控因子
整合多队列分析筛选出20个糖酵解相关基因,空间转录组分析显示仅JOSD1在三个数据集中均差异表达。90例HCC组织芯片证实JOSD1在肿瘤中显著上调,与增殖表型正相关。
JOSD1在体内外促进HCC恶性表型

JOSD1敲低抑制HCC细胞增殖、迁移和侵袭能力,过表达则相反。皮下荷瘤模型中,JOSD1敲低抑制肿瘤生长,过表达促进生长(图2)。
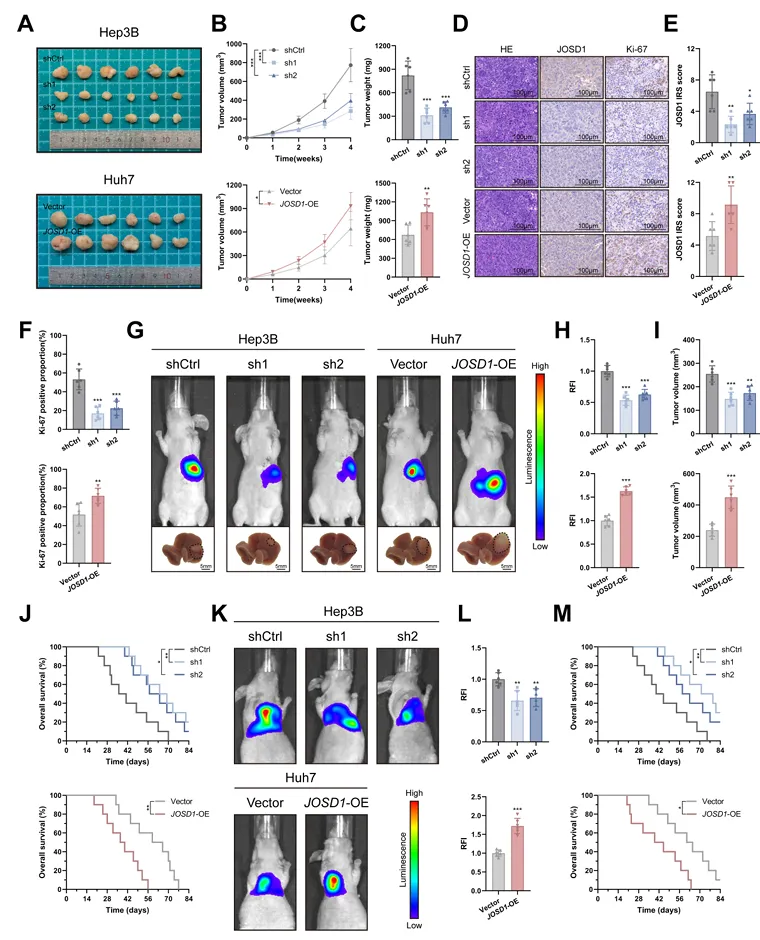
图2. JOSD1在体内促进HCC恶性进展
原位肝癌模型中,JOSD1敲低抑制肿瘤进展并延长生存期,过表达则相反。尾静脉肺转移模型中,JOSD1敲低抑制肺定植,过表达促进转移。

蛋白质组学分析显示JOSD1过表达上调糖酵解相关蛋白,GSEA证实糖酵解通路富集。¹⁸F-FDG micro-PET/CT显示JOSD1过表达增加肿瘤葡萄糖摄取(图3)。
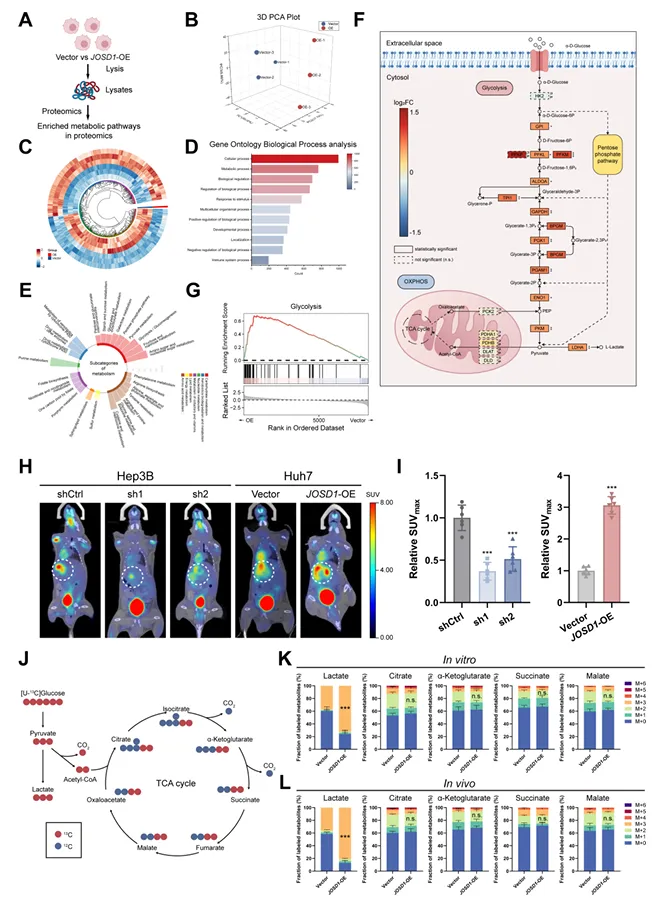
图3. JOSD1增强HCC糖酵解代谢
U-¹³C葡萄糖代谢流分析证实JOSD1过表达增强糖酵解通量。
JOSD1特异性相互作用并去泛素化稳定PGAM1

IP-MS鉴定出PGAM1为JOSD1的相互作用蛋白。Co-IP、GST pull-down和PLA证实JOSD1与PGAM1直接结合。CHX chase实验显示JOSD1延长PGAM1半衰期,MG132可逆转JOSD1敲低引起的PGAM1减少(图4)。
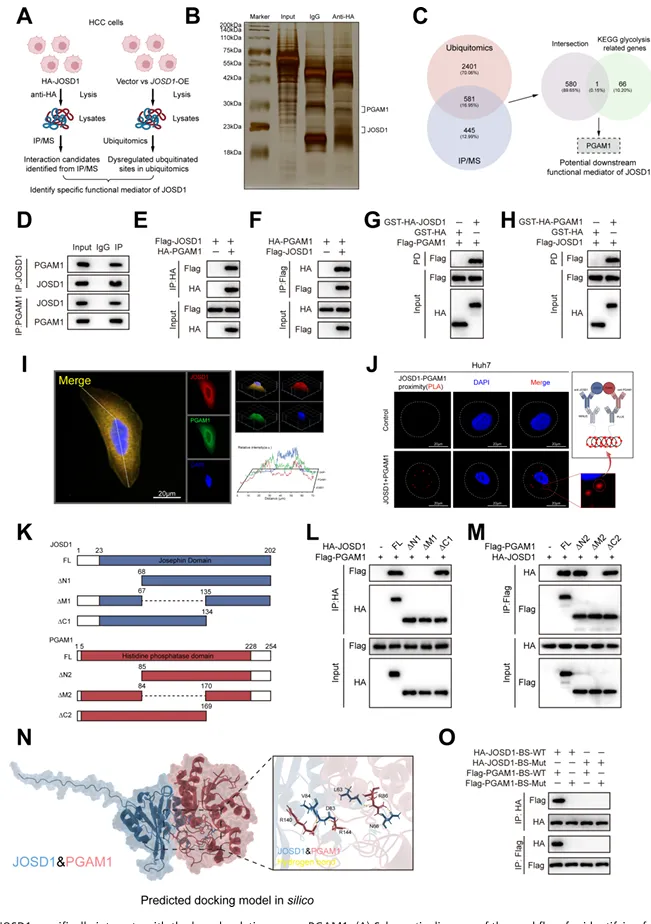
图4. JOSD1特异性相互作用于糖酵解关键酶PGAM1
JOSD1敲低增加PGAM1泛素化,过表达相反。点突变筛选鉴定K251为PGAM1上JOSD1介导去泛素化的关键位点,该位点在物种间高度保守。
本研究首次揭示了JOSD1通过协调PGAM1 K251位点的泛素化-乳酸化串扰驱动肝细胞癌糖酵解重编程和免疫逃逸的完整机制。JOSD1一方面通过去泛素化稳定PGAM1,另一方面作为分子开关使能AARS1介导的PGAM1乳酸化,协同增强PGAM1酶活性和糖酵解通量,导致乳酸积累,进而抑制CD8⁺ T细胞浸润和细胞毒性功能。
靶向JOSD1可抑制肿瘤进展并与抗PD-1治疗协同增效。本研究为肝细胞癌的代谢免疫交互机制提供了新见解,提示JOSD1是克服免疫治疗抵抗的潜在靶点。







