IF45.8!南京大学医学院“国自然”登顶《Science》:首次揭示溃疡性结肠炎全新机制!
肠道炎症元凶的“精准暗杀”手段曝光!🔍 最新研究发现,溃疡性结肠炎(UC)的幕后黑手竟是一种产气溶素的气单胞菌变体(MTB),它会悄悄“暗杀”肠道里的免疫卫士——组织驻留巨噬细胞,通过分泌气溶素特异性破坏巨噬细胞功能,瓦解肠道屏障防线,引发慢性炎症。
🧐南京大学等多团队联合攻关,通过对17例UC患者结肠组织分析、48例粪便样本筛选及动物模型验证,首次揭示MTB介导巨噬细胞耗竭是UC发病的关键机制,还证实抗气溶素抗体可有效阻断MTB的“暗杀”行动,为UC的精准诊断和靶向治疗开辟全新方向!🩺
《一种产生气溶素的气单胞菌变种可增加溃疡性结肠炎的易感性》
溃疡性结肠炎(UC)是一种慢性、复发性的炎症性肠病,全球发病率持续上升。其核心特征是结肠黏膜炎症、溃疡形成和上皮屏障功能受损,但导致上皮屏障初始损伤的驱动因素一直不明确。
本研究创新性地将关注点从上皮细胞转向肠道固有巨噬细胞,提出巨噬细胞功能受损可能先于上皮炎症的假说。
人类样本:收集UC患者和健康对照的结肠组织及粪便,通过免疫组化、流式细胞术和Western blot分析巨噬细胞数量及分布。
细菌筛选:培养UC患者粪便细菌,测试其培养上清对巨噬细胞的毒性,并通过质谱鉴定关键毒素。
小鼠模型:使用化学(氯膦酸盐脂质体)或遗传(CX3CR1-iCre介导的巨噬细胞剔除)方法耗竭巨噬细胞,结合DSS(葡聚糖硫酸钠)或IL-10敲除小鼠诱导结肠炎。
分子机制:通过重组气溶素蛋白、基因敲除菌株(Δaer MTB)和抗体中和实验验证气溶素的作用。
检测技术:包括实时PCR检测MTB定植、单细胞RNA干扰筛选GPI锚定蛋白、以及单克隆抗体治疗评估。
图解摘要
研究团队首先观察了UC患者的结肠组织,发现一个关键现象:在尚未出现明显上皮损伤的“完整区域”,皮下巨噬细胞(CD68+标记)的数量显著减少(降幅达67%),而炎症性巨噬细胞和适应性免疫细胞(如B细胞)仅在已发炎区域增多【图1A-C】。这表明巨噬细胞的耗竭可能早于上皮屏障的破坏,是UC的早期事件。
为了验证巨噬细胞耗竭的功能意义,团队在小鼠模型中通过化学(氯膦酸盐脂质体)或遗传(CX3CR1+细胞特异性清除)方法耗竭结肠巨噬细胞。
结果发现,尽管巨噬细胞耗竭本身不引发自发结肠炎,但会使小鼠对低剂量葡聚糖硫酸钠(DSS)的损伤异常敏感,导致更严重的体重下降、结肠缩短和炎症细胞浸润(如B细胞增多和炎性因子上调)。这提示巨噬细胞屏障是抵御肠道刺激的关键防线,其缺失可能是UC的“导火索”【图1H-M】。
图1.溃疡性结肠炎(UC)患者结肠上皮固有巨噬细胞减少,且在动物模型中可导致对DSS的易感性
既然气溶素来自肠道菌群,那么是哪种细菌分泌的?研究人员从UC患者粪便中分离出五株能分泌气溶素的菌株,命名为Aeromonas sp. MTB(巨噬细胞毒性细菌)【图2A- D】。
体外实验显示,巨噬细胞对气溶素的敏感性比肠道上皮细胞高出20-80倍!这意味着气溶素能精准地攻击巨噬细胞,而不太会直接伤及上皮细胞【图2H, I】。这完美解释了为何在UC早期,巨噬细胞会先于上皮细胞受损。
通过培养和基因测序,他们从UC患者粪便中成功分离出了产生这种气溶素的细菌,并将其命名为巨噬细胞毒性细菌(MTB)。系统发育分析表明,MTB是气单胞菌属的一个新变种,与已知的维氏气单胞菌亲缘关系最近但又截然不同【图2J-L】。
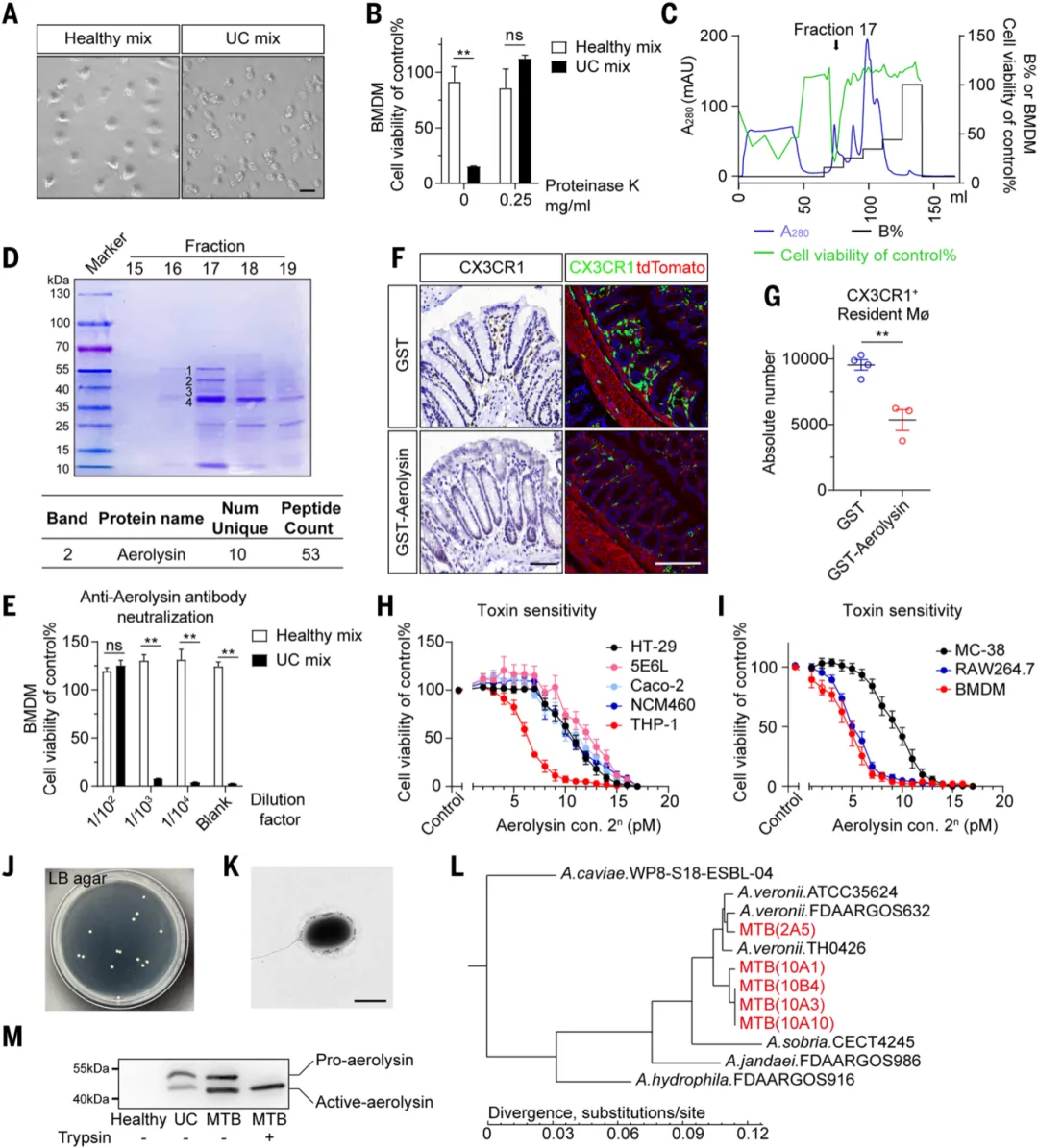
图2.巨噬细胞对气单胞菌属MTB分泌的气溶素具有超敏反应
MTB能否在活体内复制人类UC的特征?团队发现,正常小鼠口服MTB后无法长期定植,但在抗生素(AVNM cocktail)或DSS预处理造成的肠道环境紊乱下,MTB能成功定植并持续存在。定植后的小鼠表现出进行性结肠炎:体重减轻、血性腹泻、结肠缩短,以及组织学上的隐窝扭曲和炎症浸润【图3A-D】。
免疫组化显示,MTB处理的小鼠结肠上皮下的CX3CR1+巨噬细胞几乎消失,而对照组巨噬细胞排列整齐【图3E-F】。病理切片显示,MTB组结肠有大量炎症细胞浸润、隐窝扭曲、脓肿形成,病理评分显著高于对照组【图3G-H】。若预先用Clod-Lip耗竭巨噬细胞,MTB就无法加重DSS诱导的结肠炎,说明MTB正是通过破坏巨噬细胞防线来诱发炎症【图3I-K】。
图3.MTB给药诱导了溃疡性结肠炎样表型及免疫应答
在IL-10敲除小鼠(易自发结肠炎模型)中,MTB同样加速了疾病进展,且这一过程不依赖DSS,凸显了MTB在遗传易感背景下的致病力。有趣的是,无菌小鼠中MTB不诱发结肠炎,表明其致病需要肠道菌群的协同作用【图3L-S】。
图3.MTB给药诱导了溃疡性结肠炎样表型及免疫应答
为确认气溶素是MTB的关键毒力因子,研究人员构建了气溶素缺陷的MTB突变体(Δaer MTB)。结果发现,Δaer MTB对培养的巨噬细胞完全无毒性【图4A-B】。
体内实验中,Δaer MTB处理的小鼠结肠上皮下巨噬细胞完好无损,结肠炎症状轻微,结肠长度正常,病理评分低;而野生型MTB处理的小鼠出现严重结肠炎【图4C-J】。
通过互补实验重新引入气溶素后,Δaer MTB恢复了诱发结肠炎的能力【图4L-P】。这充分证明:气溶素是MTB诱发UC的“致命武器”,没有它,MTB就无法破坏巨噬细胞防线。
图4.气溶素(Aerolysin)对结核分枝杆菌(MTB)诱导的巨噬细胞破坏及结肠炎具有不可或缺的作用
为验证MTB与UC的临床关联,研究人员检测了79例UC患者、430例健康人、38例CD患者的粪便样本。结果显示,72.15%的UC患者粪便中能检测到Aeromonas属细菌,而健康人仅为11.86%,CD患者仅2.63%【图5A】。地理分布覆盖中国12个省份,说明MTB与UC的关联具有普遍性【图5B】。
更直接的证据来自UC患者的结肠组织:免疫组化显示,40%的UC结肠组织中能检测到气溶素蛋白,主要分布在黏膜和肌层的CD68+巨噬细胞周围;而正常结肠组织中完全没有气溶素表达【图5C】。
Western blot进一步证实,UC结肠黏膜和肌层中存在气溶素蛋白,而正常组织中几乎检测不到【图5D-E】。这些临床数据为MTB与气溶素作为UC的生物标志物提供了有力支持。
图5.溃疡性结肠炎(UC)粪便中分枝杆菌(MTB)的存在及UC结肠组织中气溶素蛋白的检测
既然气溶素是关键毒力因子,中和气溶素能否治疗UC?研究人员探索了靶向治疗策略,用抗气溶素多克隆抗体预处理小鼠,再给予MTB。
结果令人振奋:抗体处理的小鼠完全没有出现结肠炎症状,体重稳定,DAI评分正常,结肠长度正常,病理评分低,上皮下巨噬细胞完好无损,炎性细胞因子表达与对照组无异【图6A-J】。这说明抗气溶素抗体能有效预防MTB诱导的结肠炎。
对于已建立的结肠炎,抗气溶素单克隆抗体也能起到缓解作用:治疗后小鼠的体重下降幅度减小,DAI评分降低【图6K-M】。虽然单克隆抗体的疗效不如多克隆抗体显著,但为UC的治疗提供了新方向——靶向气溶素的生物制剂。
图6.抗气溶胶素抗体减轻MTB诱导的结肠炎
Significance and Innovations 这项研究首次将Aeromonas sp. MTB及其气溶素毒素确立为UC发病的关键环境因子,揭示了“微生物-巨噬细胞-上皮屏障”的破坏轴心。不仅深化了对UC起源的理解,还提出了从诊断(检测MTB或气溶素)到治疗(抗体中和)的转化路径。未来,针对气溶素的策略或可弥补当前免疫抑制疗法的不足,为UC患者带来新希望。
如果你也想进行“国自然热点”的研究,复现高分思路,欢迎联系,生信云分析,科研好助力!