Cell reports | 南京大学庄君龙/郭宏骞/刁文丽团队揭示驱动膀胱癌的转移与化疗耐药的调控新机制
- 2026-03-25 13:26:43
点击蓝字
关注我们

2026年2月3日,南京大学庄君龙、郭宏骞及刁文丽共同通讯,在Cell Reports 在线发表题为“Delactylation of the tumor suppressor ARHGDIB drives metastasis and chemoresistance in bladder cancer” 的研究论文。
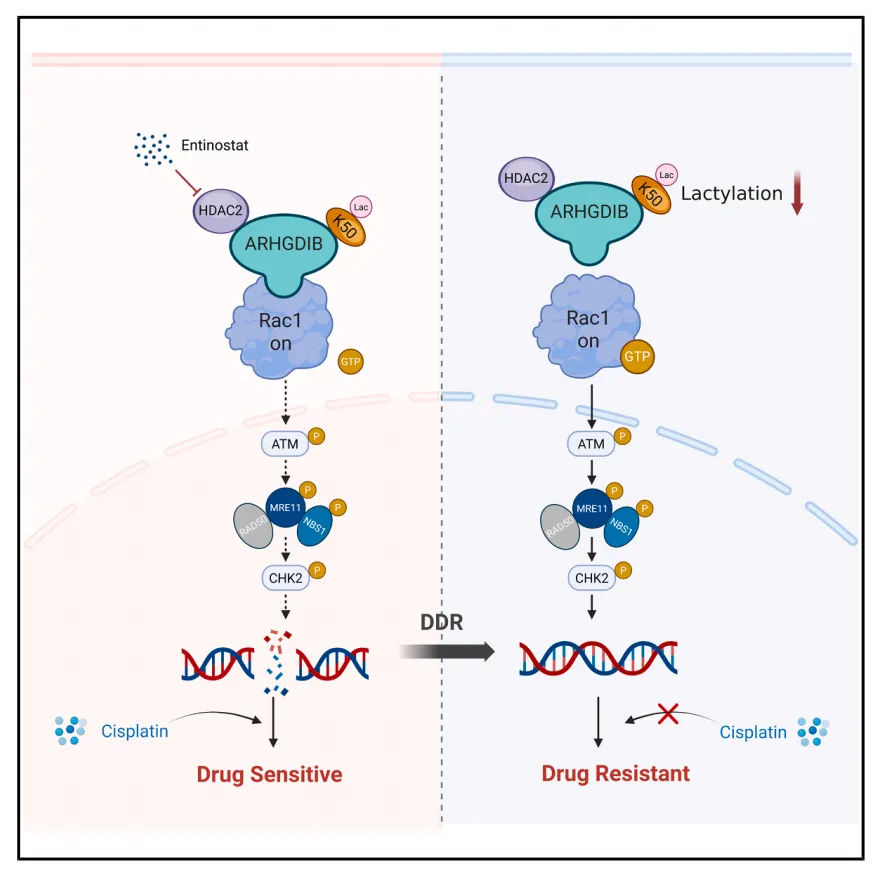
研究通过整合乳酰化修饰组学与蛋白质组学分析,系统描绘了膀胱癌中赖氨酸乳酰化的全局图谱,并鉴定出Rho二磷酸鸟苷解离抑制因子β(ARHGDIB)K47与K50位点为关键乳酰化修饰位点。研究发现,HDAC2介导的去乳酰化修饰会削弱ARHGDIB的抑癌功能,从而促进膀胱癌转移并诱导顺铂耐药。
机制层面:
ARHGDIB去乳酰化显著降低其与Rac1的结合亲和力,促进Rac1向细胞膜易位并被激活;
随后通过Rac1–MRN–ATM–CHK2信号轴增强肿瘤细胞DNA损伤修复能力,从而驱动化疗耐受形成。
临床相关性:
ARHGDIB-K50乳酰化水平降低与膀胱癌顺铂耐药及患者不良预后显著相关;
I类HDAC抑制剂恩替诺特(entinostat)可抑制ARHGDIB去乳酰化,并与顺铂产生协同抗肿瘤效应。
总体而言,本研究揭示抑癌蛋白去乳酰化驱动肿瘤转移与化疗耐药的全新分子机制,并提出通过HDAC抑制剂调控乳酰化动态变化作为膀胱癌精准治疗的潜在干预策略,为克服顺铂耐药提供了重要理论依据与转化方向。
Highlights
膀胱癌中蛋白质赖氨酸乳酸化的首次全球性分析
arhgdib去乙酰化会减弱其与Rac1的结合并增强Rac1活性
arhgdib去乙酰化促进膀胱癌转移及化疗耐药
靶向HDAC2介导的arhgdib去乙酰化可增强顺铂疗效
Abstract
01
摘要

Results
02 主要研究结果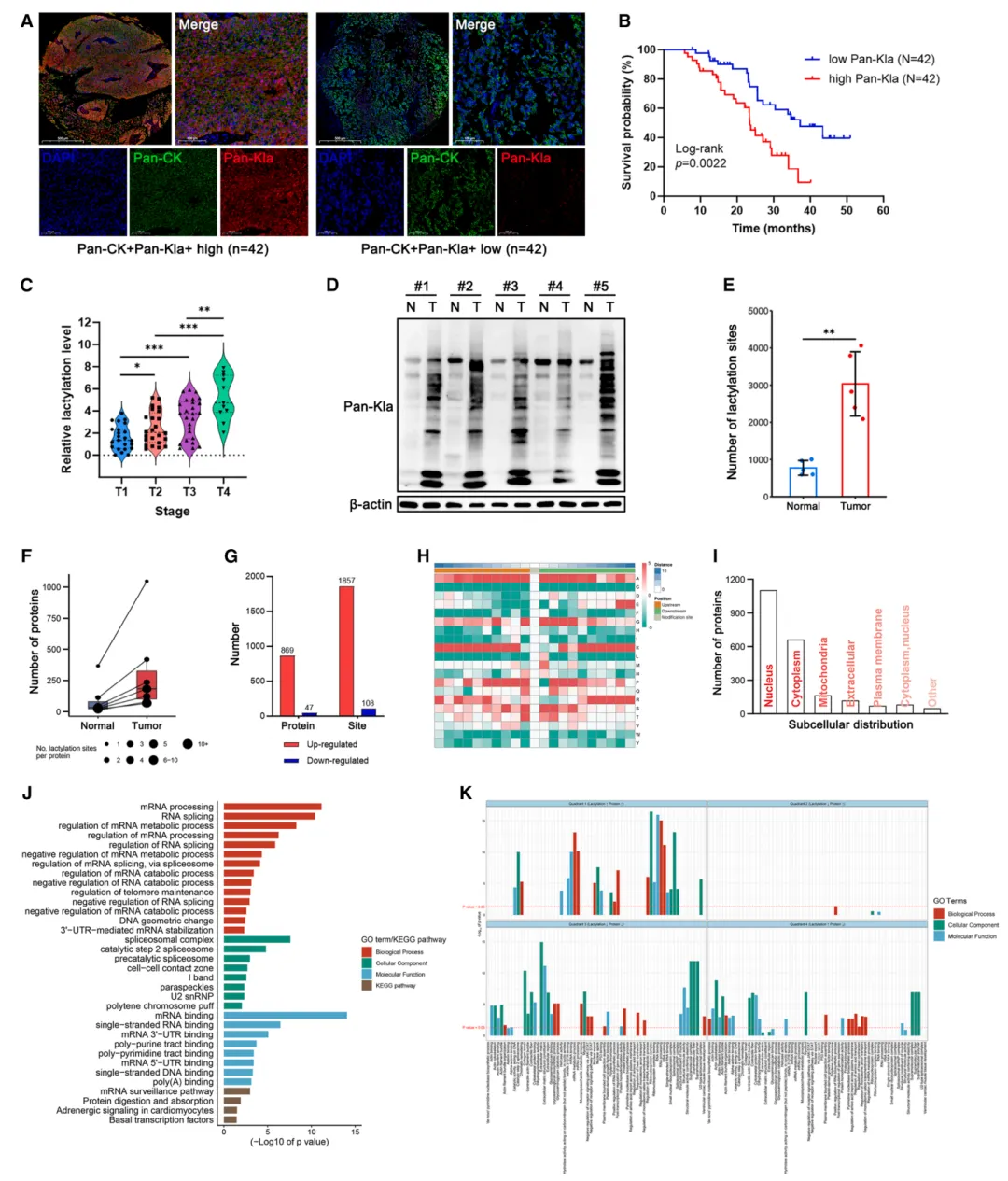
图1.膀胱癌中蛋白质赖氨酸乳酰化特征及临床意义(A)膀胱癌组织Pan-Kla的代表性多重免疫染色图像(左图:Pan-CK+Pan-Kla+高密度;右图:Pan-CK+Pan-Kla+低密度)。比例尺:左上500 μm ,其余四幅100 μm 。(B)按Pan-CK+Pan-Kla+密度分层的队列总生存期Kaplan-Meier曲线(Pan-CK+Pan-Kla+高密度组,n=42;Pan-CK+Pan-Kla+低密度组,n=42)。(C) 我们队列中膀胱癌患者Pan-Kla水平与肿瘤分期的相关性。(D) 使用Pan-Kla抗体进行免疫印迹检测旁系组织与肿瘤组织中整体蛋白质乳化水平。(E) 正常组织与肿瘤组织中鉴定出的Kla位点数量箱线图。(F) 肿瘤组织与邻近肝脏中每种蛋白质的Kla位点数量。箱线图中心点代表中位数,下铰和上铰分别代表第一和第三四分位数(第25和75百分位数)。须线延伸至最大值和最小值。(G) 条形图显示正常组织与肿瘤组织间差异表达蛋白质及乳化位点的数量。(H) 热图展示乳化赖氨酸残基上游-10至下游+10位点不同氨基酸类型的基序分析。不同颜色代表各残基的偏好性(红色表示较高频率,蓝色表示较低频率)。(I) 所有鉴定出的乳化蛋白质的亚细胞定位。(J) 差异乳化蛋白质的通路富集分析。显示校正后p值<0.01的通路。(K) 条形图展示各象限中校正后p值<0.01的高表达通路,以及肿瘤组织与正常组织相比Kla位点的相应改变。
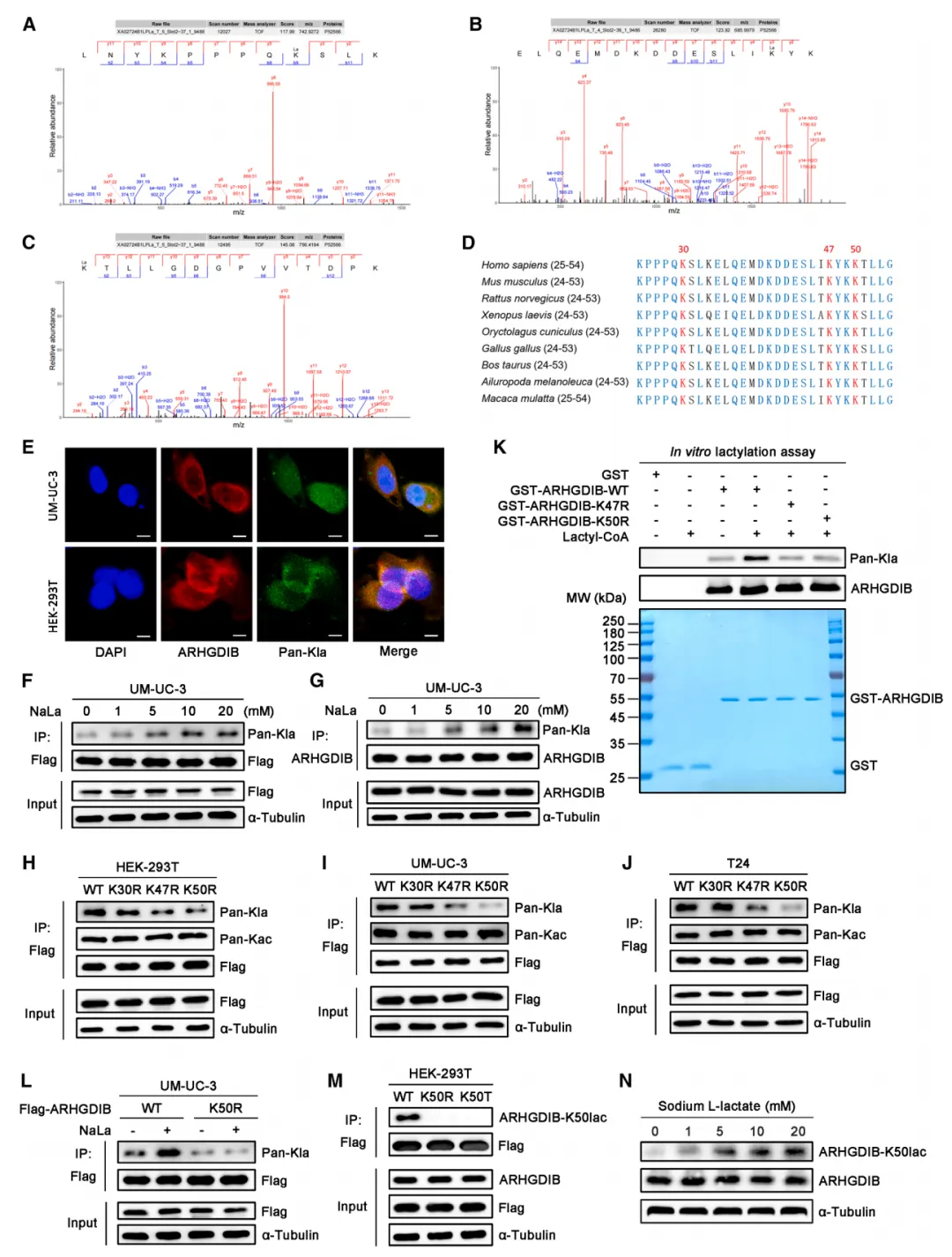
图2.arhgdib在K47和K50位点发生乳酰化。(A-C)通过LC-MS/MS分析获得的arhgdib乳酰化位点的MS/MS谱图及提取离子色谱图。(D)不同物种间arhgdib氨基酸残基的序列比对。(E)UM-UC-3和 HEK -293T细胞中内源性arhgdib与Pan-Kla的免疫荧光(IF)检测。比例尺:50 μm 。(F和G) UM-UC-3细胞经不同浓度NaLa处理24小时后,内源性arhgdib与外源性FLAG标签arhgdib的乳酰化水平。(H-J) 在表达载体、FLAG标签arhgdib-WT、K30R、K47R或K50R的 HEK -293T、UM-UC-3及T24细胞中进行免疫沉淀实验,随后使用抗FLAG和抗泛Kla抗体进行免疫印迹分析。(K) 体外arhgdib乳酰化实验。将纯化的GST、GST-arhgdib-WT及K47R或K50R与乳酰辅酶A共孵育或不共孵育,通过蛋白质印迹法检测arhgdib的Kla水平。(L) UM-UC-3细胞表达FLAG标签arhgdib-WT或K50R时,NaLa(25 mM)存在或不存在条件下的arhgdib乳酰化水平。(M) 在表达FLAG标签arhgdib-WT或K50R的 HEK -293T细胞中进行免疫沉淀实验,随后使用特异性识别arhgdib-K50lac的抗体进行免疫印迹分析。(N) 经不同浓度NaLa处理24小时的 HEK -293T细胞中arhgdib及arhgdib-K50lac的水平。
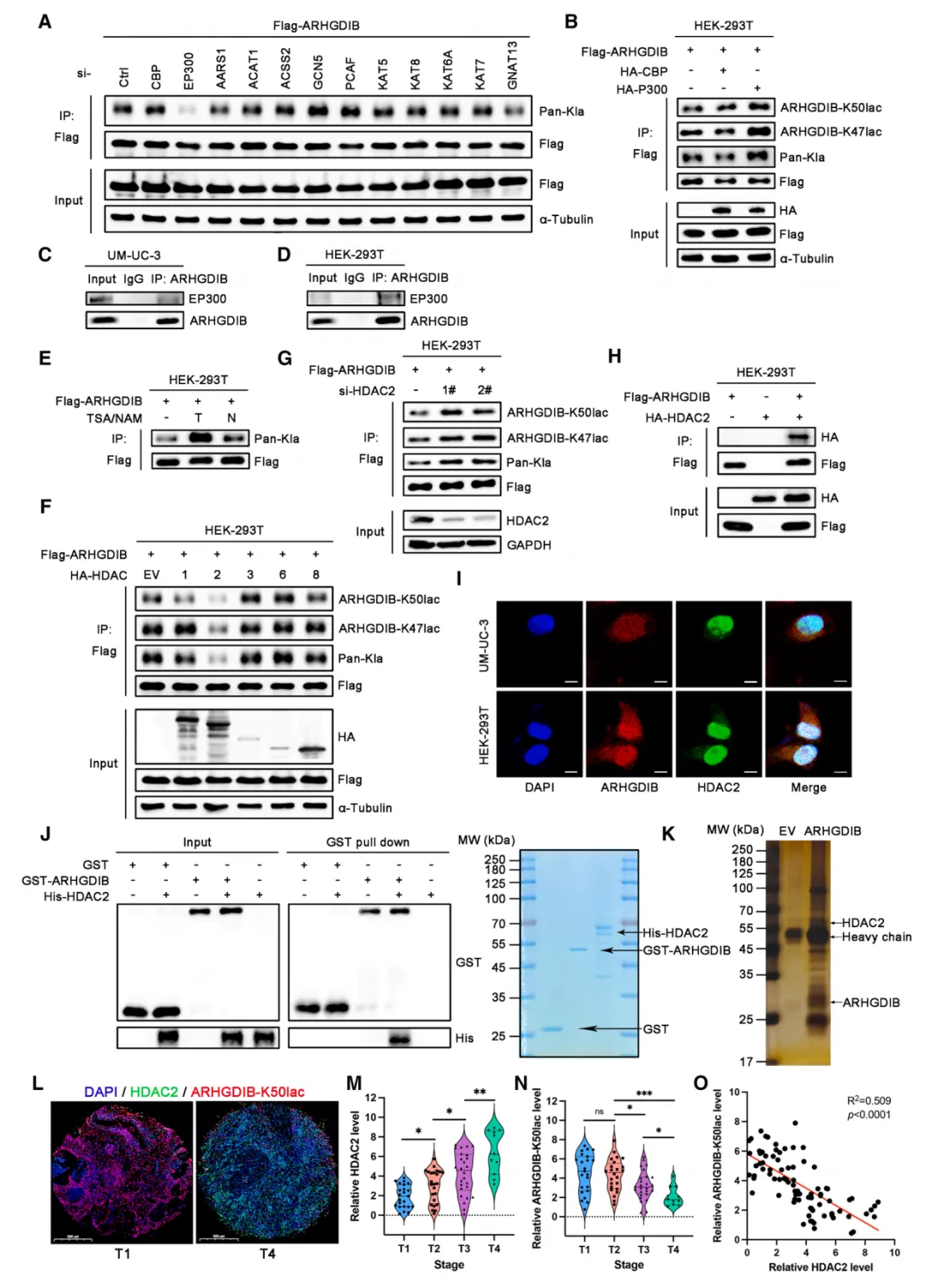
图3.鉴定P300为arhgdib的乳酰基转移酶,HDAC2为delactylase。(A)转染对照siRNA或指定乳酰基转移酶siRNA48小时的 HEK -293T细胞中FLAG-arhgdib与泛Kla表达的免疫沉淀(IP)分析。(B)转染FLAG标记arhgdib与HA标记CBP或P300的 HEK -293T细胞IP实验,随后用指定抗体进行免疫印迹。(C和D)UM-UC-3和 HEK -293T细胞中ahrgdib与P300内源性相互作用的共免疫沉淀(coIP)分析。(E) 通过免疫沉淀(IP)结合蛋白质印迹法检测经NAM(烟酰胺)或TSA(曲古抑菌素A)处理的 HEK -293T细胞中FLAG标签arhgdib的蛋白水平。(F) HEK -293T细胞共转染FLAG标签arhgdib与HA标签HDAC1、2、3、6、8,采用抗FLAG抗体进行IP检测,并通过蛋白质印迹法分析乳酰化水平。(G) 对转染FLAG标签arhgdib及靶向HDAC2的siRNA的 HEK -293T细胞进行IP实验,随后使用指定抗体进行免疫印迹分析。(H) 共免疫沉淀实验验证外源性FLAG标签arhgdib与HA标签HDAC2在 HEK -293T细胞中的相互作用。(I) UM-UC-3和 HEK -293T细胞中内源性arhgdib与HDAC2的免疫荧光(IF)检测。比例尺:50 μm 。(J) GST下拉实验中GST标签arhgdib与His标签HDAC2的代表性免疫印迹及考马斯亮蓝(CBB)染色结果。(K) 使用表达FLAG标签arhgdib的UM-UC-3细胞进行IP实验,并进行银染检测。(L) 膀胱癌组织中HDAC2与arhgdib-K50lac的多重免疫染色代表性图像(左图:T1期,HDAC2低表达而arhgdib-K50lac高表达;右图:T4期,HDAC2高表达而arhgdib-K50lac低表达)。比例尺:500 μm 。(M)本队列膀胱癌患者HDAC2水平与肿瘤分期的相关性。(N)本队列膀胱癌患者arhgdib-K50lac水平与肿瘤分期的相关性。(O)散点图显示HADC2与arhgdib-K50lac的相对表达水平,图中实线为回归线。
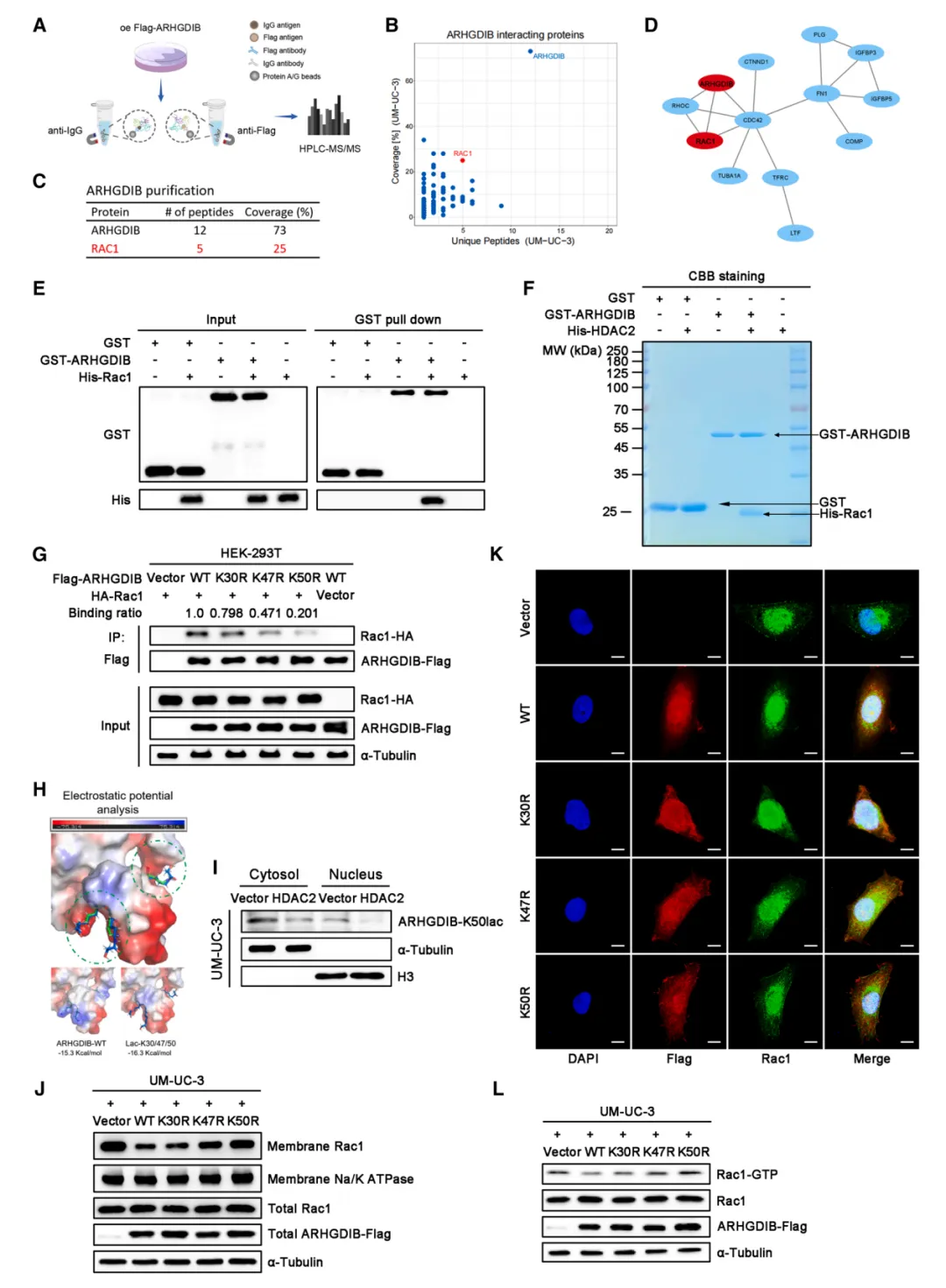
图4.arhgdib去乙酰化作用减弱其与Rac1的结合。(A-C)使用抗FLAG抗体的免疫沉淀质谱(IP-MS)示意图,用于鉴定与arhgdib相互作用的蛋白。Rac1在相互作用蛋白中排名首位并以红色标注。(D)基于STRING数据库的arhgdib蛋白质相互作用网络分析。(E和F)纯化的GST-arhgdib与His-Rac1孵育后,进行GST下拉实验,并采用抗His抗体和 CBB 染色进行免疫印迹分析。(G) HEK -293T细胞共转染HA标签Rac1与FLAG标签的arhgdib-WT、K30R、K47R或K50R,随后通过抗FLAG抗体进行免疫沉淀,并使用指定抗体进行免疫印迹。(H) arhgdib-WT和arhgdib-Lac-K30/47/50中与Rac1相互作用的K30、K47和K50周围蛋白区域的电荷分布及结构建模。arhgdib-WT和arhgdib-Lac-K30/47/50的结合自由能分别为15.3和16.3 kcal/mol。(I) 转染载体和HDAC2的UM-UC-3细胞中,arhgdib-K50lac在胞质和核组分中的免疫印迹。 α -微管蛋白作为胞质标记物,组蛋白H3作为核标记物。(J) 转染载体、FLAG标签arhgdib-WT、K30R、K47R或K50R的UM-UC-3细胞中Rac1在总蛋白和膜组分中的免疫印迹。(K) 使用抗FLAG和抗Rac1抗体进行免疫荧光分析的代表性图像,显示转染FLAG标签arhgdib-WT或其突变体的UM-UC-3细胞中Rac1的膜转位。比例尺为50 μm 。(L) 转染载体、FLAG标签arhgdib-WT、K30R、K47R或K50R的UM-UC-3细胞中总Rac1和活性Rac1(Rac1-GTP)的免疫印迹。
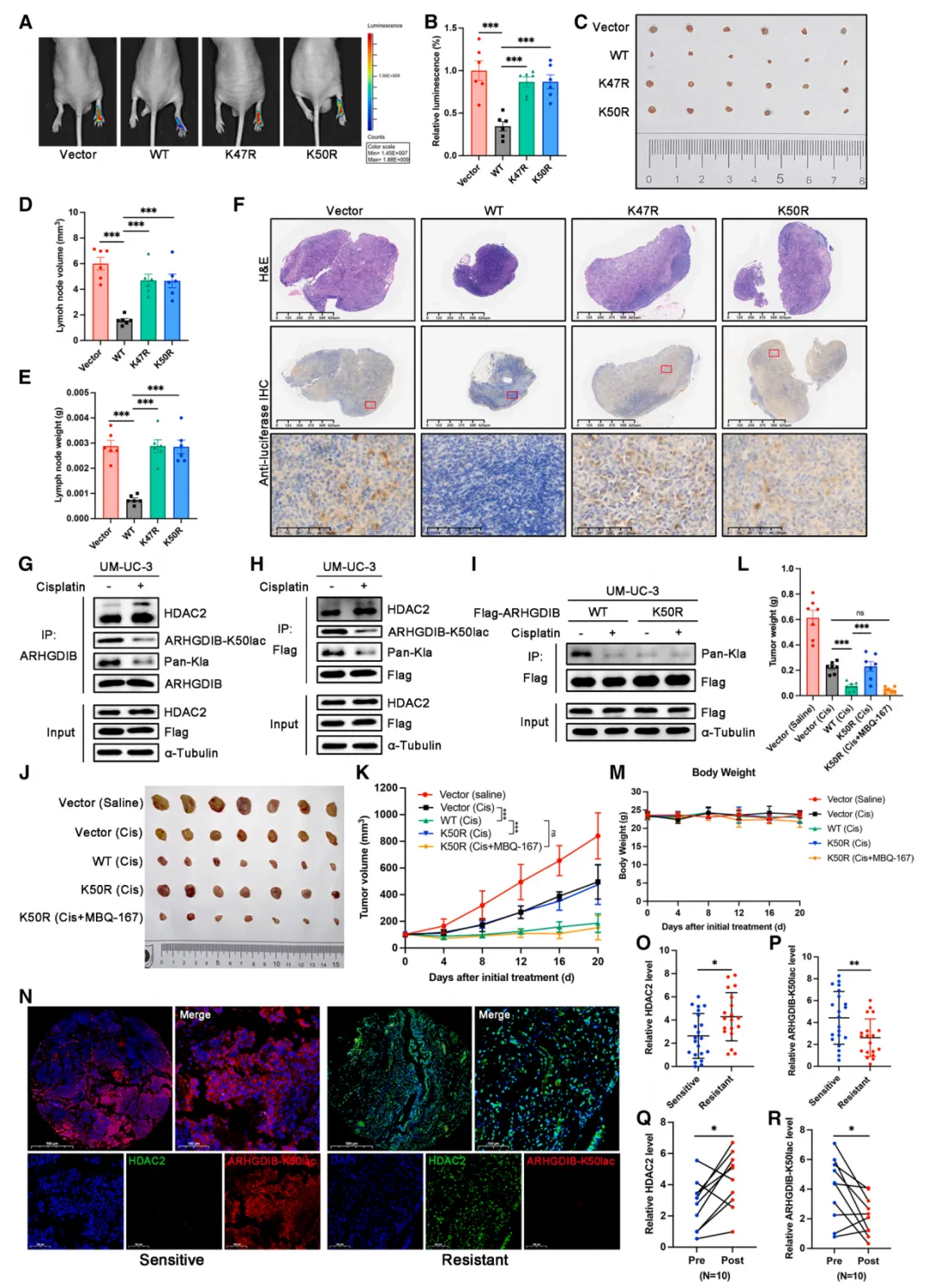
图5. arhgdib去乙酰化促进膀胱癌转移及顺铂耐药性。(A和B)腓肠淋巴结生物发光代表性图像(A),及各组发光强度的直方图分析(B)。每组n=6个生物学重复。(C–E)腓肠淋巴结剜除代表性图像,及各组淋巴结体积与重量的直方图分析。每组n=6个生物学重复。(F) 各组腘窝淋巴结经H&E染色及 IHC 染色后,使用抗荧光素酶抗体的代表性图像。每组n=6个生物学重复。比例尺:上中两行625 μm ,下一行50 μm 。(G和H) 对经顺铂(10 μM)处理24小时的UM-UC-3细胞进行内源性(G)与外源性(H)arhgdib的免疫沉淀实验,随后采用指定抗体进行免疫印迹分析。(I) 对转染FLAG标签的arhgdib-WT或K50R的UM-UC-3细胞进行FLAG免疫沉淀实验,处理方式同上,随后采用指定抗体进行免疫印迹分析。(J–M) 将指定UM-UC-3细胞皮下注射至裸鼠体内,监测并测量肿瘤生长(K)、肿瘤重量(L)及体重(M)。每组n=7个生物学重复。(N) 新辅助顺铂敏感(左图:低HDAC2+高arhgdib-K50lac+密度)与耐药(右图:高HDAC2+低arhgdib-K50lac+密度)膀胱癌标本中HDAC2与arhgdib-K50lac表达的代表性多重免疫组化图像。比例尺:500 μm(左上)和100 μm(其余四张图像)。(O和P)新辅助顺铂敏感性膀胱癌组织(n=21)与耐药性膀胱癌组织(n=19)中HDAC2(O)和arhgdib-K50lac(P)多重免疫染色水平的定量分析。(Q和R)配对样本(n=10)中新辅助顺铂治疗前后HDAC2(Q)和arhgdib-K50lac(R)多重免疫染色水平的定量分析。
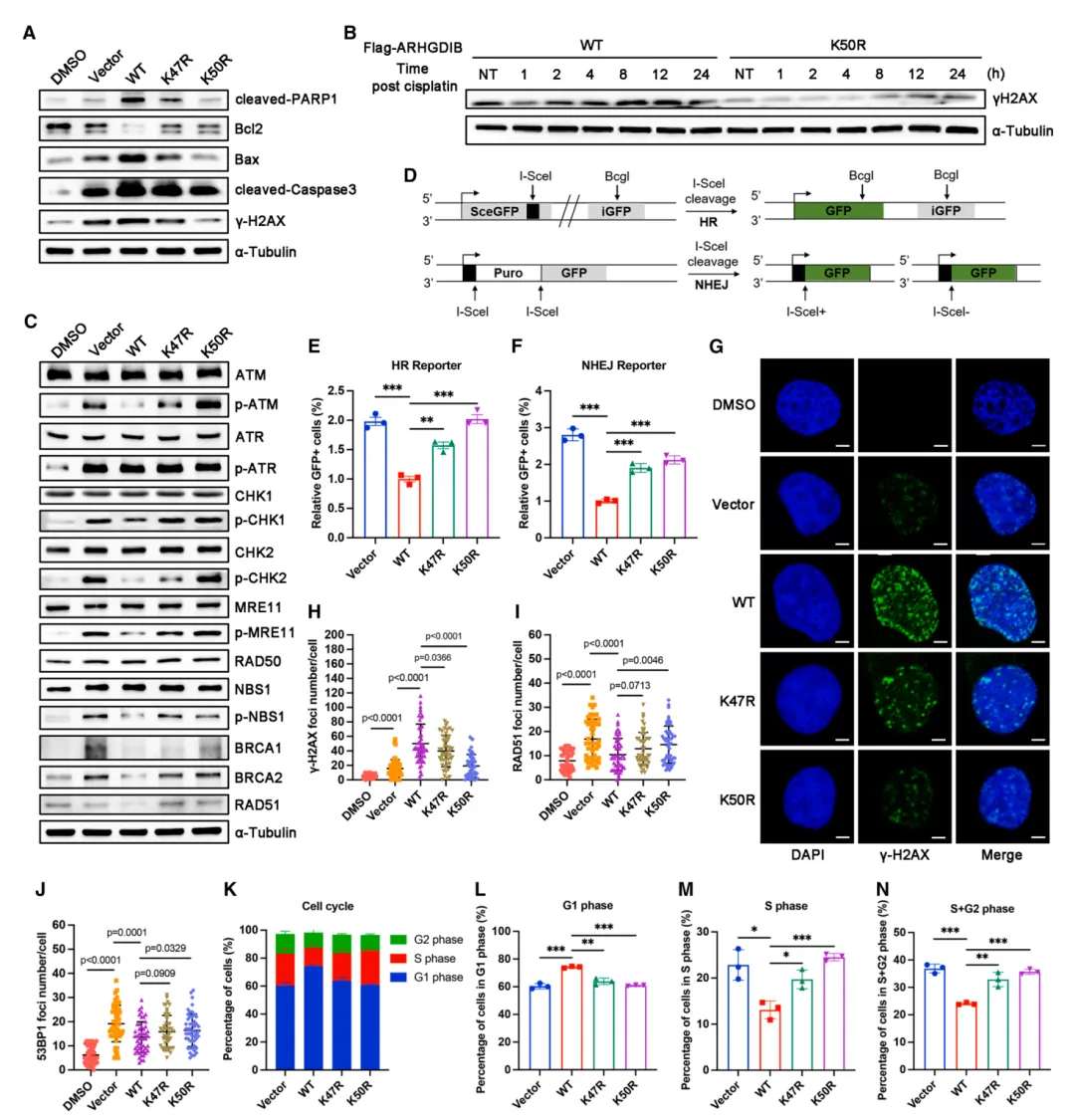
图6. arhgdib去乙酰化通过Rac1- MRN 复合物-ATM-CHK1/CHK2轴增强DNA损伤应答(DDR)(A)Western blot分析显示经DMSO和顺铂(10 μM)处理的指定UM-UC-3细胞。(B)Western blot检测顺铂(10 μM)处理的指定UM-UC-3细胞中 γ -H2AX表达随时间变化的动态变化。(C)Western blot分析DMSO和顺铂(10 μM)处理的指定UM-UC-3细胞中DDR相关蛋白的表达。(D)基于 GFP 的同源重组(HR)报告基因检测系统(DR- GFP)和 NHEJ 报告基因检测系统(EJ5- GFP)的示意图。(E和F)指定组别 HEK -293T细胞的相对HR(E)和 NHEJ (F)修复效率。每组n=3个生物学重复。(G和H)DMSO和顺铂(10 μM)处理的指定UM-UC-3细胞中 γ -H2AX焦点的代表性免疫荧光(IF)图像及定量数据。每组n=50个细胞。比例尺:50 μm 。(I和J)经DMSO和顺铂(10 μM )处理的指定UM-UC-3细胞中RAD51焦点(I)和53BP1焦点(J)的定量数据。每组n=50个细胞。(K–N)指定组别UM-UC-3细胞的细胞周期分析。每组n=3个生物学重复。
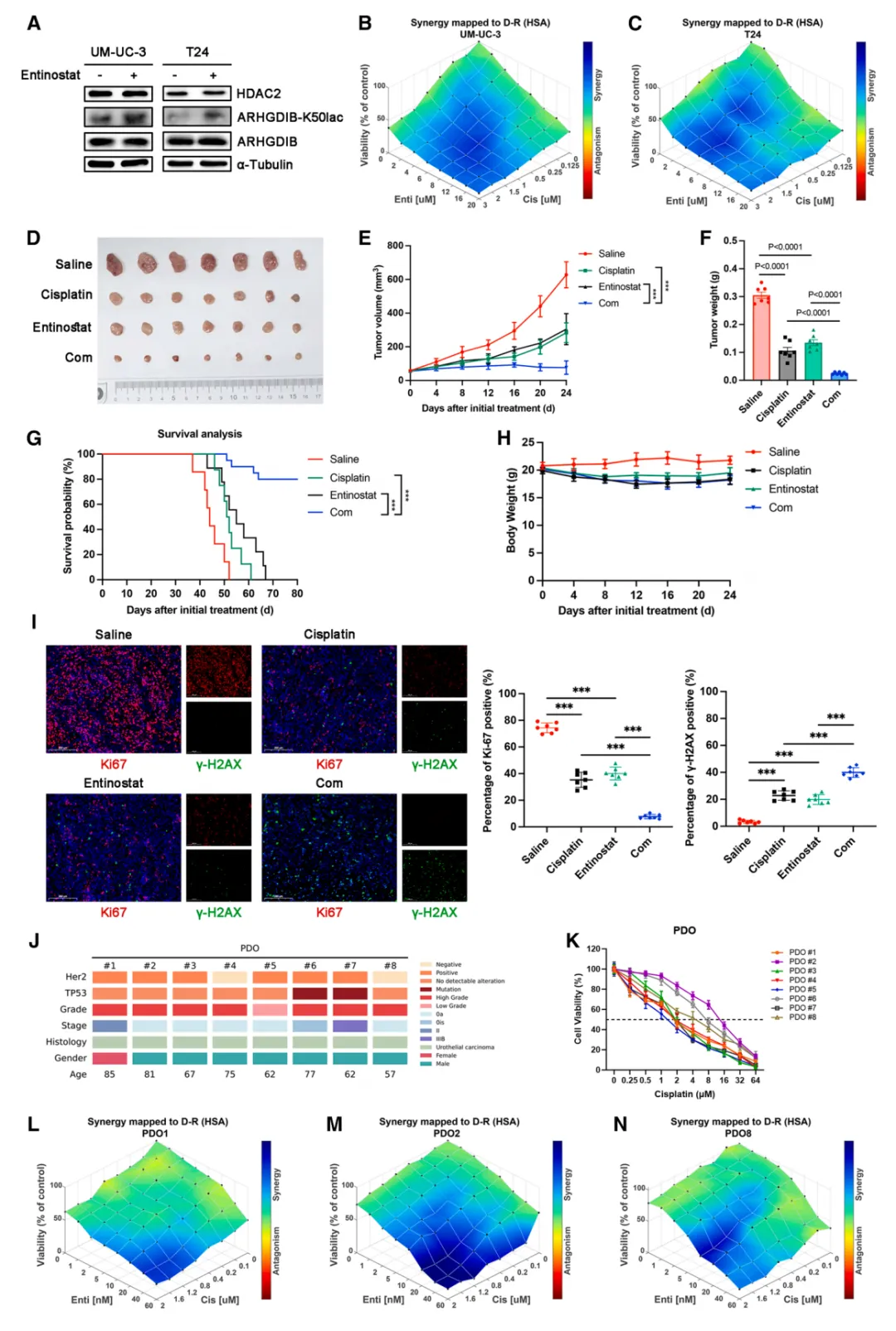
图7.Entinostat与顺铂在膀胱癌异种移植模型及PDOs中的协同作用。(A)Westernblot分析显示,经Entinostat(5 μM)处理或未处理的UM-UC-3和T24细胞。(B和C)UM-UC-3(B)和T24细胞(C)按指定方法处理48小时后,通过 CCK -8法检测细胞活力。协同作用图使用Combenefit(HSA)生成。(D-F) 在指定治疗组中监测并测量了UM-UC-3皮下模型的肿瘤生长(D和E)及肿瘤重量(F)。每组n=6个生物学重复。(G和H) 指定治疗组中移植UM-UC-3细胞的NSG小鼠的生存曲线分析(G)及体重变化(H)。(I) 指定组别切除肿瘤样本的Ki67(红色)和 γ -H2AX(绿色)免疫荧光染色代表性图像及定量数据。每组n=7个生物学重复。比例尺为200 μm 。(J) 8例新诊断膀胱癌患者的PDOs特征。(K) 8例PDOs经顺铂处理48小时后的细胞活力。(L-N) 指定PDOs按指定方案处理48小时后,通过 CCK -8法分析细胞活力。协同效应图使用Combenefit(HSA)模型生成。
文献学习脑图总结:
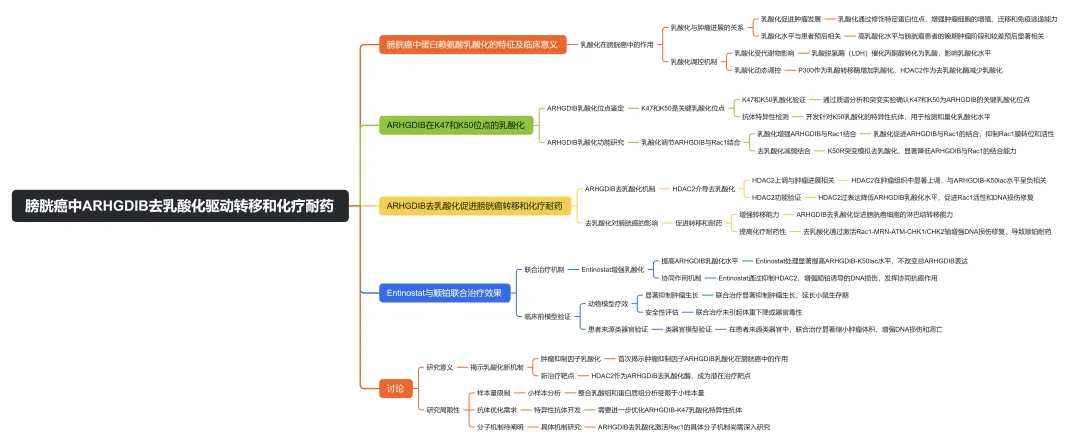
以上内容均来自期刊官网、Pubmed平台,本公众号仅做整理分享。
推荐阅读:
Gut|复旦大学附属中山医院周俭院士和杨欣荣教授团队发表CD177+中性粒细胞能够驱动肝再生最新研究结果

专业医药科研服务商
文献PDF请识别下方二维码直接下载
Delactylation of the tumor suppressor ARHGDIB drives metastasis and chemoresistance in bladder cancer.pdf

近期如有需要发表SCI可以咨询,留下你的研究方向,可走加急辅导!!
