在抗生素耐药性成为全球健康危机的当下,南京农业大学团队在《Journal of Advanced Research》发表突破性研究。他们利用深度学习模型,从反刍动物胃肠道微生物组的120个宏基因组和10,373个基因组中筛选出27,192种潜在抗菌肽(AMPs),并通过生物信息学分析锁定39个候选物。其中,肽4(Peptide 4)表现出对耐甲氧西林金黄色葡萄球菌(MRSA)的强效抑制作用(MIC低至16μg/ml),且在小鼠伤口感染模型中显著促进愈合。研究进一步揭示,肽4通过破坏细菌细胞膜发挥杀菌作用,不易诱发耐药性,且对哺乳动物细胞无毒。这项工作凸显了“AI+微生物组”策略在挖掘新型抗菌疗法中的巨大潜力,为应对MRSA感染提供了新思路。
引言:抗生素耐药的阴影下,反刍动物肠道成新希望
当抗生素在超级细菌面前逐渐失效时,科学家们开始将目光投向自然界中更古老的抗菌武器——抗菌肽(AMPs)。反刍动物如牛、羊的胃和肠道,是一个充满微生物战争的江湖:这里pH值多变、氧气分布不均,数以亿计的细菌在此争夺地盘。为了生存,它们分泌抗菌肽来压制竞争对手。南京农业大学团队想到:能否从这个天然“军火库”中,找到对抗MRSA的利器?
图1:深度学习模型通过整合BERT、CNN和LSTM模块,实现了对抗菌肽的高精度识别,其曲线下面积(AUC)高达0.99,远超传统方法。
方法篇:AI如何从2300万条序列中“大海捞针”?
研究团队首先构建了一个深度学习模型,其核心如同一个智能过滤器:先用BERT模块理解氨基酸序列的“语言逻辑”,再用CNN捕捉局部特征,LSTM分析长程依赖关系。模型在包含2.8万条已知抗菌肽的数据集上训练后,对反刍动物胃肠道微生物组中的2300万条小开放阅读框(sORFs)进行筛查。最终,27,192条潜在抗菌肽被初步锁定。但难题接踵而至——这些肽中,哪些是细菌真正分泌到环境中起效的?
团队引入13个反刍动物胃肠道的宏蛋白质组数据库进行比对,仅保留与实测蛋白质高度匹配的序列。这一筛选如同“沙中淘金”,确保候选肽不仅存在于基因中,更在真实环境中活跃。
图2:厚壁菌门和拟杆菌门是产抗菌肽的主力军,且其分布具有明显的区域特异性,例如胃部细菌更易产生多肽4这类高效抗菌物。
发现之旅:肽4的“杀机”与温柔
从39个合成肽中,肽4脱颖而出。它对MRSA的抑制浓度(MIC)仅为16μg/ml,而对其他病原体如大肠杆菌也表现出广谱活性。更令人惊喜的是,肽4对哺乳细胞“温柔以待”:即使浓度升至32倍MIC,对小鼠和牛红细胞的溶血率仍低于15%,且对肠道上皮细胞无毒性。在时间杀伤实验中,4倍MIC的肽4能在3小时内将MRSA彻底清除,而传统抗生素环丙沙星在26天内诱发了2048倍的耐药性,肽4却始终“稳如泰山”。
图3:肽4在高效杀菌的同时,对哺乳动物细胞几乎无影响,其安全性为临床转化奠定基础。
实战检验:小鼠伤口上的“微观战争”
为验证肽4的体内效果,团队构建了MRSA感染的小鼠伤口模型。结果令人振奋:每日局部涂抹肽4(1×MIC)14天后,伤口中MRSA菌落数下降1.8个对数单位,愈合率高达99.8%,优于常用药物莫匹罗星(97.2%)。组织切片显示,肽4组炎症细胞浸润显著减少,表皮修复完整。这一切表明,肽4不仅能杀菌,还能为组织修复创造有利环境。
图4:肽4治疗组在14天内几乎完全清除MRSA,并加速伤口愈合,展现其治疗潜力。
机制揭秘:肽4如何“破膜杀人”?
肽4的杀菌机制充满智慧。分子动力学模拟显示,它是一个两亲性α螺旋肽,带正电荷的末端先与细菌膜负电磷脂结合,疏水核心随即插入膜内,引发脂质紊乱。粗粒度模拟进一步发现,当两个肽4同时穿透膜时,会形成更大的水孔,导致内容物泄漏。这种“物理破防”方式使细菌难以通过突变产生耐药性,与传统抗生素的靶点机制截然不同。
图5:肽4通过破坏细菌膜完整性实现杀菌,这一机制不易诱发耐药性。
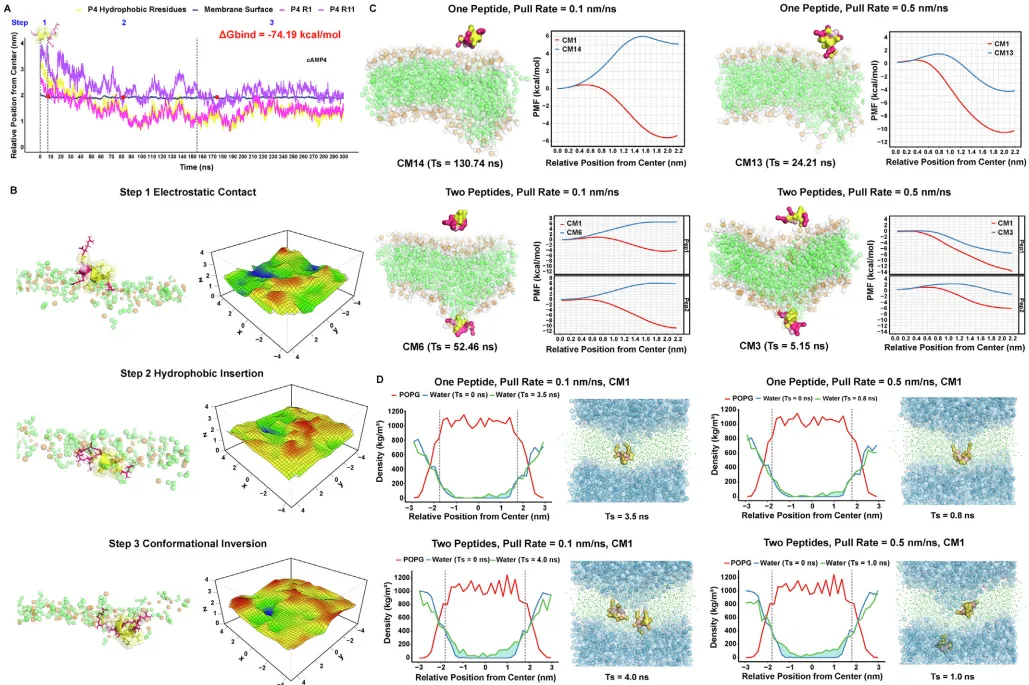
图5:模拟显示肽4的膜破坏过程分为吸附、插入和孔洞形成三阶段,其结合能低至-74.19 kcal/mol。
未来展望:从牛胃到临床,抗菌肽的星辰大海
尽管肽4的MIC高于某些天然抗菌肽,但研究者指出,化学合成可能未还原其天然修饰结构。若通过微生物表达系统生产成熟肽,活性有望进一步提升。此外,反刍动物胃肠道中尚有无数未知抗菌肽待挖掘。结合AI的加速能力,未来或可构建“抗菌肽库”,针对不同病原体定制疗法。这项研究不仅提供了对抗MRSA的新候选物,更开创了“深度学习+微生物资源”的药物发现范式。
重要参考文献
Mar Y et al. Identification of antimicrobial peptides from the human gut microbiome using deep learning. Nat Biotechnol. 2022.
核心内容:首次利用深度学习从人肠道微生物组中挖掘抗菌肽,为AI驱动抗菌肽发现提供范式。
Zasloff M. Antimicrobial peptides of multicellular organisms. Nature. 2002.
核心内容:系统阐述抗菌肽在生物界的分布与作用机制,奠定其作为抗生素替代品的基础。
Heilbronner S et al. The microbiome-shaping roles of bacteriocins. Nat Rev Microbiol. 2021.
核心内容:揭示细菌素通过调控微生物群落结构影响宿主健康,呼应本研究中AMP的生态功能。
Wang G et al. APD3: the antimicrobial peptide database as a tool for research and education. Nucleic Acids Res. 2016.
核心内容:提供全面抗菌肽数据库,支持本研究的生物信息学分析。
Yeaman MR et al. Mechanisms of antimicrobial peptide action and resistance. Pharmacol Rev. 2003.
核心内容:深入解析抗菌肽的膜靶向机制及耐药性演化规律,为肽4的机制研究提供理论支撑。
“当抗生素的智慧枯竭时,自然界的微观战争早已为我们备好答案——抗菌肽的利刃,既破膜杀菌,亦守护共生。”