南京中医药大学丨清肠化湿颗粒治疗溃疡性结肠炎新机制揭晓:靶向加氏乳杆菌介导的铁死亡通路
- 2026-05-18 03:10:44
本研究针对溃疡性结肠炎(UC)临床治疗困境,聚焦铁死亡与肠道菌群紊乱两大核心病理环节,以临床证实有效的中药复方清肠化湿颗粒(QCHS)为研究对象,先通过 DSS 诱导的 UC 小鼠模型验证 QCHS 的抗炎与肠屏障保护作用,再经 16S rDNA 测序与非靶向代谢组学锁定 QCHS 显著富集的加氏乳杆菌及铁死亡相关代谢通路,通过相关性分析明确二者的调控关联,随后体内外实验验证 QCHS 可直接促进加氏乳杆菌增殖,且加氏乳杆菌可通过激活 GSH/GPX4 通路发挥新型铁死亡抑制剂作用,最终明确 QCHS 通过调控加氏乳杆菌介导的铁死亡代谢通路改善实验性结肠炎,为 UC 靶向菌群与铁死亡的治疗提供了全新科学依据与策略方向。


研究设计

本研究首先构建 3% DSS 诱导的 C57BL/6 小鼠 UC 模型,设置低、中、高三个剂量的 QCHS 干预组,通过疾病表型、病理染色、炎症因子检测等手段,验证 QCHS 对小鼠结肠炎及肠屏障功能的改善作用;随后采用 16S rDNA 测序分析小鼠粪便肠道菌群组成,锁定 QCHS 干预后显著富集的加氏乳杆菌,同时利用 UHPLC-MS/MS 开展粪便非靶向代谢组学分析,筛选 QCHS 调控的差异代谢物并进行 KEGG 通路富集分析,明确其对铁死亡相关代谢通路的调控作用,再通过相关性分析明确加氏乳杆菌与铁死亡关键代谢物的关联;进而通过体外厌氧培养实验,验证 QCHS 对加氏乳杆菌生长的直接促进作用,再通过体内加氏乳杆菌灌胃干预实验,验证其对 UC 小鼠结肠炎、肠屏障损伤及铁死亡的改善作用;最终在人正常结肠上皮 NCM-460 细胞中,分别构建 LPS 诱导的炎症模型与 RSL3 诱导的铁死亡模型,明确加氏乳杆菌抑制肠上皮细胞炎症与铁死亡的具体作用及分子机制。

研究结果

QCHS 可剂量依赖性地缓解 DSS 诱导的 UC 小鼠体重下降、疾病活动指数升高、结肠缩短等病理表型,显著减轻结肠组织病理损伤,抑制促炎因子 TNF-α、IL-1β、IL-6 及炎症标志物、黏附分子的异常表达,同时降低小鼠肠道通透性,上调紧密连接蛋白与黏蛋白 Muc-2 的表达,修复受损的肠上皮屏障;QCHS 可重塑 UC 小鼠肠道菌群结构,调节菌群 α 与 β 多样性,逆转门水平的菌群失衡,显著上调乳杆菌属丰度,其中加氏乳杆菌的富集效应最为显著,体外实验也证实适宜浓度的 QCHS 可直接促进加氏乳杆菌的增殖;代谢组学分析显示 QCHS 显著改变 UC 小鼠粪便代谢谱,差异代谢物显著富集于花生四烯酸代谢、不饱和脂肪酸合成及铁死亡等通路,可显著上调铁死亡关键负向调控分子 GSH 的水平,且加氏乳杆菌丰度与 GSH 水平呈显著正相关;QCHS 可显著抑制 UC 小鼠结肠组织的铁死亡进程,缓解铁死亡特征性线粒体损伤,减轻脂质过氧化与铁过载,上调 GSH 与 GPX4 的表达,逆转铁死亡相关基因与蛋白的异常表达;单独补充加氏乳杆菌可显著缓解 DSS 诱导的小鼠结肠炎与肠屏障损伤,同时抑制结肠组织铁死亡,体外细胞实验证实加氏乳杆菌可抑制 LPS 诱导的肠上皮细胞炎症,还可通过激活 GSH/GPX4 通路,抑制 RSL3 诱导的肠上皮细胞铁死亡,首次证实加氏乳杆菌可作为新型铁死亡抑制剂发挥肠道保护作用。
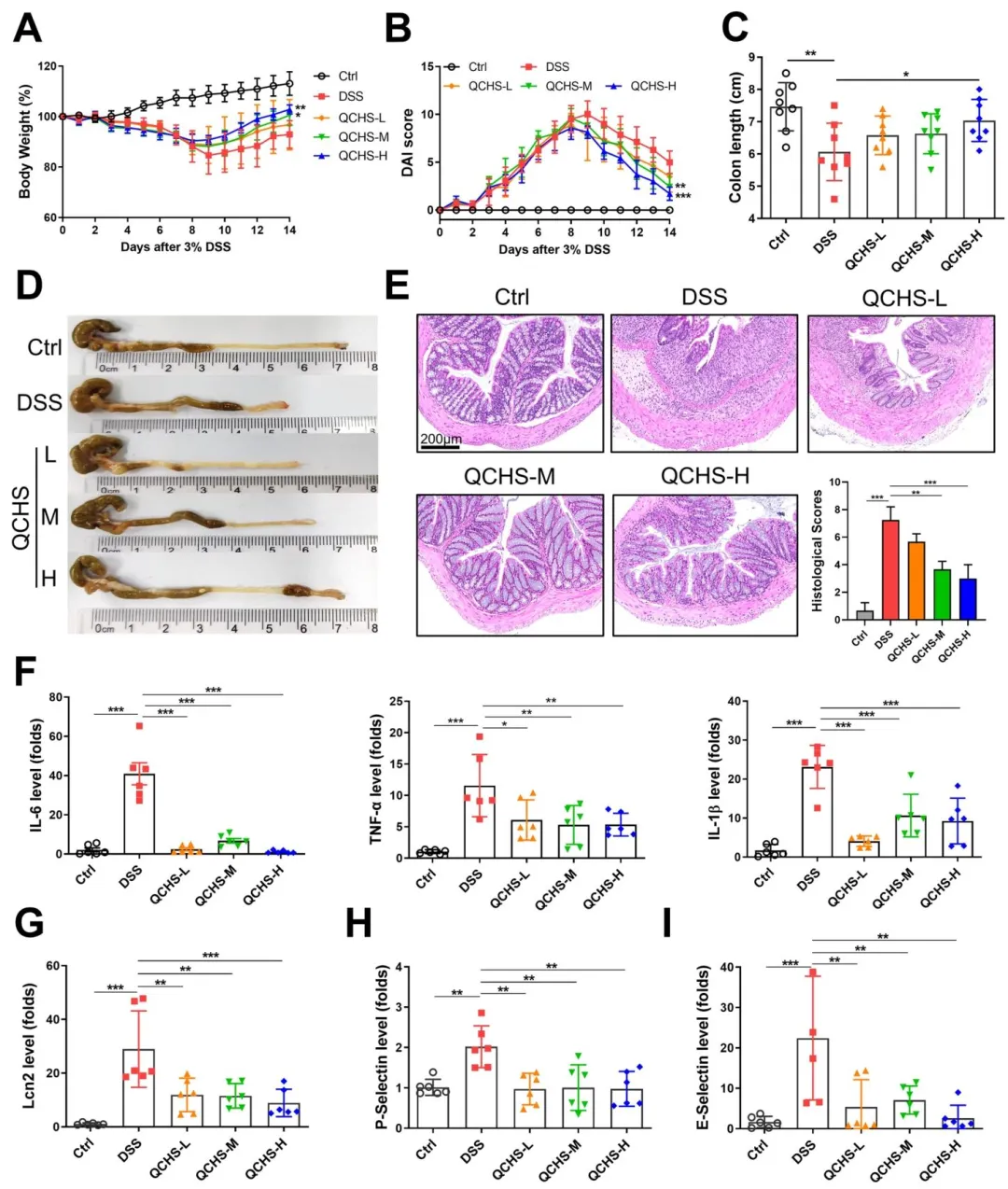
Figure 1:验证了清肠化湿颗粒(QCHS)对 DSS 诱导小鼠溃疡性结肠炎的治疗效果,明确 QCHS 可剂量依赖性改善 UC 小鼠体重丢失、疾病活动度升高等核心表型,减轻结肠病理损伤,抑制炎症相关分子异常表达,证实 QCHS 能有效缓解 UC 小鼠的结肠炎症反应。
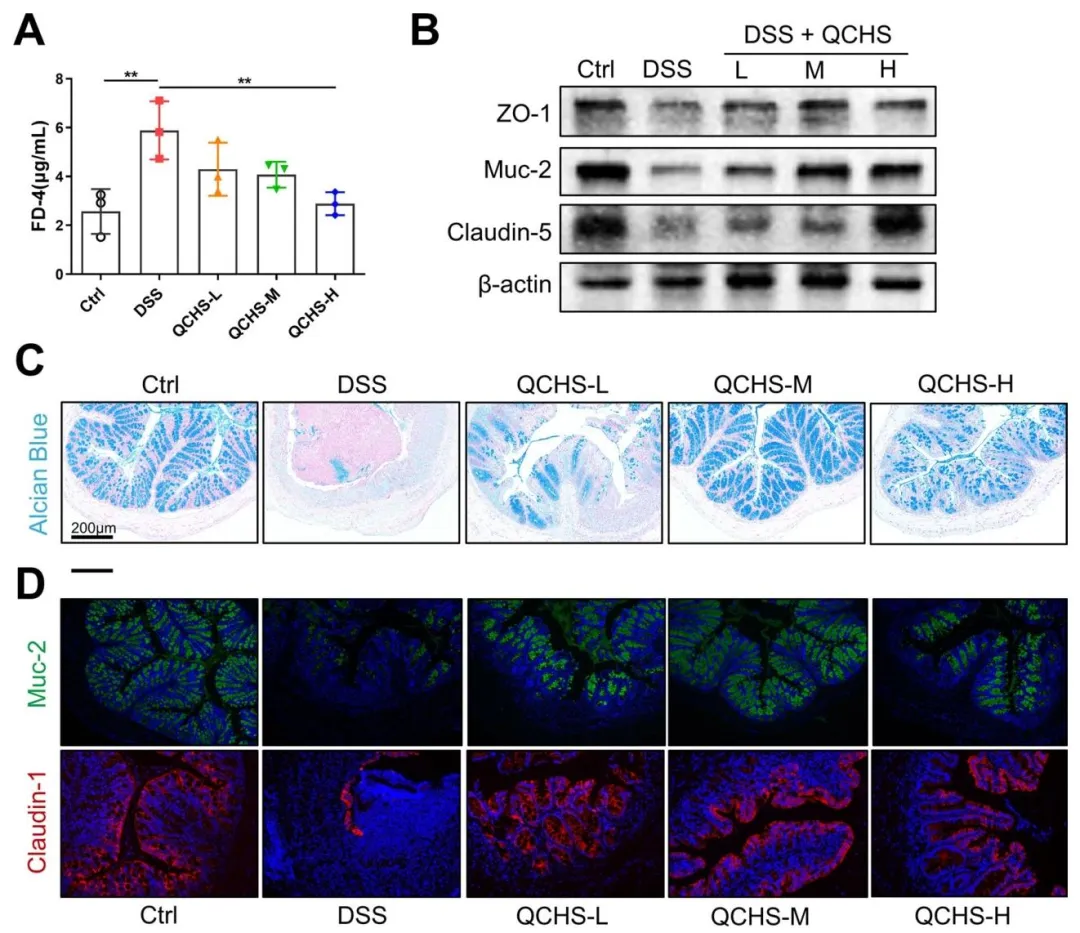
Figure 2:阐明了 QCHS 对 UC 小鼠肠道屏障功能的保护作用,证实 QCHS 可降低 UC 小鼠肠道通透性,上调结肠黏蛋白与紧密连接蛋白的表达,促进黏蛋白合成分泌,修复受损的肠上皮屏障结构与功能。
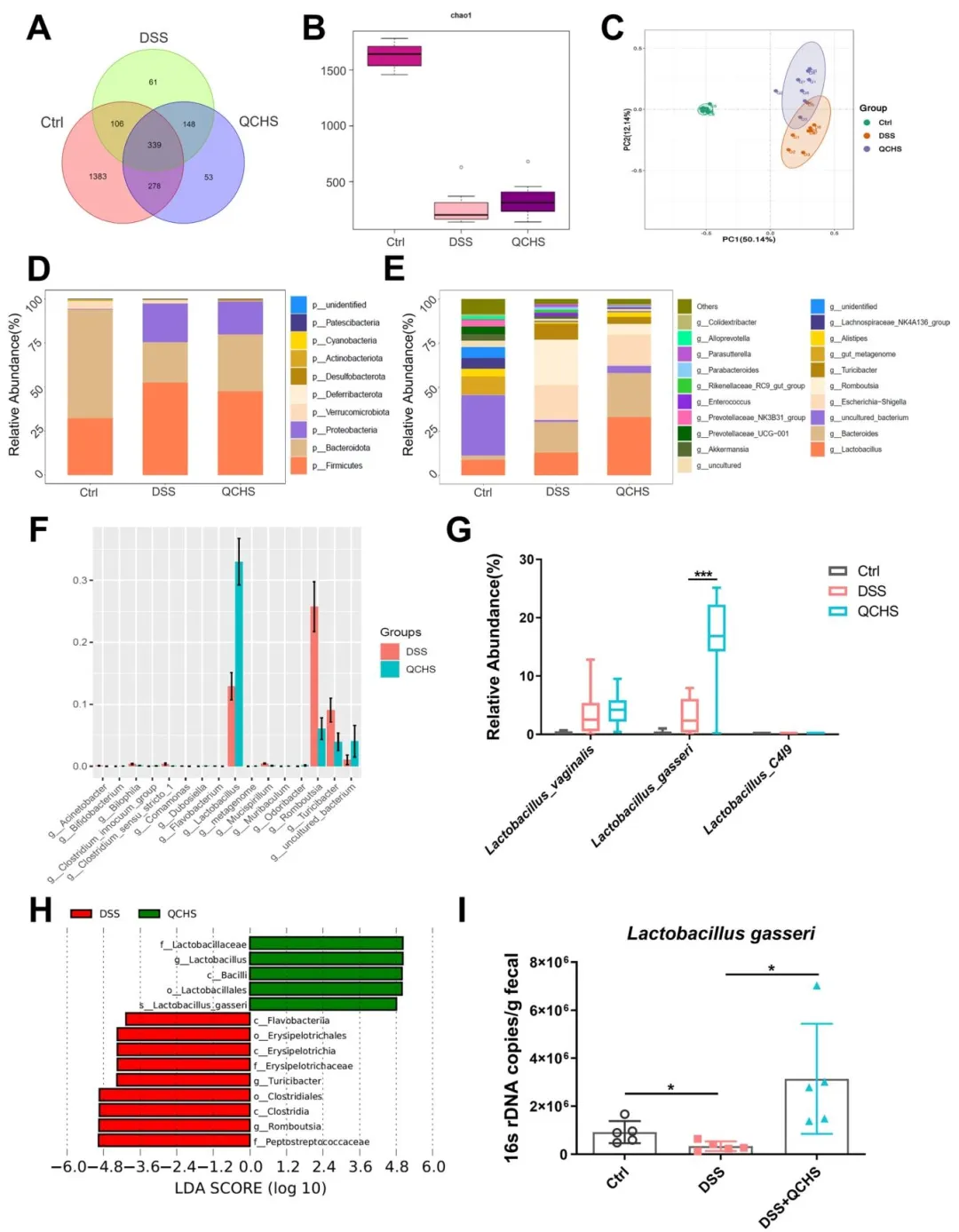
Figure 3:揭示了 QCHS 对 UC 小鼠肠道菌群的重编程作用,证实 QCHS 可调节菌群多样性、逆转菌群结构失衡,显著上调乳杆菌属丰度,在种水平明确 QCHS 可显著富集加氏乳杆菌,锁定了核心效应菌群。
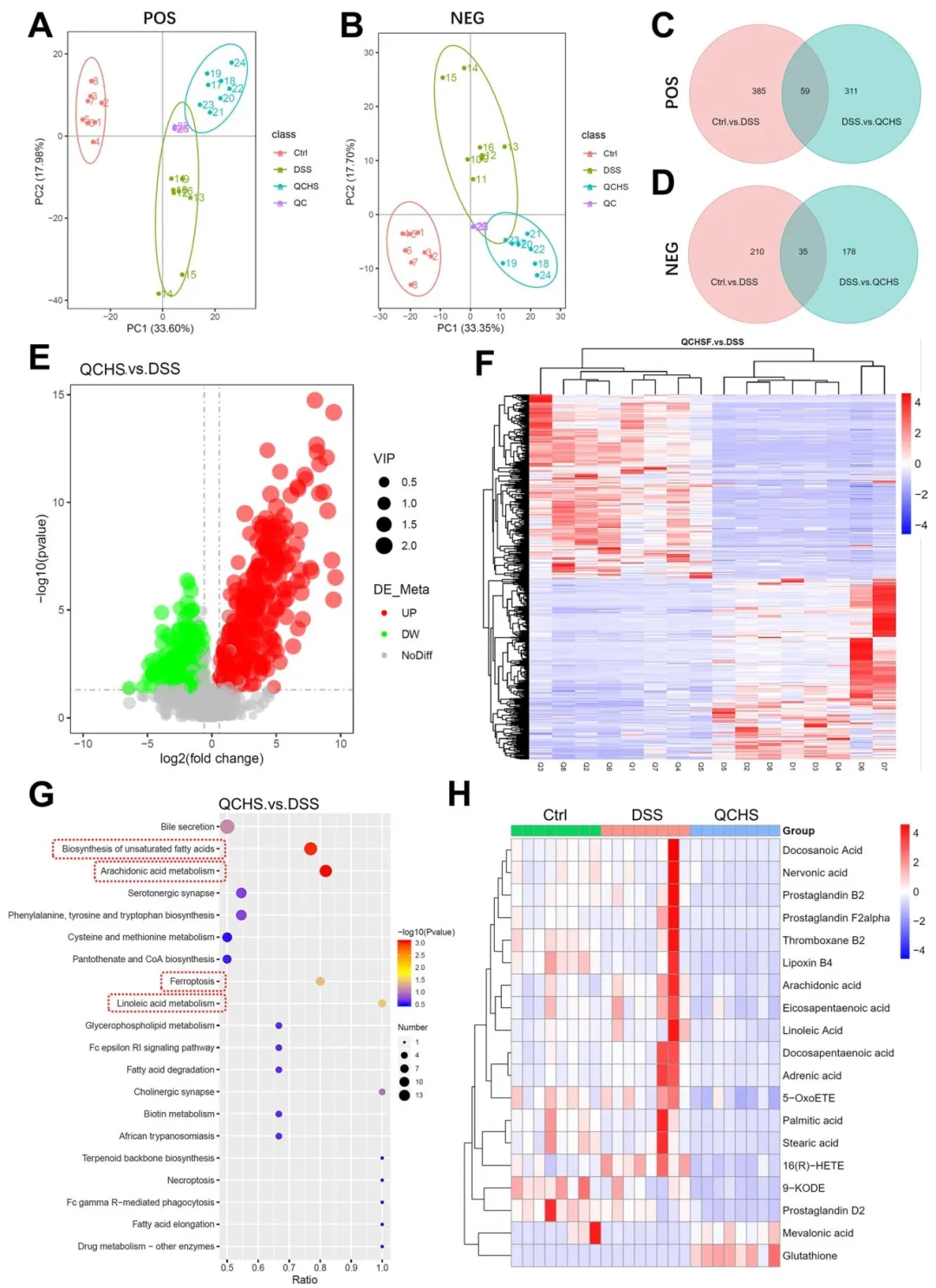
Figure 4:明确了 QCHS 对 UC 小鼠粪便代谢组的调控特征,证实 QCHS 可显著改变 UC 小鼠代谢谱,差异代谢物显著富集于铁死亡等脂质代谢相关通路,可显著上调铁死亡关键调控分子 GSH 的水平,提示 QCHS 可靶向调控 UC 的铁死亡代谢进程。
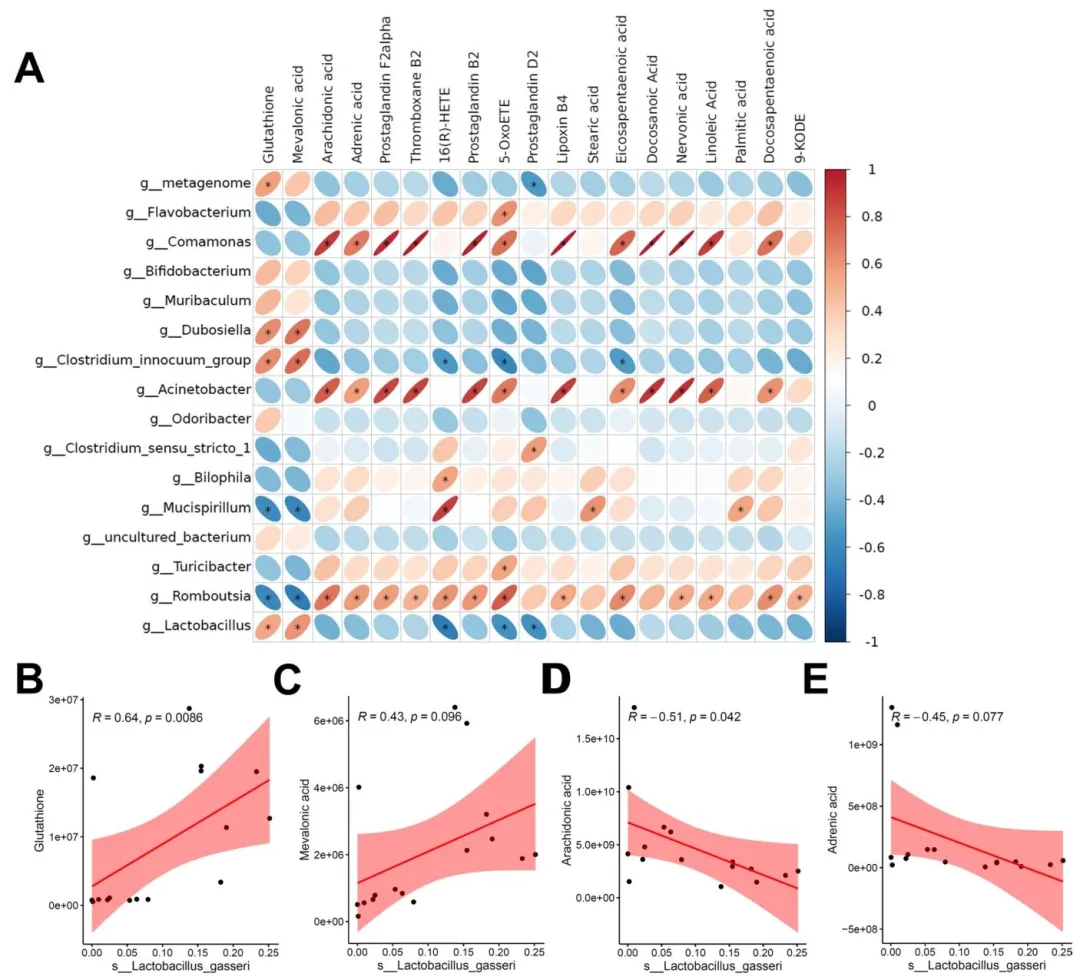
Figure 5:通过菌群 - 代谢物相关性分析,搭建了菌群与铁死亡调控的关联桥梁,证实乳杆菌属与铁死亡通路代谢物显著相关,其中加氏乳杆菌丰度与 GSH 水平呈显著正相关,为后续机制验证提供了关联依据。
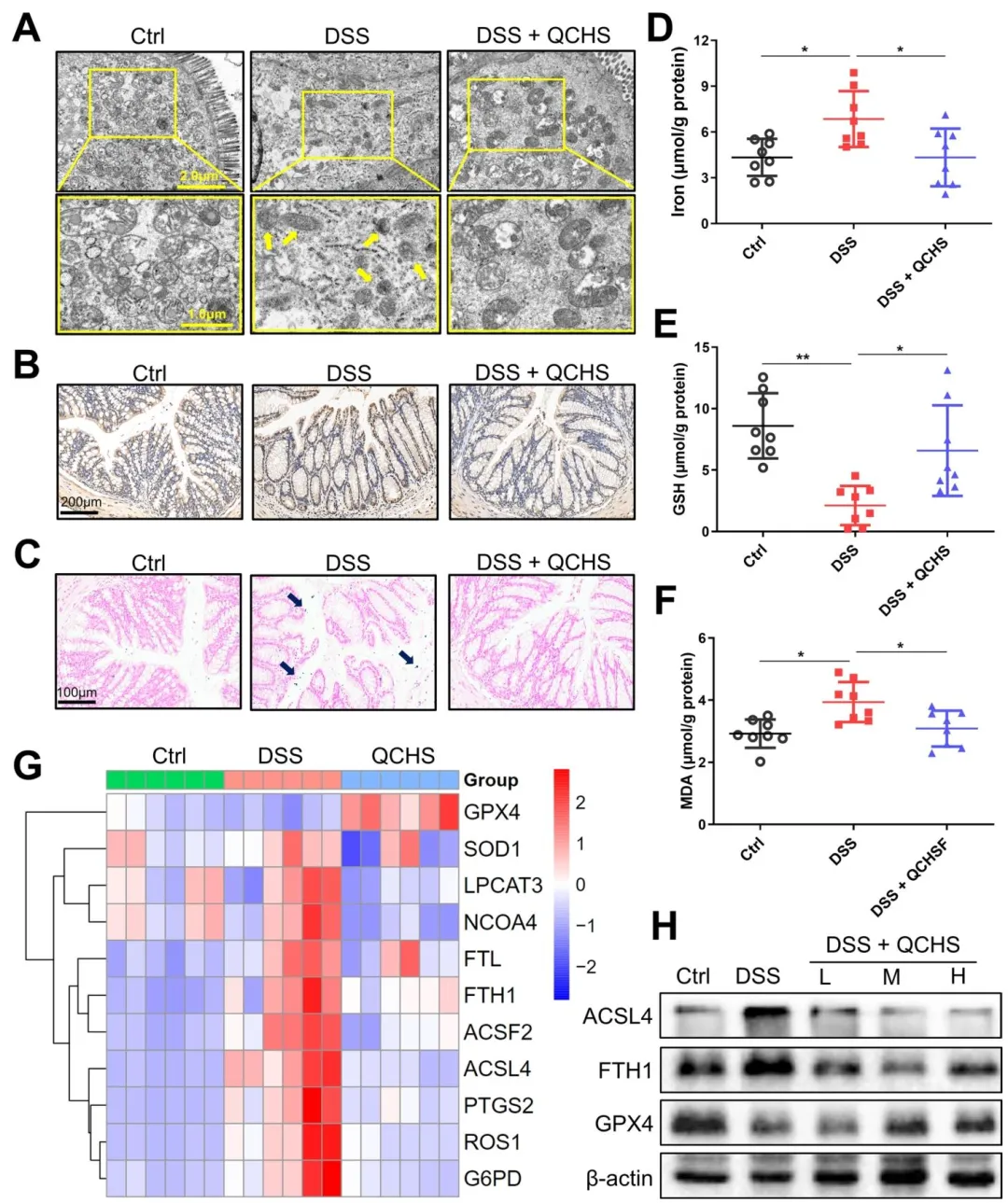
Figure 6:多维度验证了 QCHS 对 UC 小鼠结肠组织铁死亡的抑制作用,证实 QCHS 可缓解铁死亡特征性线粒体损伤,减轻脂质过氧化与铁过载,激活 GSH/GPX4 通路,逆转铁死亡相关分子的异常表达。
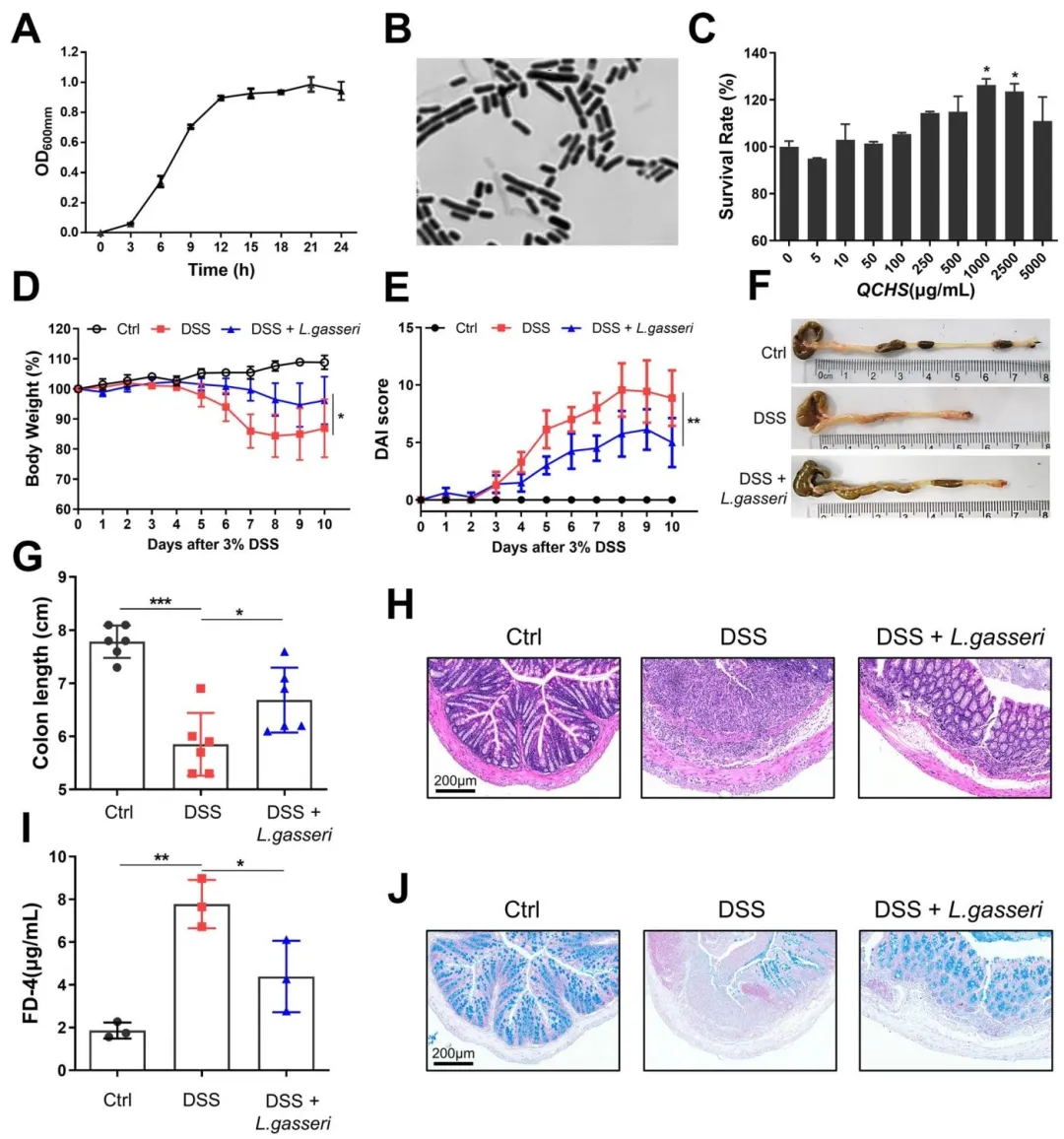
Figure 7:体外验证了 QCHS 可直接促进加氏乳杆菌增殖,同时体内实验证实单独补充加氏乳杆菌可显著缓解 DSS 诱导的小鼠结肠炎与肠屏障损伤,明确加氏乳杆菌是 QCHS 发挥 UC 治疗作用的关键介质。
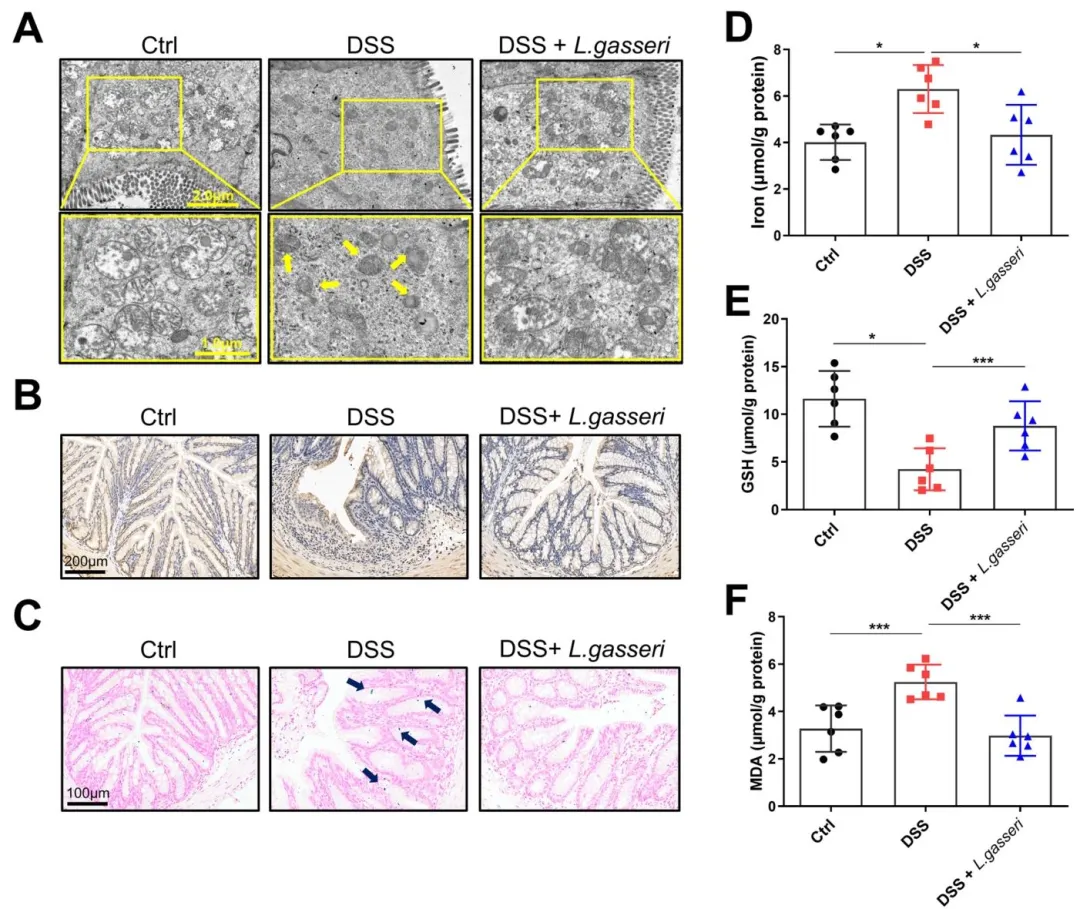
Figure 8:验证了加氏乳杆菌对 UC 小鼠结肠组织铁死亡的直接抑制作用,证实加氏乳杆菌可缓解铁死亡样线粒体损伤,减轻结肠脂质过氧化与铁过载,调控铁死亡核心生化指标,明确其可通过抑制铁死亡减轻结肠损伤。
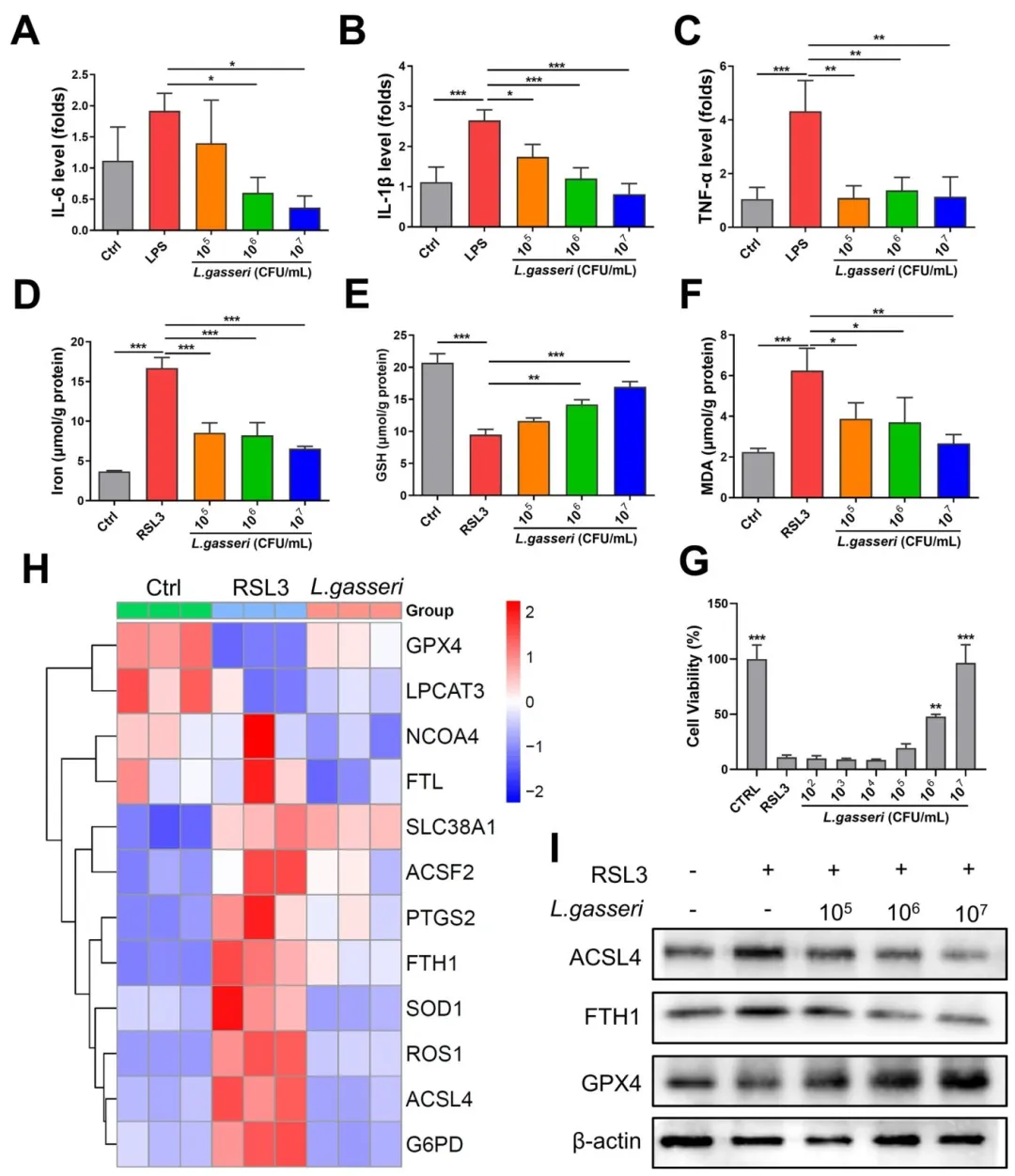
Figure 9:在细胞水平明确了加氏乳杆菌的作用与分子机制,证实其可抑制 LPS 诱导的肠上皮细胞炎症,同时通过激活 GSH/GPX4 通路,抑制 RSL3 诱导的肠上皮细胞铁死亡,首次证实加氏乳杆菌可作为新型铁死亡抑制剂发挥直接作用。
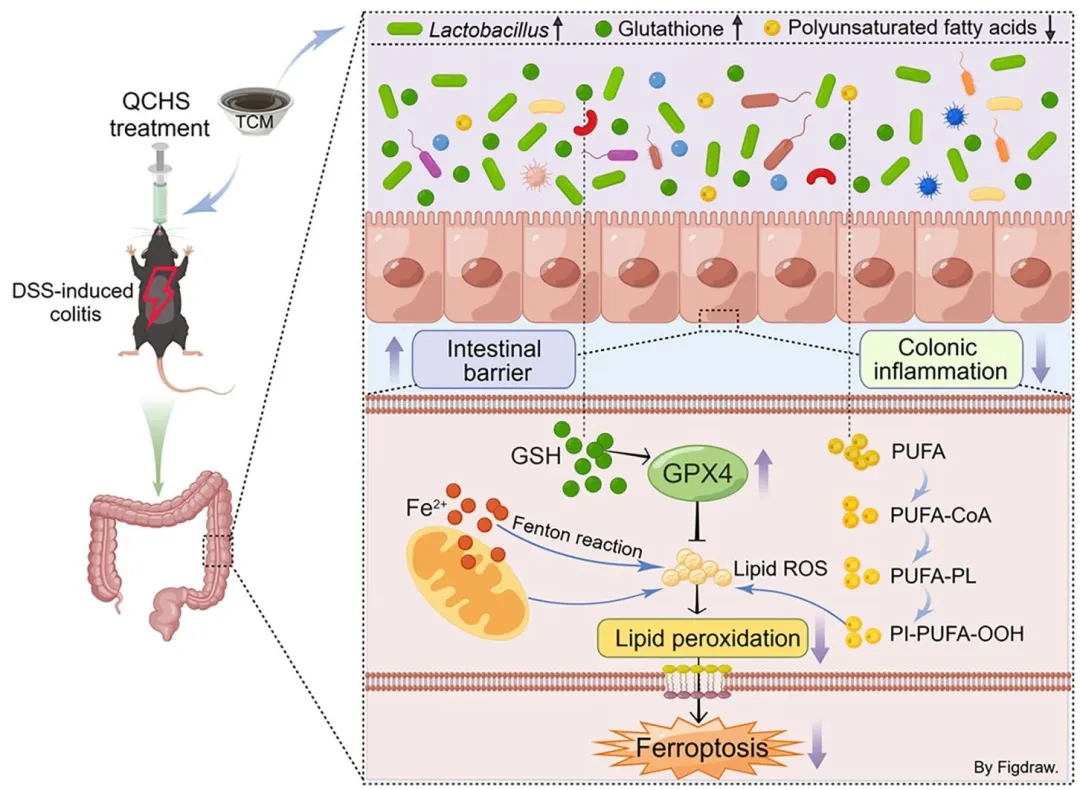
Figure 10:以图形摘要形式,可视化梳理了 QCHS 改善实验性结肠炎的完整机制,即 QCHS 通过富集肠道加氏乳杆菌,激活 GSH/GPX4 通路抑制铁死亡,同时修复肠屏障、抑制炎症,最终发挥 UC 治疗作用。

研究结论

本研究立足清肠化湿颗粒治疗 UC 的临床疗效基础,首次揭示了该复方通过调控肠道菌群 - 代谢组轴与铁死亡通路发挥 UC 治疗作用的全新机制,填补了中医药调控 UC 中肠道菌群与铁死亡关联的研究空白,同时首次发现加氏乳杆菌可作为新型铁死亡抑制剂,通过激活 GSH/GPX4 通路抑制肠上皮细胞铁死亡,不仅为 UC 靶向菌群与铁死亡的治疗策略提供了新的候选靶点与方向,也为中药复方的现代化机制解析提供了科学范式;但本研究仍存在一定的局限性,尚未通过无菌小鼠模型、加氏乳杆菌特异性耗竭模型,验证加氏乳杆菌在 QCHS 发挥治疗作用中的不可或缺性,同时未深入阐明加氏乳杆菌调控宿主 GSH/GPX4 通路的具体代谢物介质与分子靶点,相关的深层机制仍需后续研究进一步验证与完善。
本文中使用的图片来源于Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
科研信息合集
国自然中标信息
国自然思路分享
骨科领域研究分享
医学课题申报通知
心血管领域科研分享
高分文献解析
神经领域科研分享
麻醉领域科研分享
肾脏领域科研分享