【JMC】南京医科大学朱东盛等开发BRD4/CBP双靶降解剂,对急性髓性白血病有效
- 2026-06-02 12:40:35
急性髓系白血病(Acute myeloid leukemia,AML)是一种侵袭性造血系统恶性肿瘤,是成人最常见的白血病之一。AML的一个重要特征是其细胞可塑性——即白血病细胞能够动态重塑染色质结构和转录程序——这一特性导致了其对治疗压力的适应能力、生存能力以及频繁复发。溴结构域和额外末端结构域(BET)蛋白家族可识别组蛋白和转录因子上的乙酰化赖氨酸残基,从而调控基因转录。BRD4作为BET家族重要成员之一,在AML发病机制中发挥核心作用,从而维持MYC等致癌驱动基因的表达。然而,BET抑制剂单药治疗的临床疗效并不理想:疗效有限、剂量限制性毒性(例如血小板减少)及耐药问题。机制研究表明,BET抑制耐药的一个关键驱动因素是CBP/p300介导的代偿性转录激活,该过程在持续BRD4阻断条件下重新激活MYC等致癌驱动因子。尽管BET/CBP双靶抑制剂剂取得了一些进展,但双靶点抑制仍不足以完全清除AML细胞或实现持久缓解,这一局限性凸显了开发下一代策略的紧迫性,以更加全面地抑制BET与CBP的功能活性。
南京医科大学朱东盛等继前期开发出可克服FLT3耐药的BET/Kinase双靶点降解剂后(https://mp.weixin.qq.com/s/BCN7R_Yqn32XQXrzHw1StQ),近日在药物化学领域Top期刊JMC杂志发表题为Discovery of ZX079 as a Dual PROTAC Degrader Targeting BRD4/CBP in Acute Myeloid Leukemia的研究论文(doi:10.1021/acs.jmedchem.5c02766),并已于2023年9月申请相关专利。
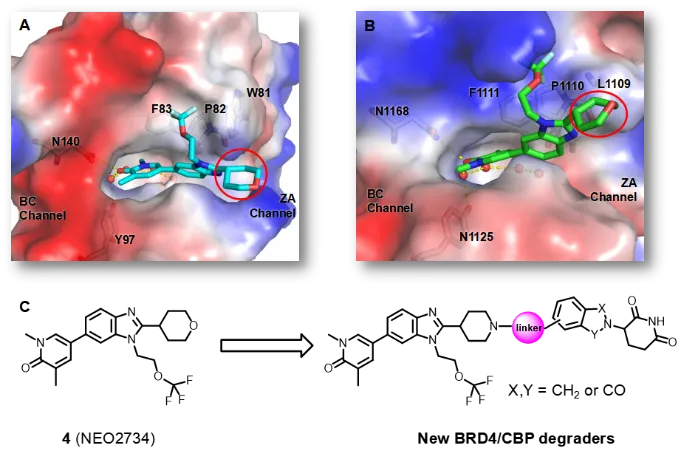
该研究基于靶向蛋白降解(PROTAC)技术,实现了一种同时降解BRD4与CBP的双靶点降解策略,为克服耐药和增强治疗效果提供了全新思路。作者设计了一类源自NEO2734骨架的新型BRD4/CBP双靶降解剂,经过几轮优化,获得最优化合物10k。10k以时间依赖和剂量依赖的方式诱导BRD4和CBP的降解,在MV4-11细胞中其DC₅₀值达到皮摩尔级活性。
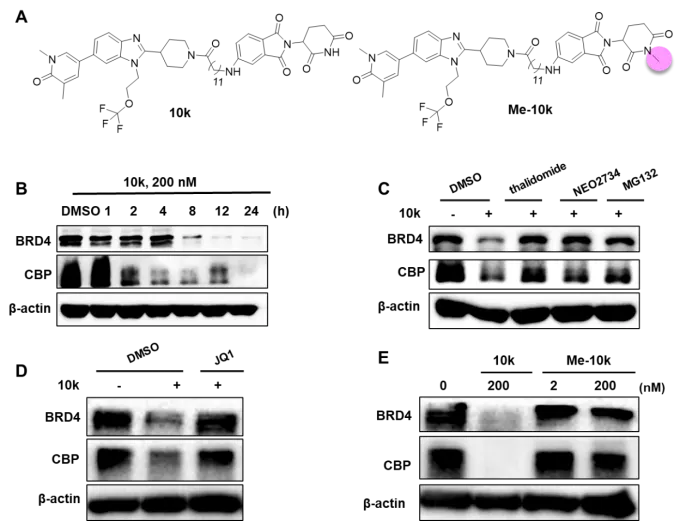
机制研究表明,10k诱导的BRD4/CBP降解依赖于cereblon(CRBN)E3连接酶的招募以及泛素-蛋白酶体系统(UPS)。
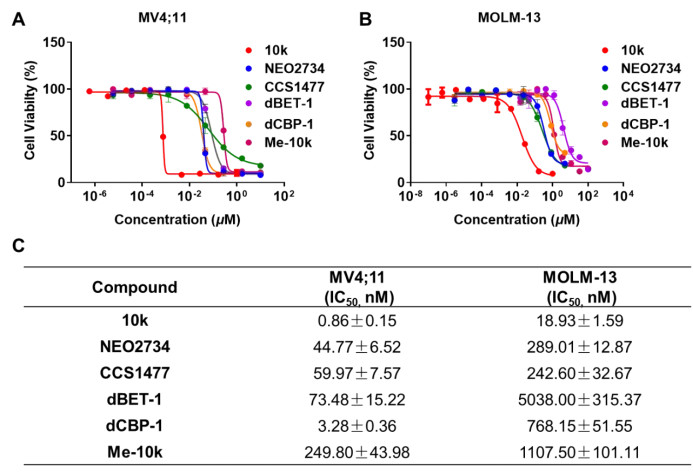
作者在多种急性髓系白血病(AML)细胞模型中开展了系统验证。结果显示,10k在MV4-11细胞中表现出显著的抗增殖活性,IC₅₀仅为0.86 nM,显著优于抑制剂NEO2734及其他对照化合物。在另一种AML细胞系MOLM-13中,10k同样展现出强效抑制能力。
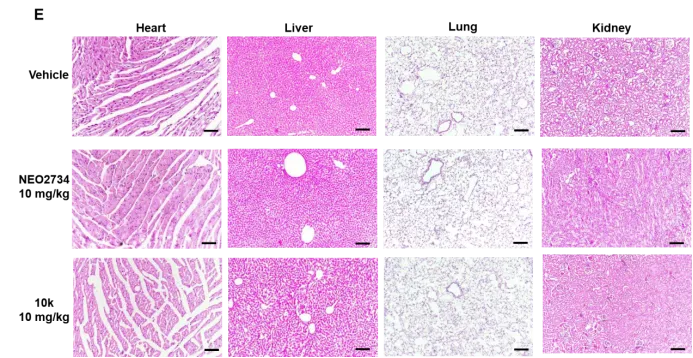
作者进一步在MV4-11白血病异种移植小鼠模型中评估了10k的体内抗肿瘤效果。在为期21天的给药实验中,10k通过腹腔注射给药,在不同给药方案下均表现出显著的抗肿瘤活性。在整个实验过程中未观察到死亡或明显体重下降,显示出良好的耐受性。主要器官的病理学评估未发现明显组织损伤,提示其具有良好的安全性特征。肿瘤组织检测结果进一步证实,10k在体内成功诱导BRD4和CBP的降解,并显著降低关键致癌蛋白c-Myc的表达。在与母体抑制剂NEO2734及临床常用药物阿糖胞苷的对比实验中,10k在相同给药条件下表现出更优的抗AML效果。

总之,本研究发现了高效BRD4/CBP双靶降解剂,代表性化合物10k不仅为深入解析相关表观遗传调控机制提供了重要工具,也为BRD4/CBP降解策略应用于AML治疗奠定了基础。
声明:发表/转载本文仅仅是出于传播信息的需要,并不意味着代表本公众号观点或证实其内容的真实性。据此内容作出的任何判断,后果自负。若有侵权,告知必删!
长按关注本公众号


