
围绝经期是女性心血管疾病发病的高危窗口期,雌激素水平的骤然下降会引发内分泌紊乱、肠道微生态失衡等一系列代谢改变,直接推动动脉粥样硬化(AS)的发生发展,使得该阶段女性动脉粥样硬化性心血管疾病(ASCVD)的患病率和死亡率显著高于同龄男性。
六味地黄丸作为中医经典补益方剂,由熟地黄、山药、泽泻等六味药材组成,临床广泛用于围绝经期骨质疏松、心血管病变等疾病的治疗,前期研究已证实其可调节肠道菌群、改善脂质代谢,缓解围绝经期动脉粥样硬化,但关于其是否通过调控TMA-TMAO代谢轴发挥作用的核心机制尚未明确。
南京中医药大学团队发表于《Phytomedicine》的最新研究,以去卵巢联合高脂饮食构建的ApoE基因敲除小鼠围绝经期动脉粥样硬化模型为研究对象,首次系统阐明了六味地黄丸通过调控肠道菌群依赖的TMA-TMAO轴改善围绝经期动脉粥样硬化的作用机制,并揭示了其与动物双歧杆菌乳亚种联用的协同治疗效应,为中医药结合益生菌防治围绝经期心血管疾病提供了全新的理论依据和临床思路。
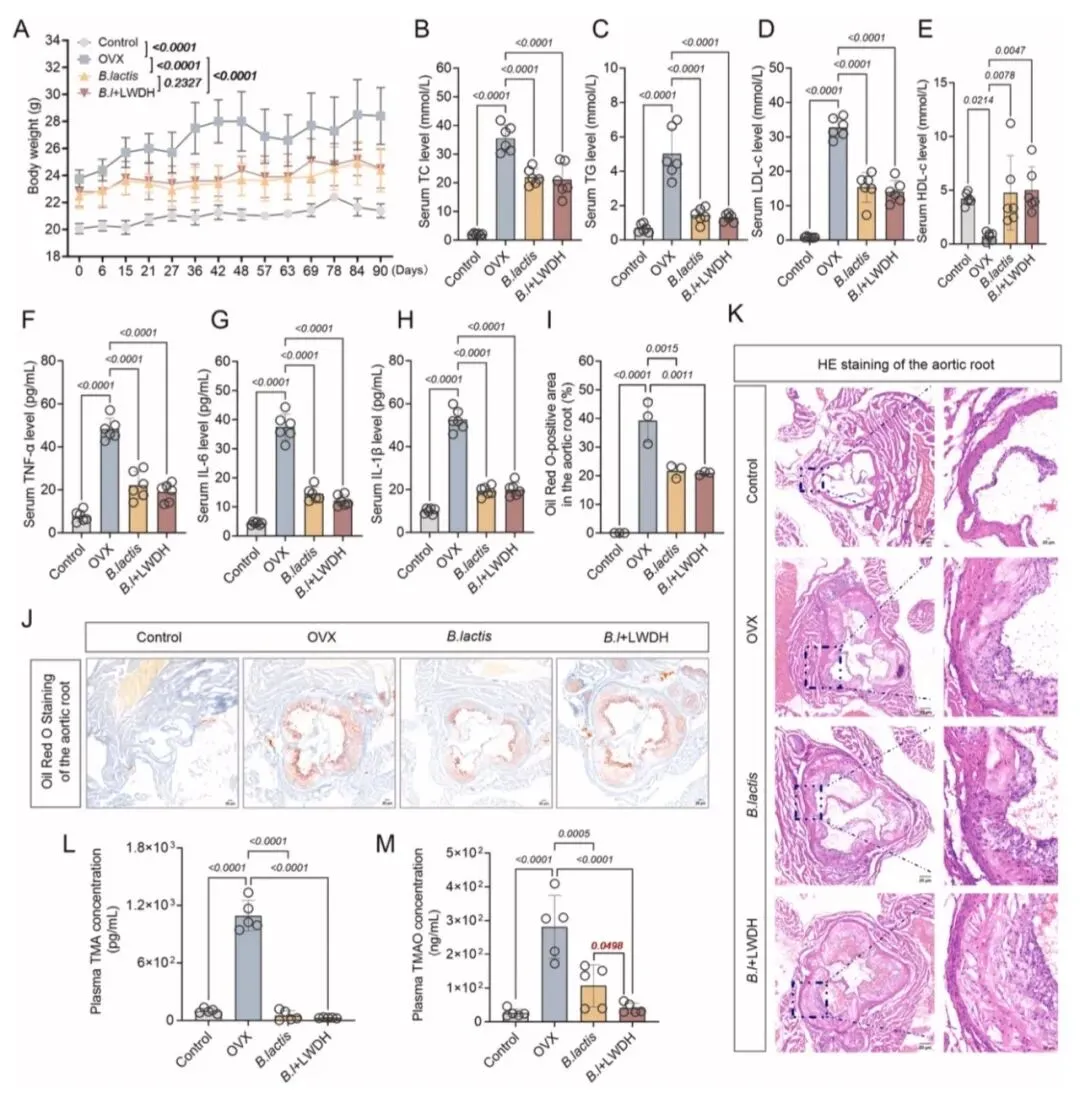
六味地黄丸改善去卵巢ApoE基因敲除小鼠的动脉粥样硬化并降低血浆氧化三甲胺水平六味地黄丸改善去卵巢ApoE基因敲除小鼠的动脉粥样硬化并降低血浆氧化三甲胺水平。研究构建的围绝经期动脉粥样硬化模型小鼠,经90天去卵巢联合高脂饮食干预后,出现明显的体重异常增长,血清脂质代谢呈现紊乱状态,总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-c)水平显著升高,高密度脂蛋白胆固醇(HDL-c)水平则明显降低,同时血清肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)等促炎因子水平大幅上调,主动脉根部出现大量脂质沉积并形成坏死核心,动脉粥样硬化病变特征显著(图2I-K)。代谢检测发现,模型小鼠血浆TMA和TMAO水平较正常对照组均显著升高,且血浆TMAO水平与主动脉脂质沉积面积呈显著正相关(R²=0.6228,p=0.0023)(图2N),提示TMAO代谢紊乱与围绝经期动脉粥样硬化的发生发展密切相关。给予六味地黄丸(9.0 g/kg)干预后,模型小鼠的体重增长得到有效抑制,血清TC、TG、LDL-c水平显著降低,HDL-c水平明显回升,脂质代谢紊乱得到有效纠正(图2B-E),同时促炎因子水平被显著下调,系统性炎症状态得到改善(图2F-H)。病理检测显示,六味地黄丸可显著减少小鼠主动脉根部脂质沉积面积,抑制坏死核心形成,缓解动脉粥样硬化病变程度(图2I-J),且能大幅降低血浆中TMA和TMAO的含量(图2L-M),这一结果提示六味地黄丸改善围绝经期动脉粥样硬化的作用,与调控TMA-TMAO代谢轴、降低循环中TMAO水平密切相关。
六味地黄丸改善去卵巢ApoE基因敲除小鼠的肝脏损伤并抑制肝脏氧化三甲胺的合成六味地黄丸改善去卵巢ApoE基因敲除小鼠的肝脏损伤并抑制肝脏氧化三甲胺的合成。肝脏是TMAO合成的核心器官,也是脂质代谢的重要场所,围绝经期动脉粥样硬化模型小鼠的肝组织出现明显的脂质代谢紊乱,肝组织TC、TG水平较正常对照组显著升高(图3A-B),肝组织切片经油红O染色可见大量脂滴堆积,肝细胞出现空泡化改变,脂肪变性严重(图3D-E)。代谢检测发现,模型小鼠肝组织TMAO含量显著升高(p=0.0445)(图3F),提示肝脏TMAO合成增加是循环中TMAO水平升高的重要原因。六味地黄丸干预可显著降低模型小鼠肝组织TC和TG水平,减少肝组织脂滴沉积,改善肝细胞脂肪变性,有效缓解肝脏脂质损伤(图3A-D),同时可显著降低肝组织TMAO含量(p=0.0102)(图3F),抑制肝脏TMAO的合成。值得注意的是,免疫组化和Western blot检测结果显示,六味地黄丸可显著上调模型小鼠肝脏FMO₃的表达(图3G-H),这一现象提示FMO₃表达与TMAO合成并非简单的线性关系,六味地黄丸可能通过减少肝脏TMA底物的供给,在上调FMO₃表达的同时,仍能有效抑制TMAO的合成,进而降低肝组织及循环中的TMAO水平。
六味地黄丸减轻去卵巢ApoE基因敲除小鼠的结肠损伤并降低三甲胺的生成六味地黄丸减轻去卵巢ApoE基因敲除小鼠的结肠损伤并降低三甲胺的生成。肠道是TMA产生的主要部位,结肠黏膜屏障的完整性对调控TMA生成至关重要,围绝经期动脉粥样硬化模型小鼠的结肠组织出现明显的病理损伤,H&E染色显示结肠上皮细胞脱落、结构崩解,黏膜下层出现单核细胞浸润(图3I),AB-PAS染色发现杯状细胞黏蛋白分泌显著减少(p=0.0014)(图3J),黏膜屏障功能受损,同时模型小鼠的结肠长度明显缩短(p=0.0281)(图3K),提示肠道存在严重的炎症反应和功能障碍。与之对应的是,模型小鼠结肠组织TMA水平显著升高(p<0.0001)(图3L),TMA合成的关键基因cutC表达上调(图3M),肠道TMA生成显著增加。六味地黄丸干预可有效改善模型小鼠结肠上皮的病理损伤,恢复结肠黏膜结构,减少黏膜下层炎症细胞浸润,同时显著增加杯状细胞黏蛋白分泌(p=0.0040)(图3J),修复结肠黏膜屏障功能,恢复结肠正常长度(p=0.0059)(图3K),有效缓解肠道炎症。此外,六味地黄丸可显著下调结肠组织cutC基因的表达(p=0.0123)(图3M),从分子水平有效抑制肠道TMA的生成,减少TMA向肝脏的转运,为肝脏TMAO合成减少提供了重要前提,进而从源头上调控TMA-TMAO代谢轴。
六味地黄丸改善去卵巢ApoE基因敲除小鼠的结肠菌群结构并促进双歧杆菌的生长六味地黄丸改善去卵巢ApoE基因敲除小鼠的结肠菌群结构并促进双歧杆菌的生长。肠道菌群是调控TMA生成的核心环节,16S rRNA测序结果显示,围绝经期动脉粥样硬化模型小鼠的结肠菌群多样性出现异常改变,Chao1指数呈下降趋势(p=0.0681),Faith_pd指数显著升高(p=0.0014)(图4A),菌群结构与正常对照组存在显著差异,主坐标分析(PCoA)显示模型组与对照组在PCo1轴上显著分离(p=0.0020)(图4B),提示卵巢切除联合高脂饮食导致小鼠肠道菌群结构发生显著紊乱。菌群组成分析发现,模型小鼠结肠中双歧杆菌的相对丰度显著降低,而产TMA菌的丰度明显升高,肠道微生态失衡(图4E)。六味地黄丸干预可有效恢复模型小鼠结肠菌群的Chao1指数(p=0.0146),下调Faith_pd指数(p=0.0057)(图4A),显著逆转卵巢切除联合高脂饮食导致的菌群结构紊乱,使菌群组成在PCo2轴上与模型组显著分离,并向正常对照组趋近(p<0.0001)(图4B)。进一步分析发现,六味地黄丸可显著升高模型小鼠结肠中双歧杆菌的相对丰度(图4E-F),而双歧杆菌丰度与结肠TMA水平、肝组织TMAO水平及血浆TMA、TMAO水平均呈负相关(图4G),提示六味地黄丸可通过重塑肠道菌群结构,富集双歧杆菌等有益菌,抑制产TMA菌的代谢活性,进而调控TMA-TMAO代谢轴,降低TMA和TMAO水平,这也是其改善围绝经期动脉粥样硬化的重要菌群机制。
六味地黄丸增强胆固醇诱导下动物双歧杆菌乳亚种介导的三甲胺降解并抑制大肠杆菌的三甲胺合成六味地黄丸增强胆固醇诱导下动物双歧杆菌乳亚种介导的三甲胺降解并抑制大肠杆菌的三甲胺合成。为进一步明确双歧杆菌在六味地黄丸调控TMA-TMAO轴中的作用,研究开展了体外细胞实验,以动物双歧杆菌乳亚种为研究对象,发现该菌株具有良好的耐酸性和耐胆盐性,可在pH2-3的酸性环境和0.1%-0.3%的胆盐环境中存活,能够适应胃肠道的生理环境(图5B-C)。生长特性检测显示,低浓度胆固醇对动物双歧杆菌乳亚种的生长无显著影响,高浓度胆固醇则会抑制其增殖,而六味地黄丸对该菌株的生长无明显抑制作用(图5D-E)。动物双歧杆菌乳亚种本身具有TMA降解能力,且在0.5-2mg/ml TMA浓度范围内对其增殖具有促进效应,六味地黄丸干预可显著增强其在高胆固醇条件下的TMA降解能力,且TMA底物浓度越高,降解效果越显著(图5K-L)。同时,研究以产TMA的大肠杆菌为研究对象,发现六味地黄丸在高胆固醇、高胆碱条件下,可显著抑制大肠杆菌的增殖,并下调其TMA合成的关键基因cutC的表达(p=0.0190)(图5R),进而有效抑制大肠杆菌的TMA合成。这一结果表明,六味地黄丸可通过双重机制调控TMA代谢,既增强有益菌的TMA降解能力,又抑制致病菌的TMA合成,从而从代谢环节有效减少肠道TMA的生成。
动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的结肠菌群,并与六味地黄丸协同促进双歧杆菌增殖动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的结肠菌群,并与六味地黄丸协同促进双歧杆菌增殖。基于体外实验结果,研究进一步探究了动物双歧杆菌乳亚种单独及与六味地黄丸联用对模型小鼠结肠菌群的调控作用,16S rRNA测序结果显示,动物双歧杆菌乳亚种单独干预可一定程度改善模型小鼠结肠菌群的多样性,调节菌群结构,显著升高双歧杆菌的相对丰度(p=0.0008)(图6E),缓解肠道微生态失衡。而六味地黄丸与动物双歧杆菌乳亚种联用后,可进一步优化菌群调控效果,相较于动物双歧杆菌乳亚种单独干预,联用组可显著调节Faith_pd、Goods_coverage等菌群多样性相关指标(图6A),主坐标分析显示联用组与单独干预组在PCo1轴上显著分离(p<0.0001)(图6B),菌群结构更接近正常对照组。同时,联用组小鼠结肠中双歧杆菌的相对丰度得到进一步提升(图6F-H),呈现出明显的协同增殖效应。菌群差异分析发现,联用组可显著降低产TMA菌肠杆菌科的丰度,而单独使用六味地黄丸或动物双歧杆菌乳亚种对其无明显影响,提示二者联用可通过菌群间的相互作用和代谢竞争,更有效地抑制产TMA菌的生存优势,进一步重塑肠道微生态平衡,为调控TMA-TMAO代谢轴奠定了更优的菌群基础。
动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的肝肠病理损伤,并与六味地黄丸协同进一步修复肠道损伤动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的肝肠病理损伤,并与六味地黄丸协同进一步修复肠道损伤。动物双歧杆菌乳亚种单独干预可显著改善模型小鼠的肝脏脂质代谢紊乱,降低肝组织TC、TG水平(图7A-B),减少肝组织脂滴沉积,缓解肝细胞脂肪变性(图7C-E),同时降低肝组织TMAO水平(p=0.0015)(图7F),上调肝脏FMO₃的表达(图7G)。在结肠组织方面,动物双歧杆菌乳亚种可改善结肠上皮病理损伤,增加杯状细胞黏蛋白分泌(p=0.0008)(图7I),修复黏膜屏障功能,使缩短的结肠长度得到一定恢复(图7J),同时抑制结肠TMA生成(p=0.0016)(图7K),下调cutC基因表达(图7L)。而六味地黄丸与动物双歧杆菌乳亚种联用后,对肝肠病理损伤的修复作用更为显著,联用组可进一步降低肝组织脂质水平和TMAO水平(p=0.0017)(图7F),显著上调肝脏FMO₃表达(p=0.0050)(图7G);在结肠组织中,联用组可更有效地恢复结肠黏膜结构,增加黏蛋白分泌,显著恢复结肠正常长度(p=0.0249)(图7J),对结肠黏膜屏障的修复效果优于动物双歧杆菌乳亚种单独干预,同时可进一步抑制结肠TMA生成(p=0.0006)(图7K),下调cutC基因表达(p=0.0331)(图7L),二者在修复肝肠病理损伤、调控TMA-TMAO代谢轴方面呈现出明显的协同效应。
动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的动脉粥样硬化相关病理改变,与六味地黄丸联用可进一步降低血浆氧化三甲胺水平动物双歧杆菌乳亚种改善去卵巢ApoE基因敲除小鼠的动脉粥样硬化相关病理改变,与六味地黄丸联用可进一步降低血浆氧化三甲胺水平。动物双歧杆菌乳亚种单独干预可有效改善围绝经期动脉粥样硬化模型小鼠的体重异常增加(图8A),调节血清脂质代谢,降低TC、TG、LDL-c水平,升高HDL-c水平(图8B-E),同时下调血清TNF-α、IL-1β、IL-6等促炎因子表达(图8F-H),减少主动脉根部脂质沉积(p=0.0015)(图8I-J),缓解动脉粥样硬化病变,同时显著降低血浆TMA和TMAO水平(p<0.0001)(图8L-M),发挥一定的抗动脉粥样硬化作用。而六味地黄丸与动物双歧杆菌乳亚种联用后,对动脉粥样硬化相关病理改变的改善作用得到显著增强,联用组小鼠体重控制效果更佳,血清脂质代谢和炎症状态得到进一步改善,主动脉根部脂质沉积面积进一步减少(p=0.0011)(图8I-J),坏死核心形成得到更有效的抑制,动脉粥样硬化病变程度显著轻于动物双歧杆菌乳亚种单独干预组。尤为重要的是,联用组可在动物双歧杆菌乳亚种单独干预的基础上,进一步显著降低模型小鼠血浆TMAO水平(p=0.0498)(图8L),这一结果与二者协同调控肠道菌群、抑制肠道TMA生成、减少肝脏TMAO合成的作用密切相关,提示六味地黄丸与动物双歧杆菌乳亚种联用可通过多靶点、多环节调控TMA-TMAO代谢轴,更有效地降低循环中TMAO水平,进而发挥协同抗围绝经期动脉粥样硬化的作用。
本研究首次从肠道菌群-TMA-TMAO代谢轴的角度,系统阐明了六味地黄丸改善围绝经期动脉粥样硬化的核心作用机制,其并非单一环节调控,而是通过重塑肠道菌群结构、修复肠肝病理损伤、调控TMA-TMAO代谢等多靶点、多途径发挥作用。六味地黄丸可通过富集双歧杆菌等有益菌,抑制产TMA菌的增殖和代谢,同时发挥双重代谢调控作用:一方面增强动物双歧杆菌乳亚种的TMA降解能力,另一方面抑制大肠杆菌等产TMA菌的cutC基因表达,减少肠道TMA生成,进而降低肝脏TMAO合成及循环中TMAO水平,同时改善脂质代谢紊乱、抑制系统性炎症,最终缓解动脉粥样硬化病变。更重要的是,研究发现六味地黄丸与动物双歧杆菌乳亚种联用具有显著的协同效应,二者可协同调节肠道菌群结构、促进双歧杆菌增殖、修复肝肠病理损伤、抑制TMA-TMAO代谢轴,更有效地降低血浆TMAO水平,增强抗动脉粥样硬化作用。