温州医科大学 / 南京中医药大学 2026 年 2 月新研究:从分子到临床,天然产物与益生菌治疗艰难梭菌感染的新突破
- 2026-05-30 14:18:43
导 读
Introduction

一、研究背景解读
Background
二、研究思路解析
Train of Though
该研究采用细胞模型 + 体外细菌实验结合多组学技术 + 功能验证的研究思路,层层递进解析黄腐酚和丁酸梭菌的抗 CDI 机制,整体实验设计分为四个核心阶段,技术路线清晰且逻辑闭环:
1. 肠道上皮细胞损伤模型构建与黄腐酚的保护作用验证
建立 DSS 诱导的 Caco-2 细胞炎症模型,模拟 IBD 患者的肠道炎症状态,在此基础上叠加艰难梭菌感染,通过 CCK-8 法检测细胞活力、qRT-PCR 检测炎症信号通路关键基因表达,验证黄腐酚对细胞的保护作用;同时利用定量蛋白质组学分析黄腐酚对感染后 Caco-2 细胞蛋白组的调控规律,明确其对宿主细胞的分子调控特征。
2. 黄腐酚与丁酸梭菌上清液的体外抗艰难梭菌活性检测
通过 CFSE 荧光标记检测细菌对 Caco-2 细胞的定植能力、OD600 检测细菌生长动力学、qRT-PCR 检测艰难梭菌毒素基因(tcdA、tcdB、tcdR)的转录水平,分别验证黄腐酚和 CBs 对艰难梭菌定植、生长、毒素产生的抑制作用,明确二者的体外抗 CDI 活性。
3. 蛋白质组学与乙酰化修饰组学解析分子调控通路
对黄腐酚和 CBs 处理后的艰难梭菌进行全蛋白组学分析,筛选差异表达蛋白(DEPs)并通过 KEGG 富集分析明确核心调控通路;进一步利用串联质量标签(TMT)的乙酰化修饰组学技术,解析二者对艰难梭菌赖氨酸乙酰化谱的调控特征,筛选共同的乙酰化修饰靶点和代谢通路。
4. 关键靶点的功能验证
基于组学结果,锁定糖酵解通路的关键酶果糖 - 1,6 - 二磷酸醛缩酶(FBA)及其 K280 乙酰化位点为核心靶点,通过质粒构建、蛋白纯化获得野生型和 K280A 突变型 FBA,利用酶活实验验证该乙酰化位点对 FBA 催化活性的调控作用,明确黄腐酚和 CBs 发挥作用的关键分子靶点。
该研究的技术手段涵盖细胞生物学、微生物学、蛋白质组学、修饰组学、分子生物学等多学科方法,同时设置了多组对照实验,保证了研究结果的可靠性和严谨性。
三、研究主要结果展示
ResultDemonstraion
结果 1:黄腐酚缓解艰难梭菌对 DSS 诱导的 Caco-2 细胞的损伤并抑制炎症信号通路
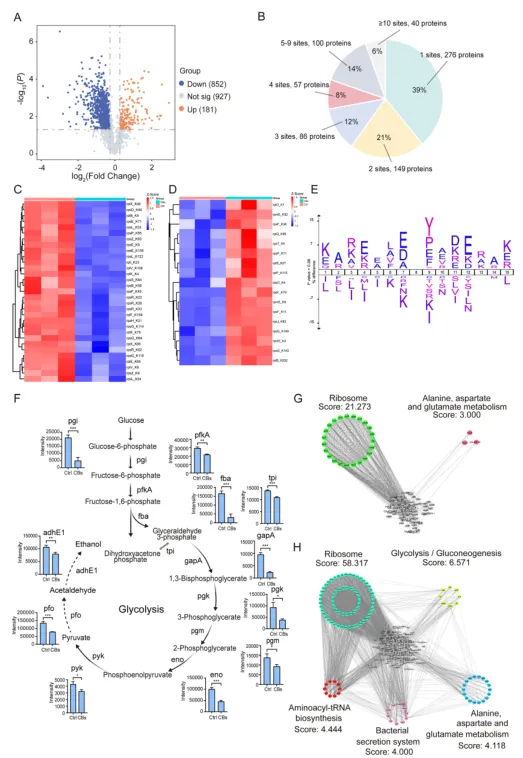
DSS 单独处理可显著降低 Caco-2 细胞活力,叠加艰难梭菌感染后细胞损伤进一步加剧,而黄腐酚处理能显著恢复细胞活力,缓解病原菌的细胞毒性。 艰难梭菌感染可显著上调 Caco-2 细胞中 NF-κB1、TAK1、TRAF6、JNK 等炎症信号通路关键基因的表达,黄腐酚则能显著下调上述基因表达,发挥强效抗炎作用。 蛋白质组学分析显示,DSS + 艰难梭菌处理使 Caco-2 细胞出现 156 个下调蛋白和 226 个上调蛋白,其中类固醇生物合成通路蛋白显著下调(破坏肠道屏障完整性);而黄腐酚可逆转 32 个被艰难梭菌下调的蛋白和 33 个被上调的蛋白,使细胞蛋白组谱向正常对照组靠拢,维护肠道上皮细胞的分子稳态。
黄腐酚可显著降低艰难梭菌对 Caco-2 细胞的定植能力,抑制细菌的生长增殖,同时显著下调毒素基因 tcdA、tcdB 及其转录调控因子 tcdR 的表达,减少毒素产生。 蛋白质组学在艰难梭菌中鉴定出 2251 个蛋白(覆盖其已知蛋白组的 60%),黄腐酚处理后筛选出 662 个差异表达蛋白(286 个下调、376 个上调),KEGG 富集分析显示氨基酸生物合成、碳代谢、次级代谢产物合成等通路显著改变。 黄腐酚显著上调艰难梭菌核苷酸、氨基酸、碳水化合物代谢及能量产生相关酶的表达(病原菌的应激代偿反应),同时显著下调鞭毛组装相关蛋白(为细菌定植能力下降提供分子解释);蛋白互作网络显示,上调蛋白主要富集于氧化磷酸化通路,下调蛋白集中于鞭毛组装通路。
与黄腐酚一致,CBs 可显著抑制艰难梭菌对 Caco-2 细胞的定植、体外生长及毒素基因 tcdA、tcdB、tcdR 的表达,抗 CDI 活性与黄腐酚相当。 CBs 处理后艰难梭菌出现 435 个差异表达蛋白(360 个下调、75 个上调),KEGG 富集分析显示同源重组和核糖体生物发生通路为核心调控通路;其中核糖体大亚基 23 个蛋白、小亚基 12 个蛋白显著下调,导致细菌蛋白质合成能力受损,限制其增殖。 蛋白互作网络显示,CBs 调控的差异蛋白与糖酵解 / 糖异生、鞭毛组装通路密切相关,且其与黄腐酚对鞭毛组装通路的调控靶点一致,提示二者存在共同的抗定植分子机制。
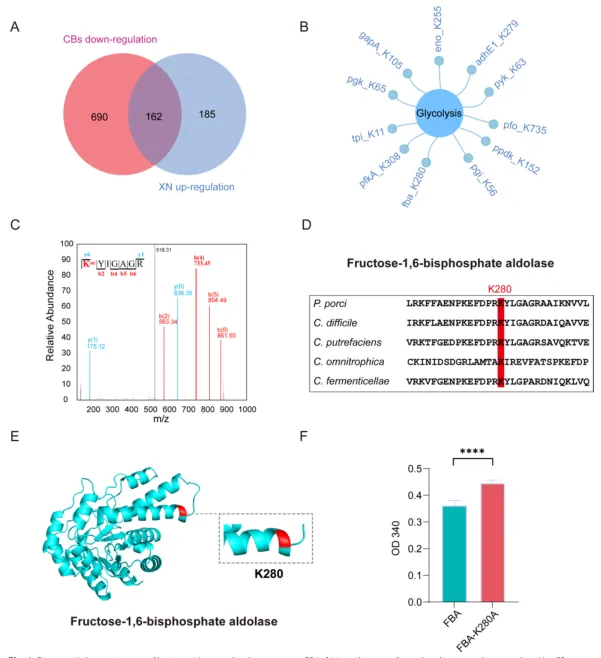
黄腐酚对乙酰化组的调控:鉴定出艰难梭菌 733 个蛋白的 2653 个乙酰化位点,黄腐酚处理后 576 个蛋白乙酰化水平改变;乙酰化蛋白主要富集于碳代谢、糖酵解 / 糖异生通路,其中糖酵解关键酶 FBA 的 K280 位点发生高乙酰化,同时核糖体通路蛋白乙酰化水平显著下调。 CBs 对乙酰化组的调控:鉴定出 708 个蛋白的 2266 个乙酰化位点,CBs 处理后 1033 个蛋白乙酰化水平改变;核心调控核糖体相关蛋白的乙酰化,同时显著下调糖酵解通路酶的乙酰化水平和蛋白丰度,导致糖酵解通量受损。 二者的乙酰化调控存在共同靶点:共筛选出 162 个共同的乙酰化修饰位点,其中 11 个位于糖酵解关键酶上,提示糖酵解通路的乙酰化调控是二者抗艰难梭菌的核心共同机制。
质谱鉴定证实艰难梭菌 FBA 的 K280 位点为乙酰化修饰位点,跨物种序列比对显示该位点在多种梭菌中高度保守,结构生物学分析表明其与 FBA 的结构完整性和催化功能密切相关。 定点突变实验构建 FBA-K280A 突变体,酶活实验显示该突变体的催化活性显著降低,证实 K280 乙酰化位点是维持 FBA 酶活的关键位点。 黄腐酚和 CBs 通过调控 FBA-K280 乙酰化,抑制艰难梭菌的糖酵解代谢通量,进而降低细菌的能量供应和毒力,这是二者发挥抗 CDI 作用的核心分子机制。
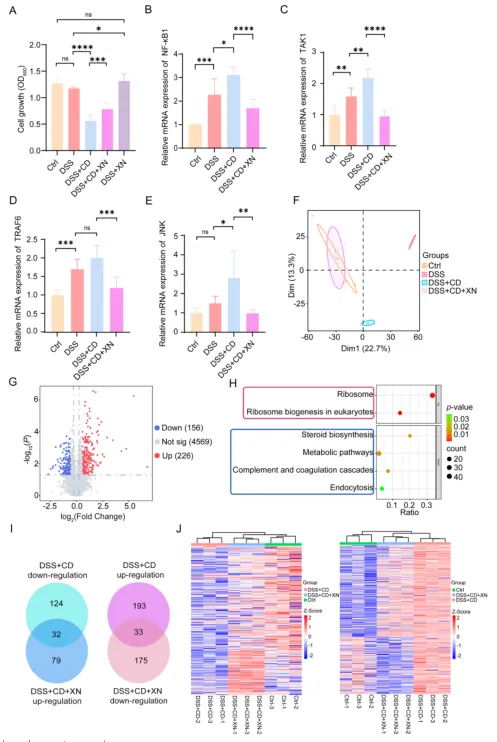
本研究通过整合 ceRNA 网络与代谢通路建模,系统解析了 XIST 调控下的分子互作与代谢重编程机制。研究首先通过功能富集分析聚焦于碳水化合物代谢相关通路,构建了包含 mRNA、lncRNA、circRNA 和 miRNA 的 ceRNA 调控网络,并验证了 B 细胞优先偏好的关键 miRNA。火山图和维恩图分析筛选出不同处理组间的差异表达基因(DEGs),结合代谢通路分析发现,这些 DEGs 显著富集于多条代谢通路,且存在明显的蛋白互作网络调控。热图和条形图进一步显示,XIST 调控导致了代谢通路中蛋白表达的显著差异,其中部分代谢通路蛋白显著下调,提示 XIST 可能通过 ceRNA 网络调控代谢重编程,进而影响细胞代谢功能。综合来看,XIST 通过调控 ceRNA 网络介导代谢通路重编程,在相关生理或病理过程中发挥重要调控作用。
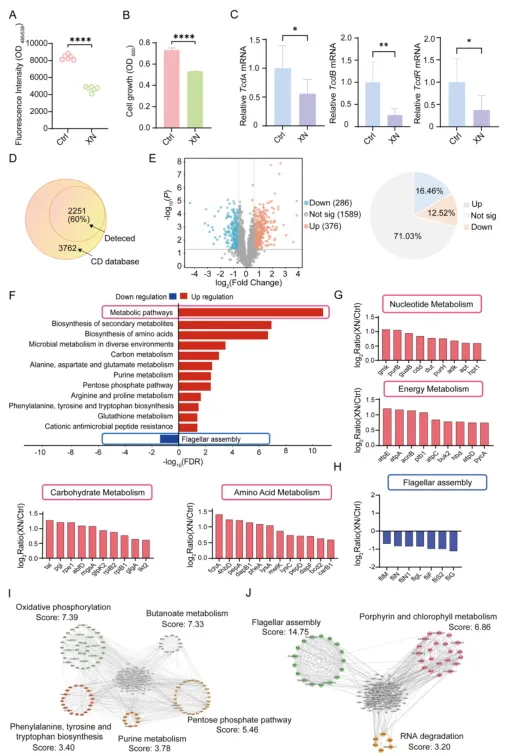
本研究通过多组学分析系统解析了 CFB 敲低对结直肠癌(CRC)细胞的调控作用。功能富集分析显示,CFB 敲低显著改变了 CRC 细胞的代谢和表观遗传相关通路;qPCR 验证了 2 个关键细胞周期基因的表达变化,提示 CFB 敲低可能抑制细胞周期进程。火山图和维恩图筛选出大量差异表达基因,KEGG 通路富集分析进一步明确了这些基因主要富集于代谢和表观遗传调控通路。蛋白质组学分析构建了差异蛋白互作网络,发现代谢通路中存在大量上调蛋白,且上调与下调蛋白分别形成了独立的互作网络。综合来看,CFB 敲低可通过重塑代谢与表观遗传景观,调控细胞周期及关键通路蛋白互作网络,从而有效抑制结直肠癌细胞的恶性表型。
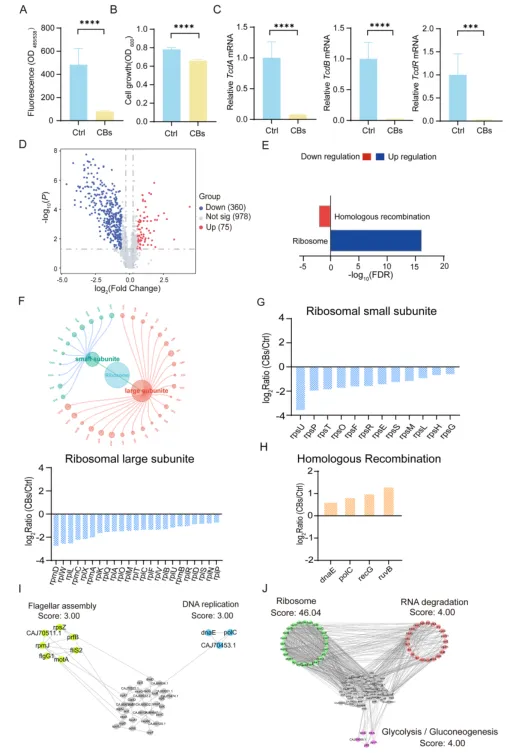
本研究通过系统代谢组学与乙酰化蛋白质组学分析,全面解析了咖啡酸在结直肠癌(CRC)细胞中的调控作用。研究发现,咖啡酸处理显著改变了 CRC 细胞的乙酰化修饰谱,影响了 233 个乙酰化位点,并重塑了氨基酸代谢、碳代谢及糖酵解 / 糖异生等关键代谢通路。热图与通路分析显示,咖啡酸可通过调控糖酵解、三羧酸循环及相关代谢酶的表达与修饰,干扰肿瘤细胞的能量代谢重编程。蛋白互作网络(PPI)进一步揭示,咖啡酸介导的差异蛋白形成了复杂的调控网络,协同影响代谢与信号通路。综合来看,咖啡酸可通过重塑乙酰化修饰与代谢通路网络,干扰结直肠癌细胞的能量代谢与关键信号通路,从而发挥潜在的抗肿瘤作用。
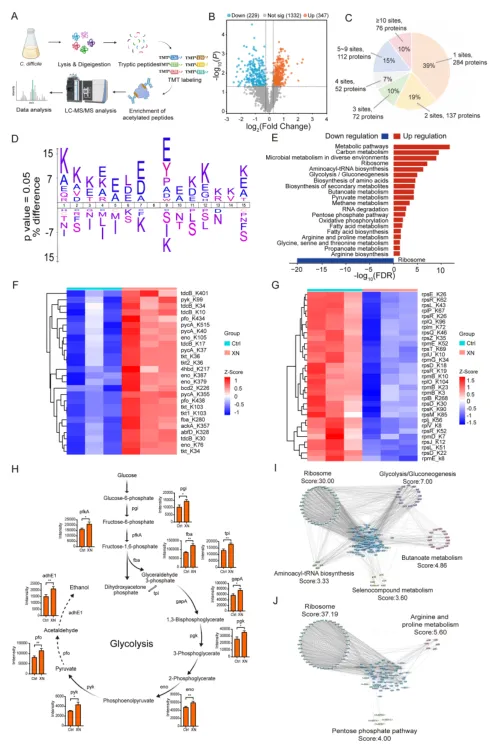
本研究系统解析了结直肠癌(CRC)细胞中 CYB5A 在咖啡酸处理下的功能特征。火山图分析显示,咖啡酸处理显著影响了 CYB5A 的表达或修饰状态;结构分析明确了 CYB5A 的三维构象及关键乙酰化位点(K280),并通过 MS/MS 谱图验证了该位点的乙酰化修饰。Co-IP 实验证实,CYB5A 可与酰基辅酶 A 结合蛋白(ACB)发生相互作用,提示其可能参与脂代谢调控;免疫荧光染色显示 CYB5A 主要定位于细胞质中。酶活分析进一步表明,K280 位点的乙酰化修饰对 CYB5A 的酶活性具有关键调控作用。综合来看,咖啡酸可通过调控 CYB5A 的 K280 位点乙酰化修饰,影响其与 ACB 的相互作用及酶活性,进而在结直肠癌的脂代谢重编程中发挥重要调控功能。
四、总 结
Summary
1. 该研究核心研究结论
该研究通过细胞模型、体外细菌实验结合多组学技术与功能验证,首次系统阐明了黄腐酚和丁酸梭菌上清液抗艰难梭菌的分子机制:二者均通过调控艰难梭菌的赖氨酸乙酰化修饰水平,靶向干扰糖酵解代谢通路,抑制细菌的定植、生长和毒素产生,从而降低其致病性;同时黄腐酚可通过抑制 NF-κB/JNK 等炎症信号通路激活、逆转病原菌诱导的宿主细胞蛋白组紊乱,缓解炎症状态下肠道上皮细胞的损伤,维护肠道屏障完整性。其中,糖酵解关键酶 FBA 的 K280 乙酰化位点是二者发挥作用的核心共同靶点,该位点的乙酰化调控直接影响 FBA 的催化活性和艰难梭菌的糖酵解代谢,进而调控其毒力。
2. 研究的创新点
首次揭示天然产物与益生菌抗艰难梭菌的共同分子机制:发现赖氨酸乙酰化 - 糖酵解通路调控是黄腐酚和丁酸梭菌发挥抗 CDI 作用的核心共同通路,填补了该领域的分子机制空白。
鉴定出抗艰难梭菌的关键分子靶点:明确 FBA-K280 乙酰化位点为调控艰难梭菌糖酵解和毒力的关键靶点,为 CDI 的靶向治疗提供了新的分子靶点。
结合宿主与病原体双视角解析作用机制:不仅解析了黄腐酚和丁酸梭菌对艰难梭菌的直接调控作用,还阐明了黄腐酚对宿主肠道上皮细胞的保护和抗炎机制,为宿主 - 微生物相互作用的研究提供了新视角。
为天然产物与益生菌的联合应用提供实验依据:证实黄腐酚(植物源)和丁酸梭菌(微生物源)的抗 CDI 活性具有协同性和互补性,为开发二者联合的 CDI 新型治疗策略奠定了实验基础。
3. 研究的临床意义与应用前景
本研究突破了传统抗生素治疗 CDI 的局限性,证实天然产物黄腐酚和益生菌丁酸梭菌可作为低毒性、新型的抗 CDI 治疗候选物,为临床 CDI 尤其是 IBD 合并 CDI 的治疗提供了新的思路和策略。同时,鉴定的 FBA-K280 乙酰化位点为 CDI 的靶向药物研发提供了关键分子靶点,基于该靶点的靶向修饰或抑制剂开发有望成为 CDI 治疗的新方向。此外,本研究建立的蛋白质组学与修饰组学结合的技术体系,也为其他肠道病原菌的分子机制研究提供了可借鉴的方法。
4. 研究的局限性与未来展望
本研究的局限性在于采用的 DSS 诱导 Caco-2 细胞模型为体外简化模型,与体内复杂的肠道微生态环境存在差异,尚未在动物模型和临床样本中验证研究结果。未来的研究方向包括:一是在结肠炎和 CDI 合并感染的动物模型中验证黄腐酚和丁酸梭菌的治疗效果及分子机制;二是通过靶标组学技术明确黄腐酚和丁酸梭菌调控赖氨酸乙酰化的直接分子靶点;三是开发基于 FBA-K280 乙酰化位点的靶向抑制剂,结合黄腐酚与丁酸梭菌开展联合治疗的临床前研究,推动其向临床应用转化。
5. 研究的科学价值
本研究从分子水平揭示了天然产物与益生菌对肠道病原菌的调控规律,为理解宿主 - 微生物 - 天然产物的相互作用提供了新的理论依据;同时拓展了赖氨酸乙酰化修饰在细菌毒力调控中的功能认知,丰富了肠道微生态调控的分子机制研究,为天然产物和益生菌在肠道感染性疾病中的应用提供了新的科学支撑。
https://link.springer.com/article/10.1186/s13020-026-01343-x


