2026年2月,南京医科大学儿童医院团队在期刊《Digestive Diseases and Sciences》(IF:2.5)在线发表题为:CASC15 Promotes Cholangiocyte Proliferation and Liver Fibrosis by Regulating the HNRNPU-IGFBP3 Axis in Biliary Atresia的高水平研究论文。
目的:活跃的胆管细胞具有大量增殖能力,可激活肝星状细胞(HSCs),并可能导致最终的肝纤维化(LF),然而,这种交互在胆道闭锁(BA)中的作用仍不清楚。我们旨在评估癌症易感候选基因15(CASC15)在BA中的参与情况。
方法:采用胆管细胞类器官培养和测序来鉴定与胆管细胞增殖相关的差异表达长链非编码RNA。检测CASC15在肝组织中的表达水平。运用CCK-8、EdU实验、共培养实验和亚细胞分馏方法研究其功能和亚细胞定位。同时,采用RNA纯化染色质分析结合质谱、RNA免疫共沉淀及RNA测序阐明CASC15的潜在作用机制。
结果:CASC15在BA患者胆管细胞类器官和肝组织中显示出表达升高。胆管细胞中过表达CASC15可增强细胞增殖,并在体外促进HSC激活。CASC15主要位于细胞核中,并被发现与异质核核糖核蛋白U(HNRNPU)相互作用,以维持下游靶基因胰岛素样生长因子结合蛋白3(IGFBP3)的表达,从而促进HSC活化。
结论:本研究揭示了CASC15/HNRNPU-IGFBP3调控网络在BA肝纤维化发病机制中的关键作用。
1. 首次发现长链非编码RNA CASC15在胆道闭锁患者肝组织中高表达,且与胆管细胞增殖标志物CK19及肝纤维化标志物ACTA2呈正相关,提示其参与疾病进展。
2. 建立胆道闭锁患者胆管细胞类器官培养体系,通过Smart-seq测序筛选出差异表达lncRNA,为研究胆道闭锁分子机制提供新模型。
3. 阐明CASC15通过核内结合RNA结合蛋白HNRNPU,调控下游靶基因IGFBP3表达的分子机制,揭示CASC15/HNRNPU-IGFBP3调控轴。
4. 证实CASC15促进胆管细胞增殖并通过旁分泌IGFBP3激活肝星状细胞,揭示胆管细胞与肝星状细胞间新的相互作用模式。
5. 发现CASC15表达水平与肝纤维化程度相关,严重纤维化组表达显著高于轻度组,为胆道闭锁肝纤维化进展提供潜在诊断标志物和治疗靶点。
胆道闭锁(BA)是一种严重的婴幼儿胆道疾病,以肝内外胆管进行性炎症闭塞为特征,导致胆汁淤积和肝纤维化。尽管Kasai手术是标准治疗手段,但超过50%患儿最终仍需肝移植。肝纤维化进展是决定预后的关键因素,其中胆管反应(DR)——即胆管细胞大量增殖并分泌炎症因子激活肝星状细胞(HSCs)——是核心病理环节,但具体分子机制尚不明确。
长链非编码RNA(lncRNA)因其组织特异性和细胞类型特异性,在肝纤维化调控中受到广泛关注。已有研究证实lncRNA H19通过S1PR2/SphK2和let-7/HMGA2轴促进胆管细胞增殖及肝纤维化;lncRNA MEG9则通过结合S100A9驱动炎症反应和纤维化进展。然而,lncRNA在胆道闭锁胆管反应相关肝纤维化中的作用仍缺乏系统研究。CASC15作为细胞增殖调控因子,在多种肿瘤及糖尿病肾病纤维化中已有报道,但其在胆道闭锁中的功能尚未被探索。本研究旨在通过胆管细胞类器官培养结合多组学技术,揭示CASC15在胆道闭锁肝纤维化中的具体作用及分子机制。
1. 临床样本收集与类器官培养:收集47例胆道闭锁(BA)患儿和11例胆总管囊肿对照患儿肝组织,分离EpCAM+胆管细胞,建立气-液界面类器官培养体系,进行Smart-seq测序筛选差异表达lncRNA。
2. 表达验证与相关性分析:采用qRT-PCR检测CASC15在肝组织中的表达水平,免疫组化检测CK19和α-SMA表达,利用Metavir评分系统评估肝纤维化分期,分析CASC15与临床指标的相关性。
3. 功能实验验证:构建CASC15过表达慢病毒载体转染人肝内胆管上皮细胞(HIBECs),通过CCK-8、EdU实验检测细胞增殖能力;建立Transwell共培养体系,将处理后的HIBECs与肝星状细胞系LX-2共培养,Western blot检测纤维化标志物(α-SMA、COL1A1、FN)表达。
4. 机制研究:亚细胞定位实验明确CASC15核质分布;ChIRP-MS联合catRAPID算法筛选结合蛋白,RNA免疫沉淀(RIP)验证CASC15与HNRNPU的相互作用;RNA-seq筛选下游靶基因, rescue实验验证CASC15/HNRNPU-IGFBP3调控轴功能。
Figure 1:该图展示CASC15在胆道闭锁中的表达特征及其与胆管细胞增殖和肝纤维化的相关性。图a显示BA患者来源的胆管细胞类器官出现明显结构萎缩和生长受限;图b的火山图表明CASC15是胆管反应相关lncRNA中差异最显著的分子;图c-j的qRT-PCR、免疫组化和相关性分析结果证实,BA患者肝组织中CASC15表达显著上调,与CK19(胆管细胞标志物)和ACTA2(肌成纤维细胞标志物)呈正相关,且严重肝纤维化组(F3-F4期)CASC15水平高于轻度组(F1-F2期),提示CASC15参与BA肝纤维化进展。
Figure 2:该图验证CASC15过表达对胆管细胞增殖和肝星状细胞激活的影响。图a-b显示慢病毒介导的CASC15过表达效率良好;图c-e的CCK-8、EdU实验和MKI67检测表明,CASC15过表达显著促进HIBECs增殖;图f的共培养实验显示,与过表达CASC15的HIBECs共培养后,LX-2细胞中α-SMA、COL1A1和FN等纤维化标志物蛋白水平明显升高,证实CASC15可通过旁分泌机制激活肝星状细胞。
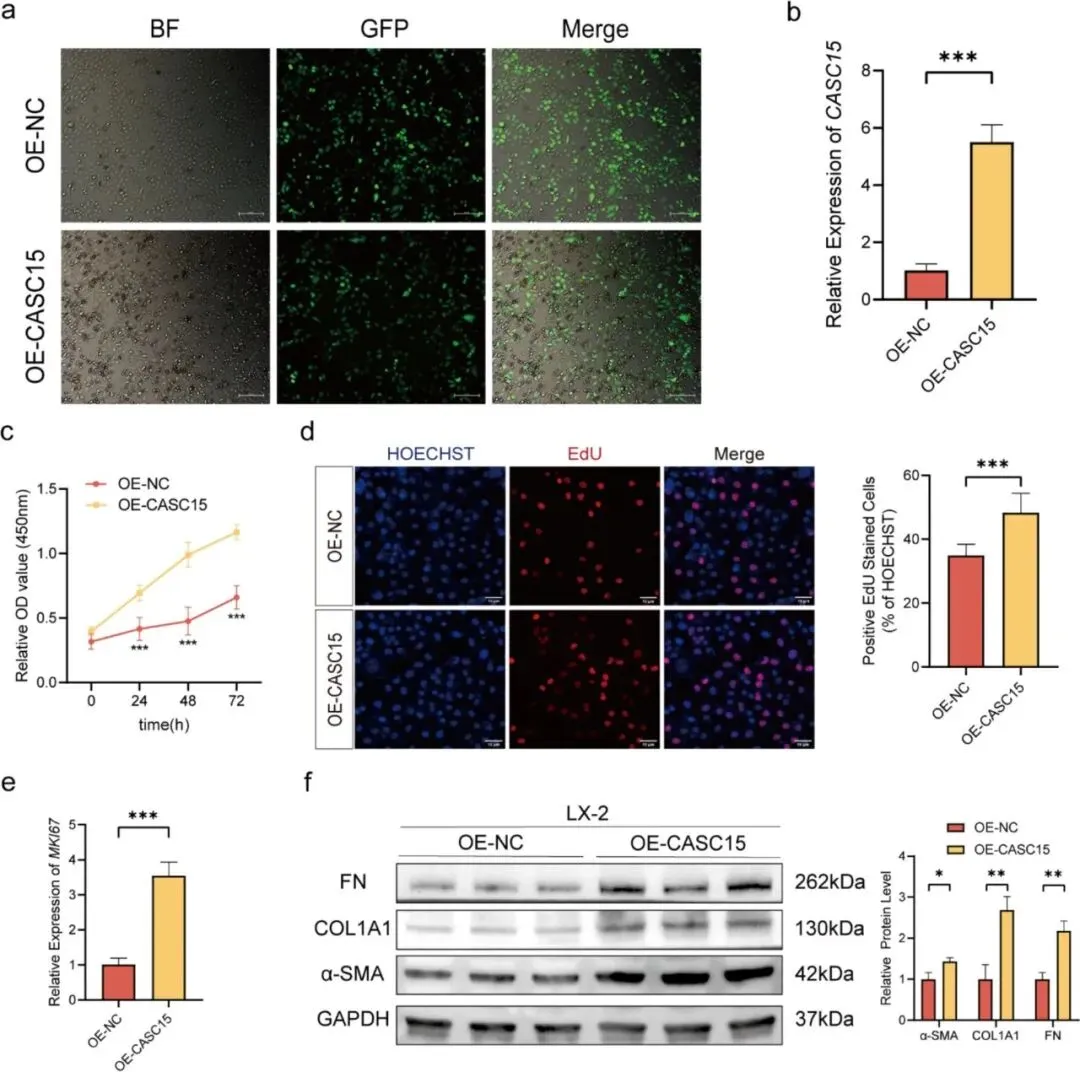
Figure 3:该图揭示CASC15通过调控IGFBP3影响胆管细胞增殖和肝星状细胞激活。图a-b的RNA-seq和GO分析显示,CASC15过表达后差异基因主要富集于细胞增殖和纤维化相关通路;图c-d证实IGFBP3在mRNA和蛋白水平均显著上调;图e-f的临床样本检测显示BA患者IGFBP3表达升高且与纤维化程度正相关;图g-h的功能实验表明,外源性IGFBP3重组蛋白可直接促进HIBECs增殖并诱导LX-2细胞纤维化标志物表达,确认IGFBP3是CASC15的下游效应分子。
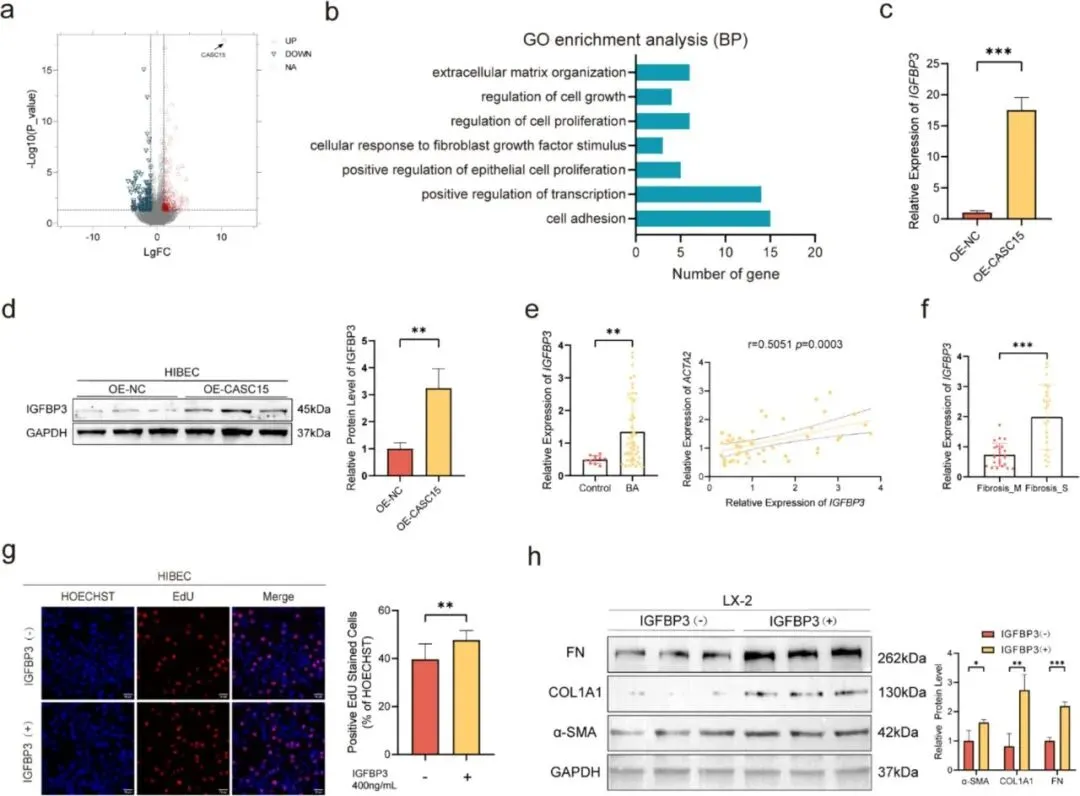
Figure 4:该图阐明CASC15与RNA结合蛋白HNRNPU的相互作用机制。图a的亚细胞定位实验显示CASC15主要分布于细胞核;图b-d的ChIRP-MS、catRAPID算法分析和RIP实验证实,CASC15与核内RNA结合蛋白HNRNPU直接结合,且结合亲和力最高;图e的免疫荧光双标显示HNRNPU与CK19在BA肝组织中共定位,支持两者在胆管细胞中存在功能性相互作用。
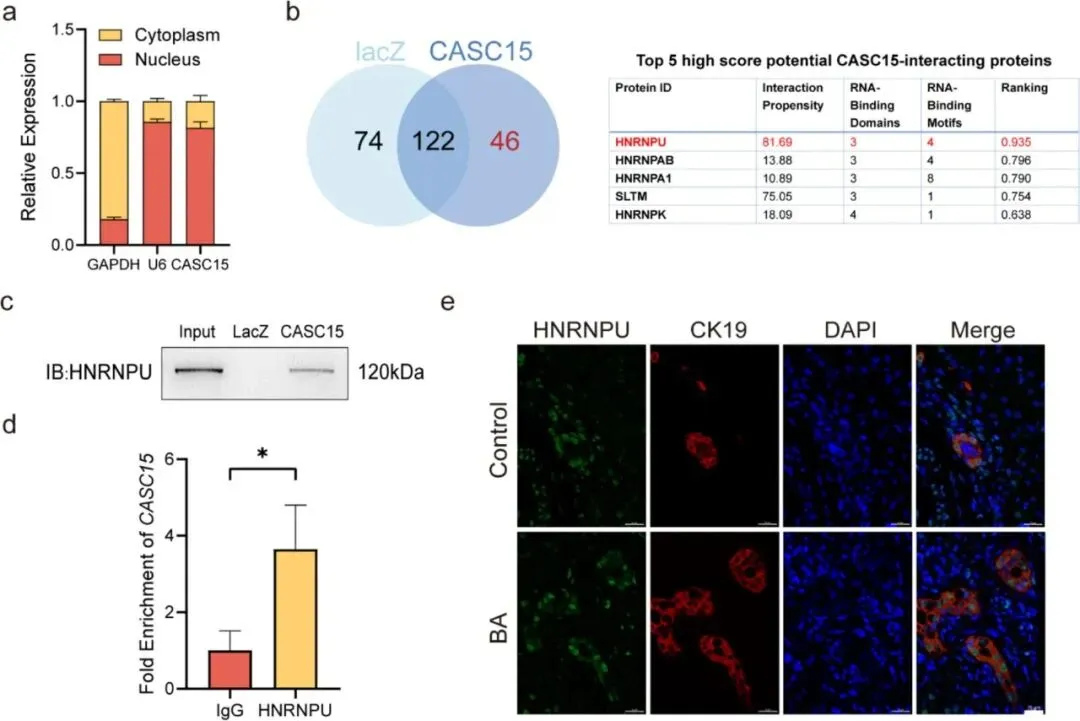
Figure 5:该图通过rescue实验验证CASC15/HNRNPU-IGFBP3轴的功能完整性。图a-b显示,在CASC15过表达的HIBECs中敲低HNRNPU可部分逆转IGFBP3的上调;图c的EdU实验表明,HNRNPU敲低减弱了CASC15促进胆管细胞增殖的效应;图d的共培养实验证实,HNRNPU缺失可阻断CASC15过表达诱导的LX-2细胞纤维化标志物上调,证明CASC15通过结合HNRNPU调控IGFBP3表达,进而驱动胆管细胞增殖和肝星状细胞激活。
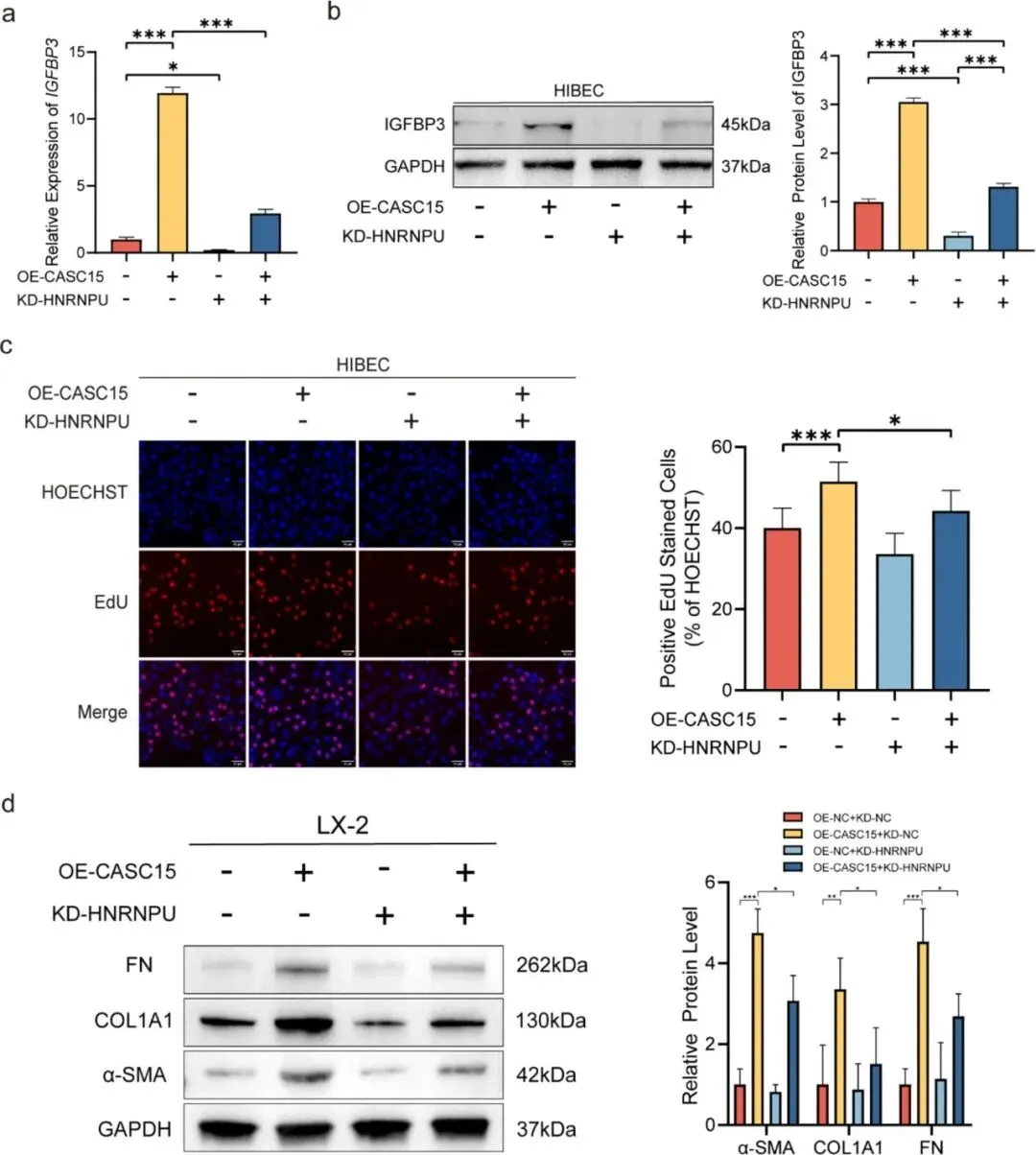
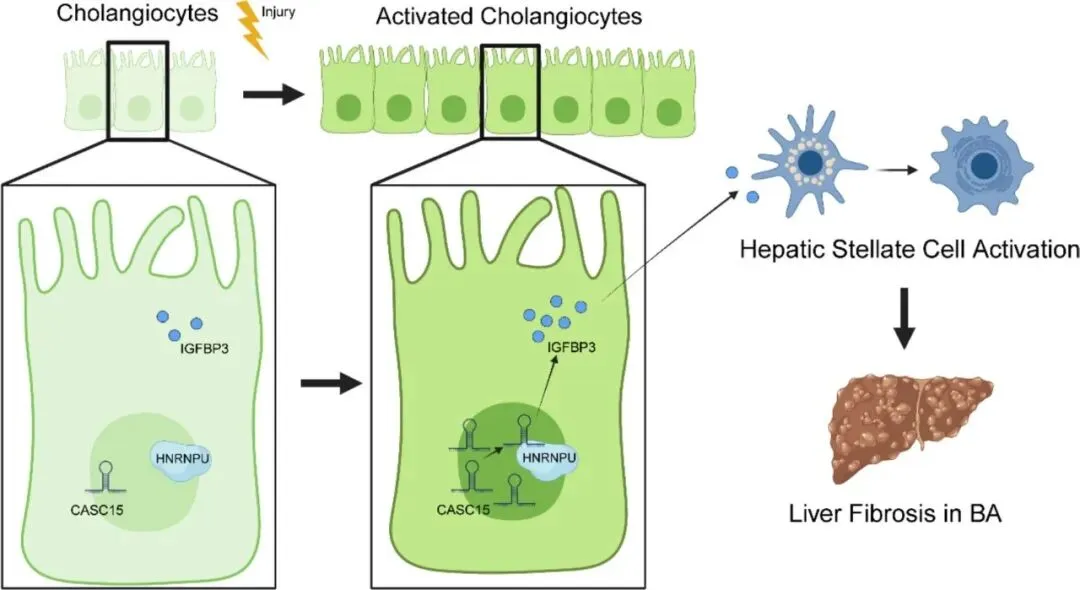
Figure 6:该图为机制示意图,直观展示CASC15/HNRNPU-IGFBP3调控轴在胆道闭锁肝纤维化中的作用模式。正常胆管细胞受损伤刺激后,核内CASC15表达上调并与HNRNPU结合,促进IGFBP3转录和分泌;IGFBP3通过旁分泌作用激活肝星状细胞,导致细胞外基质沉积和肝纤维化,最终形成胆道闭锁特征性的病理改变。
原文链接
https://pubmed.ncbi.nlm.nih.gov/41688795/
版权声明
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅出于学术交流和传播信息的需要,不代表本平台观点或证实其内容的真实性。原文版权归原作者所有,作者如不希望被转载或有侵权行为,请联系本平台删除。