南京大学王毅教授课题组CCS Chem:电化学钴催化脱氟酮-烯烃偶联
- 2026-05-17 16:06:09

导语
醛类/酮类和烯烃是有机合成中的基础分子骨架,因其在自然界中的广泛存在以及商业上的易得性而备受重视。碳碳双键(C=C)和碳氧双键(C=O)是合成化学中极为重要的官能团。它们既能参与极性反应,也能通过自由基途径进行多种转化,从而高效地将平面的sp²杂化碳单元转化为三维的sp³杂化结构。这一特性凸显了它们在现代合成化学中构建复杂分子骨架的核心地位。近日,南京大学王毅教授课题组发展了一种钴催化的电化学还原反应,成功实现了醛/酮与α-三氟甲基烯烃之间的脱氟-烯化偶联,在温和条件下高效构建了一系列2, 2-二氟高烯丙醇类化合物。相关成果在线发表于CCS Chem(DOI: 10.31635/ccschem.026.202506717)。
概述
偕二氟烯烃作为羰基的生物电子等排体,因其能抵抗还原降解而显著改善代谢稳定性,在药物化学中具有重要价值。同时,它们也是构建多种含氟结构的重要中间体。然而,如何高效、绿色地实现醛/酮与三氟甲基烯烃的偶联,特别是避免使用化学计量还原剂和活化试剂,一直以来是一个挑战。王毅教授研究团队利用电化学还原策略,在钴催化剂作用下,实现了醛或酮与α-三氟甲基烯烃的脱氟交叉偶联。该反应条件温和,底物适用范围广,兼容多种醛、酮以及带有取代基的α-三氟甲基烯烃,并可扩展至烯丙醇类底物。尤其值得一提的是,该电化学合成策略在连续流动反应系统中也成功实施,凸显了其良好的可放大性和实际应用潜力。
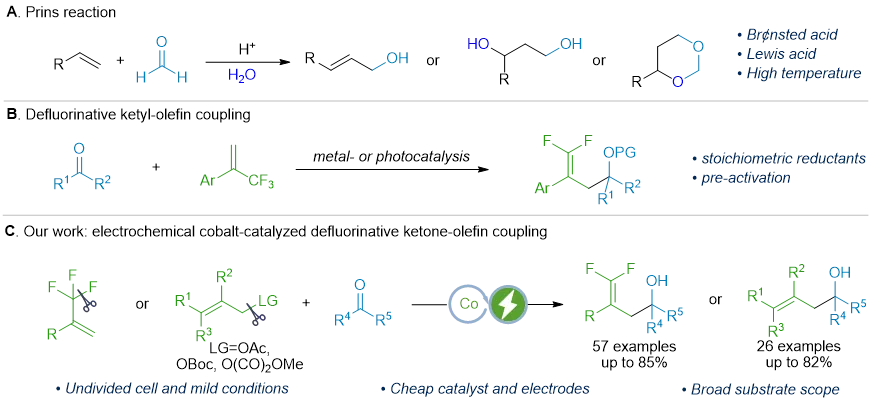
图1. 烯丙位脱氟酮基自由基–烯烃偶联反应:用于合成gem-二氟高烯丙醇(图片来源:CCS Chem)
图文解析
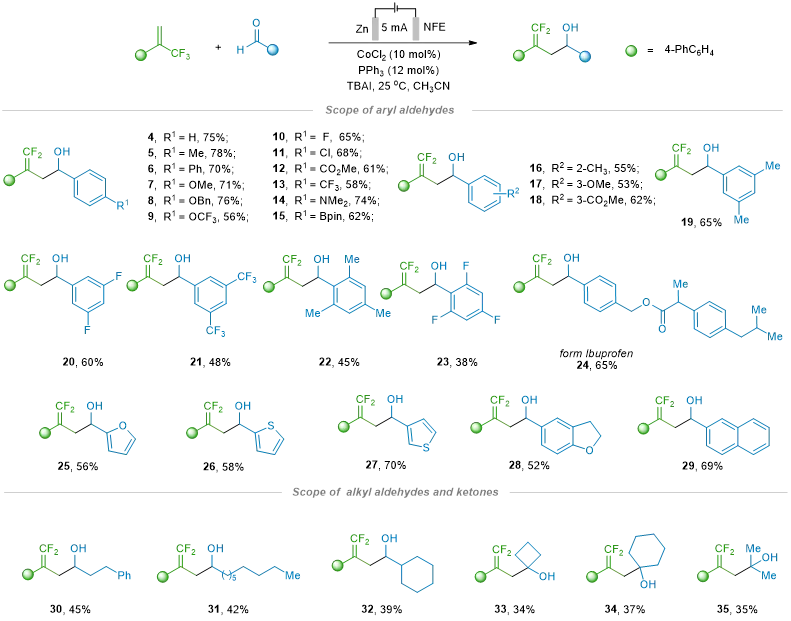
图2. 醛和酮的底物适用范围(图片来源:CCS Chem)
在最优反应条件确立后,作者考察了该电化学转化的底物适用范围,如图2所示。供电子基团取代的底物(3–9)的产率高于吸电子基团取代的底物(10–13)。诸如NMe₂(14)和Bpin(15)等官能团也表现出良好的兼容性,凸显了该方法的温和性。邻位、间位或多取代的醛(19–23)也能顺利反应,证明了该方法的稳健性。布洛芬衍生的醛(24)及具有药理活性的骨架(29)均可获得良好产率的相应产物。呋喃(25)和噻吩(26-27)等杂环也是合适的底物,将该方法拓展至药物化学领域的重要结构单元。脂肪醛(30–32)和烷基酮(33–35)同样具有兼容性,但其产率较芳基底物低,可能是由于过度还原所致。尽管如此,它们的成功转化揭示了进一步优化的可能性。
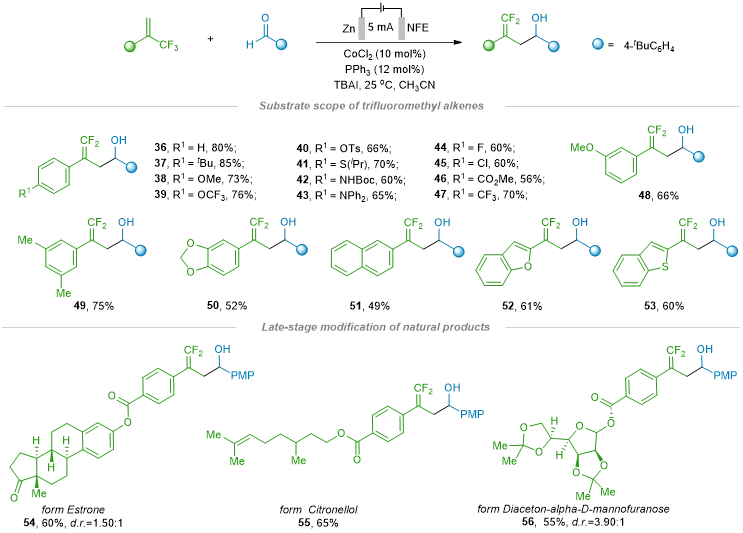
图3.α-三氟甲基烯烃的底物适用范围(图片来源:CCS Chem)
卤素(44, 45)和酯基(46)等官能团均表现出良好的耐受性。含有供电子基团(36-44)或弱吸电子基团(44-45)的α-三氟甲基烯烃能够高效转化为相应的偕二氟烯烃(36–45),产率为60-85%。苯并呋喃和苯并噻吩衍生物等杂环底物也表现出良好的反应活性,分别以61%和60%的产率得到产物(52)和(53)。该反应对复杂分子表现出广泛的兼容性,包括雌酮衍生物(54)、香茅醇衍生物(55)以及甘露糖衍生物(56),为后期官能团化提供了可能。
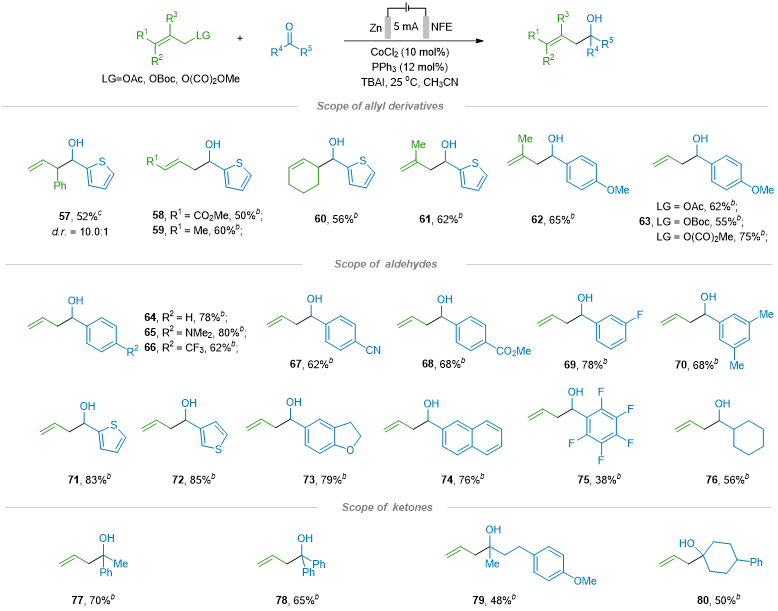
图4. 烯丙醇还原偶联的底物适用范围(图片来源:CCS. Chem.)
如图4 所示,烯丙醇类化合物也是合适的底物。肉桂基衍生物(57)的反应产率为52%,非对映异构体比例为10:1;含酯基的底物或环状底物(58–62)的反应产率为50–65%。芳香醛表现出良好的反应活性,产率范围为62–80%。代表性底物包括含OMe(63)和NMe₂(65)等供电子基团的底物,以及含CF³(66)、CN(67)和CO₂Me(68)等吸电子基团的底物。此外,不同位置带有取代基的底物(69)和多取代体系(70)也能顺利反应。芳基醛(包括杂环芳醛71–73)均表现优异。值得注意的是,全氟代醛也可作为底物参与反应,并以38%的产率得到产物(75)。相比之下,烷基醛和烷基酮的反应活性较低,产率分别为38%和56%。
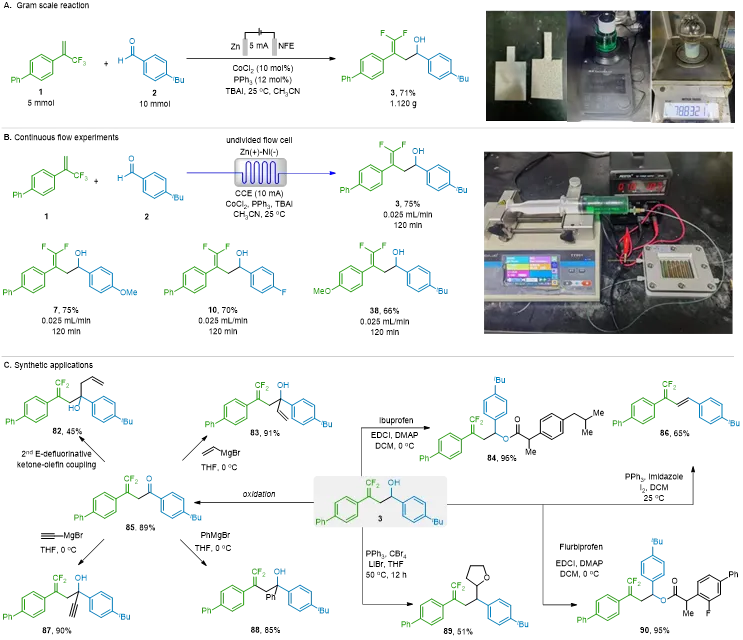
图5. A. 克级反应;B. 连续流实验;C. 合成应用(图片来源:CCS.Chem)
为进一步验证该方法的合成实用性和可放大性,作者在优化条件下进行了克级反应。通过增大电流和电极表面积,以71%的分离产率获得了1.12 g产物(图5A)。随后,作者对连续流系统的流速和电流进行了优化。在最佳参数(0.025 mL/min流速、10 mA电流、2小时停留时间)下,目标产物的产率达到75%。在一系列芳基醛的转化中,连续流装置的表现超越了间歇反应体系,展现了更优的过程可控性,凸显了该连续流工艺在潜在工业应用中的效率和可扩展性(图5B)。通过一系列衍生化反应,进一步展示了产物3的合成多样性(图5C)。与布洛芬和氟比洛芬的酯化反应分别以95%和96%的产率得到产物(84)和(90)。羟基氧化后以89%的产率得到相应的酮(85)。随后与格氏试剂的反应以85-91%的产率得到了烯丙醇(83)、炔醇(87)以及芳基叔醇(88)。通过碘代-消除反应,以65%的产率将(3)转化为产物(86)。有趣的是,Appel型反应以51%的产率得到四氢呋喃偶联产物(89),揭示了该骨架此前未被认知的反应特性。
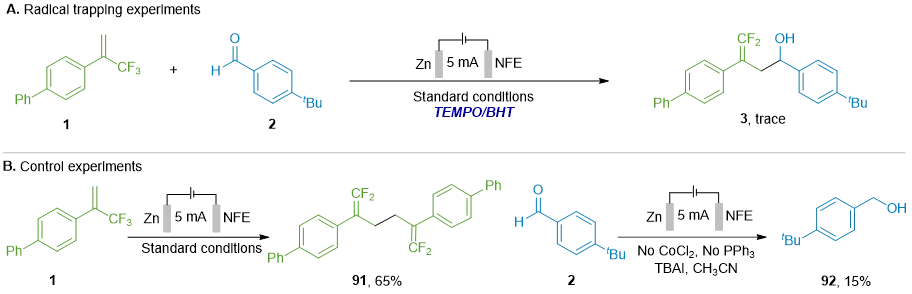
图6. A. 自由基捕获实验;B. 控制实验(图片来源:CCS. Chem)
为了阐明反应机理,作者进行了一系列控制实验,如图6所示。加入TEMPO或BHT等自由基捕获剂后,产物形成完全被抑制,表明反应涉及自由基途径(图6A)。在缺失醛的情况下,α-三氟甲基烯烃发生自偶联;而当缺失烯烃时,主要反应路径为醛的还原,同时伴随少量(<5%)由醛自身偶联产生的频哪醇生成(图6B)。
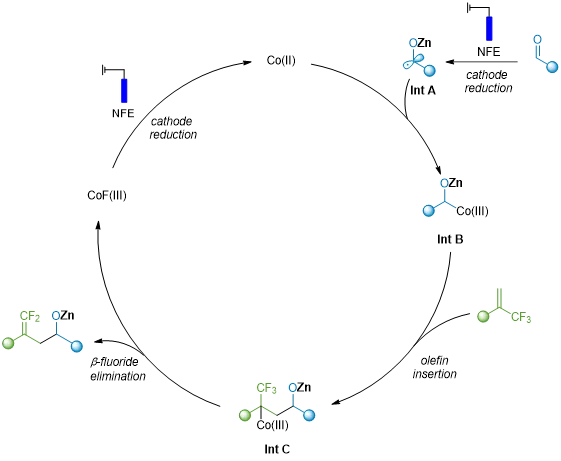
图7. 可能的催化循环(图片来源:CCS. Chem)
基于上述结果及前期文献,作者提出了如图7所示的可能催化循环。在阴极,醛/酮被还原生成羰自由基中间体(Int-A),该中间体会被Co(II)催化剂捕获,形成Co(III)物种(Int-B)。随后,Int-B对α-三氟甲基烯烃进行加成,得到中间体Int-C,该中间体可能经历β-氟消除过程,生成目标产物并再生Co(III)物种。最后,Co(III)在阴极被还原为Co(II),完成催化循环。
总结
综上,作者开发了一种Co/PPh₃催化的电化学脱氟酮-烯烃偶联策略,用于合成偕二氟高烯丙醇。该方法能够在无需化学计量还原剂的温和电化学条件下高效构建结构多样的产物,并表现出广泛的官能团兼容性。机理研究表明该反应涉及电化学产生的羰自由基中间体。克级合成实验验证了该反应的规模化潜力。目前,本实验室正致力于将该反应平台拓展至药物相关的含氟骨架的构建。
南京大学博士生许志敏为该论文的第一作者,王毅教授、Lutz Ackermann教授和倪升阳博士为共同通讯作者。潘毅教授为该论文提出了重要修改意见。
该研究得到了国家自然科学基金、国家重点研发计划(项目编号:2025YFA151110, 22071101, 22271147, 22471123)、江苏省自然科学基金(资助号:BK20230771)、欧洲研究理事会高级资助项目(资助号:101021358)以及德国研究基金会(戈特弗里德·威廉·莱布尼茨奖)的支持。相关成果发表于化学领域期刊CCS Chem,为含氟功能分子的绿色合成及电化学在复杂偶联反应中的应用提供了新思路。
谨以此文纪念胡宏纹先生百年诞辰。
王毅教授课题组简介

王毅教授课题组合影
王毅教授课题组的研究方向涵盖有机氟化学、金属有机合成与催化、半导体材料及能源材料等领域。在有机氟化学方向,课题组聚焦于氟化工生产过程中大量惰性副产物难以活化利用的关键挑战,提出了“弱键牵引”策略,通过对惰性氟源进行分子改造,设计并制备了肟氯酯、磺酰咪唑盐、羟胺甲酸乙酯及肼基甲酸酯等多种新型活化试剂。这些活化基团能够有效激活惰性含氟工业品,将其转化为高附加值的含氟试剂和功能砌块,实现资源化利用。该研究不仅为减少氯氟烃等有害物质的排放提供了可行路径,也显著降低了高附加值氟化工产品的生产成本。当前具体研究方向包括:光催化含氟官能化反应、电化学含氟官能团修饰以及含氟功能单体与材料的开发。
王毅教授简介

王毅,南京大学教授、博士生导师。2005年毕业于南京大学获学士学位,2010年在英国爱丁堡大学获得有机化学博士学位。随后,他先后在圣安德鲁斯大学和哈佛大学医学院从事博士后研究和担任访问学者。2014年起,王毅教授回到南京大学工作,历任副教授、教授。王毅教授长期致力于新型氟化试剂的开发及其在含氟材料领域的应用研究。针对当前氟化工产业中大量惰性副产物难以活化利用的关键科学问题,他提出了基于单电子转移的策略,通过对惰性含氟强酸进行结构改造,成功开发了多种具有自主知识产权的高效氟化试剂。这些试剂能够在温和条件下实现惰性工业含氟原料的高效活化与转化,为构建高附加值的含氟功能分子及含氟聚合物材料提供了新路径。相关研究成果已在国际权威期刊发表论文50余篇,其中包括J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Nat. Commun.、Sci. Adv.、CCS Chem、ACS Catal.等。同时,申请氟化试剂相关发明专利6项。王毅教授的研究工作获得了同行的广泛认可,于2021年获Theme化学奖,并于2023年获得国家级青年拔尖人才计划资助。

| 点击即可阅读合集 | ||
| 催化化学 | ||
| 分析化学 | ||
| 生物化学 |

