文献分析工具:科应智能助手(www.scienceing.com)
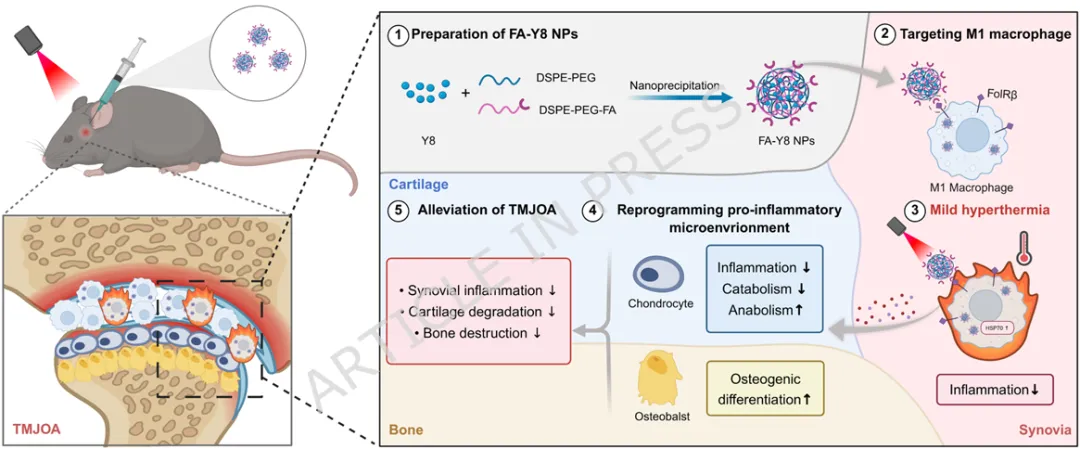
今天,分享一篇南京大学医学院附属口腔医院韩伟教授、李煌教授团队的最新研究文章:Photothermal Title Page Reprogramming of Synovial M1 Macrophages Reshapes the Pro-inflammatory Microenvironment to Reverse Temporomandibular Osteoarthritis(光热重编程滑膜M1巨噬细胞重塑促炎微环境以逆转颞下颌骨关节炎)。
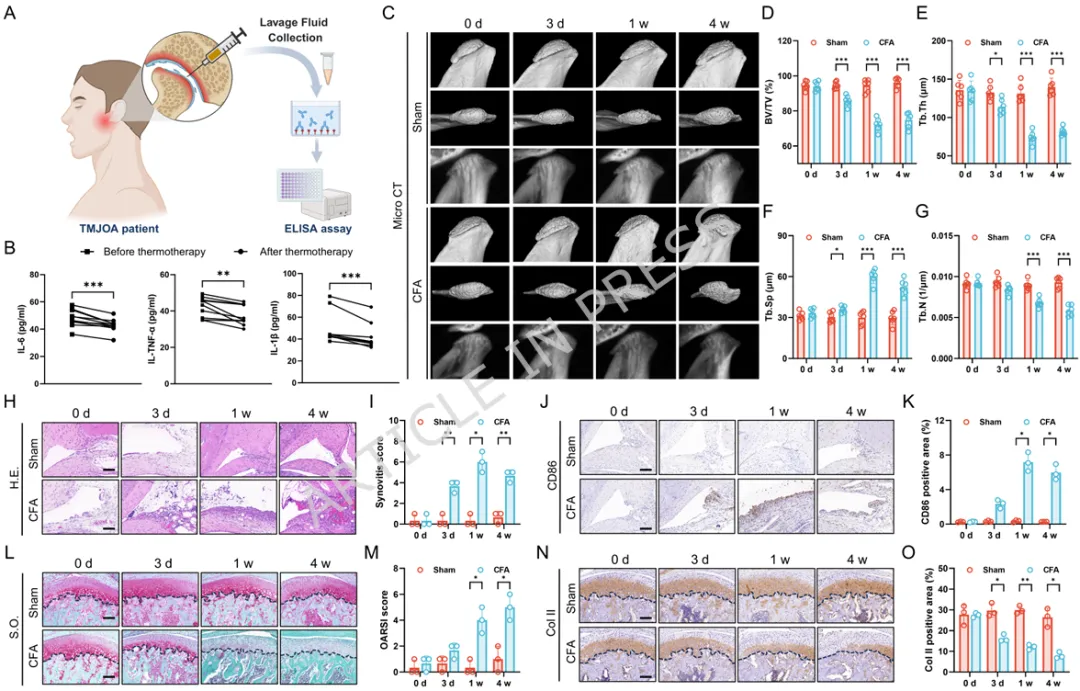
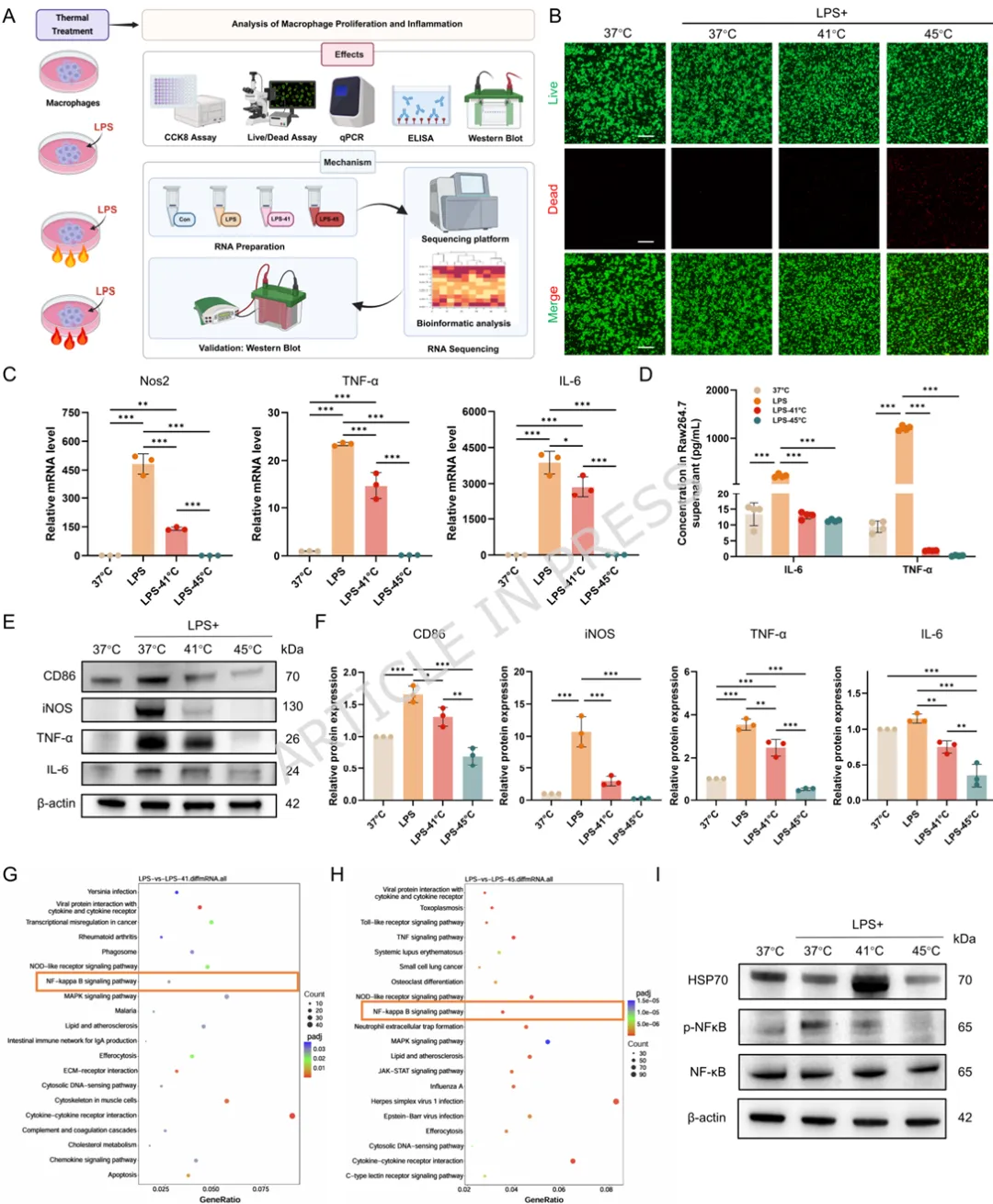
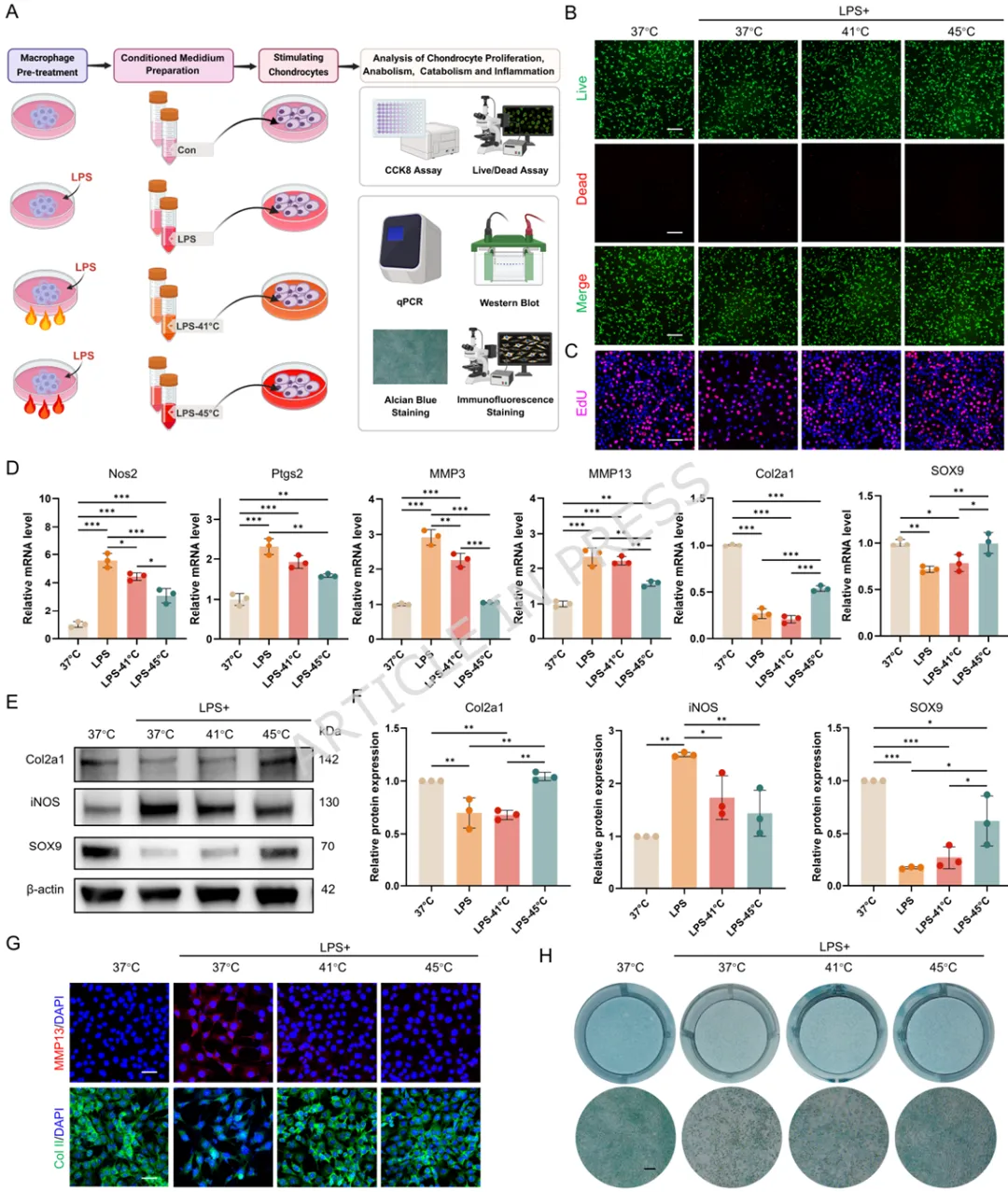
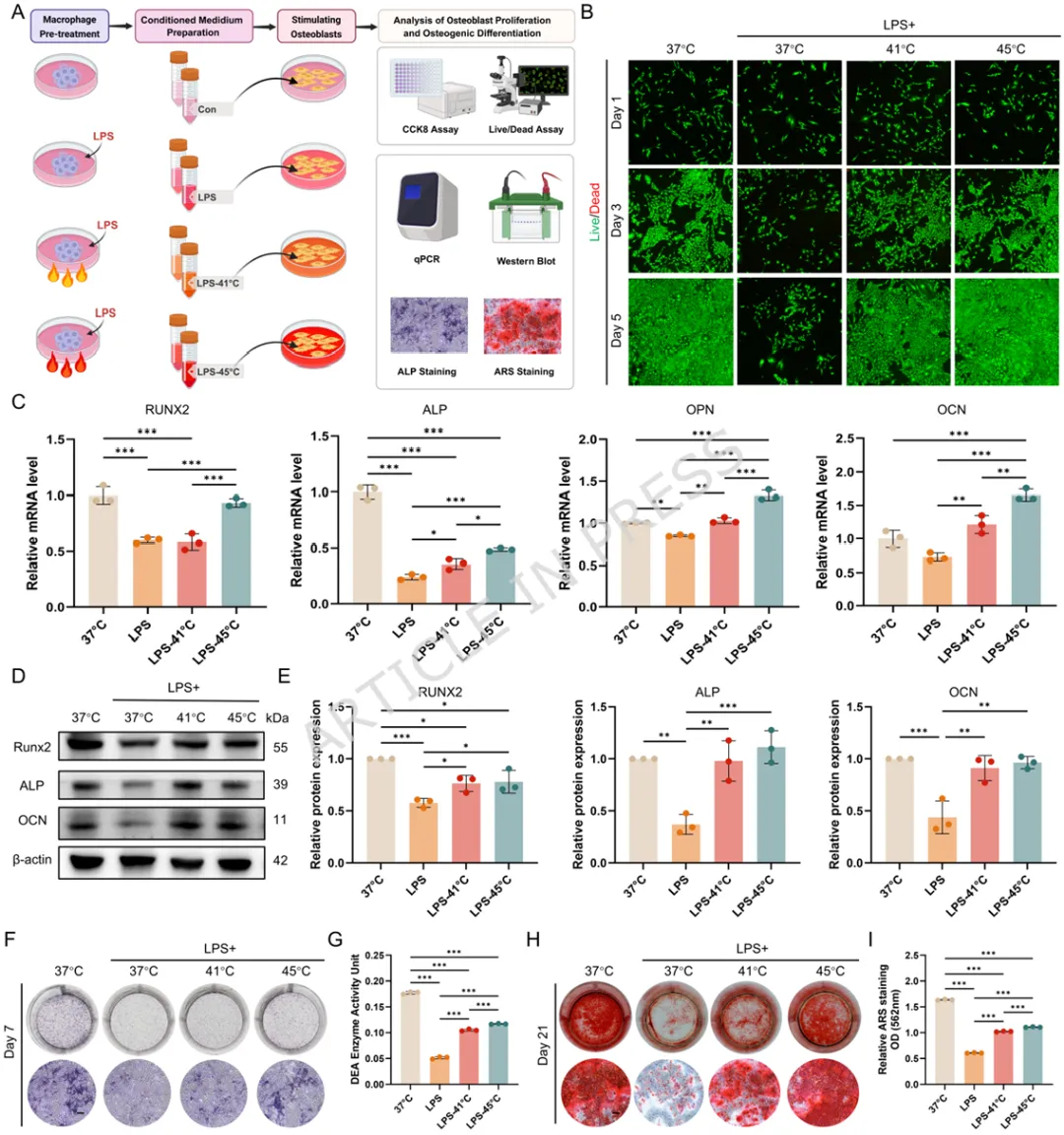
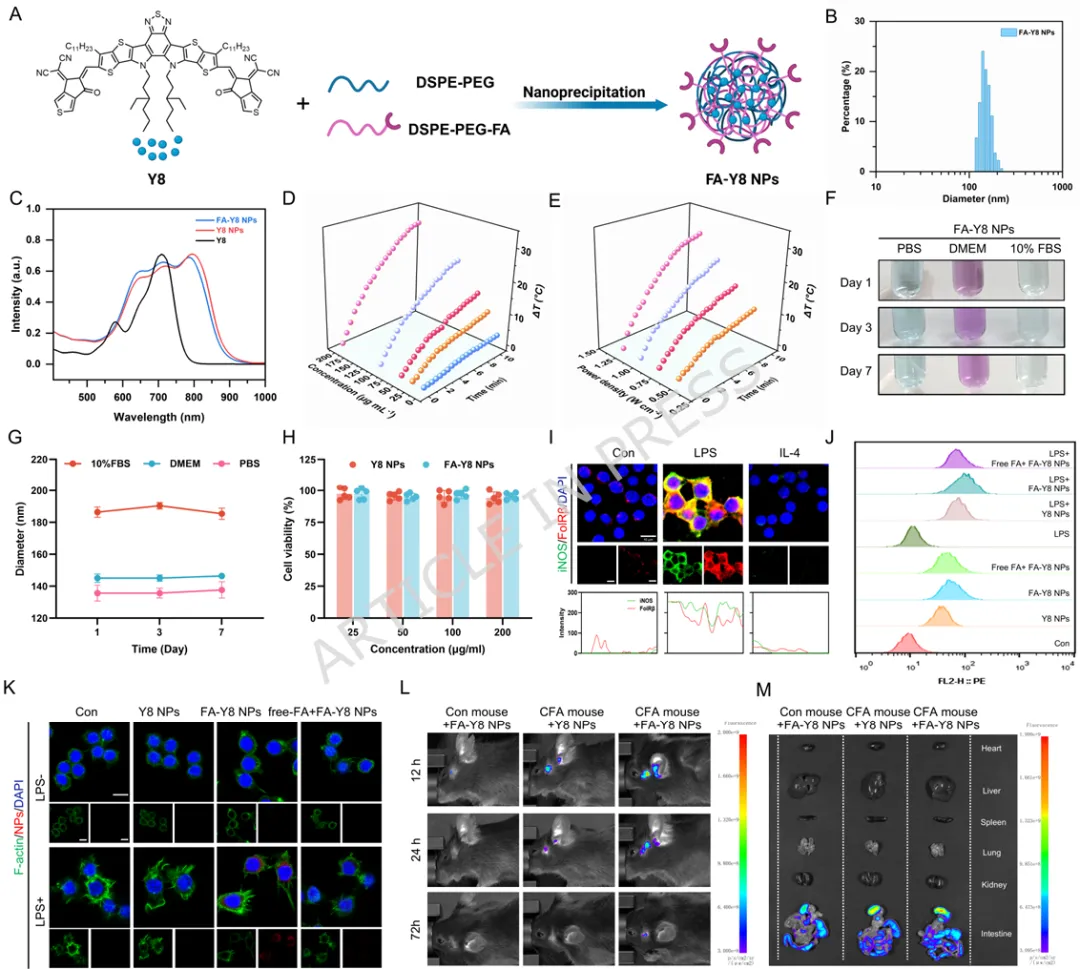
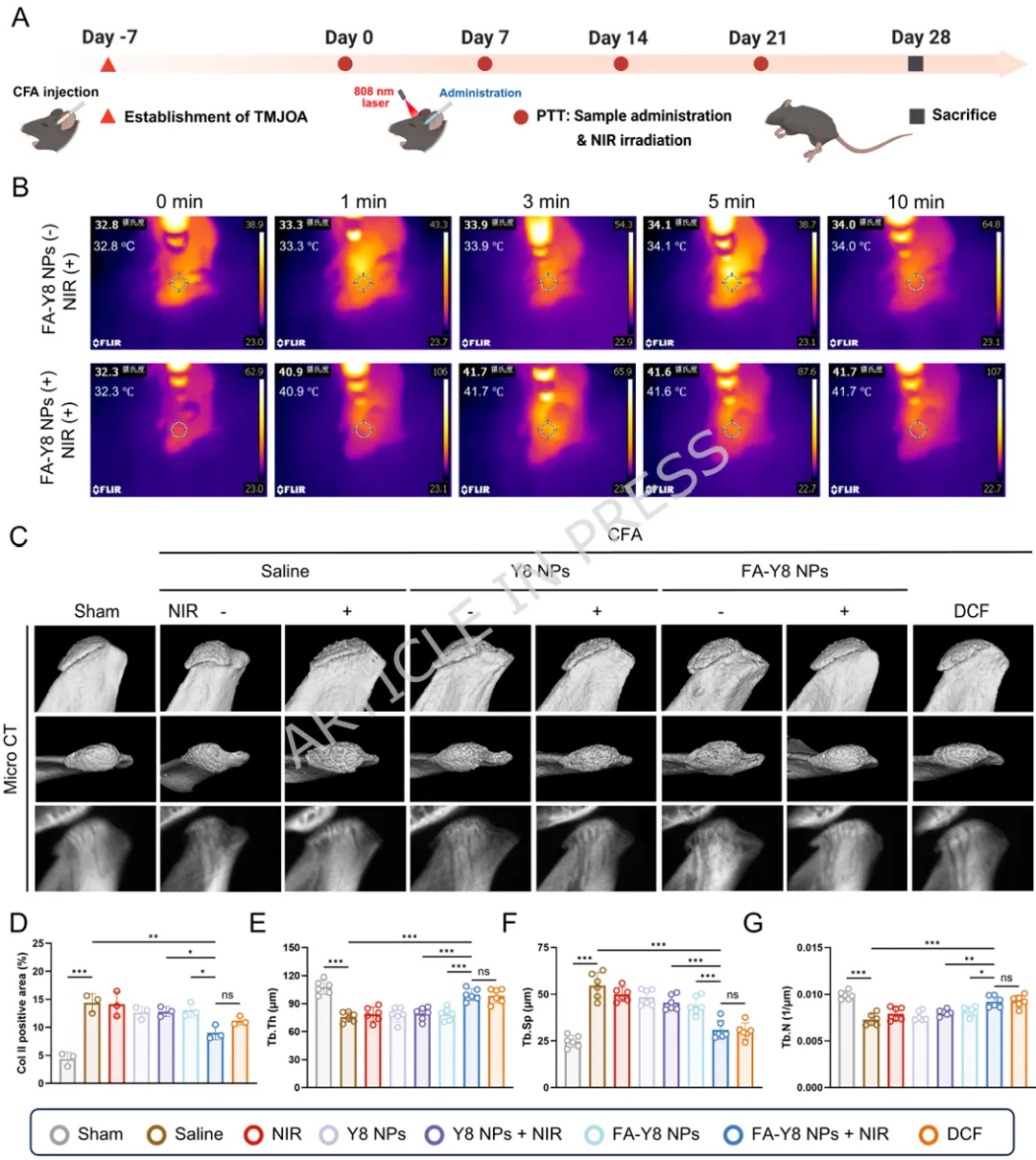
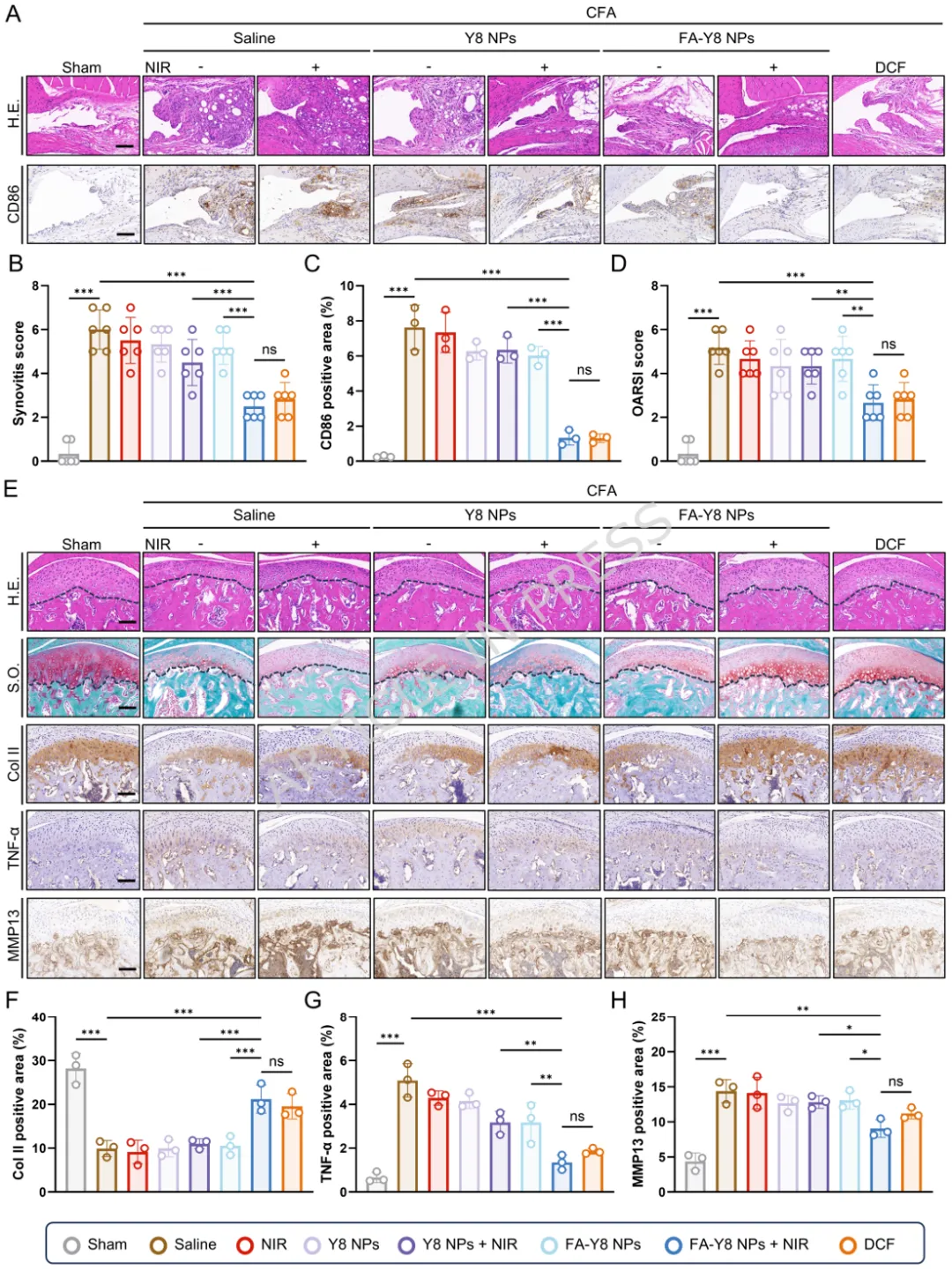
1️⃣ 首次揭示温和热刺激可通过HSP70-NF-κB通路重编程滑膜M1巨噬细胞。2️⃣ 构建叶酸靶向FA-Y8光热纳米平台,实现炎症滑膜M1巨噬细胞精准靶向。3️⃣ 温和光热刺激(41℃)可重塑巨噬细胞分泌谱,抑制软骨分解并促进骨形成。4️⃣ 在TMJOA小鼠模型中,该光热免疫调控策略显著缓解滑膜炎并保护软骨结构。5️⃣ 提出一种从“热疗止痛”到“免疫微环境重塑”的骨关节炎治疗新机制。颞下颌关节骨关节炎(Temporomandibular Joint Osteoarthritis,TMJOA)是一种常见的退行性关节疾病,其主要病理特征包括滑膜炎症、软骨降解以及软骨下骨结构破坏。流行病学研究显示,该疾病在30岁以下人群中的患病率约为14.6%,而在30–80岁人群中可高达28%–32%。随着疾病进展,患者常出现持续性疼痛、张口受限及咀嚼功能障碍,严重影响生活质量。目前临床治疗主要依赖非甾体抗炎药、物理治疗以及手术干预等方式。然而药物治疗往往只能缓解症状,长期使用还可能产生系统性副作用;而手术治疗则创伤大、费用高且不可逆。因此,开发能够从病理机制层面逆转关节炎症及组织退变的新型治疗策略成为该领域的重要研究方向。近年来研究发现,滑膜巨噬细胞在TMJOA炎症进展中发挥关键作用。尤其是促炎型M1巨噬细胞大量浸润滑膜组织后,会分泌TNF-α、IL-6、IL-1β等炎症因子,诱导软骨细胞分解代谢并加速关节退变。因此,调控M1/M2巨噬细胞极化平衡被认为是一种具有潜力的免疫治疗策略。本研究首先通过临床样本分析发现,接受热疗的TMJOA患者滑液中炎症因子(IL-6、IL-1β、TNF-α)明显降低,提示热刺激可能具有抗炎作用。进一步实验表明,温和高温(约41℃)能够通过诱导HSP70表达并抑制NF-κB信号通路,从而显著降低M1巨噬细胞炎症反应。在此基础上,作者设计了一种叶酸靶向光热纳米材料FA-Y8 NPs。该纳米平台能够识别M1巨噬细胞表面的叶酸受体β(FolRβ),从而实现炎症滑膜巨噬细胞的精准靶向。当纳米颗粒在近红外光(808 nm)照射下时,可产生局部温和热效应,实现对巨噬细胞炎症表型的重编程。作者进一步发现,经热调控后的巨噬细胞分泌谱发生显著变化,其条件培养基不仅能够抑制软骨细胞炎症和分解代谢,还能促进成骨细胞矿化能力,从而在多层面改善关节微环境。在CFA诱导的TMJOA小鼠模型中,FA-Y8光热治疗能够显著减少滑膜炎症细胞浸润,降低M1巨噬细胞比例,同时改善软骨退变和软骨下骨结构破坏。整体疗效与临床常用NSAIDs药物相当,但具有更高的靶向性和更低的系统副作用。FA-Y8纳米粒子的构建及其针对TMJOA的靶向光热治疗示意图作者首先收集10例TMJOA患者的关节滑液,并比较热疗前后的炎症因子变化。ELISA检测结果显示,热疗显著降低IL-6、IL-1β和TNF-α水平,说明热刺激能够缓解关节炎症反应。同时在CFA诱导的TMJOA小鼠模型中,通过micro-CT及组织学染色发现滑膜炎症伴随软骨退变及骨结构改变,进一步验证了滑膜炎症在疾病发生中的关键作用。Figure 1、滑膜中的M1型巨噬细胞是CFA诱导的TMJOA的关键驱动因素。(A) TMJOA患者滑膜灌洗液采集与分析示意图。(B) 人TMJOA患者滑膜灌洗液中IL-1β、TNF-α和IL-6的浓度。(C) TMJ髁突的显微CT图像。第1、4行:三维图像矢状面;第2、5行:三维图像水平面;第3、6行:二维图像矢状面。(D-G) 基于显微CT图像对TMJ髁突软骨下骨的BV/TV、Tb.Sp、Tb.Th和Tb.N的定量分析。(H) 关节滑膜H.E.染色的代表性图像。(I) TMJ滑膜炎评分的定量分析。(J) 滑膜区CD86免疫组化染色的代表性图像。(K) CD86表达的定量分析。(L) 关节软骨区S.O.染色的代表性图像。(M) OARIS评分的定量分析。(O) 关节软骨Col II免疫组化染色的代表性图像。(P) Col II表达的定量分析。为探索热疗的免疫机制,作者对LPS诱导的M1巨噬细胞进行不同温度刺激。结果显示,41℃温和热刺激能够显著降低炎症基因表达,同时维持细胞活性;而45℃高温则导致明显细胞毒性。RNA-seq及Western blot结果表明,温和热刺激通过诱导HSP70表达并抑制NF-κB信号通路,从而实现对M1巨噬细胞炎症反应的调控。Figure 2、热疗可减轻巨噬细胞的炎症反应及其潜在机制。(A) 不同温度处理对巨噬细胞增殖及炎症反应影响与机制的实验设计示意图。(B) 按所示条件处理后巨噬细胞活/死染色的代表性图像。(C) 按所示条件处理后巨噬细胞中炎症基因(Nos2、TNF-α、IL-6)mRNA的qPCR分析。(D) 按所示条件刺激后,巨噬细胞培养上清中IL-6和TNF-α的ELISA分析。(E-F) 按所示条件处理后巨噬细胞中M1型巨噬细胞标志物(CD86)及炎症蛋白(iNOS、TNF-α、IL-6)的WB及定量分析。(G) 与LPS组相比,LPS-41°C组上调和下调通路的KEGG分析。(H) 与LPS组相比,LPS-45°C组上调和下调通路的KEGG分析。(I) 按所示条件处理后巨噬细胞中HSP70、磷酸化NF-κB及NF-κB的WB分析作者进一步收集不同条件下巨噬细胞的培养上清,并作用于软骨细胞。结果发现,炎症巨噬细胞上清会显著抑制软骨细胞增殖并促进MMP13等分解代谢基因表达,而热处理后的巨噬细胞上清则能够恢复Col2a1与SOX9表达,并减少软骨基质降解,从而发挥明显的软骨保护作用。Figure 3、巨噬细胞热处理可减轻软骨细胞的炎症损伤。(A) 收集不同巨噬细胞条件培养基并与DMEM完全培养基(CCM)混合用于软骨细胞培养及功能分析的实验设计示意图。(B) 软骨细胞与不同CCM共培养后的活/死染色代表性图像。(C) 软骨细胞与不同CCM共培养后的EdU掺入实验。(D) 用不同CCM培养的软骨细胞中Nos2、Ptgs2、MMP3、MMP13、Col2a1和SOX9基因的相对mRNA表达水平。(E-F) 软骨细胞与不同CCM共培养后Col2a1、iNOS和SOX9的Western blot分析及定量。 (G) 软骨细胞与不同CCM共培养后MMP13和ColI的代表性免疫荧光图像。(H) 软骨细胞与不同CCM共培养后的阿尔新蓝染色代表性图像。在成骨细胞实验中,炎症巨噬细胞上清显著抑制ALP活性及矿化结节形成,而热处理后的巨噬细胞上清则能够恢复RUNX2、OCN等成骨基因表达,并促进矿化沉积,说明热调控巨噬细胞能够改善骨形成微环境。Figure 4、热处理巨噬细胞在炎症环境中挽救成骨细胞功能。(A) 收集不同巨噬细胞条件培养基并与成骨诱导培养基(OCM)混合,用于成骨细胞培养及成骨诱导的实验设计示意图。(B) 软骨细胞与不同条件培养基共培养1、3、5天后的活/死染色代表性图像。(C) 成骨细胞与不同OCM共培养7天后,成骨相关基因RUNX2、ALP和OCN的相对mRNA表达水平。(D-E) 成骨细胞与不同条件培养基共培养7天后,RUNX2、ALP、OPN和OCN的Western blot分析及定量结果。(F) 成骨细胞与不同OCM共培养7天后ALP染色的代表性图像。(G) ALP染色的定量分析。(H) 成骨细胞与不同OCM共培养21天后ARS染色的代表性图像。(I) ARS染色的相对定量分析。作者构建了叶酸修饰的FA-Y8纳米颗粒。TEM与DLS分析显示其粒径约为138 nm,具有良好的稳定性和光热转换效率。在808 nm近红外激光照射下,该纳米材料能够快速升温至约41℃,适合温和光热治疗。细胞实验表明该纳米颗粒可被M1巨噬细胞高效摄取。Figure 5、FA-Y8纳米粒的制备、表征及靶向能力。(A) FA-Y8纳米粒制备示意图。(B) FA-Y8纳米粒的流体力学直径。(C) 游离Y8(THF中)、Y8纳米粒与FA-Y8纳米粒的紫外-可见吸收光谱对比。(D) 不同浓度FA-Y8纳米粒溶液在808 nm激光照射(1 W/cm²,880 nm,10 min)下的温度变化曲线。(E) 不同功率密度下FA-Y8纳米粒溶液(100 μg/mL,880 nm,10 min)的温度变化曲线。(F-G) FA-Y8纳米粒在不同介质中第1、3、7天的代表性图像及流体力学尺寸。(H) 无近红外照射时,Raw264.7巨噬细胞经不同浓度Y8纳米粒或FA-Y8纳米粒处理24 h后的细胞活力。(I) 非激活与激活巨噬细胞中iNOS和FolRβ免疫荧光图像的代表性图像及强度定量。(J) 流式细胞术分析及(K) 罗丹明标记的FA-Y8纳米粒在非激活与激活巨噬细胞中的代表性免疫荧光图像。(L) Y8纳米粒或FA-Y8纳米粒注入TMJ关节腔后12、24、72 h的体内动物荧光成像。(M) 不同处理组主要器官的荧光图像。在CFA诱导的TMJOA小鼠模型中,FA-Y8 NPs联合近红外激光治疗显著改善关节炎症状态。micro-CT结果显示软骨下骨结构得到恢复,而组织学分析则表明滑膜炎症明显减轻,软骨降解减少。整体疗效与传统抗炎药物相当,但具有更精准的局部调控能力。Figure 6、FA-Y8纳米颗粒在近红外照射下的治疗效果评估。(A) 体内实验设计示意图。 (B) 注射FA-Y8纳米颗粒后,颞下颌关节在有无808 nm激光照射下的体内红外热成像图。(C) 不同处理样本后,颞下颌关节髁突的显微CT代表性图像。第1行:三维图像矢状面视图;第2行:三维图像水平面视图;第3行:二维图像矢状面视图。 (D-G) 基于显微CT图像对颞下颌关节髁突软骨下骨的BV/TV、Tb.Th、Tb.Sp和Tb.N进行定量分析。Figure 7、FA-Y8纳米颗粒在CFA诱导的TMJOA小鼠模型中经照射后的治疗效果组织学分析。(A) 关节滑膜经相应处理后H.E.染色和CD86免疫组化染色的代表性图像。(B) TMJ滑膜炎评分的定量分析。(C) CD86的定量分析。(D) OARIS评分的定量分析。(E) 小鼠关节软骨经相应处理后H.E.染色、S.O.染色以及Col II、TNF-α和MMP13免疫组化染色的代表性图像。(F-H) Col II、TNF-α和MMP13表达的定量分析。本研究系统揭示了热疗在颞下颌关节骨关节炎中的免疫调控机制,并提出了一种基于光热纳米技术的精准治疗策略。研究表明,温和高温(约41℃)能够通过诱导HSP70表达并抑制NF-κB信号通路,从而有效抑制M1巨噬细胞炎症反应,并重塑其分泌谱。经过热调控的巨噬细胞能够在旁分泌水平促进软骨细胞合成代谢并抑制基质降解,同时增强成骨细胞分化和矿化能力,从而在多层面改善关节微环境。在此基础上,研究团队构建了叶酸靶向光热纳米平台FA-Y8 NPs,实现对炎症滑膜M1巨噬细胞的精准定位。通过近红外光照射,该系统能够在关节局部产生温和光热效应,从而实现对巨噬细胞炎症表型的重编程。在TMJOA动物模型中,该策略显著减少滑膜炎症、保护软骨结构并改善软骨下骨微结构,其疗效与传统抗炎药物相当,同时具有更好的靶向性和安全性。本研究将传统热疗从单纯的物理止痛手段提升为一种免疫微环境调控策略,并通过纳米光热技术实现精准控制,为颞下颌关节骨关节炎的治疗提供了一种具有重要转化潜力的新思路。参考文献:Wang Y., Ren J., Ren T. et al. Photothermal reprogramming of synovial M1 macrophages reshapes the pro inflammatory microenvironment to reverse temporomandibular joint osteoarthritis. J Nanobiotechnol (2026). https://doi.org/10.1186/ s12951-026-04258-9