高分综述 | 不解剖也能看清楚!南京中医药大学团队一文讲透心脏类器官的成像魔法,揭秘心血管疾病真相
- 2026-04-16 06:48:42

你知道吗?在实验室里,科学家们早已培育出能复刻人体心脏结构与功能的“迷你心脏”——心脏类器官。
它们就像缩小版的心脏模型,不仅能模拟心肌收缩、血管形成,还能重现心血管疾病的病理变化,成为破解心脏奥秘、研发新药的“超级助手”。
但这个“微型心脏”的3D结构复杂、细胞种类多样,还能自主跳动,想看清它的内部构造、追踪电信号传导,可不是件容易事。
先进的成像技术,正是解锁这些秘密的“超高清镜头”,从让组织 “变透明” 的预处理技术,到能捕捉动态跳动的显微镜,这些前沿工具正在为我们打开一扇观察心脏微观世界的大门,解锁心血管研究与新药研发的全新可能!
文章介绍

题目:心脏类器官中的先进成像策略:弥合结构复杂性与功能分析之间的鸿沟
英文题目:Advanced imaging strategies in cardiac organoids: bridging the gap between structural complexity and functional analysis
杂志:Cardiovascular Diabetology
影响因子:10.6
发表时间:2026年1月
PMID: 41618376
Part.01
研究背景
心脏类器官能复刻体内心脏微环境、结构与功能,成为心血管疾病研究和药物研发的关键模型,且FDA推动类器官等非动物实验技术,3C策略也为生物医药研究提供新方向,但心脏类器官的3D结构复杂性、细胞异质性和功能动态性,使传统2D成像无法满足研究需求,3D成像成为其研究的核心挑战。
现有成像技术难以兼顾心脏类器官的结构解析与功能分析,存在光穿透浅、信号衰减、数据处理难等问题,长期4D成像仍处于起步阶段。
因此,亟需系统梳理心脏类器官成像的全流程技术框架,明确各技术的优劣与适用场景,为技术选择提供指导,同时推动成像策略优化,弥合其结构复杂性与功能分析间的鸿沟。
Part.02
研究结果
1. 心脏类器官的主要特征及其独特的成像挑战
心脏类器官由人多能干细胞通过生物材料支架、自组装或工程技术构建,能模拟心脏发育与疾病的关键病理生理特征,用于复制心肌细胞空间排列及糖尿病心肌病、心肌缺血等疾病建模,还可观察节律性收缩和电生理传导。但其三维结构、细胞异质性和功能重塑带来独特成像挑战,需专门解决方案(图1)。
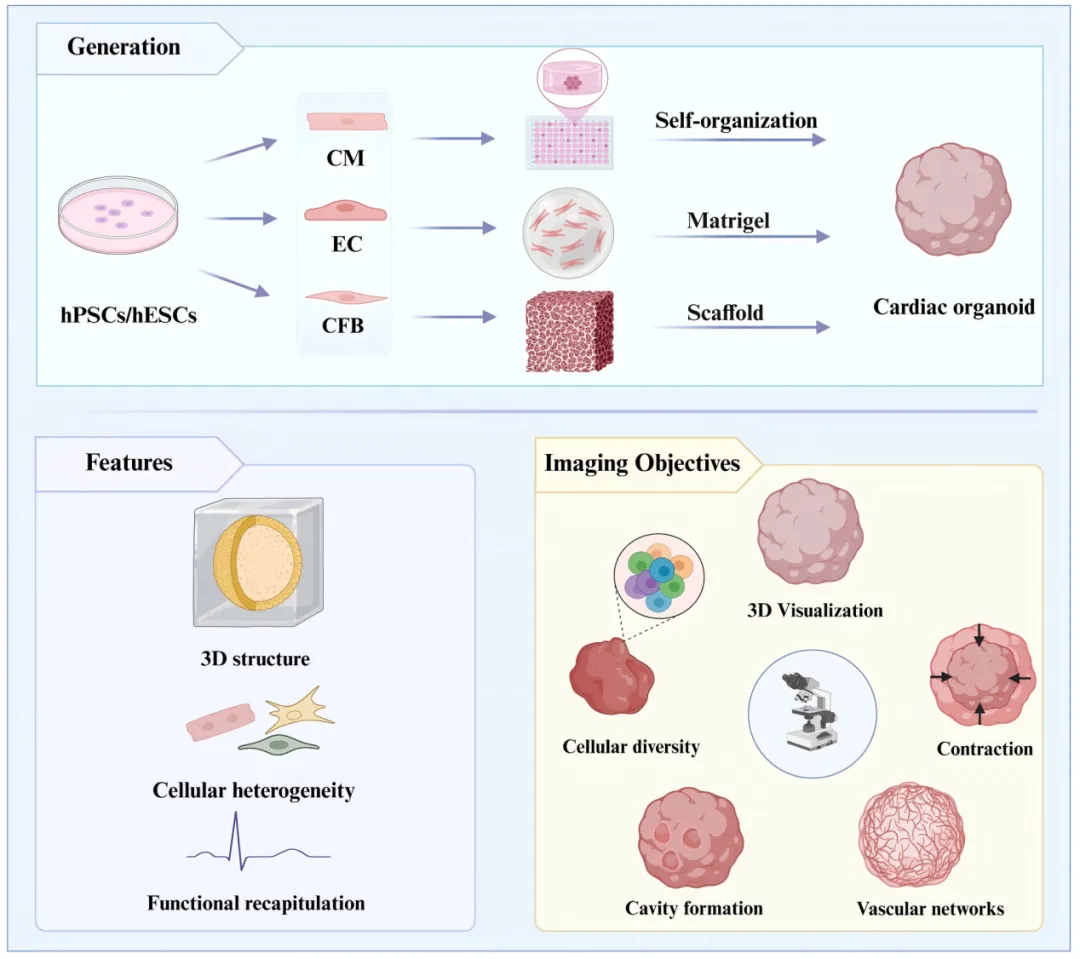
图1
1.1 三维结构复杂性:阻碍深度成像和分辨率均匀性
心脏类器官的核心特征之一是3D结构复杂性,干细胞在3D培养条件下定向分化并空间组织,形成多层心肌组织,能复刻心肌细胞有序排列及3D血管网络,且通过与细胞外基质的相互作用引导细胞空间取向、促进组织重塑,精准模拟天然心脏组织架构与生理微环境。
但这一特性给成像带来关键挑战:类器官细胞致密堆积且有细胞外基质沉积,会导致光散射和自发荧光,传统共聚焦显微镜成像深度仅100-200 μm,即便先进的光片荧光显微镜在未透明化样本中,成像深度超过500 μm也会出现信号衰减,无法清晰呈现血管网络、疾病模型中的纤维化灶等深层结构,难以全面探究类器官的结构全貌。
1.2 细胞异质性:挑战多谱系空间定位和量化
细胞异质性是心脏类器官的核心特征之一,也是其复刻人体心脏结构与功能复杂性的关键,主要体现在细胞多样性与空间分布两方面。细胞类型上,类器官包含心肌细胞、内皮细胞、成纤维细胞等,部分模型还涵盖平滑肌细胞、免疫细胞,丰富了生理相关性;空间分布上,细胞呈区域特异性排列且动态重构,如心肌细胞集中在中央、内皮细胞分布于外周,损伤状态下成纤维细胞会向受损区域定向迁移参与修复。
这一特征给成像带来挑战:需通过多色标记区分不同细胞,但荧光团光谱重叠、染料渗透不均会限制同步检测,模糊细胞间空间关系;此外,糖尿病或衰老类器官中积累的晚期糖基化终末产物(AGE)会产生自发荧光,与常见GFP标记重叠,掩盖微弱的细胞相互作用信号,还会干扰纤维化微环境的定量分析,阻碍疾病模型中细胞间通讯机制的解析。
1.3 功能重述:动态过程跟踪的高时空分辨率要求
功能重现性是心脏类器官的核心特性,使其能复刻心脏关键生理功能,成为疾病建模和药物研发的重要平台。通过模拟心脏发育信号通路及构建多细胞共培养体系,类器官可重现心肌自发收缩、电信号传导、细胞间通讯等原生心脏功能,还能通过电生理记录模拟心律失常,结合空间代谢组学映射代谢活性梯度。
这一特性给成像带来严峻挑战:类器官的节律性收缩易造成运动模糊,影响亚细胞结构和快速钙瞬变的高分辨率观测;化学固定虽能抑制运动,却会破坏离子通道动态和代谢状态,干扰生理真实性。此外,同步捕获电活动与机械收缩需多模态技术协同,但电压敏感染料易光漂白,机械传感器可能破坏细胞外基质完整性,均会影响数据准确性,对成像技术的时空分辨率提出极高要求。
2. 成像前样品制备中心脏类器官的清除方法
心脏类器官成像分实时活体成像与固定样本成像,后者因结构细节更优被广泛用于心脏疾病建模。与传统2D细胞单层不同,其固定样本成像前需经组织透明化预处理。
该流程含样本固定、预处理等多步骤,核心是减少光散射,提升信号穿透力与成像分辨率,主流方法有油基、水凝胶基和水基三类(图2)。
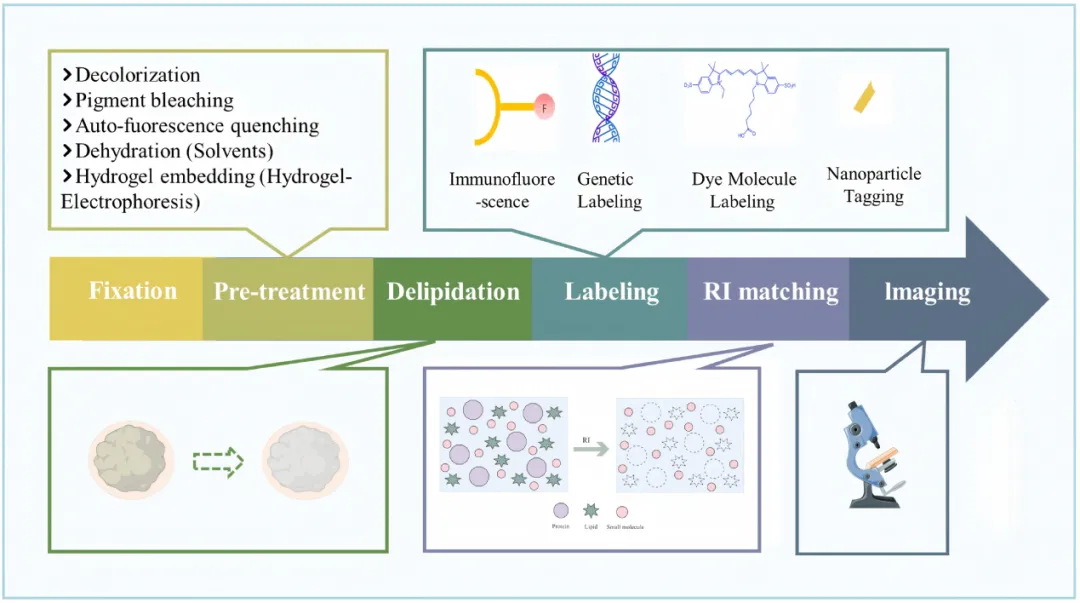
图2
2.1 油基清理法
油基组织透明化技术以iDISCO和BABB方案为代表,核心是利用有机溶剂快速提取脂质、减少光散射,实现组织光学透明。iDISCO的流程包括样本固定、梯度脱水、二氯甲烷脱脂及BABB溶液折射率匹配,BABB方案则更为简便,直接通过溶剂透明化。
该类技术的优势在于处理时间较短,能快速实现中小型、细胞致密的心脏类器官透明化,且依赖常规实验室设备,便于实施,可支持类器官多角度成像与3D重建以解析细胞空间排布。但局限性明显,BABB易导致GFP等荧光蛋白信号淬灭甚至完全丢失,还可能造成蛋白质变性,iDISCO虽适用于结构分析,但其所用有机溶剂也可能损害蛋白质完整性,需搭配免疫标记优化版本(如iDISCO+)才能更好保留荧光信号。
2.2 基于水凝胶的清除方法
水凝胶基组织透明化技术以CLARITY和PACT为代表,核心是将组织嵌入水凝胶基质以保护结构和生物分子完整性,再通过SDS驱动的电泳(CLARITY)或自然扩散(PACT)去除脂质、减少光散射,最终实现透明化,流程含固定、水凝胶灌注与聚合、脱脂及折射率匹配等步骤。
该技术优势显著,能最大程度保留蛋白质结构、内源性荧光信号及组织超微结构,适合大样本或清透后免疫染色,已成功应用于研究药物诱导的心肌损伤。但局限性也较为突出,电泳步骤耗时久,对较大心脏类器官,清透后免疫染色的抗体渗透需长时间孵育,延长实验周期,不利于高通量药物筛选。
2.3 基于水的清除方法
水基透明化技术通过组织脱水、膜通透化及蛋白质构象改变减少光散射,实现高分辨率3D成像,主流技术包括CUBIC和糖醇类方法。
CUBIC采用温和试剂与生理缓冲液,流程简单且pH稳定,能良好保留内源性荧光,已成功用于观察心肌细胞与内皮细胞的3D分布。糖醇类方法以甘油-果糖溶液为代表,可替换细胞内水分,保护生物分子并增强荧光,支持长期储存与可逆染色。
该类技术的局限性在于,组织脱脂和自发荧光消除耗时较长,对致密或大体积心脏类器官,易因脱水、通透不均导致深层残留散射中心,影响透明化均匀性。
2.4 其他新方法
尽管现有组织透明化技术已取得进展,但仍面临组织肿胀或收缩、荧光衰减、低温脆性等问题,难以平衡结构完整性、信号保存与染色兼容性。为此,Gao等人提出了基于离子液体的新型透明化方法VIVIT。
该方法通过脱脂、过电离和离子液化三步将组织转化为玻璃态,借助离子液体特性,实现了优于现有技术的透明度,组织变形控制在1%以内,还能将常见荧光团信号增强2-30倍。同时,它支持低温无损透明化,可避免冰晶形成,便于冷冻切片和长期储存,且处理后的组织可进行多轮免疫染色。目前VIVIT已应用于小鼠和人类大脑,在心脏类器官研究中展现出良好应用前景。
3. 心脏类器官的先进成像方式
3.1 结构可视化技术
3.1.1 共聚焦激光扫描显微镜(CLSM)
CLSM通过Z轴光学切片、逐点激光扫描及共轭针孔滤波实现3D重建,能消除离焦背景信号,支持活组织亚细胞分辨率的无创动态成像,且具备多通道荧光追踪能力,是解析心脏类器官结构与功能的核心工具。
其可结合多通道荧光标记与组织透明化,清晰呈现心肌细胞排列、血管网络等3D架构,还能识别纤维化、血管畸形等病理特征,动态监测收缩节律、电生理活动等生理过程。
但局限性显著,成像深度仅100-200 μm,难以覆盖完整类器官,扫描速度较慢,高激光强度易引发光漂白和光毒性,限制了活细胞长时程观察(图3)。
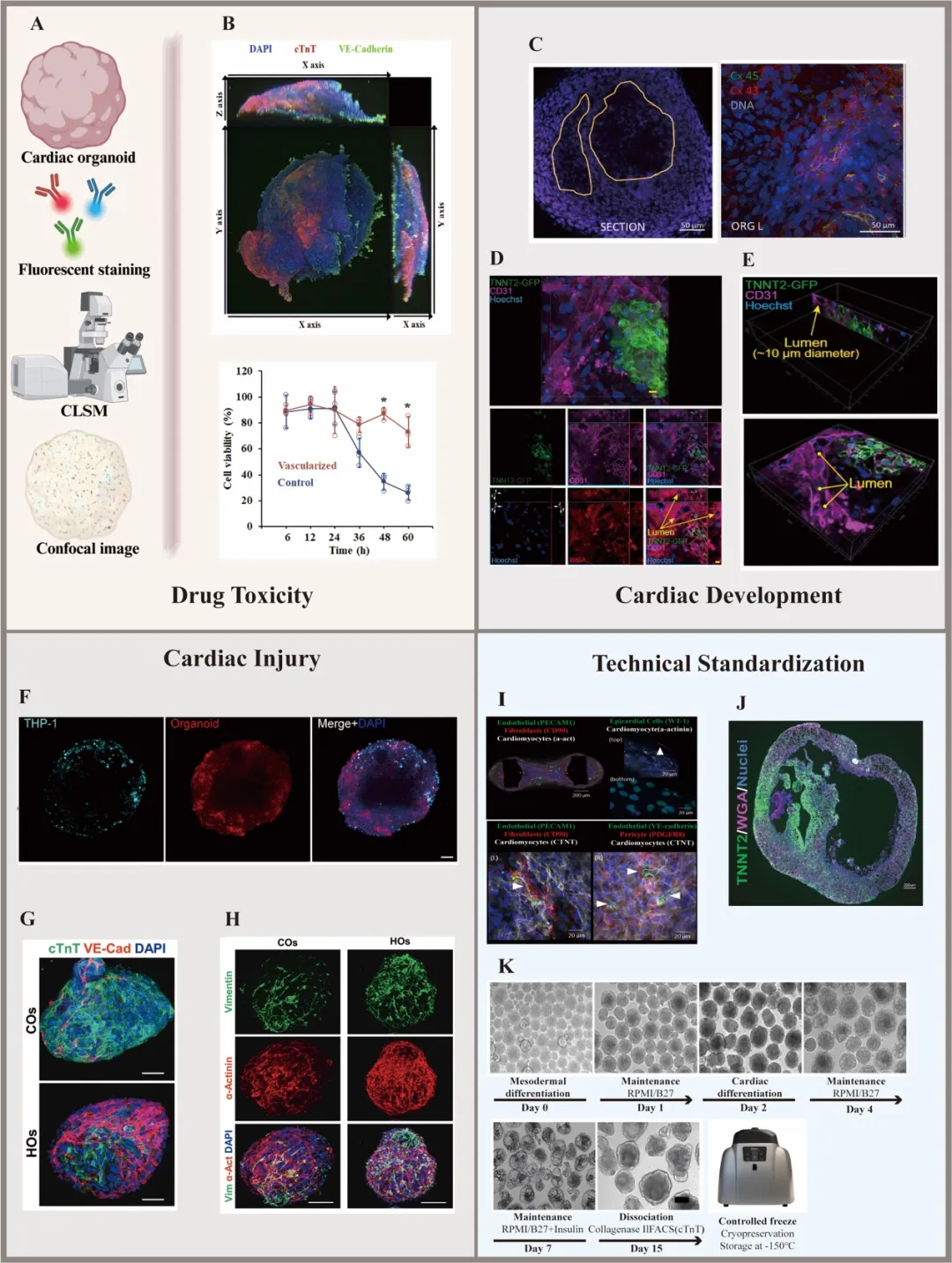
图3
3.1.2 双光子显微镜(TPM)
TPM基于非线性双光子激发原理,以近红外飞秒激光为辐射源,可让荧光分子在亚微米焦体积内同时吸收两个光子,能最大程度减少光损伤,突破传统光学成像的深度限制。
相较于CLSM,TPM的组织穿透深度更优,可达300-1000 μm,约为CLSM的5-10倍,非常适合厚样本的深层成像。其可结合多通道荧光标记,实现心脏类器官的3D荧光重建,还能同步捕捉类器官跳动与器件力学形变,助力类器官-生物电子界面的构建验证。
此外,定制化TPM系统可实现高时空分辨率钙瞬态成像,解析心肌损伤后的信号异质性,但对快速电动力学的成像分辨率有限,更适用于活类器官的长时程动态追踪与多参数数据采集(图4A)。
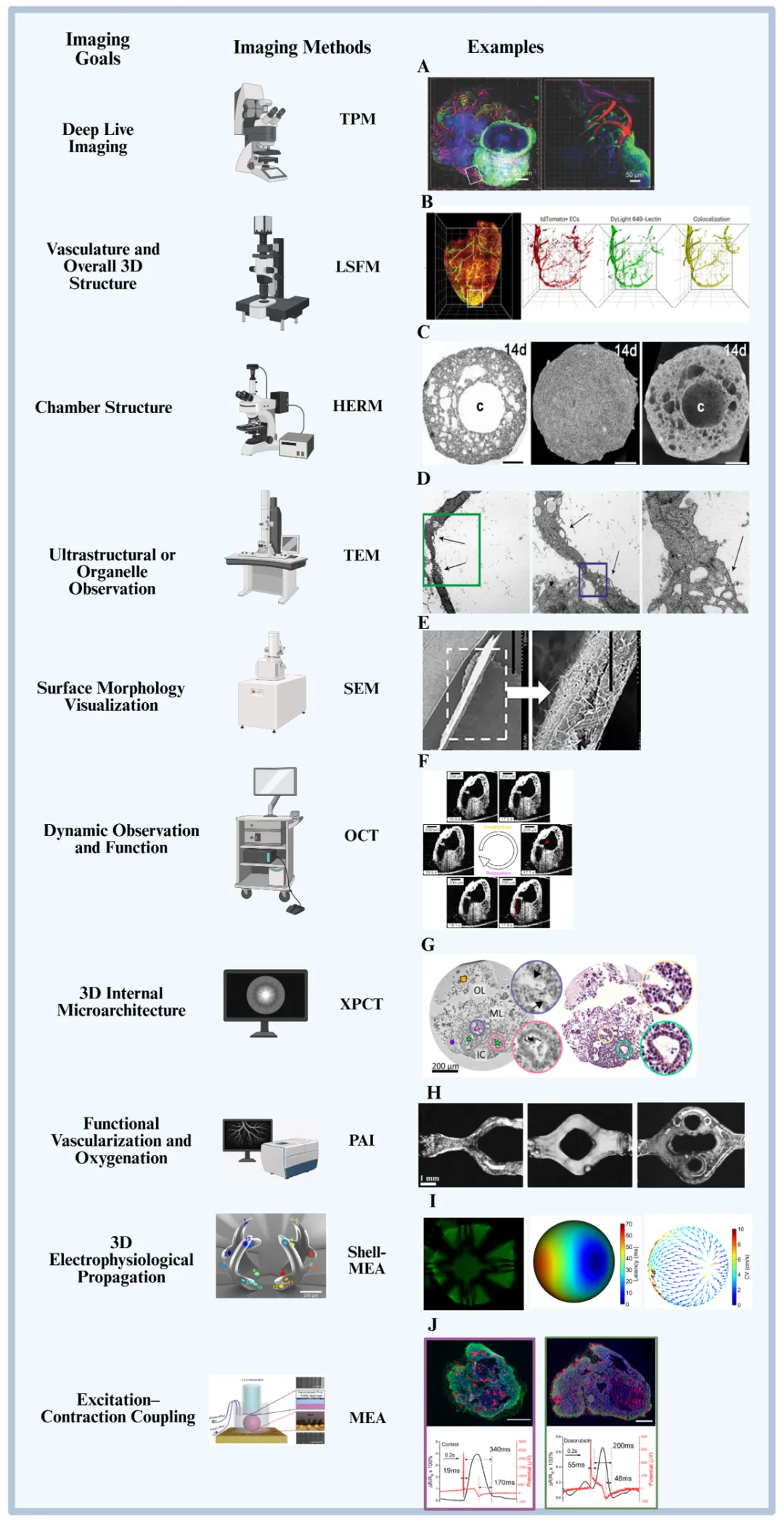
图4
3.1.3 光片荧光显微镜(LSFM)
LSFM采用正交照明与检测模式,通过选择性平面照明结合宽场读取实现成像,能将光暴露限定在焦平面,具备真正的光学切片能力和高轴向分辨率。
其优势显著,扫描速度快(帧率可达数十至数千帧/秒),光毒性和光漂白极低,成像深度超1000μm,适合大型透明化样本的高分辨率3D成像及动态过程长时程追踪。
该技术已广泛应用于动物模型研究,但在心脏类器官领域应用尚少。已有研究将其与荧光凝集素灌注结合,清晰可视化健康与梗死心脏组织的血管网络,为心血管疾病靶向治疗提供空间分辨数据,未来在中大型成熟心脏类器官的光学切片与3D重建中极具应用前景(图4B)。
3.1.4 高分辨率落射显微镜(HREM)
HREM通过将样本嵌入树脂等可固化介质,经微米级刀片自动连续切片,同步落射照明与图像采集,所获二维图像可直接堆叠成高分辨率3D数据集,无需后续对齐处理。
其优势显著,视野大(可达1 cm³)、分辨率达微米级,且无需组织透明化,适合非透明样本的三维形态与病理研究,还可与多种成像技术联用实现多尺度分析。借助改良的S-HREM技术,已实现人类左心室心脏类器官的全息重建与定量评估。
但该技术存在不足,样本制备可能引发非均匀收缩变形,扫描拼接易产生伪影,且无法进行长时程实时追踪,需与其他技术整合以弥补短板。
3.1.5 透射电镜(TEM)
TEM凭借亚纳米级分辨率,成为评估心脏类器官超微结构成熟度的关键工具。其可清晰观测肌节排列、线粒体成熟度、T管形成等亚细胞结构,揭示类器官在体外培养中逐步贴近原生心肌的结构特征,还能通过对比正常与基因缺陷类器官的超微结构差异,验证特定基因在心肌成熟中的作用。
但TEM存在明显局限,仅能成像超薄切片,无法实现完整3D结构重建,样本制备复杂易引入伪影,且需在真空、固定条件下进行,无法用于活样本或动态过程观测,成像视野狭窄也难以评估类器官整体空间异质性,更适用于静态结构表征而非功能或整体分析(图4D)。
3.1.6 扫描电子显微镜(SEM)
SEM通过高能电子束扫描样本表面并检测反射信号,获取三维形态信息,是观察类器官架构与表型重塑的常用工具,能清晰呈现心脏类器官的外部组织形态和细胞排列特征。
其在心脏类器官研究中已有实际应用,例如可观察到类器官外层心肌细胞紧密黏附、排列有序,还能评估电纺纳米纤维支架对类器官形成的影响,发现心肌细胞会沿支架纤维纵轴均匀分布并呈细长形态,体现出良好的细胞黏附与定向排列效果。但局限性明显,仅能捕捉表面拓扑结构,无法穿透组织观察内部,样本制备过程可能导致细胞表面轻微变形,且仅能提供静态结构信息,无法反映动态功能过程(图4E)。
3.1.7 光学相干层析成像(OCT)
OCT基于低相干干涉原理,利用近红外光散射特性实现无创3D断层成像,无需电离辐射或荧光标记,轴向分辨率达1-15 μm,可清晰勾勒心脏类器官的腔室边界、心肌排列及新生血管。
其优势在于兼具高空间分辨率与实时性,结合扫频或谱域检测技术,能实现每秒数万次线扫描,动态监测类器官跳动收缩。通过与深度学习、M模式成像等结合,可自动分割腔室、量化功能参数,追踪发育过程中形态与收缩功能的成熟变化。但局限性明显,成像深度仅1-2 mm,高分辨率容积成像会产生海量数据,对计算处理能力要求较高(图4F)。
3.1.8 x射线相衬断层扫描(XPCT)
XPCT利用X射线相位信息增强软组织对比度,相较于传统X射线技术,其软组织分辨率更高,且无需造影剂。
该技术可实现无标记、无损的高分辨率3D成像,特别适合观察心脏类器官中细胞与组织分布、血管化及腔室形成等复杂结构。已有研究将其应用于心脏形成类器官成像,成功捕获细胞分布、腔室结构和组织层等详细内部信息,且成像后样本仍可用于后续病理检测。
但目前XPCT在心脏类器官研究中多依赖石蜡包埋的固定样本,活体成像潜力尚未充分开发,且其成像数据的3D重建与后处理流程复杂,常规应用门槛较高。
3.1.9 性能对比
不同心脏类器官结构可视化技术在通量、性能和资源需求上各有取舍。点扫描技术如CLSM和TPM,能提供亚细胞级高空间分辨率,但因串行扫描通量低,且存在成像深度浅、光毒性等问题,不适合大规模药物筛选。
平面/体积成像技术如LSFM和OCT为高吞吐量选择,LSFM可快速对大型复杂类器官进行3D成像,光损伤小,OCT无需标记即可实时监测结构与收缩功能。TEM、SEM、HREM等专用互补技术,能揭示亚细胞超微结构、表面形态或实现全类器官重建,但需固定样本,存在变形风险,且在活体或高含量研究中无通量优势。高吞吐量技术会产生海量数据,依赖AI辅助处理,低吞吐量技术数据集小,后续处理需求低。
3.2 功能表型成像技术
3.2.1 电生理成像
电生理成像技术是评估心脏类器官功能成熟度的关键工具,可实时监测细胞或组织的电信号传导与钙动力学,为疾病建模、药物筛选和再生医学提供支持。
该技术能精准测量类器官发育过程中钙动力学和膜电位变化,如shell-MEA装置可包裹类器官实时记录区域场电位,提升空间分辨率;标准化方案借助MEA和微电极技术,实现场电位与动作电位的定量分析。
在病理模拟中,其可揭示缺血性心脏病、心律失常等机制,“Heart-on-a-Miniscope”平台能高效监测药物诱导的电信号与钙信号变化,为心脏修复研究和 毒性筛选提供可靠数据。
3.2.2 力学成像和力传感
收缩力是反映心脏类器官成熟度与生理相关性的核心功能指标,力学成像与力传感技术是定量评估其收缩功能的关键工具,主要包括原子力显微镜(AFM)、牵引力显微镜(TFM)和布里渊显微镜,广泛应用于2D心肌细胞模型与3D心脏类器官系统。
AFM可通过检测心脏类器官的力学动态区分心律失常亚型,借助悬臂梁捕捉垂直偏转和侧向力信号,结合回归残差方差分析量化收缩同步性,经药物验证可实现高保真心脏毒性筛选。TFM是量化心肌细胞收缩力的金标准,尤其适用于遗传性心血管疾病模型,能通过检测突变心肌细胞的峰值力和位移,揭示基因变异与心肌功能缺陷的关联。
布里渊显微镜则以非接触、无标记优势,通过声子散射量化力学特性,规避了接触式技术对细胞微环境的干扰,为心脏力学研究提供了新方向。
3.2.3 代谢成像
代谢成像是评估心脏类器官功能成熟度的重要手段,聚焦ROS、NADH等关键代谢物的动态变化,反映能量代谢状态,核心技术以拉曼显微镜为代表。
拉曼光谱成像是无标记、无损技术,通过分子振动特征频率识别生物分子,可区分心肌谱系区域,为心脏类器官研究提供化学层面验证,助力解析心脏发育的空间模式与组织分化。
此外,NADH/FAD自发荧光成像等技术,有望实时监测心脏类器官中代谢中间体的积累,评估其对线粒体功能和氧化应激的影响,为探究缺血再灌注损伤等场景下的代谢重编程与组织修复机制提供支持。
3.3 多技术集成与跨技术组合策略
3.3.1 机电耦合与多模态功能评估
在心脏类器官功能评估中,收缩力与机械功能检测和电活动监测同等重要。多模态技术的整合搭建了全面评估平台,可同步捕获电活动与机械功能,深入揭示类器官的机电耦合特性。
Lyu等人设计的柔性超灵敏“力传感膜”,与MEA技术结合,能实时监测类器官的电活动和收缩力,药物处理后可观察到节律场电位时程与收缩力的显著变化,实现机电耦合分析。
Yin等人将电生理成像与机械传感器联用,实时监测动态跳动的心脏类器官,通过关联电活动与收缩力,为研究兴奋-收缩耦合提供新平台,为疾病模型的药物筛选和心脏毒性评估提供有价值的数据支持。
3.3.2 微型心脏集成平台
Heart-on-a-Miniscope是一款紧凑的集成平台,融合长工作距离小型荧光显微镜与芯片心脏技术,整合了光学成像、电刺激和芯片培养功能。
其改良后的小型显微镜空间分辨率达3.3-3.7μm,时间分辨率为60帧/秒,可透过80-120μm玻璃基底对Cal-520染色的类器官进行钙信号成像。PDMS芯片设有七个微孔和平行碳电极,经伊伐布雷定预处理抑制自发收缩后,能实现0.5-2Hz的均匀电起搏。
该系统可量化钙瞬态参数,区分多类药物的心脏毒性,其经济高效的开源设计适用于高通量生理相关药物筛选,且通用性强,可拓展至亚细胞动态成像。
3.3.3 OCT -荧光双模成像系统
OCT-荧光双模态成像系统整合谱域OCT与荧光显微镜,可同步采集人类心脏类器官的3D结构与电生理数据。OCT模块采用850nm激光,轴向和横向分辨率分别达2.1μm和3.9μm,支持实时容积成像;荧光模块共享物镜,以470nm LED激发钙指示剂GCaMP6f获取电生理读数。
该系统通过OCT M模式与钙成像同步获取一致的跳动模式,能检测类器官不同区域的双重频率,动态对比度OCT分析可精准定位具不同频率的跳动簇。其将结构动态与钙信号关联,支持无创体外监测,助力揭示心肌细胞亚型复杂性,为相关研究提供有力技术支撑。
3.4 新兴成像技术及其在心脏类器官中的潜力
除常用成像技术外,多种新兴技术在心脏类器官研究中展现出巨大潜力。光声成像(PAI)融合光学与超声技术,可实时监测血管、血流及血氧水平,已成功应用于3D打印血管网络成像,能量化血氧变化与血栓形成影响,有望用于心脏类器官血管化进程等实时监测。
低相干全息断层扫描(LCH)等新兴无标记模态,经脑、肠道等类器官系统验证,可实现活类器官的长期无标记3D成像,亚细胞分辨率下成像深度达190μm,为心脏类器官研究提供了新的技术方向,具有广阔应用前景。
3.5 成像技术和生物学相关性
先进成像技术是连接其3D结构与动态功能的关键,为疾病建模、药物筛选提供观测手段,更是解析心脏发育、心律失常、缺血损伤等核心机制及免疫-心脏相互作用的重要桥梁。
其中干细胞报告基因成像是基础工具,通过GFP、GCaMP等标记,可实时追踪心肌谱系细胞的分化、空间定位与电生理活动,还能结合微图案化、CRISPR-Cas9等技术,揭示基因调控与结构对收缩功能的影响,为发育毒性筛选提供支撑。
同时,高时空分辨率成像技术可观测心腔形成的细胞自组装过程,钙成像结合报告基因能量化心律失常的钙信号异常,光片荧光显微镜可解析缺血再灌注后的血管重构;ROS响应纳米传感器还能可视化免疫细胞与心肌细胞的相互作用,阐明心脏修复的免疫调控机制。
此外,电生理和多模态功能成像进一步拓展分析维度,结合各类新兴无标记成像技术,构建了结构、功能、代谢、免疫多维度整合的心脏类器官综合评估体系。
4. 心脏类器官图像分析的计算和生物信息学方法
成像技术是解析心脏类器官3D结构、动态功能与病理表型的核心,但这类器官固有的空间复杂性、细胞异质性和节律收缩特性,对成像分析方法提出高要求。其图像分析工作流含四大核心模块,需协同软件与算法,在系统化框架下完成多维度表征(图5)。
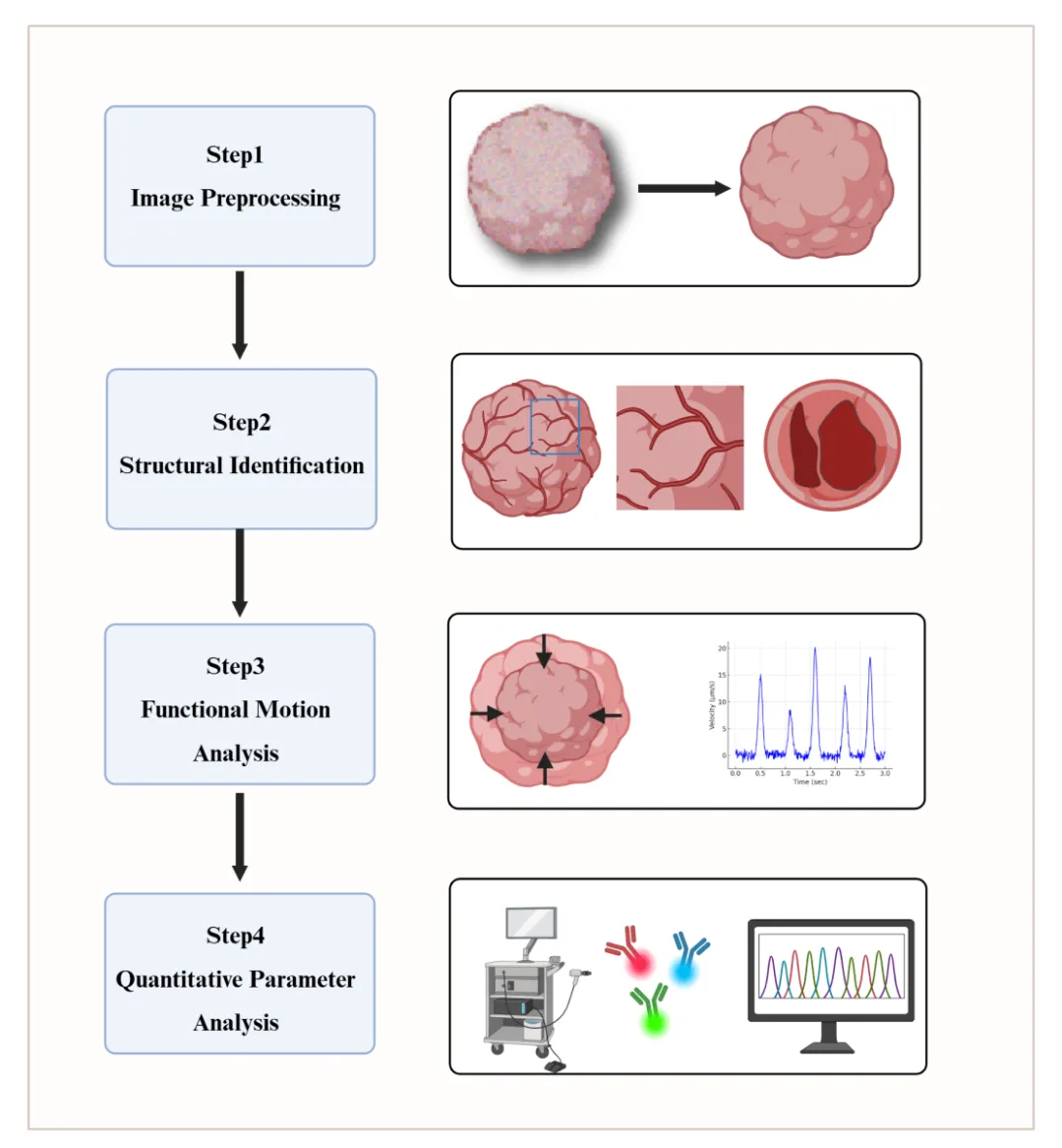
图5
4.1 图像预处理
图像预处理是心脏类器官结构识别与功能分析的基础,其核心是解决原始成像数据因类器官3D复杂性和自主收缩产生的运动伪影、噪声干扰、背景荧光等问题,通过去伪影、抑噪声、消背景提升图像清晰度与对比度。
经透明化处理的样本易出现球差、色差等光学像差,需校准透明介质折射率并多视角成像,保障3D重建准确性。针对成像高噪声问题,可借助AI多尺度分割和超分辨率算法融合3D数据集优化图像。
Organalysis是该领域专用软件,集成图像增强、定量分析、降噪等功能,可为类器官发育、空间架构研究提供技术支撑。
4.2 结构识别
结构识别是心脏类器官图像分析的第二阶段,核心是基于预处理后的图像,借助图像分割和机器学习算法,精准定位并分割类器官边界、心腔、心肌层等核心结构特征。
因心脏类器官成像存在细胞密度高、结构异质性强等问题,需依托人工标注数据训练模型,常用Trainable Weka Segmentation、ilastik等平台。U-Net算法因能融合高低分辨率特征图,成为该领域主流分割算法。在此基础上开发的OrgSegNet模型,可自动分割类器官边界与内部腔室,实现大小、跳动频率等参数定量评估。
同时,相关显微图像数据集的构建,也推动了AI分析工具的发展,助力类器官生理状态的量化判断。
4.3 功能运动分析
功能运动分析是评估心脏类器官成熟度和药物反应的关键环节,核心围绕其自发或刺激下的收缩活动展开分析,通过边缘检测、运动矢量追踪、AI增强追踪等技术,定量跳动频率、最大舒缩速度、搏动时长等核心生理参数,这些参数是判断其功能状态、构建病理模型及评估药物变力效应的直接依据。
边缘检测适用于形态规则的成熟类器官,而光流分析通过像素级运动矢量估算,成为无标记追踪心肌形变的金标准,PIV-MyoMonitor系统还能提取22项运动相关参数。深度学习的整合进一步实现了大数据集自动特征提取,为药物筛选和毒性评估提供了高效的分析手段。
4.4 定量参数分析
定量参数分析是心脏类器官图像分析的最后一环,核心是整合前序步骤数据,提取有效指标并挖掘变量关联,实现多维度解读。分析需覆盖从腔室形态、血管网络到细胞分布的多空间尺度,可结合OCT和免疫荧光标记完成结构与分布的微创检测。
针对类器官自发收缩特性,需高时间分辨率方法捕捉钙瞬变、电生理动态,提取心率、钙瞬变时长等核心生理参数。该环节整合时空维度定量数据,全面评估类器官形态、功能与病理特征,为解析心脏发育、疾病机制和药物响应提供关键依据,是实现图像数据向生理机制解读转化的核心步骤。
5. 心脏类器官成像定量的标准化和可重复性
心脏类器官成像定量分析的标准化和可重复性,是其从基础研究走向药物筛选、疾病建模等实际应用的关键。目前不同实验室在样本制备、培养及成像流程上的差异,易导致检测结果不一致,阻碍研究间的数据对比与整合,因此亟需建立覆盖从图像采集到定量分析全流程的标准化框架。
在结构定量上,现有成像技术虽能无损捕获高分辨率3D结构信息,但领域内缺乏图像分割、3D重建的统一标准,影响结果可重复性;功能定量需摆脱定性观察,转向自动化、无偏分析,2025年推出的开源工具Arrhythpy可自动分析钙瞬变信号、量化心律失常评分,提升了功能评估的客观性与通量。
疾病建模中,病理变化的精准定量对验证模型和评估疗法至关重要,传统阈值分割法易受噪声等影响,结果一致性差,开发能对比不同量化算法的质控软件,对减少分析偏差、建立量化标准具有重要意义。
结论
从样本预处理到多维成像,再到AI辅助分析,心脏类器官成像技术已搭建起一套完整的“观察体系”!
这些技术各有所长:组织透明化技术让“迷你心脏”告别光学遮挡,CLSM、TPM等成像技术既能看清心肌细胞排列、血管网络分布,又能捕捉收缩节律、电信号传导,而多技术融合与AI算法更突破了成像深度、分辨率的瓶颈。
不过目前,成像深度与分辨率的平衡、长时程动态成像等仍是待解难题。未来,随着新型光学探针、无标记成像、多模态整合等技术的发展,我们将更精准地解码心脏病理的时间动态规律。
相信在这些技术加持下,心脏类器官会成为更贴近人体的研究模型,为心血管疾病治疗和新药研发注入更强动力,让医学研究更高效、更精准!
参考文献
Zhao K, Tang B, Gu R, Liu C, Zhang H, Gao Y, Wang P, Gu Y, Shi M, Li Z. Advanced imaging strategies in cardiac organoids: bridging the gap between structural complexity and functional analysis. Cardiovasc Diabetol. 2026 Jan 31. doi: 10.1186/s12933-026-03086-3.
“

”
添加客服小助理,获取原文PDF
往期推荐