南京+直播:5月22-23日 《新法规下药品计算机化系统验证与数据可靠性核心模块要点及案例实操研修班》
- 2026-05-01 08:26:48
关于举办“新法规下药品计算机化系统验证与数据可靠性核心模块要点及案例实操研修班”的通知
各相关单位:
当前,全球药品监管格局持续迭代,国内外计算机化系统与电子数据监管法规要求不断收紧,计算机化系统验证(CSV)合规、数据可靠性(DI)管控已成为药品研发、生产、检验全链条的核心监管红线,更是药企规避风险的必修课。在监管趋严、飞检常态化的当下,企业面临国内外法规差异难以厘清、CSV全流程执行不规范、数据可靠性漏洞频出、AI系统与新型仪器合规无章可循、迎审应对缺乏实操经验等行业痛点。基于此种背景,飞天教育将于2026年5月22-23日在南京+线上举行“新法规下药品计算机化系统验证与数据可靠性核心模块要点及案例实操研修班”,届时将邀请业内资深的CSV和DI专家,精准聚焦药企合规需求,针对全球法规进展进行解读,重点从系统分类、风险评估、验证全流程(URS/DQ/IQ/OQ/PQ)、再验证与退役,到数据可靠性管控、ALCOA+原则落地、DI体系搭建、仪器/信息/AI系统实操等核心模块进行解析,搭配迎审案例、常见问题解析以及案例实操,打通从法规理解到流程执行,最终到体系落地的全流程,帮助企业提升计算机化系统和数据可靠性的合规能力。
中国医药教育协会制药技术专委会副主任委员;山东大学管理学院研究生导师及特聘行业导师,以及多家医药相关高校的特邀讲师。拥有20年医药行业质量管理工作经验,为数百家国内制药企业和多地药监局提供GMP咨询、培训和审计服务。

1、帮助学员熟悉计算机化系统国内外最新法规及差异性要求;
2、帮助学员掌握CSV核心流程操作及文件编制要点;
3、帮助学员掌握数据可靠性管理要求以及体系建立与维护要点;
4、帮助学员掌握仪器设备系统、信息系统与AI系统的数据可靠性实操要点;
主题 | 主要内容 |
一、计算机化系统验证法规进展及趋势分析 | 1.全球计算机化系统验证管理法规和指南差异性解析 ① 国际计算机化系统验证分类(评定原则) ② GAMP5分类计算机系统验证管理 ③ 欧盟附录11《计算机化系统》、附录22《人工智能》的更新要点及验证管理要求 |
二、计算机化系统验证核心流程以及关键输出 | 1.计算机化系统分类与风险评估 2.验证计划(VP):风险评估转化为验证策略 3.用户需求规范(URS):如何撰写高质量URS 4.CSV执行全流程要点解析及核心输出 ① 设计阶段:功能规范(FS)、设计规范 (DS)、代码审核(CR)的目的及编制要点 ② 确认阶段-设计确认(DQ)如何确保设计符合URS要求 ③ 安装、运行、性能确认(IQ/OQ/PQ)的核心内容 ④ 需求追溯矩阵(RTM)的内容及目的 ⑤ 验证总结报告(VSR)的核心要素及批准流程 ⑥ 系统移交活动的主要内容 |
三、计算机化系统再验证及退役要点解析 | 1.计算机化系统的周期性回顾 2.计算机化系统再验证的必要性 3.计算机化系统退役要点解析 |
四、计算机化系统的数据可靠性考量解析 | 1.账户的权限管理控制要点解析 ① 账户分类管理的原则、访问权限控制措施与维护要求 ② 账户角色职责与权限分工、工作状态的确定 ③ 账户角色功能变更管理要求 ④ 权限管理常见问题解析 2.审计追踪(数据稽查)操作要点分析 ① 需要进行审计追踪的系统 ② 审计追踪的操作要点 ③ 老旧系统的审计追踪管理 ④ 审计追踪常见问题解析 |
四、计算机化系统的数据可靠性考量解析 | 3.系统安全性管理要求 4.数据采集与输入要点解析 5.电子表格和数据分析模板管理 6.计算机硬件现场检查迎审案例(模拟问答) |
五、数据可靠性法规和指南核心简介 | 1.数据可靠性基本概念 2.国内外法规与指南核心要求 3.典型迎审违规案例与监管趋势 |
六、电子数据和纸质数据可靠性管理原则 | 1.通用管理原则(ALCOA+) 2.纸质数据管理原则 3.电子数据管理原则 4.混合数据管理原则 5.常见问题案例分析 |
七、数据可靠性体系建立与维护 | 1.数据可靠性体系框架构建 2.数据可靠性关键要素实施 3.数据可靠性体系维护与改进 4.数据可靠性的第三方管理 5.常见问题案例分析 |
八、仪器设备系统、信息系统与AI系统的数据可靠性实操 | 1.仪器设备系统实操 2.信息系统实操 3.AI系统数据可靠性实操 4.常见问题案例分析与解决方案 |

会议费:2600元/人, 【含培训费、资料费、证书费、发票、茶歇】
加入企业会员免费参会

如果你是:
药品企业IT负责人及IT管理人员、质量负责人、生产负责人、质量部负责人、生产部负责人、QA经理/主管、QC经理/主管、设备经理/主管、验证经理/主管、生产经理/主管等。


报名联系人:吴坤 15510572152(同微)
点击课题进入课程详情 工信部人才交流中心颁证:《药品合规审计官》《药品验证工程师》《药品质量体系工程师》《药品数据管理工程师》《实验室管理工程师》《药品研发工程师》《EHS管理工程师》《设备管理工程师》高级、《CSV工程师》高级、《项目管理工程师》高级、《药物分析工程师》高级
【CCAA国家注册审核员】一个让您增加额外收入的证书,可兼职,工作地点时间自由
上海+直播:3月26-27日《基于最新法规要求的药品清洁验证、工艺验证及持续工艺确认要点及案例实操班》
北京+直播:3月31-4月1日《药品杂质研究策略要点开发应用解析及研发质量体系建立专题》
线上直播:3月31日《新版GMP无菌药品附录的要求变化与应对策略要点解析》
线上直播:4月15日《新法规下制药企业物料、仓储的合规提升关键点及验证案例解析》
苏州+直播:4月24-25日《药品企业审计关键模块要点解析与核心技能提升实战研修班》
线上直播:4月30日《中欧原料药和制剂注册及再注册全过程实操要点解析》
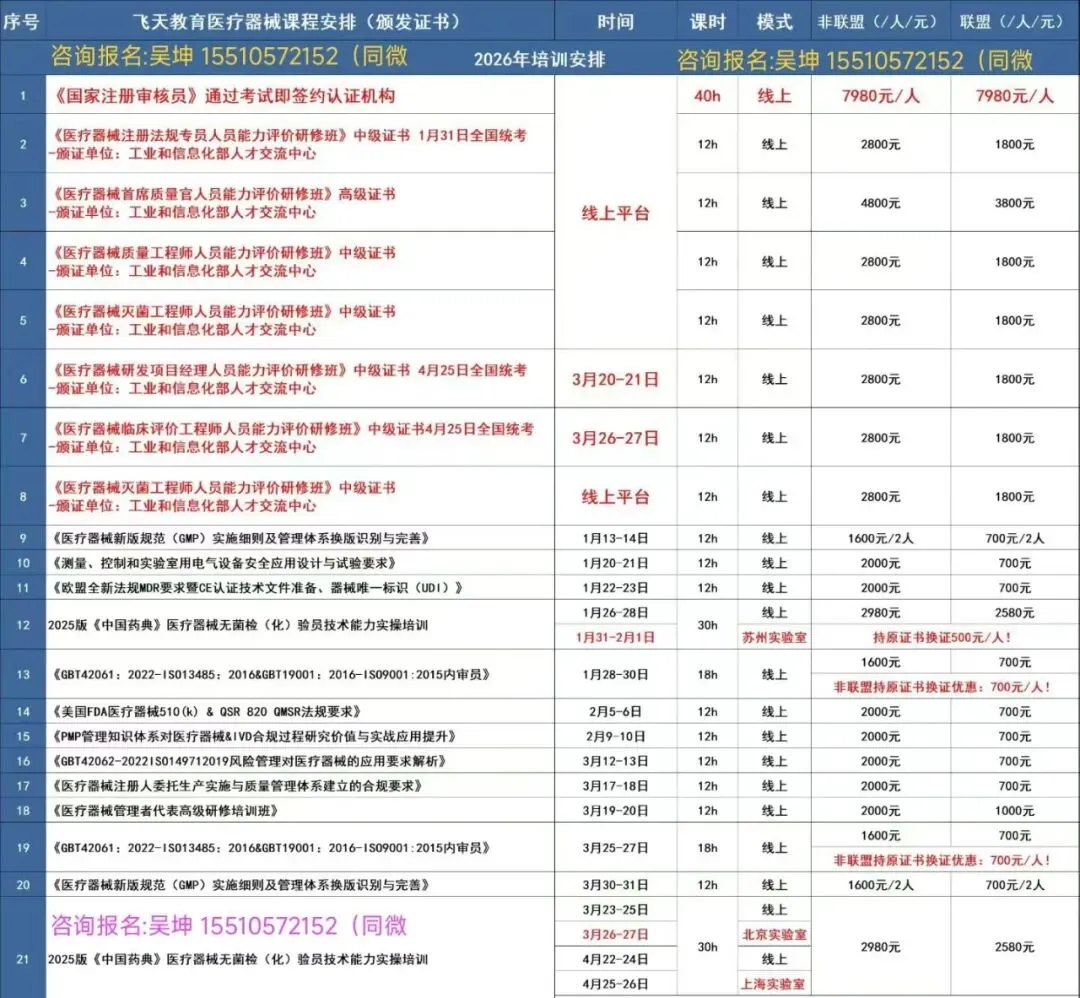
医疗器械项目-课程表 联系人吴坤 15510572152(同微) End
内训、咨询服务项目
认证咨询(FDA/WHO/中国GMP) 计算机化系统验证丨工艺核对咨询 模拟飞行检查丨顾问式咨询 模拟GMP认证检查丨数据可靠性审计 药品一致性评价丨GMP认证咨询 可根据企业需求