AI制药大突破:南京农业大学团队用BroadAMP-GPT造出“超级肽”,Gut Microbes研究或拯救千万生命
- 2026-04-10 04:49:54

在全球抗生素耐药危机日益严峻的背景下,ESKAPE病原体每年导致数百万人死亡。南京农业大学黄锦虎团队在《Gut Microbes》发表最新研究,推出AI驱动平台BroadAMP-GPT,通过Transformer模型生成并筛选广谱抗菌肽(AMPs)。该平台从10万条AI生成肽中筛选出110个候选肽,实验验证显示57%的肽对ESKAPE病原体具有强效活性。明星肽AMP_S13表现尤为突出:在极端pH、高温和蛋白酶环境下保持稳定,对多重耐药菌的MIC低至2-16μg/mL,且细胞毒性极低。动物实验中,AMP_S13使感染MRSA的蜡螟幼虫存活率提升至90%,并加速小鼠皮肤伤口愈合。这项研究为抗耐药菌治疗提供了可扩展的AI解决方案,有望扭转抗生素失效的困局。
沉默的杀手——ESKAPE病原体如何让抗生素走向末路?
当抗生素逐渐失效,我们仿佛回到了“前抗生素时代”。每年,ESKAPE病原体(如耐甲氧西林金黄色葡萄球菌MRSA、鲍曼不动杆菌)直接导致127万人死亡,并间接影响495万生命。世界卫生组织预警,到2050年,抗生素耐药每年将夺走1000万人的生命。这一切的根源,是细菌通过基因突变轻松绕过传统抗生素的靶点。然而,自然界中有一类“天然武器”——抗菌肽(AMPs),它们能通过物理破坏细菌膜结构,让耐药菌无路可逃。但传统AMP设计效率低下,数万种肽序列中可能仅有一两种有效。南京农业大学团队能否用AI打破这一僵局?让我们走进BroadAMP-GPT的诞生故事。
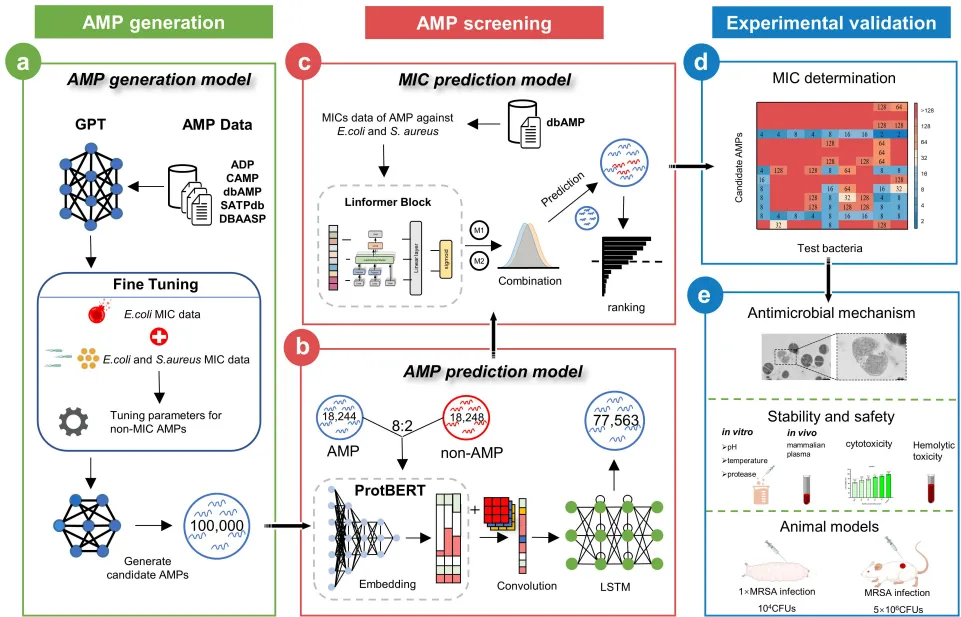
图1. BroadAMP-GPT整体框架。
AI如何像“写诗”一样创作抗菌肽?BroadAMP-GPT的底层逻辑
“如果让AI学习数万首古诗,它能写出李白级别的诗句吗?”南京农业大学团队用同样的思路训练了BroadAMP-GPT。研究团队从五大数据库(如dbAMP、APD)收集了2.6万条天然AMP序列作为“诗歌库”,先用GPT模型进行预训练,再针对大肠杆菌和金黄色葡萄球菌的MIC数据微调,使AI学会“押韵”——即生成兼具阳离子电荷和两亲性的肽结构。生成的10万条序列中,AI通过两级筛选锁定了110个候选肽:第一级用AMP预测模型(准确率超90%)剔除无效序列,第二级用Linformer模型预测MIC值,确保肽能同时对抗革兰氏阴性和阳性菌。令人惊叹的是,AI生成的肽不仅保留了天然AMP的膜靶向特性,还通过富集赖氨酸(Lys)和丙氨酸(Ala)增强了正电荷和疏水性,犹如给武器镀上“破甲涂层”。
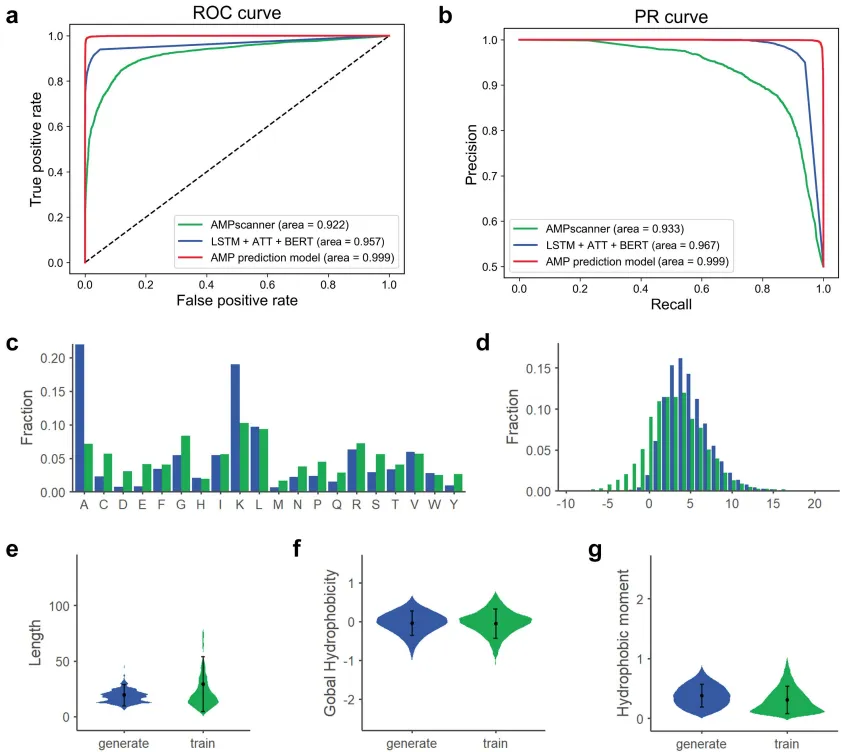
图2. 生成肽序列的AMP预测模型性能及理化特性。(a) 不同AMP预测模型的AUROC值。(b) 不同AMP预测模型的AUPRC值。(c-g) 生成序列与训练序列在氨基酸组成、电荷、长度、整体疏水性及疏水矩等属性上的分布情况。
双雄出世!AMP_S13为何成为“耐药菌克星”?
在14个合成候选肽中,AMP_S4和AMP_S13犹如一对“黑白双煞”。实验显示,两者对40株临床分离的MRSA和大肠杆菌均保持4-32μg/mL的低MIC值,且对ESKAPE家族(如鲍曼不动杆菌、铜绿假单胞菌)全覆盖。更关键的是,它们能在30分钟内杀灭99%的细菌,而传统抗生素需数小时。为何它们如此高效?秘密藏在分子动态模拟中:AMP_S13的C端甘氨酸残基能像“钥匙”一样插入细菌膜,破坏质子动力势能;电镜照片清晰显示,经AMP_S13处理的细菌膜出现巨大孔洞,内容物泄漏而亡。更令人振奋的是,连续28代亚抑菌浓度暴露下,细菌未产生耐药性,而环丙沙星仅9代即失效。
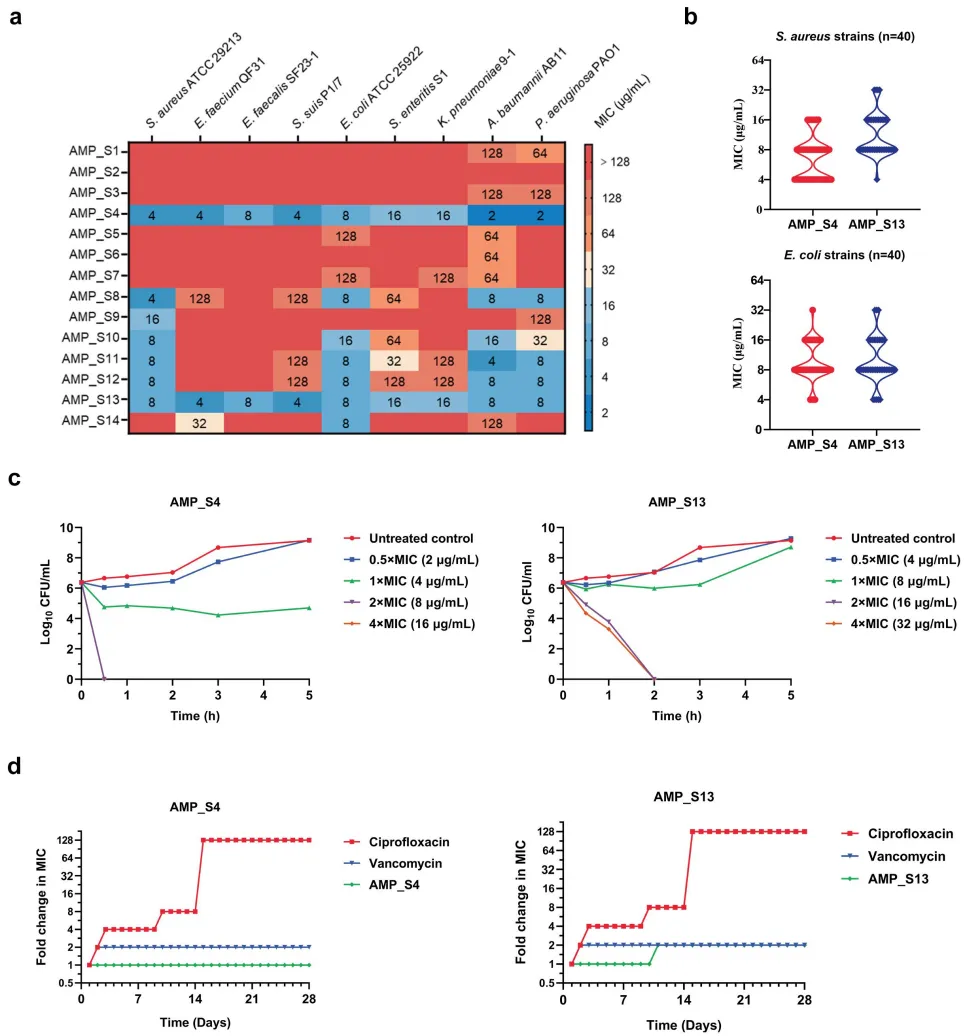
图3. 候选抗菌肽的抗菌活性与耐药性诱导实验。(a) AMP_S4与AMP_S13对不同菌种的抑菌浓度。(b) AMP_S4与AMP_S13对金黄色葡萄球菌(n=40)和大肠杆菌(n=40)的抑菌浓度。(c) AMP_S4与AMP_S13对金黄色葡萄球菌ATCC 29213的杀菌动力学曲线。(d) 在亚抑菌浓度(1/2x)的环丙沙星、万古霉素、AMP_S4及AMP_S13作用下,金黄色葡萄球菌ATCC 29213的耐药性诱导研究。
烈火验真金!AMP_S13的“极端环境生存记”
一款肽能否成为药物,关键看其稳定性。研究人员将AMP_S13置于pH=2的胃酸环境、100℃沸水、甚至蛋白酶包围的“修罗场”。结果惊人:它的活性仅下降2倍,而许多天然肽早已“尸骨无存”。在50%兔血浆中,AMP_S13仍能高效杀灭肺炎克雷伯菌等病原体,证明其能抵御体内酶解攻击。安全性方面,AMP_S13对人类细胞毒性极低(CC50超1000μg/mL),而溶血活性可忽略不计,选择性指数是AMP_S4的30倍。这种“智能靶向”特性,让AMP_S13有望避开传统抗菌肽的毒副作用陷阱。
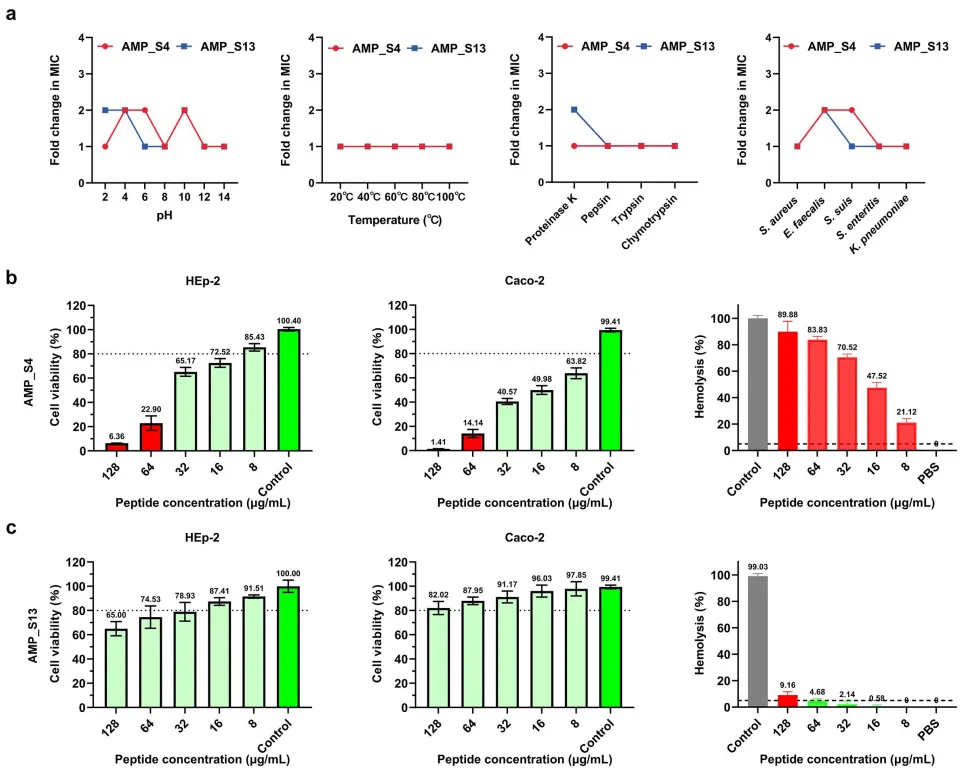
图4. AMP_S4与AMP_S13的稳定性与毒性分析。(a) pH值、温度、蛋白酶及血浆对AMP_S4与AMP_S13抗菌活性的影响分析。多肽在不同条件下孵育1小时后测定其最小抑菌浓度。AMP_S4(b)与AMP_S13(c)对HEp-2细胞、Caco-2细胞的细胞毒性及小鼠红细胞的溶血毒性。
动物体内“实战”!从蜡螟到小鼠,AMP_S13如何逆转生死?
研究团队用感染MRSA的蜡螟幼虫模拟败血症:未治疗组48小时内全部死亡,而AMP_S13治疗组(20mg/kg)存活率高达90%。在小鼠皮肤感染模型中,涂抹1% AMP_S13膏体的伤口第5天即出现上皮再生,11天后细菌载量下降1000倍,效果媲美明星药物莫匹罗星。组织切片显示,AMP_S13组毛囊和皮脂腺重建明显,而对照组仍是一片“焦土”。“这意味着它不仅能杀菌,还促进组织修复。”黄锦虎教授表示。这种双重优势源自AMP_S13的膜破坏机制——快速清创为愈合创造了环境。
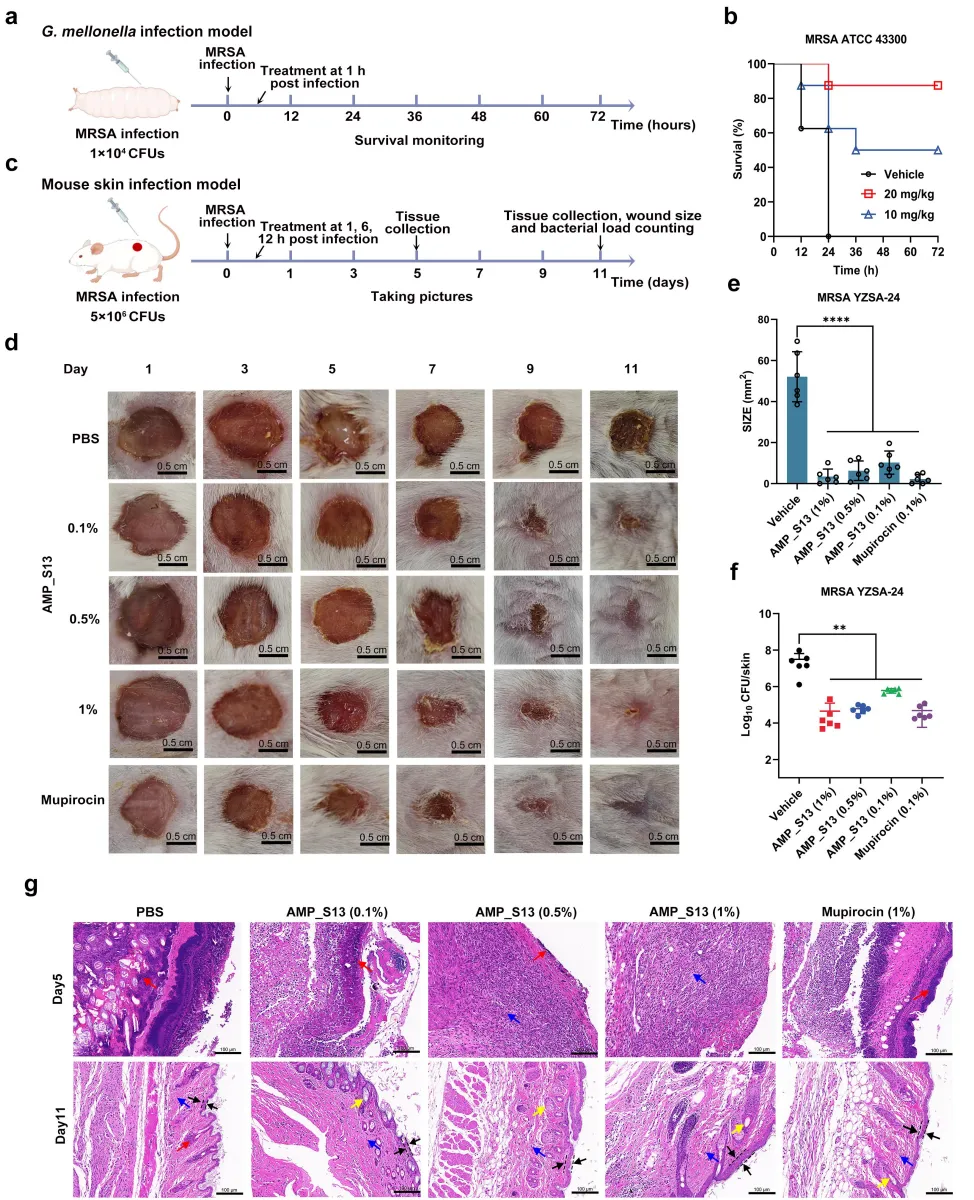
图5. AMP_S13在大蜡螟幼虫感染模型及皮肤伤口感染模型中的体内抗菌效果。(a)动物试验中采用的MRSA感染大蜡螟模型示意图。(b)研究中72小时内,经AMP处理的MRSA感染大蜡螟的存活率。(c)动物试验中采用的小鼠皮肤感染模型示意图。(d)不同处理后第1、3、5、7、9及11天皮肤伤口的典型照片。(e)11天后皮肤伤口的大小及(F)皮肤伤口的细菌载量。(g)不同处理组MRSA感染皮肤组织的苏木精-伊红(H&E)染色组织学分析。
AI设计抗菌肽的星辰大海
BroadAMP-GPT的价值远超本次研究。平台可适配新病原体数据,未来或用于设计抗病毒肽、抗癌肽。相比传统试错法,AI将发现周期从数年缩短至数周,且成本降低90%。尽管临床转化仍需优化递送系统,但这项研究无疑为后抗生素时代点燃了曙光。
重要参考文献
Murray CJL et al. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis. Lancet. 2022.
核心内容:量化了2019年全球抗生素耐药导致127万直接死亡,强调ESKAPE病原体的主导作用。
Fjell CD et al. Designing antimicrobial peptides: form follows function. Nat Rev Drug Discov. 2011.
核心内容:提出AMP设计应遵循“形式追随功能”原则,强调两亲性和电荷分布的关键性。
Jumper J et al. Highly accurate protein structure prediction with AlphaFold. Nature. 2021.
核心内容:AlphaFold2的蛋白质结构预测技术为AMP机制模拟提供基础。
Mookherjee N et al. Antimicrobial host defence peptides: functions and clinical potential. Nat Rev Drug Discov. 2020.
核心内容:综述宿主防御肽的双重功能(抗菌与免疫调节),指出其临床转化挑战。
Wong F et al. Discovery of a structural class of antibiotics with explainable deep learning. Nature. 2024.
核心内容:深度学习驱动的新型抗生素发现案例,验证AI在抗菌药物开发中的潜力。
历史文章
6 大设计策略 + 3 重王牌应用!川大团队解锁超分子肽抗菌材料新未来
抗生素危机迎转机:山东大学团队用PeptiD-Agent框架发现广谱抗菌肽DA2,动物实验100%存活
AI驱动抗菌策略前沿 | 生成式人工智能在抗菌肽发现与优化中的革命性突破
从42.5%到80%:山东大学《Advanced Science》突破性研究 | AI如何将抗菌肽优化效率翻倍?背后暗藏D-氨基酸取代密码
《Nature Commun》最新报道:香港中文大学科学家AI挖出祖传秘方,2500前粪便中抗菌肽完爆青霉素
“当微生物用百万年筑起耐药高墙,人类用AI铸就破壁之矛——生命的韧性,终将照亮黑暗中的进化博弈。”
