中国药科大学/南京大学合作,最新Nature Chemistry!
- 2026-04-10 03:57:12
中国科学家发现细菌P450酶:解锁五环三萜类化合物“隐秘”位点,开辟药物研发新路径
在药物研发的版图中,天然产物及其衍生物一直扮演着关键角色,尤其是结构复杂的五环三萜类化合物,因其多样的生物活性而备受瞩目。然而,这类分子富含大量化学性质相似的惰性脂肪族碳-氢键,且拥有多个手性中心和前手性中心,使得对其特定位置进行精准修饰,特别是那些缺乏导向基团且反应活性低的位点,成为有机合成领域一项极具挑战性的任务。传统的合成策略通常依赖于分子自身的电子或位阻特性,或使用导向基团进行官能团化,但这些方法在面对五环三萜日益增长的分子复杂度时,往往效率低下,且难以触及C7、C15等“隐秘”位点,严重限制了其化学空间的拓展和药物潜力的发掘。
针对这一难题,中国药科大学董廖斌教授、南京大学梁勇教授合作,开发了一种生物信息学驱动的“萜烯-P450”发现策略,成功从细菌中挖掘出一种名为ApPT的细胞色素P450酶。该酶能够高区域选择性和非对映选择性地激活五环三萜中惰性的脂肪族碳-氢键,并展现出卓越的底物普适性,为这些复杂分子的后期多样化修饰提供了一种强大的化学生物学平台,开辟了此前难以触及的化学空间。相关论文以“Exploring bacterial cytochrome P450s for selective activation of aliphatic C–H bonds in pentacyclic triterpenoids”为题,发表在Nature Chemistry上。

为了寻找能够处理五环三萜这类庞大且疏水分子的生物催化剂,研究团队首先对已知的12种细菌P450酶进行了筛选。然而,测试结果显示,这些酶大多活性低下或底物谱过窄,例如仅有来自枯草芽孢杆菌的CYP109B1能对白桦脂酸产生痕量氧化产物(图2d)。这表明,传统的基于底物类似物的策略难以找到理想的催化剂。因此,研究人员将目光转向了细菌基因组。基于萜类合酶与修饰性P450在生物合成基因簇中通常紧密相邻的自然规律,他们对20株细菌的基因组进行了深度挖掘,锁定了46个萜类合酶,并利用EFI-GNT工具分析了其周围10个基因范围内的序列,最终从11株细菌的29个萜类生物合成基因簇中鉴定出41个候选P450酶。通过构建高效的体外筛选平台(包含P450-RhFRed融合蛋白和用于辅酶再生的opt13),他们惊喜地发现,来自Pretoria放线菌的ApPT(CYP161H12)对三种代表性五环三萜——甘草次酸、熊果酸和白桦脂酸均表现出显著的羟基化活性(图2c, d)。其中,催化甘草次酸时,ApPT能以超过99%的收率生成C7位单羟基化和C7、C15位双羟基化产物,且非对映选择性高达99%,尤为引人注目的是,在整个反应过程中未检测到单独的C15位羟基化产物,暗示其经历了独特的C7-to-C15接力氧化过程。单晶X-射线衍射分析最终确认了双羟基产物和白桦脂酸C2位羟基化产物的绝对构型(图2e)。
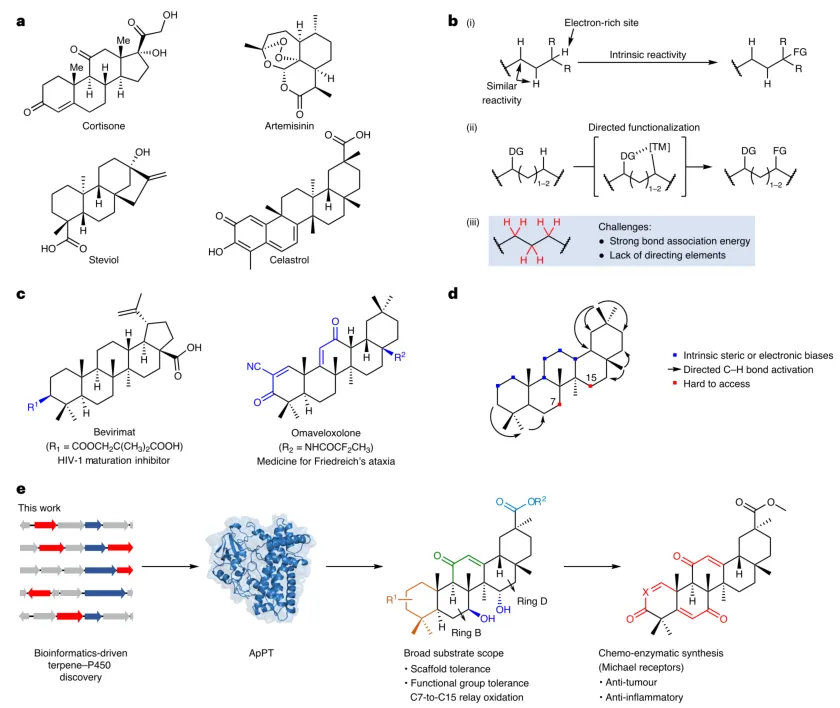
图1 | 选择性脂肪族C-H键活化的策略。 a, 包含多个脂肪族C-H键的多环萜类化合物示例。 b, 已报道的脂肪族C-H键活化有机合成策略:(i) 内在反应性介导的选择性C-H键官能团化;(ii) 利用导向基团的配位导向官能团化;难以触及的位点。 c, 已上市药物或临床候选药物中的五环三萜骨架。 d, 五环三萜中传统有机合成方法难以修饰的C7和C15位点。 e, 本工作中用于选择性活化五环三萜脂肪族C-H键的萜烯-P450发现策略与生物催化剂。
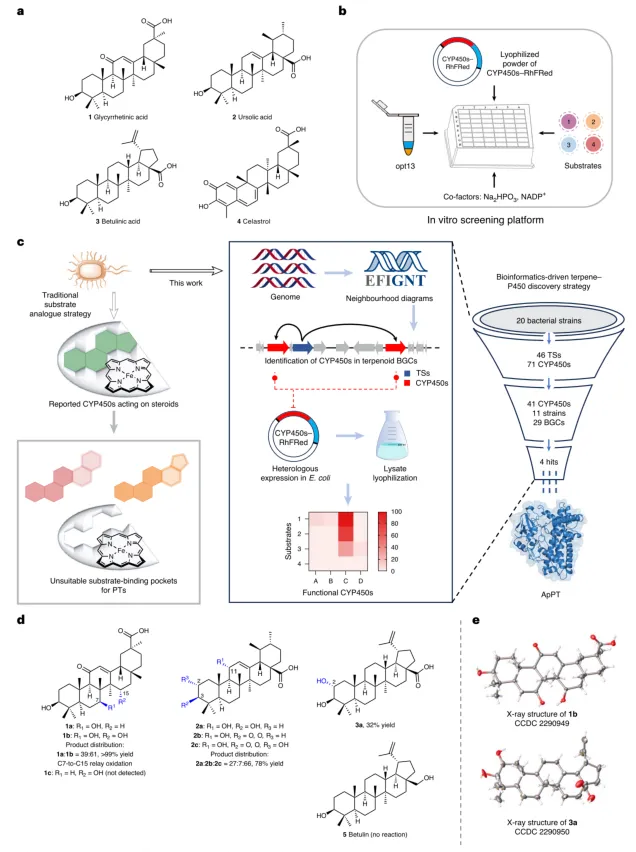
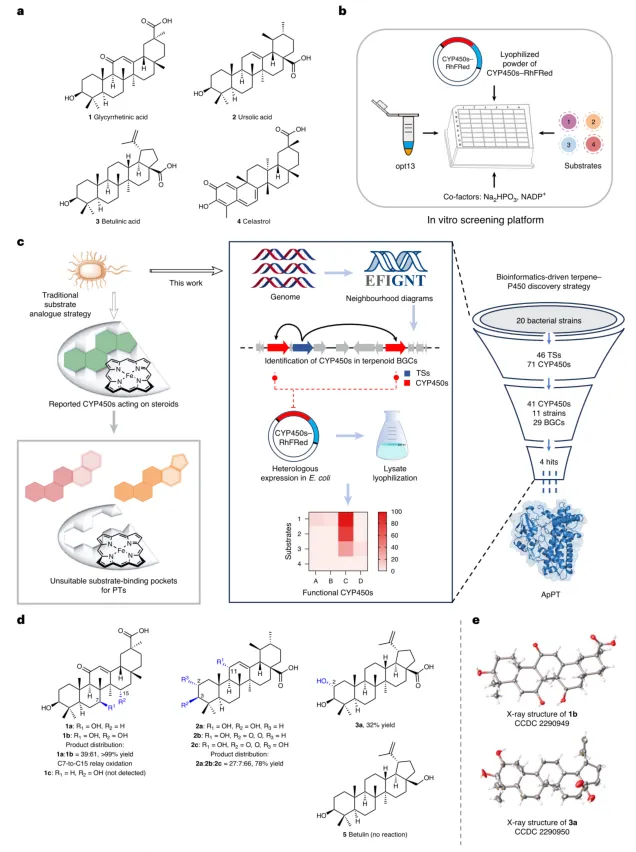
图2 | 探索用于五环三萜C-H键活化的细菌P450的工作流程概述。 a, 用于筛选的四种代表性且可商业获得的五环三萜。 b, 使用每种P450的裂解物冻干粉的体外筛选平台。 c, 探索用于五环三萜C-H键活化的细菌P450的策略:传统底物类似物策略与本工作中生物信息学驱动的萜烯-P450发现策略对比。热图展示了四种功能型P450对模型底物1-4的产率(%)。A, A0A291SNNS; B, 10VSF6; C, ApPT; D, Q821.47。 d, ApPT催化的对不同五环三萜的选择性C-H键活化。 e, 化合物1b和3a的X射线单晶结构。
ApPT酶最令人兴奋的特性之一是其独特的催化机制和广泛的底物兼容性。为深入探究其催化的C7-to-C15接力氧化过程,研究团队首先优化了反应条件,并在最优条件下对多种甘草次酸衍生物进行了底物谱考察。结果表明,无论是A环带有酮基、烯酮、内酯或异恶唑等取代基的衍生物,还是C环为共轭二烯或氧代烯烃的底物,ApPT均能高效催化,并普遍获得高收率的C7位羟基化产物(图3a)。例如,C3位为酮基的底物6,其双羟基化产物的收率高达89%。然而,当C3位羟基被酰化后,反应更倾向于停留在单羟基化阶段。单晶X-射线衍射分析明确了其中一种C7位羟基化产物的结构(图3b)。重要的是,这些C环被修饰的底物会干扰C7-to-C15的接力氧化过程,表明该过程对底物特定的构象有要求。基于此,团队进一步设计了一条化学-酶促合成路线,利用ApPT高效催化获得C7位单羟基化及C7、C15位双羟基化中间体,并以此为原料,通过一系列简洁的化学转化,快速构建了一系列结构新颖、在B环和D环引入α,β-不饱和酮和氰基等药效团的甘草次酸衍生物(图4a)。体外生物活性测试显示,这些通过化学-酶促策略获得的新化合物展现出优异的抗炎和抗肿瘤活性。其中,化合物21的抗炎活性(IC50=9.5 μM)优于阳性对照,而化合物23和25对HeLa细胞表现出极强的抑制活性(IC50值分别为0.7 μM和5.2 μM),且对肿瘤细胞的选择性显著优于未修饰B/D环的类似物(图4b),充分彰显了该策略在挖掘新型先导化合物方面的巨大潜力。
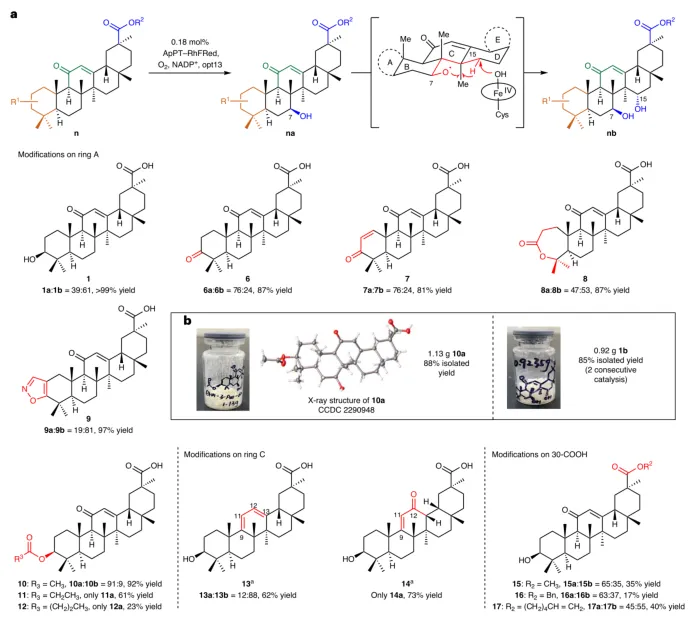
图3 | ApPT对甘草次酸衍生物的底物谱研究。 a, ApPT催化的甘草次酸及其衍生物的C7到C15接力氧化过程。对A环(青色)、C环(蓝色)和E环(绿色)进行的修饰被探究。 b, 化合物10a的X射线单晶结构。
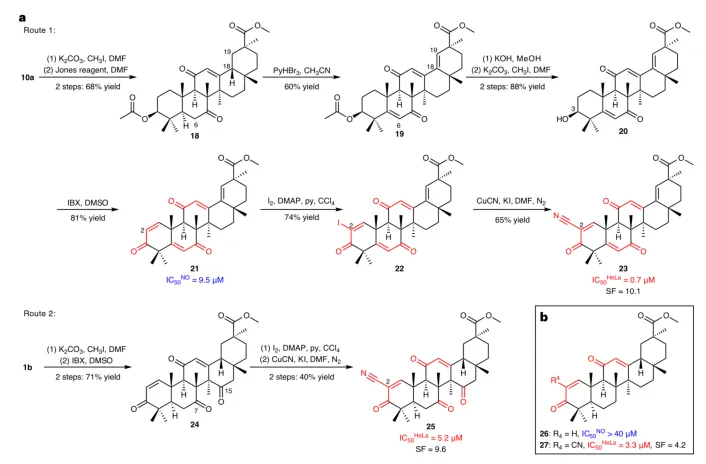
图4 | 甘草次酸衍生物的化学-酶法合成。 a, 甘草次酸衍生物作为迈克尔受体的化学-酶法合成及其生物活性。 b, 未在B环和D环修饰的甘草次酸衍生物及其生物活性。
为了揭示ApPT酶实现卓越选择性的分子机制,研究团队解析了其分辨率为1.80 Å的晶体结构(PDB:8W7G)。结构显示,ApPT呈现典型的P450酶折叠方式,其底物通道入口处由于B-C环和F-G环区域的特殊构象而显著扩大,形成一个宽阔的“开口”(图5a),这可能是其能够容纳体积庞大的五环三萜底物的关键。进一步,通过密度泛函理论计算、分子对接和长达700纳秒的分子动力学模拟,研究人员阐明了其催化甘草次酸时优先氧化C7位而非C15位的机理。计算表明,C7位氢原子的提取能垒更低,且关键残基I80、Q81、G292和L293通过氢键网络与底物的羧基牢固结合,将C7位精准地定位在血红素活性中心附近,从而确保了C7位羟基化的高选择性(图5b, c)。
对于C7-to-C15的接力氧化过程,研究团队提出了两种可能途径:直接C15位氢原子攫取,或先由C7位羟基形成烷氧自由基,进而引发1,5-氢原子转移。为验证这一假设,他们合成了C7位为羰基或甲氧基的底物类似物(1e, 1f)。反应结果显示,这些底物几乎无法有效转化为C15位羟基化产物,表明C7位羟基上的氢原子对后续反应至关重要(图5e, f)。结合DFT计算和分子动力学模拟,他们发现,虽然直接C15位氢攫取途径的固有能垒较低,但酶环境使其过渡态能量显著升高;相反,1,5-氢原子转移途径在酶催化下,其活化自由能垒仅为12.6 kcal/mol,远低于直接途径,因而是反应的主导路径(图5g, h)。这是首次在天然P450酶中发现并证实由烷氧自由基介导的1,5-氢原子转移机制,极大地拓展了人们对P450酶催化多样性的认知。
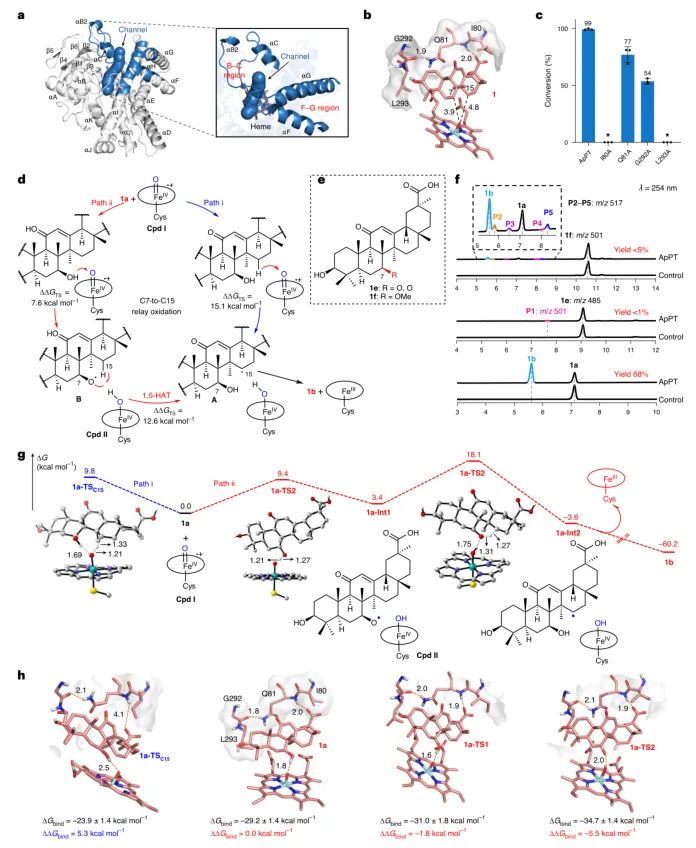
图5 | 机理研究。 a, ApPT的晶体结构(PDB: 8W7G, 1.80 Å)。通道以蓝色显示。 b, 在t = 700 ns时,底物1和化合物I(Cpd I)以及关键残基的分子动力学模拟快照。 c, ApPT及其突变体对底物1的催化效率(n = 3个生物学重复实验;平均值 ± s.d.)。星号表示未检测到产物形成。 d, 形成1b的两条可能路径。 e, 化合物1e和1f的化学结构。 f, ApPT与底物1a、1e和1f反应的高效液相色谱图谱。 g, 化合物1a生成1b的吉布斯自由能图谱及DFT优化的过渡态结构。 h, ApPT与1a-TS1、1a、1a-TS1和1a-TS2之间的结合自由能(ΔGbind)。以底物1a为参照,校正后的过渡态相对自由能(ΔGTS)由DFT优化的过渡态能量与使用MM/GBSA方法计算的ΔGbind之和得到。距离单位为Å。
这项研究不仅成功开发了一种能够高效、高选择性地激活五环三萜类化合物中“隐秘”位点的细菌P450酶ApPT,更重要的是,它展示了一种将基因组挖掘与高通量筛选相结合的通用性生物催化剂发现策略,为其他复杂天然产物的后期修饰提供了全新的范式。ApPT所催化的独特C7-to-C15接力氧化机制,不仅为合成化学家提供了一种强大的工具,能够快速构建传统方法难以获得的复杂分子,更开启了五环三萜类化合物B环和D环这一“未被开垦”的化学空间,为发现具有新颖骨架和更高生物活性的药物先导化合物铺平了道路。这项研究充分体现了生物催化在突破有机合成瓶颈、推动新药发现中的巨大潜力,标志着化学生物学领域的一项重大进展。
转自:高分子科学前沿
4、完整、高清版:麻省理工MIT化学院实验室手册(中文版PDF/76页)
16、常用有机溶剂分类、干燥、性质及管理(实验室必备知识)||实用资料
30、分析化学电子教案(第五版、武汉大学教材)(PPT/565页)
39、19页!史上最全、最详细的NMR核磁杂质峰、溶剂峰对照表
44、ChemDraw学习干货合集,85份干货资料+35个教程视频
45、实验室安全手册(Lab Safety Manual,University of Texas at Austin)(PDF/80)
46、ChemDraw学习干货合集,85份干货资料+35个教程视频
47、经典的有机化学反应后处理(PPT/25页),来自药明康德
59、MestReNova谱图处理简明教程(PPT/29页)
68、化学类必备工具书!实验室化学品纯化手册(原著第五版)-中文版
123、大学化学基础化学实验详解-有机化学实验(PPT/179页)
125、265条全合成路线汇总
132、实验室玻璃仪器手册
135、化学化工物性数据手册(有机篇/PDF1116页)
--------END-------
