南京中医药大学丨延胡索乙素通过TRPV1‑SP‑巨噬细胞轴缓解癌性骨痛:全新镇痛机制揭秘
- 2026-04-16 03:12:20
本研究以癌性骨痛(CIBP)临床治疗困境与延胡索乙素(THP)镇痛机制不清为切入点,构建小鼠 CIBP 模型及 TRPV1 敲除模型,采用行为学、免疫荧光、qPCR、ELISA、钙成像、细胞迁移与流式细胞学等方法,先明确 THP 对 CIBP 小鼠痛觉过敏与自发痛的改善作用,再探究其对 DRG 及坐骨神经巨噬细胞浸润、P 物质(SP)释放的影响,进而验证 TRPV1 在 THP 调控 SP 释放与巨噬细胞趋化中的核心作用,最后明确 THP 对巨噬细胞 M2 极化的直接促进效应;结果显示 THP 不影响肿瘤与骨密度,早期通过抑制 TRPV1 减少 SP 释放以阻断巨噬细胞募集,全程直接促进巨噬细胞向抗炎 M2 表型极化,双通路协同缓解 CIBP,为 THP 用于癌性骨痛治疗提供机制依据。


研究设计

建立 CIBP 小鼠模型与 TRPV1 敲除 CIBP 模型,经灌胃给予 THP 后通过行为学评估机械、冷热痛觉过敏及自发痛,借助免疫荧光、qPCR、ELISA 检测 DRG 与坐骨神经巨噬细胞浸润、SP 释放、炎症因子及极化标志物水平,利用钙成像、分子对接验证 THP 对 TRPV1 功能的直接抑制作用,通过细胞迁移、流式细胞学明确 THP 对巨噬细胞迁移与 M2 极化的调控,最终解析 THP 缓解 CIBP 的双阶段分子机制。

研究结果

THP(80 mg/kg)可显著改善 CIBP 小鼠机械、冷热痛觉过敏与自发痛,且不影响肿瘤生长与骨密度;THP 能减少 DRG 及坐骨神经巨噬细胞浸润,降低 M1 型标志物 iNOS、促炎因子 TNF‑α、IL‑1β,升高 M2 型标志物 CD206、抗炎因子 IL‑4、IL‑10;THP 可抑制 DRG 神经元 SP 释放及 Tac1 表达,阻断 SP 介导的巨噬细胞迁移;TRPV1 敲除会消除 THP 对巨噬细胞募集、SP 释放的抑制作用,钙成像证实 THP 直接抑制 TRPV1 功能(IC50=77.9 μM);THP 在 CIBP 进展期可直接促进巨噬细胞向 M2 极化,维持镇痛效果。
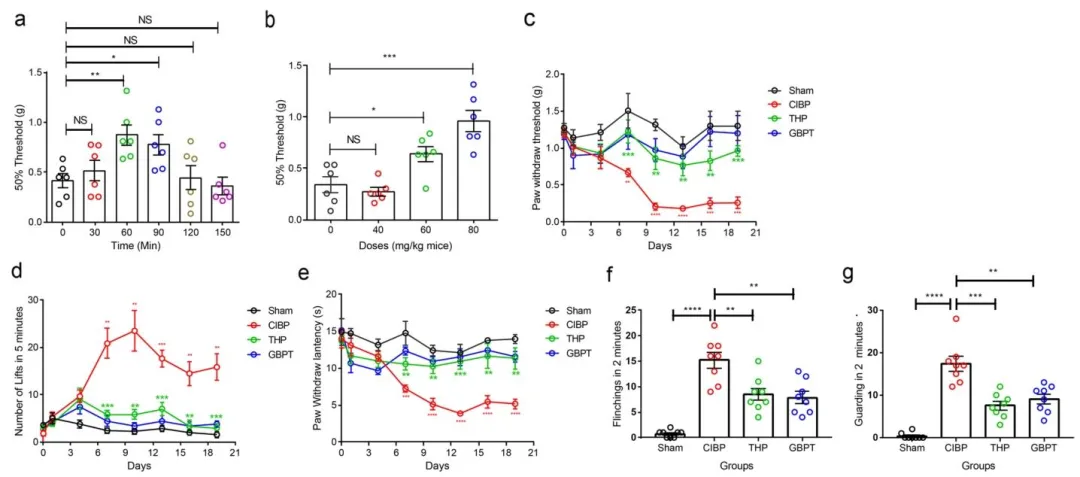
Fig.1:证实 THP 可剂量依赖性、时间依赖性缓解 CIBP 小鼠机械、冷热痛觉过敏及自发痛,确定 80 mg/kg 为有效剂量。
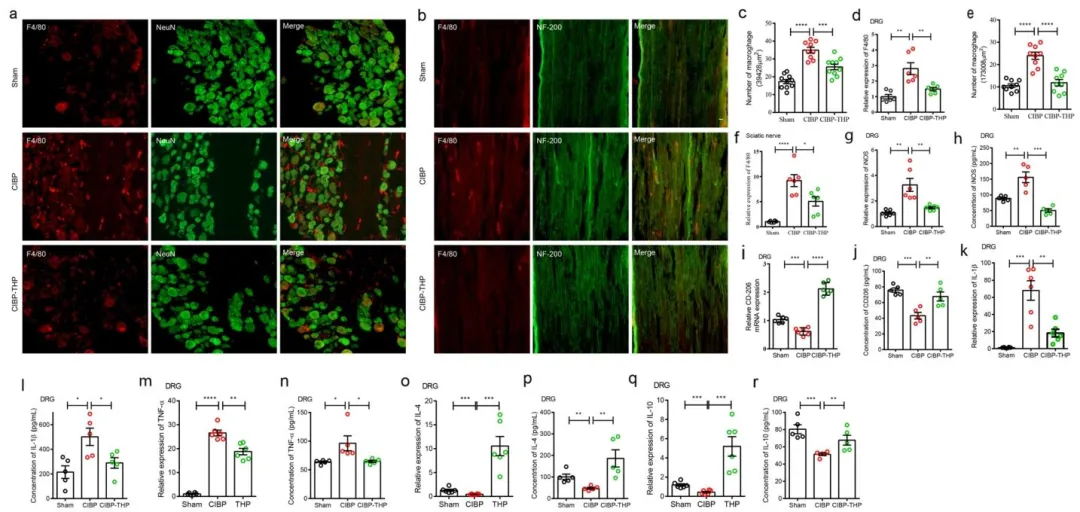
Fig.2:证明 THP 能减少 CIBP 小鼠 DRG 与坐骨神经巨噬细胞浸润,抑制 M1 型极化、促进 M2 型极化并调控炎症因子表达。
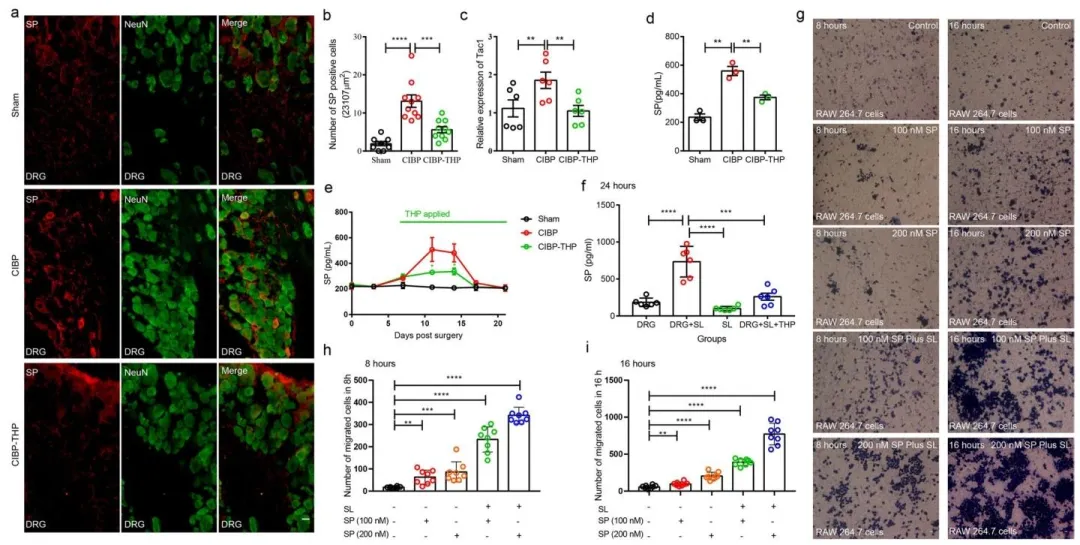
Fig.3:明确 THP 可抑制 DRG 神经元 SP 释放,阻断 SP 介导的巨噬细胞迁移,验证 SP 是 THP 调控巨噬细胞趋化的关键介质。
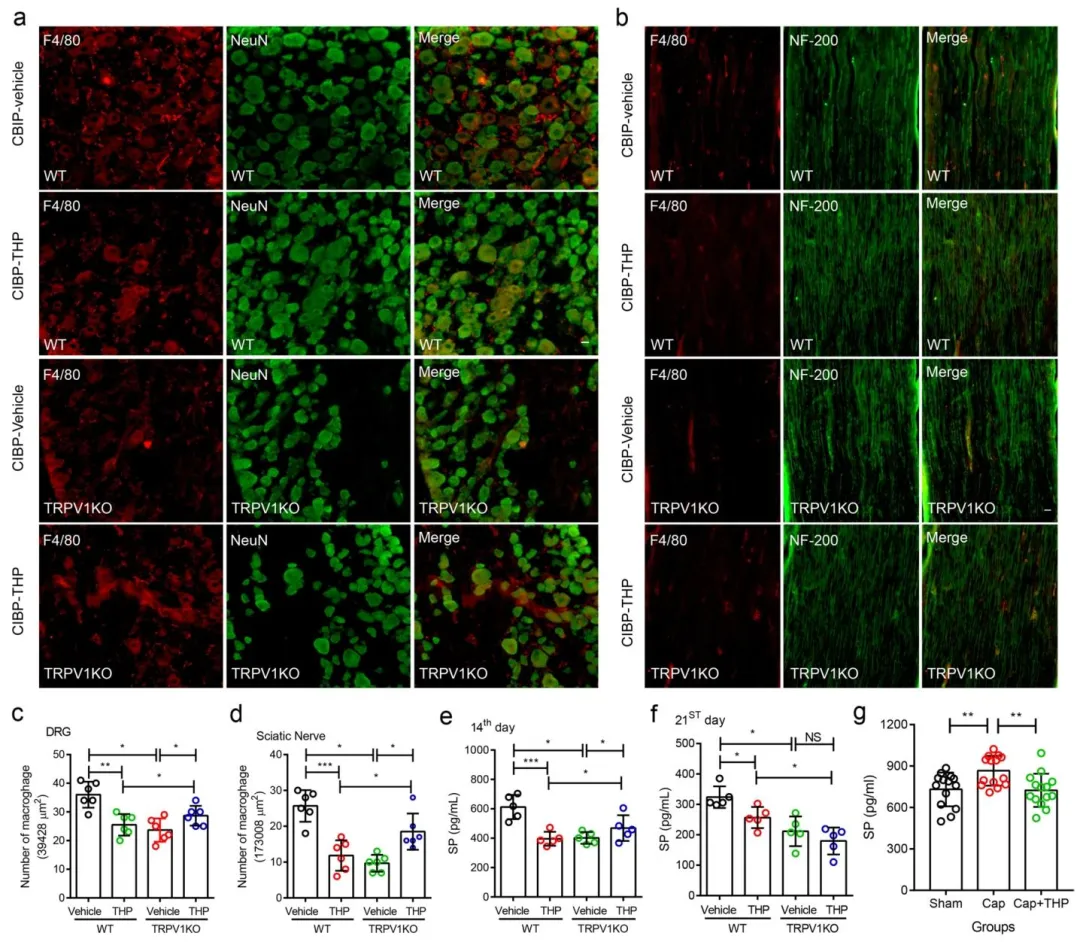
Fig.4:证实 TRPV1 是 THP 抑制巨噬细胞募集、减少 SP 释放的必需靶点,敲除后 THP 上述作用消失。
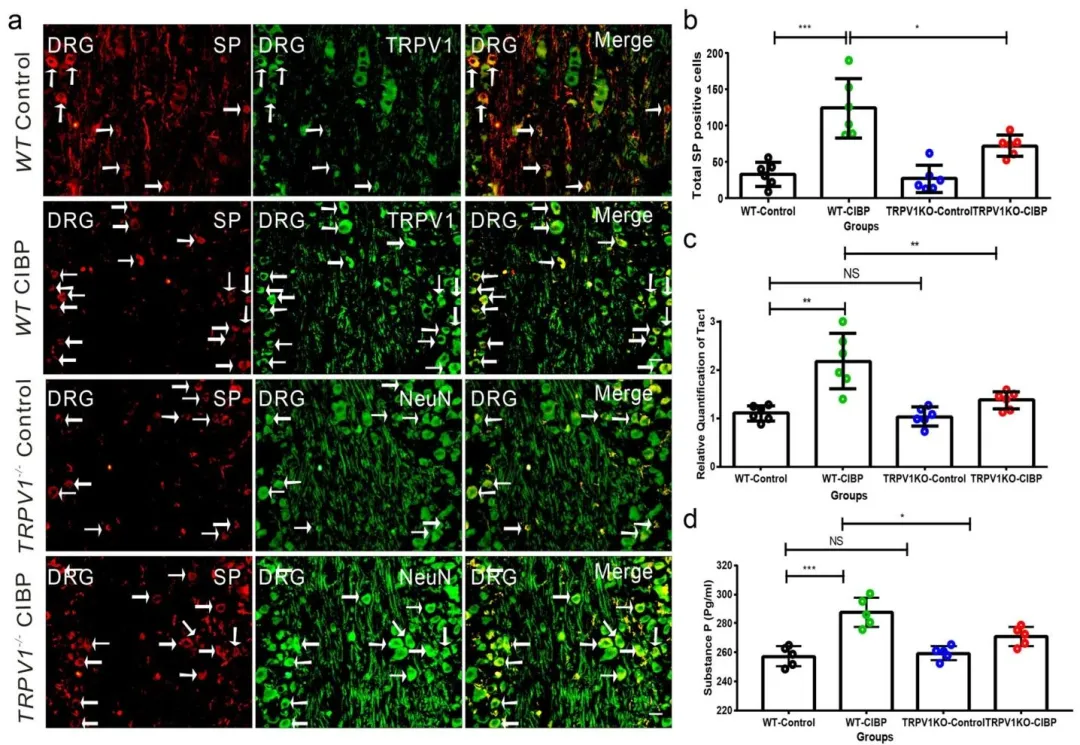
Fig.5:验证 TRPV1 在 CIBP 中可促进 DRG 神经元 SP 释放,是 SP 释放的上游关键调控分子。
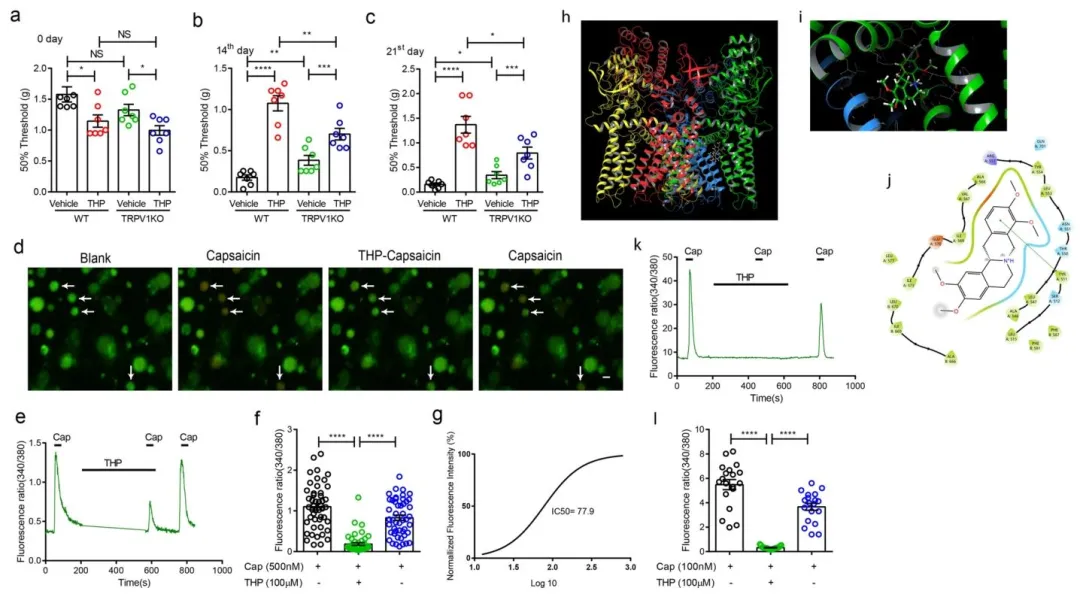
Fig.6:从钙成像、分子对接等角度证明 THP 直接抑制 TRPV1 通道功能,是其镇痛的关键分子作用。
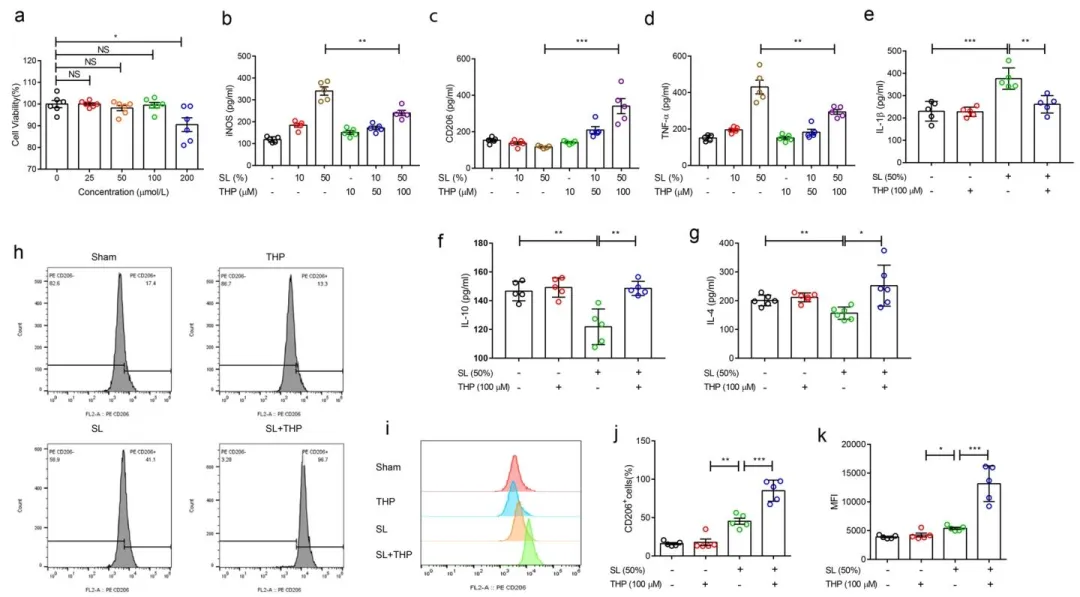
Fig.7:证实 THP 在 CIBP 进展期可直接促进巨噬细胞向 M2 型极化,独立发挥抗炎镇痛作用。
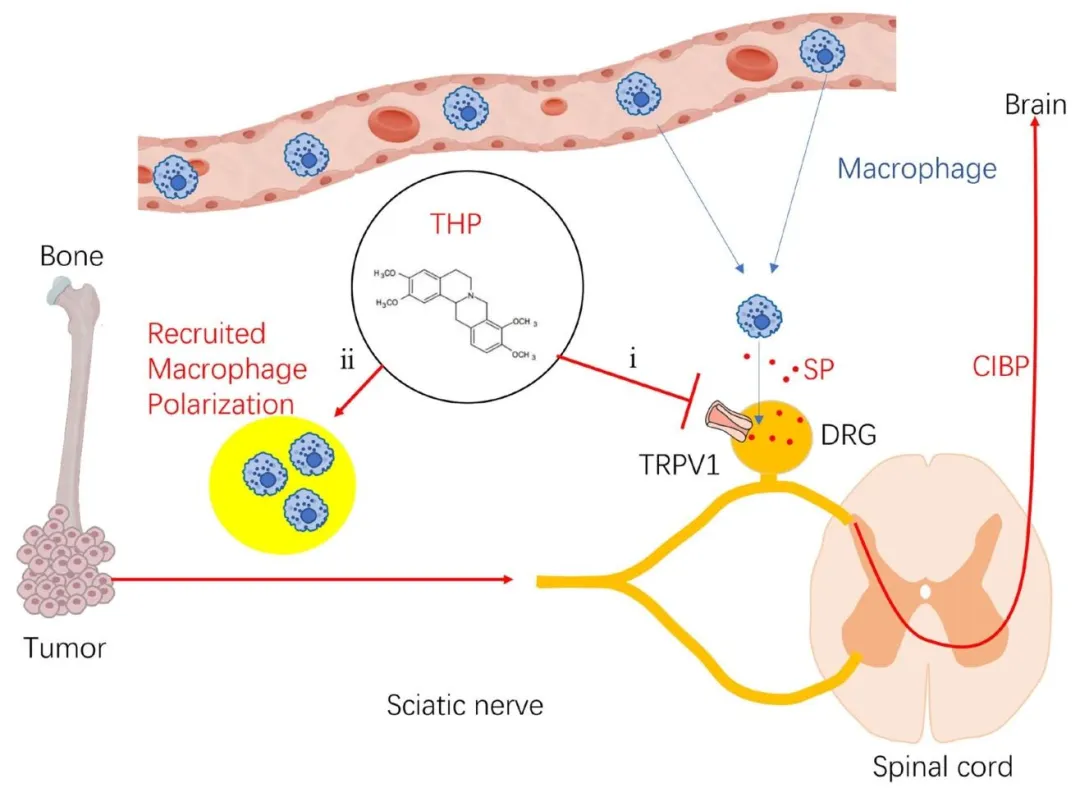
Fig.8:总结 THP 缓解 CIBP 的双阶段机制,早期 TRPV1‑SP 通路抑制巨噬细胞募集,全程促进 M2 极化。

研究结论

本研究首次揭示 THP 通过早期抑制 TRPV1‑SP 轴阻断巨噬细胞募集、全程直接促进巨噬细胞 M2 极化的双机制缓解 CIBP,且镇痛作用不依赖抗肿瘤效应,结合其临床安全、无成瘾性优势,为 CIBP 治疗提供新候选药物与靶点;机制上明确 TRPV1 是 THP 发挥早期镇痛的核心靶点,完善了 CIBP 神经‑免疫交互调控理论,同时补充了中药单体调控巨噬细胞极化的镇痛新机制;但研究存在局限性,仅使用雄性小鼠、单一肺癌细胞系,未建立完整量效关系,体外浓度与体内血浆浓度存在差异,采用巨噬细胞系而非原代细胞,且仅用经典标志物表征极化未做功能验证,未来需开展性别差异、多肿瘤模型、药代动力学及原代细胞功能验证等研究以支撑临床转化。
本文中使用的图片来源于Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
科研信息合集
国自然中标信息
国自然思路分享
骨科领域研究分享
医学课题申报通知
心血管领域科研分享
高分文献解析
神经领域科研分享
麻醉领域科研分享
肾脏领域科研分享