氘代标记化合物在药物发现和吸收、分布、代谢及排泄(ADME)研究中具有广泛应用,但精确控制氘原子引入的位置和程度仍是有机合成中的重大挑战。
传统的氢同位素交换(HIE)方法虽然能够实现芳烃的氘代,但其内在的可逆性常常影响位置控制和同位素精度,难以适用于部分氘代分子的定点构建。
相比之下,基于芳基卤化物脱卤氘化的策略可通过碳−卤键预先确定同位素引入位点,但针对最强化学键之一的C−F键进行精确脱氟氘化,特别是多氟芳烃的选择性部分氘化,仍是该领域的难点。
多氟芳烃在医药和材料科学中广泛存在,开发其选择性脱氟氘化方法不仅能为药物发现提供新策略,还能利用商业易得的多氟芳烃作为原料,实现氘代氟芳烃的精准合成。
近日,南京大学谢劲、朱成建、Weipeng Li在Journal of the American Chemical Society发表了题为"Nickel-Catalyzed Selective Defluorinative Deuteration of Polyfluoroarenes"的研究论文,Zhi Liu为论文第一作者,谢劲、朱成建、Weipeng Li为论文通讯作者。
1. 开发了镍催化的多氟芳烃选择性脱氟氘化新策略,实现了对C−F键的高区域选择性活化。 2. 利用廉价易得的氘代甲醇作为氘源,克服了传统氢同位素交换方法位置控制不足的局限。 3. 建立了模块化四步序列反应,可程序化地在芳香环上引入一至四个氘原子,精确控制氘代程度。 4. 揭示了锂盐在促进选择性C−F键活化中的协同效应,以及锌盐在转金属化和抑制过度还原中的关键作用。 5. 方法适用于复杂药物分子(如达拉非尼、左氧氟沙星中间体)的后期修饰,并可规模化制备氘代药物。
📄 全文速览
氘代标记化合物广泛应用于药物发现和ADME研究,但在有机合成中精确控制氘原子引入的位点和程度仍具挑战性。该研究报告了一种镍催化的多氟芳烃脱氟氘化方法,使用氘代甲醇(MeOD)作为易得的氘源。
该方法能够实现C−F位点的高选择性氘化,并可程序化地引入一至四个氘原子。机理研究揭示了镍催化C−F键活化中有趣的协同效应:锂盐可提高C−F键活化的反应活性和选择性,而锌盐则能促进转金属化并抑制过度还原。
该方法建立了多氟芳烃作为精准氘代标记和氘富集氟芳烃合成的通用平台,用于药物开发和代谢研究,代表了从商业可得原料选择性合成多氘代化合物的新合成平台。
📊 图文解读
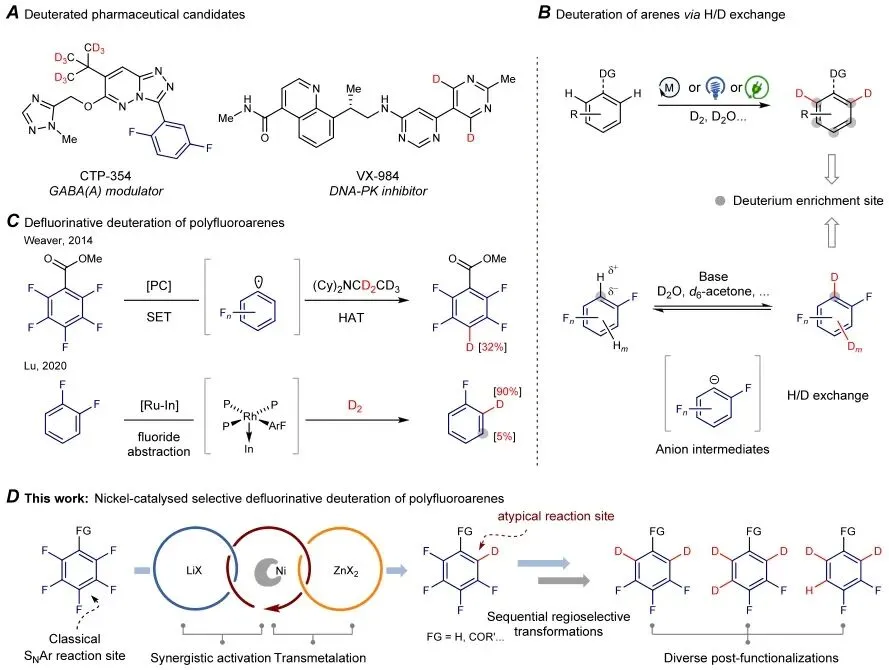
图1 | 多氟芳烃选择性氘化策略示意图,包括代表性氘代药物候选物、传统H/D交换方法、脱氟氘化策略及镍催化锂盐协同效应机制。
该图展示了多氟芳烃选择性氘化的不同策略。图A列举了代表性氘代药物候选物;图B说明了通过氢−氘交换实现芳烃氘化的一般方法;图C展示了利用易得的多氟芳烃进行脱氟氘化的策略;
图D阐述了镍催化选择性脱氟氘化反应,强调锂盐的协同效应和锌盐的转金属化作用,该策略使用Ni(cod)₂作为催化剂,dtbbpy作为配体,LiI作为添加剂,Zn作为还原剂,MeOD作为氘源。
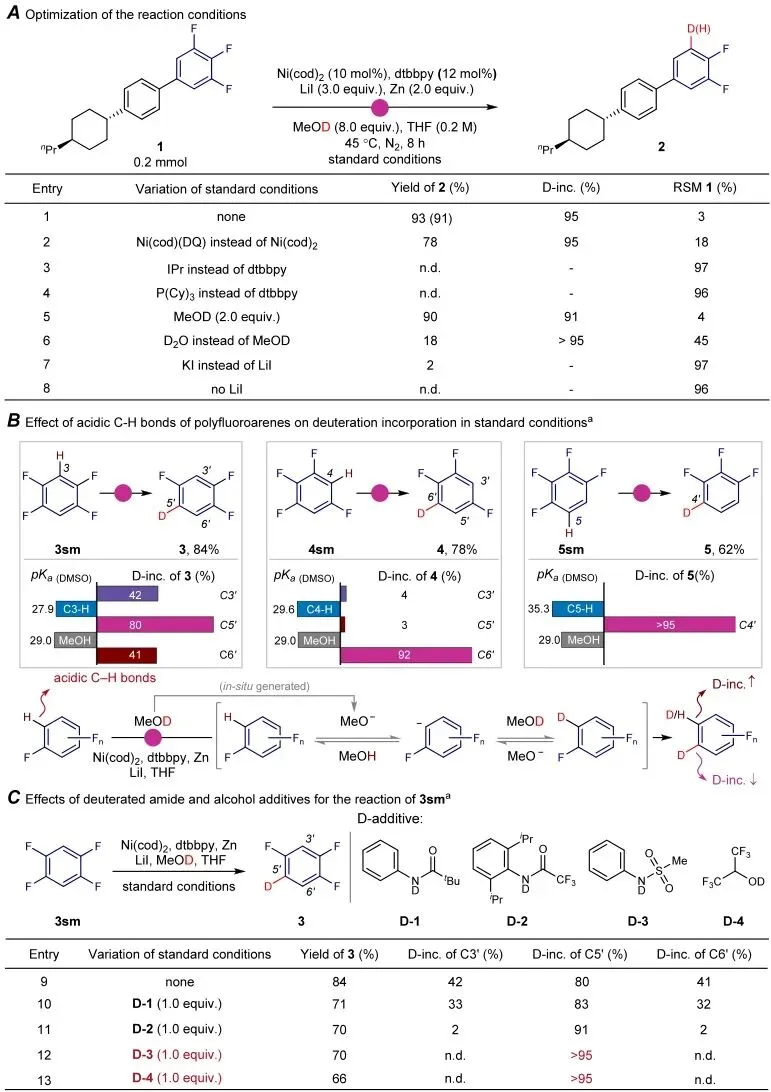
图2 | 反应条件优化及对照实验,包括反应参数筛选、多氟芳烃酸性C−H键对氘代率的影响,以及氘代酰胺和醇添加剂的作用。
该图详细展示了反应条件的优化过程。图A显示使用Ni(cod)₂/ dtbbpy/ LiI/ Zn/ MeOD体系可获得91%分离收率和95%氘掺入率;
图B探讨了不同取代模式四氟苯中酸性C−H键对氘代位置选择性的影响,发现甲氧基负离子会与酸性C−H位点发生H/D交换竞争;
图C测试了氘代酰胺和醇类添加剂对3sm反应的影响,发现苯甲磺酰胺-d₁(D-3)和(CF₃)₂CHOD(D-4)可获得>95%的氘掺入率,有效抑制了过度氘化。
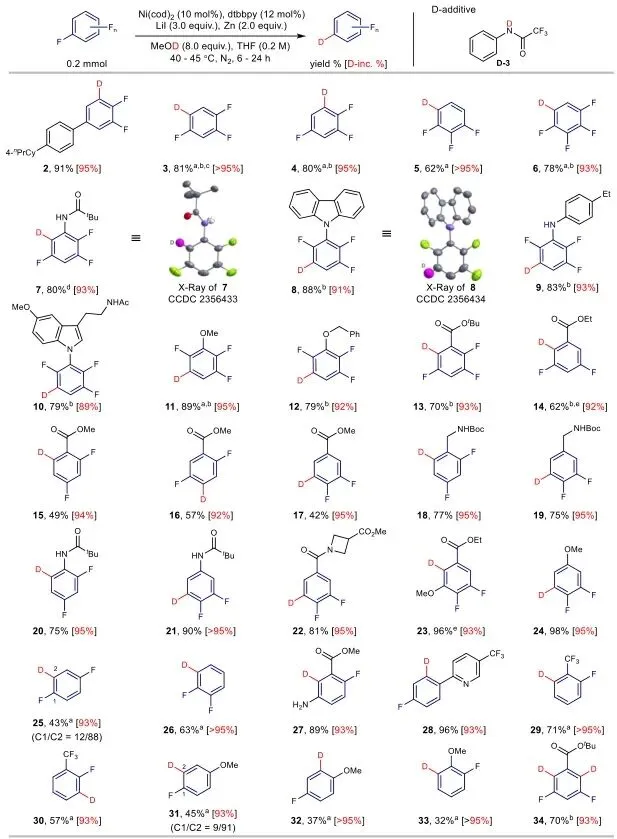
图3 | 多氟芳烃选择性脱氟氘化反应的底物适用范围考察,展示多种五氟、四氟、三氟及二氟芳烃衍生物的反应结果。
该图展示了广泛的底物适用范围。五氟、四氟、三氟甚至含供电子取代基的二氟芳烃(如苯胺、醚、酰胺、杂环等)均能顺利反应,以32−98%的收率获得产物(2−33),区域选择性≥95:5,氘掺入率高。
该方法对酰胺(7, 10, 20−22)、杂环(8, 10, 22)、未保护胺(9, 27)、醚(11, 12, 24, 31−33)和氨基甲酸酯(18, 19)等官能团具有良好的兼容性,且三氟甲基取代基(28−30)在反应条件下保持完整。通过调节反应时间或添加剂用量可有效抑制过度还原。
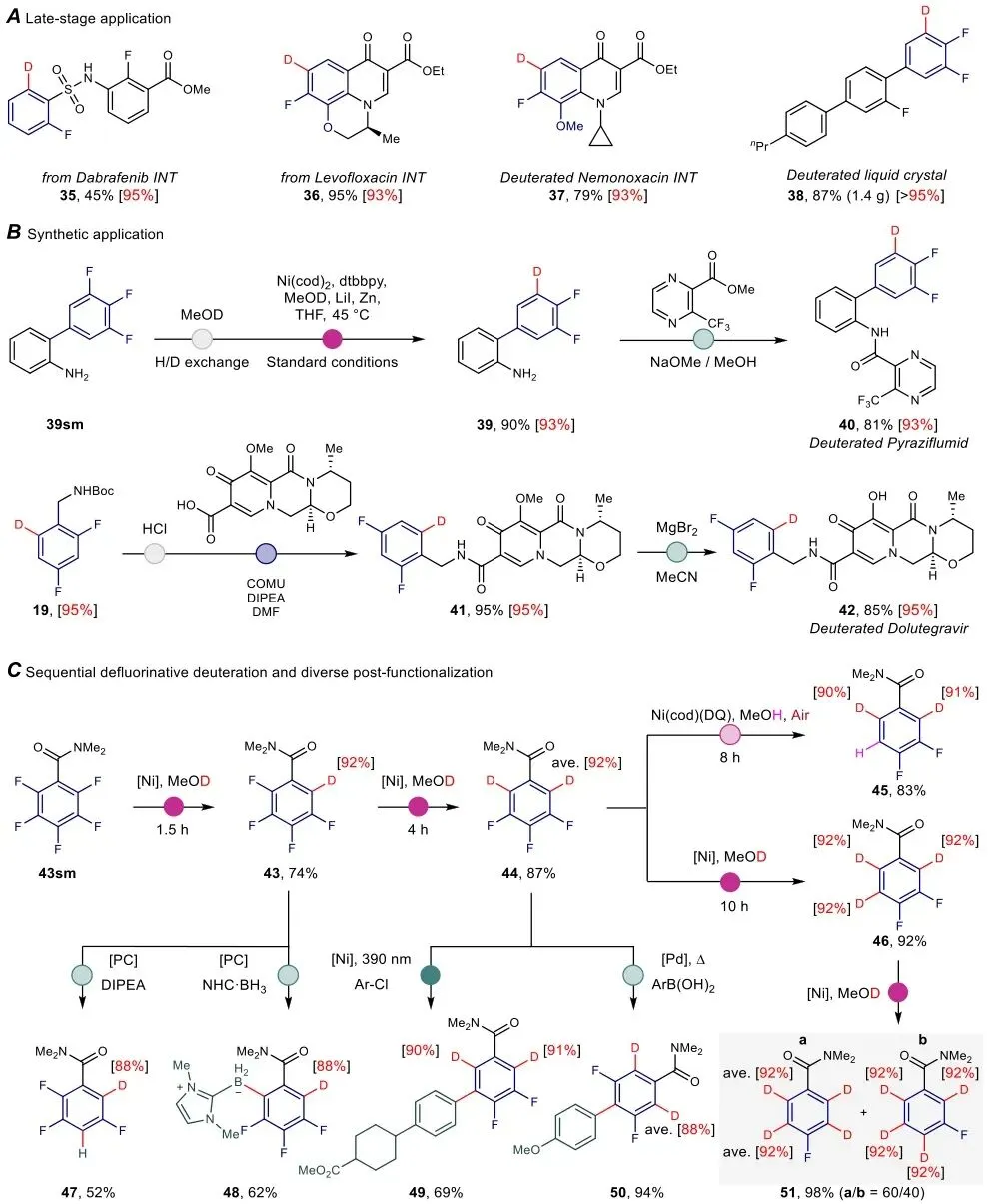
图4 | 复杂药物分子后期氘代修饰、氘代药物合成及连续脱氟氘化与多样后功能化应用。
该图展示了方法在药物化学中的应用价值。图A显示达拉非尼和左氧氟沙星中间体可转化为氘代产物(35和36),尼莫沙星骨架(37)可直接制备,反应可放大至5 mmol规模(87%收率);
图C展示了五氟苯甲酰胺的连续脱氟氘化序列,可依次获得单氘(43)、双氘(44)、三氘(45)和四氘(51)产物,且可进一步通过光氧化还原或Ni/Pd催化进行多样化转化(47−50)。
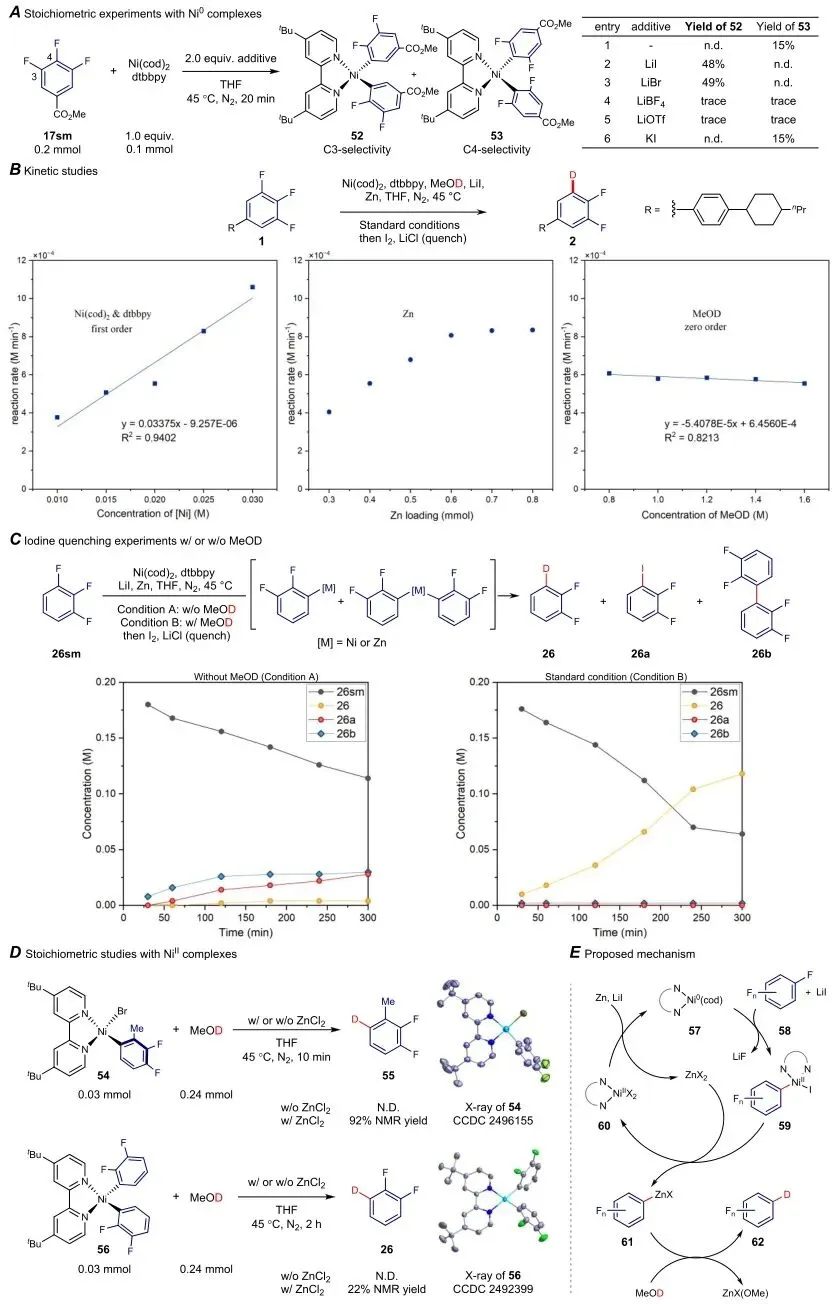
图5 | 机理研究,包括化学计量氧化加成实验、动力学分析、有机金属物种监测、中间体验证及提出的催化循环机理。
该图通过系列实验阐明反应机理。图A显示LiI可将氧化加成区域选择性从C(4)位(SNAr位,中间体53,15%收率)转变为C(3)位(中间体52,48%收率),证明锂盐协同效应;
图B动力学研究表明反应对Ni催化剂为一级,对底物和MeOD为零级,Zn还原Ni²⁺为决速步;图C时间进程实验监测到ArFn−MX和(ArFn)₂M中间体的稳态浓度;
图D显示ArFnNiᴵᴵBr(54)与MeOD不反应,但加入ZnCl₂后高效生成产物,支持有机锌中间体形成;图E提出了Ni⁰氧化加成、转金属化生成有机锌物种、与MeOD淬灭得到氘代产物的催化循环,ZnX₂原位积累可自限性抑制过度转化。
📝 总结
该团队开发了一种通用且稳健的镍催化多氟芳烃C−F键脱氟氘化策略,在广泛的底物范围内实现了高区域选择性和高效氘掺入。与传统氢同位素交换方法互补,该方法利用易得的多氟芳烃和氘源,允许以良好的位点选择性可控地引入一至四个氘原子。
该反应与复杂药物中间体兼容,所得氘代产物可用作氘标记药物的通用前体。机理研究突出了锂盐在促进选择性C−F键活化中的关键作用,以及原位生成的ZnX₂在介导转金属化和调节还原中的作用,为Ni、Zn和添加剂的协同作用提供了见解。
该工作为选择性氘化多氟芳烃提供了广泛适用的平台,并为合成多氘代化合物和药物化学中的后期同位素标记开辟了新机遇。
Nickel-Catalyzed Selective Defluorinative Deuteration of Polyfluoroarenes,Journal of the American Chemical Society,2026,DOI:10.1021/jacs.6c05353
#南京大学#谢劲#朱成建#催化#JACS