一分钟快读
该研究揭示肿瘤产生的氨通过调控调节性T细胞(Tregs)代谢阻碍抗肿瘤免疫。肿瘤微环境中谷氨酰胺分解产生氨,高氨低尿素循环活性区域富集Tregs,氨可诱导Tregs存活增殖并抑制CD8⁺、CD4⁺T细胞。Tregs通过两种特异性途径适应氨环境:一是经SRC3/STAT3通路上调精氨酸琥珀酸裂解酶(ASL)激活尿素循环解毒氨;二是FOXP3调控精胺合成酶(SMS)将鸟氨酸转化为精胺,精胺结合PPARγ增强氧化磷酸化(OXPHOS)提升Tregs功能。抗PD-1治疗导致肿瘤细胞死亡,通过转脱氨作用释放氨,强化Tregs功能引发治疗抵抗。GLUD1抑制剂(R162)联合抗PD-1治疗可降低氨水平和Tregs浸润,在肝癌、结直肠癌等模型中提升疗效,为肿瘤免疫治疗提供新策略。
文章信息
题名:Tumor-produced ammonia is metabolized by regulatory T cells to further impede anti-tumor immunity译名:肿瘤产生的氨被调节性T细胞代谢,从而进一步阻碍抗肿瘤免疫期刊:Cell5YIF:48.8发表时间:2025-12-29DOI:10.1016/j.cell.2025.11.034
图文摘要
研究背景
调节性T细胞(Tregs)通过在肿瘤微环境(TME)中代谢适应形成免疫抑制龛以促进肿瘤进展,但其适应恶劣代谢环境、抑制抗肿瘤免疫的机制尚未明确,这是肿瘤免疫治疗领域的长期研究难题。肿瘤细胞具有高活性能量代谢特征,谷氨酰胺作为肿瘤细胞主要能量来源,经谷氨酰胺分解产生α-酮戊二酸(α-KG)以支持三羧酸循环(TCA)供能和蛋白质合成,同时氨作为谷氨酰胺分解的副产物在TME中积累,已被证实可诱导CD8⁺效应T细胞死亡或耗竭,而记忆T细胞能通过尿素循环解毒氨存活,提示肿瘤Tregs可能存在类似适应机制。肝细胞癌(HCC)恶性程度高,5年生存率仅70%,对PD-1/PD-L1治疗的响应率不足20%,且肝脏作为氨解毒主要器官,其相关肿瘤的氨代谢微环境特征亟待解析。
研究思路
先通过空间代谢组学、空间转录组学结合UMAP聚类分析,明确人肝癌组织中高谷氨酰胺分解、低尿素循环活性的亚区域与Treg富集的空间关联,再经体外细胞培养、小鼠肿瘤模型验证氨对Treg富集的因果作用;随后利用scRNA-seq、qPCR、Western blotting等技术,揭示Treg通过SRC3/STAT3通路上调ASL激活尿素循环解毒氨的机制;通过RNA-seq、LC-MS/MS、ChIP-qPCR等验证FOXP3驱动SMS表达,将氨代谢中间产物转化为精胺,精胺结合PPARγ增强OXPHOS的通路;最后借助临床样本分析、小鼠肿瘤模型治疗实验,探究抗PD-1治疗诱导肿瘤细胞转脱氨作用释放氨导致治疗抵抗的机制,验证GLUD1抑制剂与抗PD-1联合治疗的增效作用,全程结合X射线晶体学、MST、ITC等技术验证关键分子相互作用。
主要研究结果
氨驱动肿瘤内Treg富集
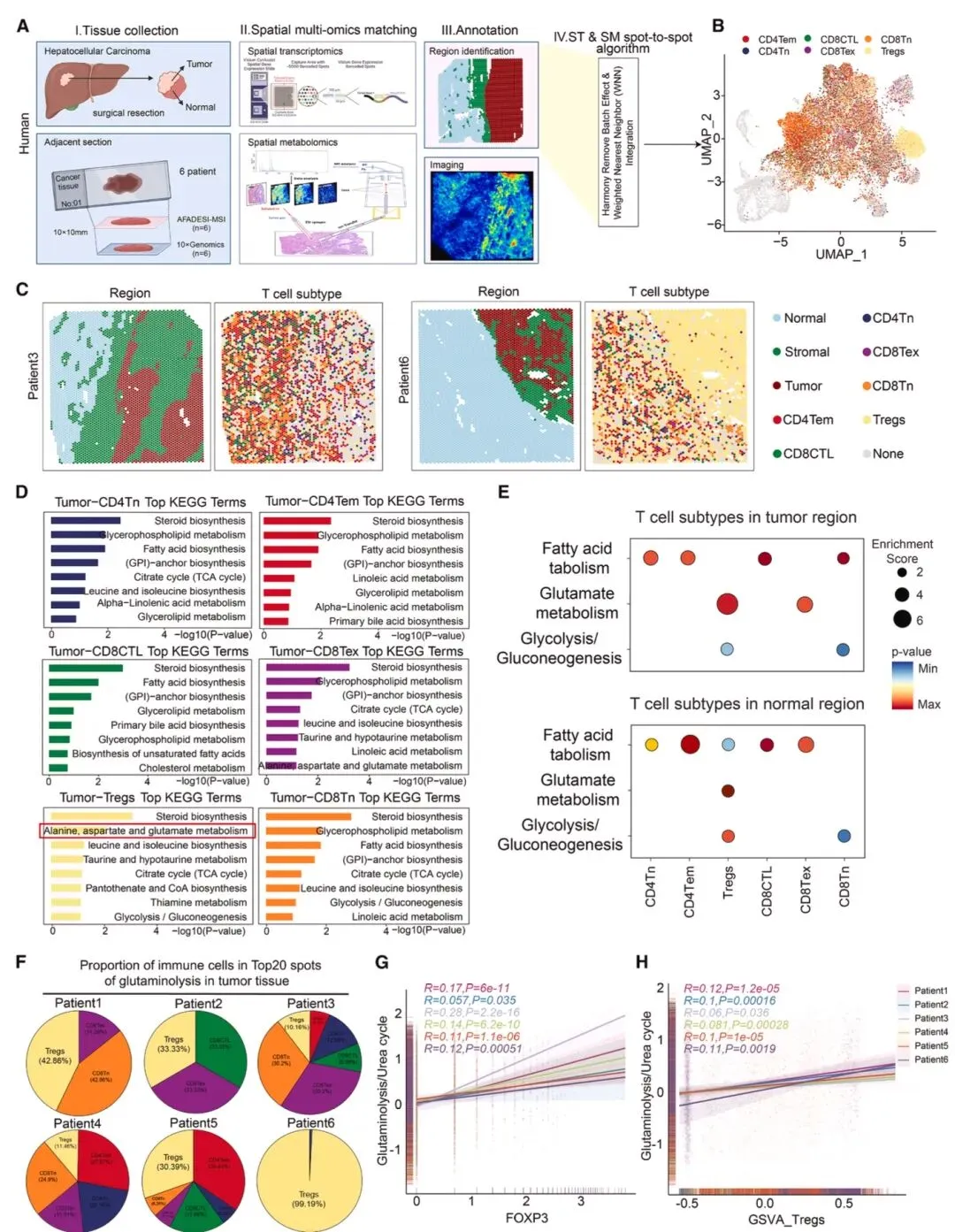 图1 高谷氨酰胺分解与低尿素循环活性是调节性T细胞富集的肿瘤亚区域的关键代谢特征通过空间代谢组学与转录组学结合UMAP聚类分析(图1),发现人肝癌组织中高谷氨酰胺分解、低尿素循环活性的亚区域与Treg富集存在空间关联,这类区域CD8⁺和CD4⁺效应T细胞凋亡增加。临床肝癌样本中,氨浓度与Treg比例呈正相关,皮下Hep-53.4肿瘤模型中,瘤内注射5mM或10mM NH₄Cl可显著增加肿瘤生长、瘤内氨水平及Treg频率。在病毒性肝炎和MASLD相关肝癌中,肝内氨含量和Treg浸润均高于正常肝脏及配对非肿瘤组织,且该关联在结直肠癌、肺腺癌等肿瘤中同样存在。体外实验显示,5mM氨(模拟瘤内水平)不影响Treg丰度却抑制CD8⁺和CD4⁺T细胞增殖,Tregs在低、高氨环境下死亡率均低于其他T细胞,且能维持胞内稳态抵抗凋亡(图2),证实氨是驱动肿瘤内Treg富集的关键因素。
图1 高谷氨酰胺分解与低尿素循环活性是调节性T细胞富集的肿瘤亚区域的关键代谢特征通过空间代谢组学与转录组学结合UMAP聚类分析(图1),发现人肝癌组织中高谷氨酰胺分解、低尿素循环活性的亚区域与Treg富集存在空间关联,这类区域CD8⁺和CD4⁺效应T细胞凋亡增加。临床肝癌样本中,氨浓度与Treg比例呈正相关,皮下Hep-53.4肿瘤模型中,瘤内注射5mM或10mM NH₄Cl可显著增加肿瘤生长、瘤内氨水平及Treg频率。在病毒性肝炎和MASLD相关肝癌中,肝内氨含量和Treg浸润均高于正常肝脏及配对非肿瘤组织,且该关联在结直肠癌、肺腺癌等肿瘤中同样存在。体外实验显示,5mM氨(模拟瘤内水平)不影响Treg丰度却抑制CD8⁺和CD4⁺T细胞增殖,Tregs在低、高氨环境下死亡率均低于其他T细胞,且能维持胞内稳态抵抗凋亡(图2),证实氨是驱动肿瘤内Treg富集的关键因素。
Treg通过尿素循环解毒氨
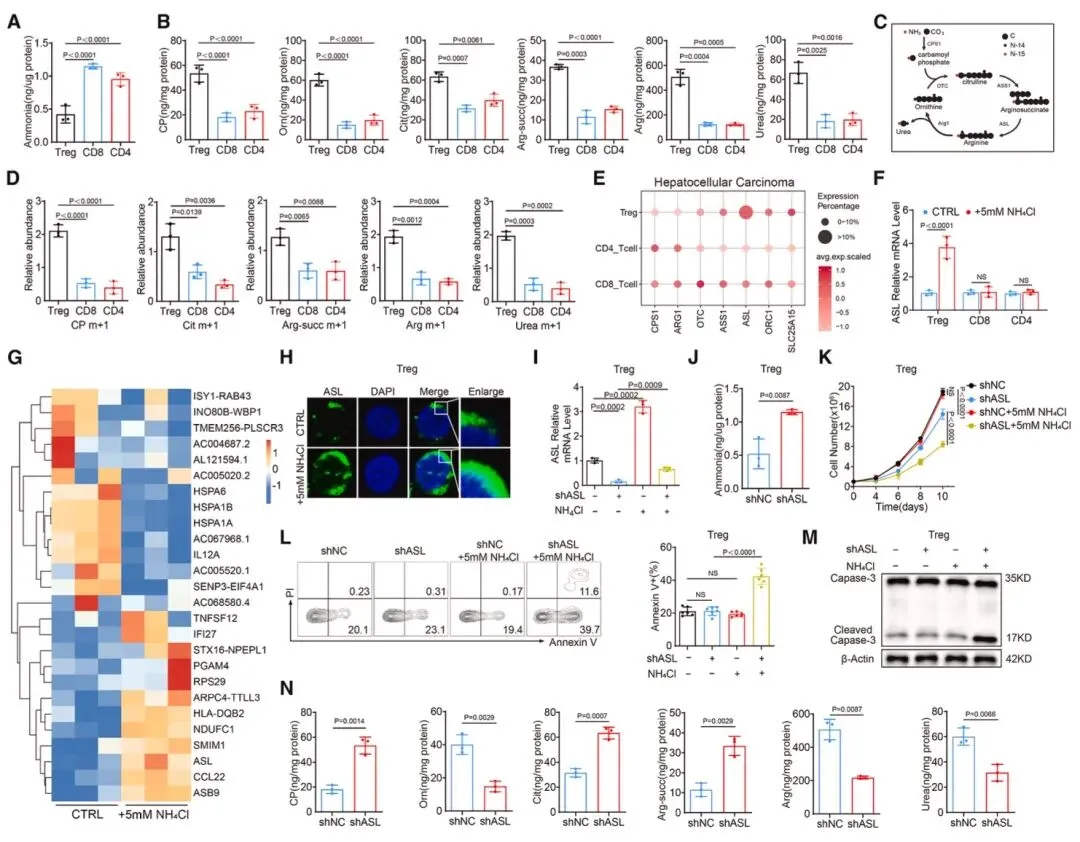 图3 氨暴露通过上调精氨酸琥珀酸裂解酶(ASL)表达诱导调节性T细胞的尿素循环激活在人体肝癌样本中,Treg的细胞内氨水平显著低于CD8⁺和CD4⁺T细胞,且尿素循环中间产物含量更丰富(图3),15N标记NH₄Cl追踪实验证实Treg能将更多氮元素整合到尿素循环中间产物中。scRNA-seq数据显示,肿瘤浸润Treg的精氨酸琥珀酸裂解酶(ASL)表达量显著高于其他T细胞亚群,5mM NH₄Cl处理可在mRNA和蛋白水平上调Treg的ASL表达,而CD8⁺和CD4⁺T细胞无此变化。shRNA介导的ASL沉默会升高Treg内氨水平,削弱其增殖能力和抗凋亡能力,扰乱尿素循环代谢物平衡,Asl敲除小鼠的Treg在氨暴露下更易凋亡,且肿瘤进展受抑、对反PD-1治疗响应增强,证实ASL是Treg通过尿素循环解毒氨的关键分子。
图3 氨暴露通过上调精氨酸琥珀酸裂解酶(ASL)表达诱导调节性T细胞的尿素循环激活在人体肝癌样本中,Treg的细胞内氨水平显著低于CD8⁺和CD4⁺T细胞,且尿素循环中间产物含量更丰富(图3),15N标记NH₄Cl追踪实验证实Treg能将更多氮元素整合到尿素循环中间产物中。scRNA-seq数据显示,肿瘤浸润Treg的精氨酸琥珀酸裂解酶(ASL)表达量显著高于其他T细胞亚群,5mM NH₄Cl处理可在mRNA和蛋白水平上调Treg的ASL表达,而CD8⁺和CD4⁺T细胞无此变化。shRNA介导的ASL沉默会升高Treg内氨水平,削弱其增殖能力和抗凋亡能力,扰乱尿素循环代谢物平衡,Asl敲除小鼠的Treg在氨暴露下更易凋亡,且肿瘤进展受抑、对反PD-1治疗响应增强,证实ASL是Treg通过尿素循环解毒氨的关键分子。
氨经SMS-精胺-PPARγ增强Treg的OXPHOS
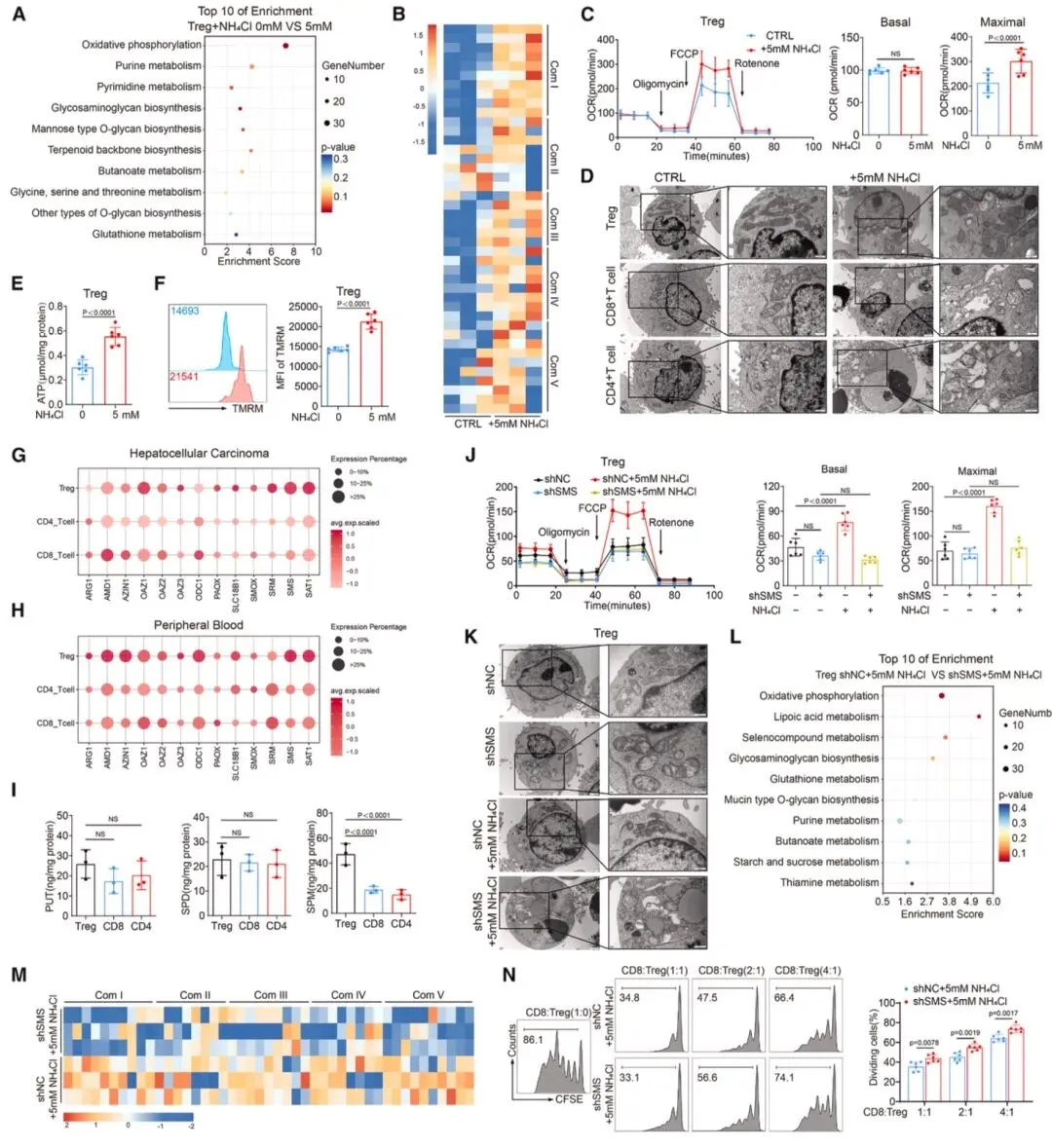 图4 氨通过FOXP3驱动的精胺合成酶(SMS)表达促进调节性T细胞的氧化磷酸化(OXPHOS)RNA-seq结果显示,5mM NH₄Cl处理后Treg的OXPHOS通路显著富集,线粒体复合体基因上调,氧消耗率(OCR)较CD8⁺、CD4⁺T细胞显著升高(图4)。HCC及外周血Treg中精胺合成酶(SMS)特异性高表达,LC-MS/MS证实肿瘤来源Treg的精胺水平升高,FOXP3可结合SMS启动子的2、5区域驱动其表达。SMS将尿素循环中间产物鸟氨酸转化为精胺,MST和ITC证实精胺与PPARγ直接结合(KD值分别为11.557±3.075μM、5.21μM),且依赖Glu319、Ser370、Glu371位点(图6)。精胺-PPARγ结合可调控线粒体复合体(I-V)相关基因转录,增强Treg的ATP生成和免疫抑制功能,SMS或PPARγ敲低则会阻断该效应。
图4 氨通过FOXP3驱动的精胺合成酶(SMS)表达促进调节性T细胞的氧化磷酸化(OXPHOS)RNA-seq结果显示,5mM NH₄Cl处理后Treg的OXPHOS通路显著富集,线粒体复合体基因上调,氧消耗率(OCR)较CD8⁺、CD4⁺T细胞显著升高(图4)。HCC及外周血Treg中精胺合成酶(SMS)特异性高表达,LC-MS/MS证实肿瘤来源Treg的精胺水平升高,FOXP3可结合SMS启动子的2、5区域驱动其表达。SMS将尿素循环中间产物鸟氨酸转化为精胺,MST和ITC证实精胺与PPARγ直接结合(KD值分别为11.557±3.075μM、5.21μM),且依赖Glu319、Ser370、Glu371位点(图6)。精胺-PPARγ结合可调控线粒体复合体(I-V)相关基因转录,增强Treg的ATP生成和免疫抑制功能,SMS或PPARγ敲低则会阻断该效应。
抗PD-1治疗诱导氨释放致耐药
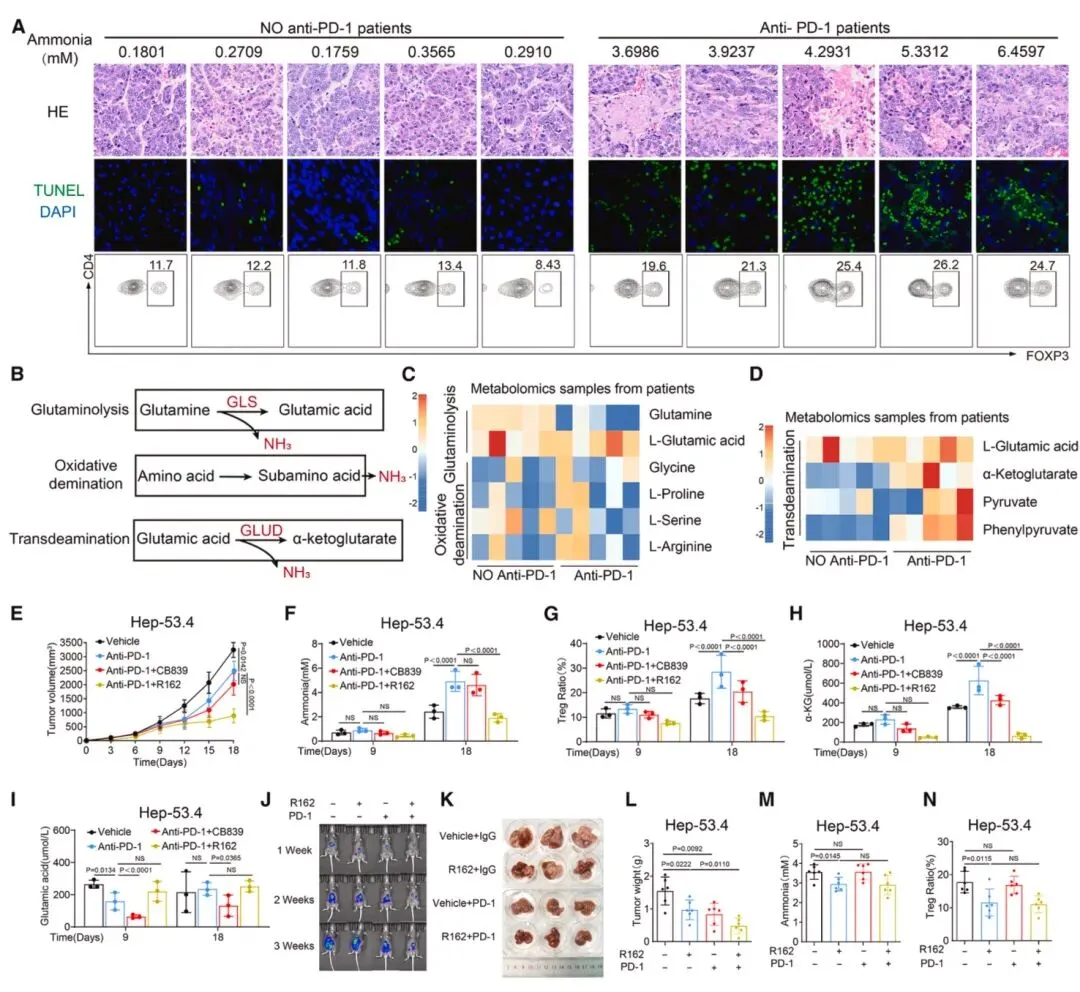 图7 抗PD-1治疗诱导肿瘤细胞死亡产生的氨增强调节性T细胞功能并导致免疫治疗耐药临床HCC样本显示,接受抗PD-1治疗的患者肿瘤组织氨水平和Treg比例显著升高(图7),靶向代谢组学证实肿瘤细胞凋亡时转脱氨作用被激活,而非谷氨酰胺分解或氧化脱氨,这是氨产生的主要来源。皮下Hep-53.4肿瘤模型中,抗PD-1治疗初期(第9天)抑制肿瘤生长,但后期(第18天)出现耐药,瘤内氨水平和Treg比例显著上升。GLUD1抑制剂R162可有效降低氨水平,联合抗PD-1治疗能逆转耐药,在orthotopic肝癌模型中显著抑制肿瘤进展,减少Treg浸润并提升CD8⁺T细胞功能,该联合方案在HTVI-HCC和MASH-HCC模型中同样有效,证实氨释放是抗PD-1治疗耐药的关键机制。
图7 抗PD-1治疗诱导肿瘤细胞死亡产生的氨增强调节性T细胞功能并导致免疫治疗耐药临床HCC样本显示,接受抗PD-1治疗的患者肿瘤组织氨水平和Treg比例显著升高(图7),靶向代谢组学证实肿瘤细胞凋亡时转脱氨作用被激活,而非谷氨酰胺分解或氧化脱氨,这是氨产生的主要来源。皮下Hep-53.4肿瘤模型中,抗PD-1治疗初期(第9天)抑制肿瘤生长,但后期(第18天)出现耐药,瘤内氨水平和Treg比例显著上升。GLUD1抑制剂R162可有效降低氨水平,联合抗PD-1治疗能逆转耐药,在orthotopic肝癌模型中显著抑制肿瘤进展,减少Treg浸润并提升CD8⁺T细胞功能,该联合方案在HTVI-HCC和MASH-HCC模型中同样有效,证实氨释放是抗PD-1治疗耐药的关键机制。
小结
该研究阐明肿瘤产生的氨是驱动调节性T细胞(Tregs)富集并阻碍抗肿瘤免疫的关键因素,揭示了Tregs适应氨富集肿瘤微环境的两种特异性代谢机制:通过SRC3/STAT3通路上调ASL激活尿素循环解毒氨,以及经FOXP3驱动SMS表达将鸟氨酸转化为精胺,精胺结合PPARγ增强氧化磷酸化提升免疫抑制功能。研究还发现抗PD-1治疗诱导肿瘤细胞通过转脱氨作用释放氨,强化Tregs功能导致治疗耐药,而GLUD1抑制剂与抗PD-1联合治疗可有效降低氨水平、减少Tregs浸润,在多种肿瘤模型中提升疗效。该研究不仅深化了对肿瘤代谢与免疫抑制相互作用的理解,还为克服免疫治疗耐药提供了靶向氨代谢的新策略,具有重要临床转化价值。
本文原创为原创编译,不主张原文版权,侵删。本文个人闲暇时间收集,个人水平有限,若有纰漏,麻烦留言指出,我尽快修改!