复旦 / 南京医科大学等多团队发 Top 刊 nAMD 治疗新突破,MSC 外泌体 lnc-AGT-3 经 p53 信号通路抑制新生血管性黄斑变性
- 2026-04-01 00:04:55
导 读
Introduction

一、研究背景解读
Background
目前临床主流的抗 VEGF 药物(如雷珠单抗、阿柏西普)虽能延缓病情进展,但约 30% 患者会产生耐药性,且需每 4-8 周进行眼内注射,长期治疗易引发感染、视网膜损伤等并发症,亟需开发更安全、长效的替代疗法。
间充质干细胞(MSC)来源外泌体作为天然纳米囊泡,可携带蛋白质、脂质、RNA 等生物活性物质介导细胞间通讯,在心血管、神经及眼部疾病中展现出强大的组织修复与调控潜力。长链非编码 RNA(lncRNA)作为外泌体核心功能 cargo,可通过转录后调控参与疾病进程,但外泌体源性 lncRNA 在 nAMD 血管生成中的作用及机制尚未明确。
二、研究思路解析
Train of Though
该研究以 “MSC 外泌体调控 nAMD 病理性血管生成的关键分子及机制” 为核心,采用 “临床样本验证 - 细胞功能筛选 - 分子机制解析 - 动物模型验证” 的层层递进研究思路:
1. 临床与模型验证 lnc-AGT-3 的表达特征:通过 nAMD 患者房水样本、激光诱导 CNV 小鼠模型及 NRV2 自发视网膜新生血管小鼠模型,检测 lnc-AGT-3 的表达差异,明确其与疾病的关联性。
2. 外泌体分离与功能验证:从人脐带 MSC 中分离纯化外泌体,通过体内外实验验证其抗血管生成作用,同时排除视网膜毒性。
3. 关键功能 lncRNA 筛选:利用基因芯片技术分析 MSC 外泌体处理后血管内皮细胞的 lncRNA 表达谱,筛选并验证核心调控分子 lnc-AGT-3。
4. 分子机制解析:通过 RNA pull-down、质谱分析、RIP 等实验鉴定 lnc-AGT-3 的结合蛋白;利用泛素化实验、Western blot 等明确其对 p53 信号通路的调控方式。
5. 体内治疗效果验证:通过 AAV 介导的 lnc-AGT-3 过表达,在 CNV 小鼠模型中验证其治疗潜力,同时明确其与 hnRNP K、p53/TSP1 轴的依赖关系。
三、研究主要结果展示
ResultDemonstraion
该研究从临床、细胞、分子及动物层面系统阐明了 MSC 外泌体 lnc-AGT-3 的抗血管生成作用及机制,核心结果如下:
MSC 外泌体具有显著抗血管生成活性且无视网膜毒性:①分离的 MSC 外泌体呈典型杯状结构,直径 84-223 nm,高表达 CD9、Hsp70、TSG101 等外泌体标志物。②体内实验显示,MSC 外泌体眼内注射可显著缩小激光诱导 CNV 小鼠的病灶面积,疗效与抗 VEGF 药物阿柏西普相当;在 NRV2 小鼠模型中,可减少视网膜脱色素区域及血管渗漏。③长期安全性评估表明,MSC 外泌体对视网膜神经节细胞、光感受器细胞无损伤,不影响视网膜厚度及视觉功能(ERG 检测证实 a 波、b 波振幅无显著变化)。
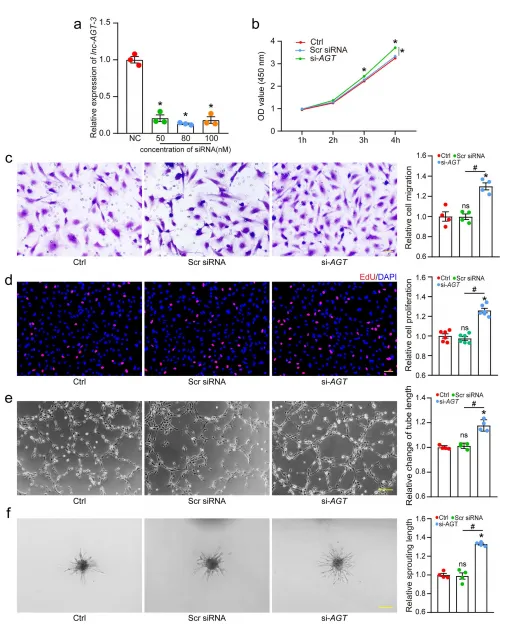
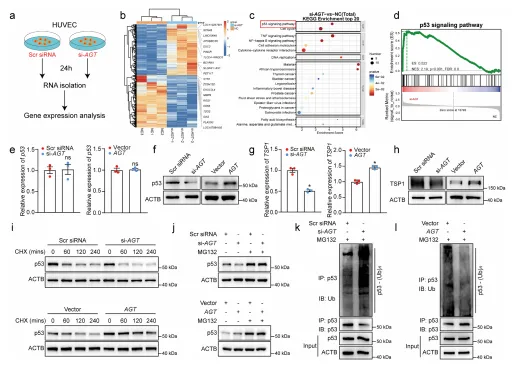
lnc-AGT-3 是 MSC 外泌体中核心抗血管生成 lncRNA:①基因芯片分析发现,MSC 外泌体处理后,血管内皮细胞(HUVECs)中 99 种 lncRNA 上调,171 种下调,其中 lnc-AGT-3 在 MSC 外泌体中富集度最高。②临床样本验证:nAMD 患者房水中 lnc-AGT-3 表达显著低于年龄相关性白内障(ARC)对照组;CNV 模型小鼠的视网膜 / 脉络膜组织中,lnc-AGT-3 表达亦显著下调。③体外功能实验:lnc-AGT-3 沉默可促进 HUVECs 增殖、迁移及管腔形成;反之,其过表达可抑制氧化应激(H₂O₂处理)诱导的血管内皮细胞异常活化。
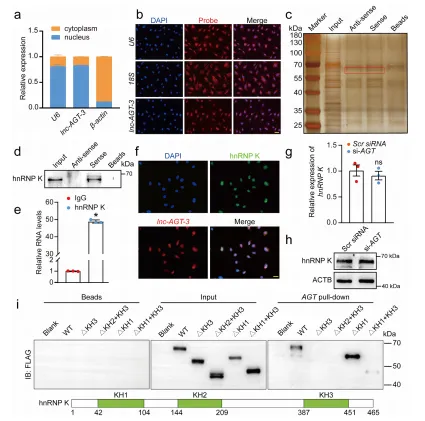
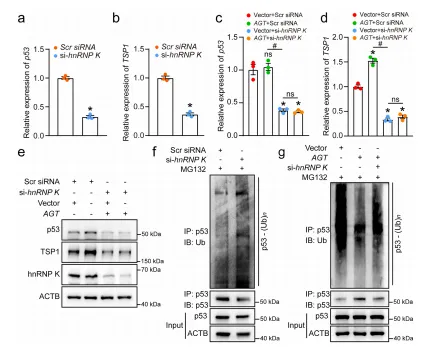
lnc-AGT-3 通过结合 hnRNP K 调控 p53 信号通路:①亚细胞定位显示,lnc-AGT-3 主要定位于细胞核,RNA pull-down 联合质谱分析证实其与 hnRNP K 直接结合,且结合依赖 hnRNP K 的 KH3 结构域。②分子机制:lnc-AGT-3 可阻断 p53 的泛素化降解,提高 p53 蛋白稳定性;p53 进一步上调下游抗血管生成因子 TSP1 的表达,从而抑制血管生成。③挽救实验证实,敲低 p53 或 TSP1 可逆转 lnc-AGT-3 的抗血管生成效应,表明其功能依赖 p53/TSP1 轴。
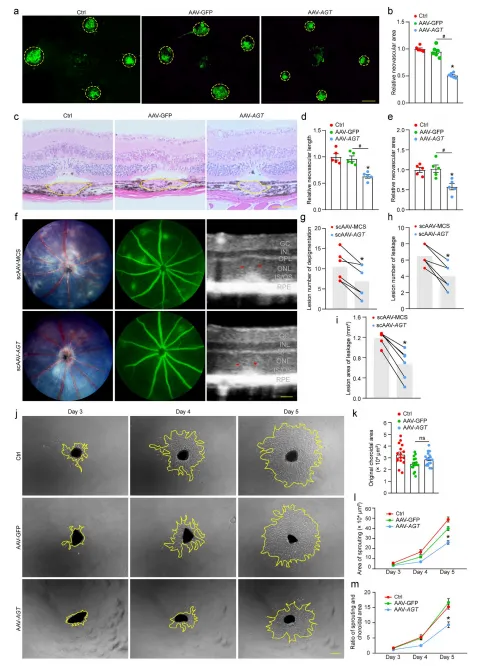
lnc-AGT-3 过表达在体内显著抑制 CNV 进展:①AAV 介导的 lnc-AGT-3 过表达可显著缩小 CNV 小鼠的病灶长度及面积,改善视网膜外层结构紊乱。②外植体实验显示,lnc-AGT-3 过表达可抑制脉络膜组织的血管芽生能力,减少新生血管向外生长。③机制验证:敲低 hnRNP K 可阻断 lnc-AGT-3 对 p53 泛素化的抑制作用,同时消除其体内外抗血管生成效果,证实 hnRNP K 是 lnc-AGT-3 发挥功能的关键中介。
Fig. 1:间充质干细胞(MSCs,500 µm - 50 纳米)在疾病再平衡中的潜在治疗作用
间充质干细胞(50 µg)可有效减轻脂多糖诱导的视网膜和角膜水肿,并能抑制坏死性凋亡复合物的形成,其治疗效果具有时间依赖性,且在治疗后 4 天对视网膜 / 角膜水肿的改善作用具有统计学意义。
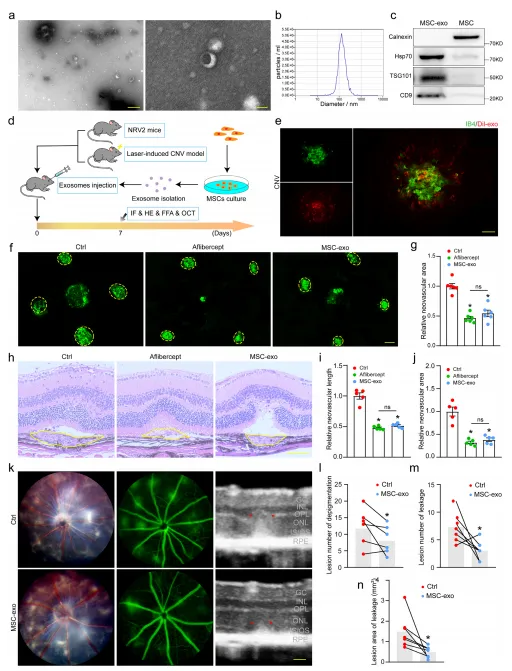
Fig. 2:间充质干细胞(MSCs)在人角膜血管细胞(HUVECs)中发挥的抗炎作用
间充质干细胞外泌体可通过调控特定 miRNA 的表达,抑制 HUVECs 中促炎细胞因子的基因表达、VCAM-1 的蛋白表达,以及 HIF-1α 介导的血管生成,从而在角膜血管细胞中发挥抗炎作用。
五、总 结
Summary
该研究首次揭示 “MSC 外泌体 - lnc-AGT-3-hnRNP K-p53/TSP1” 轴在 nAMD 中的作用机制:MSC 外泌体将 lnc-AGT-3 递送至病变部位,lnc-AGT-3 通过与 hnRNP K 的 KH3 结构域结合,阻断 p53 的泛素化降解,激活 p53/TSP1 信号通路,最终抑制病理性血管生成。
该研究不仅明确了 lnc-AGT-3 作为 nAMD 抗血管生成治疗新靶点的潜力,还为 MSC 外泌体疗法提供了分子机制支撑。相较于传统抗 VEGF 疗法,MSC 外泌体 lnc-AGT-3 疗法具有多靶点调控、不易产生耐药性、安全性高等优势,为 nAMD 的精准治疗开辟了新方向。未来可进一步开发基于 lnc-AGT-3 的靶向递送系统,推动其临床转化。


