IF33双一区!南京医科大学第一附属医院等科研机构联合团队,eIF3f-ACSL4 轴:肝 ai 代谢与免疫治疗的双重靶点!
- 2026-06-05 17:06:35
IF33双一区!南京医科大学第一附属医院等科研机构联合团队,eIF3f-ACSL4 轴:肝 ai 代谢与免疫治疗的双重靶点!


脂肪酸代谢重编程是肝癌的核心特征,但调控机制尚未完全阐明。这篇发表于《Journal of Hepatology》的研究,通过多组学与多模型验证,揭示了 eIF3f 通过稳定 ACSL4 促进脂肪酸合成的关键机制,为肝癌精准治疗提供了新靶点,同时为免疫联合治疗提供了新思路,值得深入解读。 


1. eIF3f 在肝癌组织中高表达,与不良预后相关,是驱动肝癌恶性进展的关键分子。 2. 核心机制为 eIF3f 通过 K48 位去泛素化稳定 ACSL4,促进脂肪酸从头合成与脂质积累,进而抑制 CD8⁺T 细胞浸润与活化。 3. SRPK1 介导的 eIF3f Ser266 磷酸化可增强其与 ACSL4 的相互作用,放大促癌效应。 4. 靶向 eIF3f(如 LNP-siEIF3F)可抑制肝癌进展,且与抗 PD-1 治疗协同增效,显著提升抗肿瘤疗效。 5. ACSL4 是 eIF3f 调控脂肪酸代谢与肝癌恶性表型的关键下游介质,二者构成的信号轴具有重要临床转化价值。 
1. HCC 是全球第四大致癌相关死亡肿瘤,代谢重编程(尤其脂肪酸代谢异常)是其核心特征,但调控机制尚未完全阐明; 2. 脂肪酸合成增加可为肿瘤细胞提供能量与膜结构原料,同时重塑肿瘤免疫微环境,但上下游调控通路仍需挖掘; 3. eIF3f 作为翻译起始因子亚基,具有去泛素化活性,但其在 HCC 中的作用及机制此前未见报道。 
1. 首次揭示 eIF3f-ACSL4-FAB - 免疫逃逸的完整调控轴,填补 HCC 代谢与免疫交叉领域空白; 2. 明确 eIF3f 为 HCC 预后标志物与治疗靶点,为精准分层提供依据; 3. 验证 LNP-siEIF3F 联合抗 PD-1 的协同疗效,为免疫治疗耐药提供解决方案。 

1. 模型构建:患者来源类器官(PDO)、PDOX 模型、细胞系Hep3B/Huh7/Hepa1-6、异种移植模型(NCG 裸鼠、C57BL/6 小鼠); 2. 测序与组学:单细胞 RNA-seq、空间转录组、非靶向代谢组、无标记蛋白质组; 3. 分子实验:Co-IP、GST pull-down、泛素化 assay、磷酸酶处理、点突变构建; 4. 功能验证:CCK-8、Transwell、伤口愈合、脂质染色(Bodipy/Nile red)、透射电镜; 5. 免疫分析:飞行时间质谱流式、多重免疫组化、CD8+T 细胞耗竭实验; 6. 靶向递送:脂质纳米颗粒(LNP)介导 siRNA 体内靶向沉默 eIF3f。

1. 临床样本量有限,eIF3f 与 ACSL4 的相关性需更大队列验证; 2. 未明确脂肪酸调控 CD8+T 细胞功能的具体分子机制(如是否通过脂肪酸受体或代谢重编程); 3. LNP-siEIF3F 的体内药代动力学、长期安全性及靶向特异性仍需优化; 4. 未探讨 eIF3f 在其他肝脏疾病(如非酒精性脂肪肝)向 HCC 转化中的作用。 
1. 扩大临床队列,结合多中心样本分析 eIF3f/ACSL4 表达与治疗反应的相关性; 2. 深入研究脂肪酸调控 CD8+T 细胞的下游信号通路,寻找联合靶点; 3. 优化 LNP 载体的靶向性(如添加肝特异性配体),降低脱靶效应; 4. 构建 eIF3f 条件敲除小鼠,探索其在 HCC 发生发展中的时序性作用; 5. 研究 eIF3f 与其他代谢通路(如糖酵解、氨基酸代谢)的交叉调控。 
1. 代谢酶的泛素化 / 去泛素化调控是 HCC 治疗的重要突破口,需关注 “翻译因子 - 代谢酶 - 免疫微环境” 的跨界调控网络; 2. 靶向代谢重编程可逆转免疫抑制微环境,为免疫治疗耐药提供解决方案; 3. LNP 介导的 siRNA 靶向递送为不可成药靶点(如 eIF3f)提供转化可能; 4. 联合检测 eIF3f 与 ACSL4 可作为 HCC 预后及免疫治疗疗效预测的 biomarkers。 
1. 开发 eIF3f 特异性抑制剂(如针对其 MPN 结构域的小分子化合物); 2. 探索 eIF3f 磷酸化抑制剂(如 SRPK1 抑制剂)与免疫治疗的联合应用; 3. 构建 eIF3f/ACSL4 高表达 HCC 患者的精准治疗队列,开展临床试验; 4. 研究脂肪酸代谢抑制剂(如 TVB-2640)与 eIF3f 靶向治疗的协同效应; 5. 探索 eIF3f 在其他代谢相关肿瘤(如结直肠癌、乳腺癌)中的保守机制。 
1. 靶点筛选:利用 scRNA-seq + 空间转录组分析肿瘤代谢相关基因,结合 TCGA 数据库进行预后关联分析; 2. 表型验证:构建 PDO 模型与细胞系的过表达 / 沉默体系,通过 CCK-8、Transwell、移植瘤模型验证功能; 3. 机制探索:采用 IP-MS 筛选互作蛋白,通过 Co-IP、泛素化 assay 验证结合与修饰关系; 4. 免疫微环境分析:利用流式细胞术、多重免疫组化检测免疫细胞浸润情况; 5. 靶向治疗验证:选用 LNP 等载体递送 siRNA,联合免疫检查点抑制剂进行体内实验。 eIF3f-ACSL4 轴为 HCC 代谢与免疫交叉调控提供了全新视角,其靶向治疗联合抗 PD-1 的策略具有明确转化前景。您在研究中是否遇到过代谢酶与免疫逃逸的交叉机制?对 LNP 递送系统的优化有何见解?欢迎在评论区分享经验,一起探讨肝 ai 精准治疗的新可能! 关注【生信启示录】,生信不迷路。持续获取生信前沿研究解读、实用方案技术,科研路上,我们共同前行。 

点击上方 蓝字关注我们!

引言



核心观点概括

文献解读

文章标题: eIF3f 通过重塑肝细胞癌中脂肪酸的生物合成促进肿瘤恶性发展
发表期刊: J Hepatol.
发表时间: 2025年9月
影响因子: IF33.0/Q1
研究背景

价值意义

研究路线和方法

研究路线
患者来源类器官→单细胞 RNA-seq + 空间转录组筛选 FAM 相关基因→鉴定 eIF3f 为候选靶点→体内外验证 eIF3f 促癌表型→机制探索eIF3f-ACSL4 相互作用及泛素化调控→免疫微环境影响分析→靶向治疗与联合免疫治疗验证。
核心方法
研究结果

1. 筛选 FAM 与 HCC 恶性相关核心基因 eIF3f
(1)对 5 例 HCC 患者 PDO 进行 scRNA-seq,通过 UMAP 聚类与 FAM 评分分析,区分 FAM 高 / 低活性细胞群; (2)轨迹分析显示 FAM 高活性群与肿瘤细胞恶性命运相关,交叉筛选出 12 个共有差异基因; (3)结合 TCGA 数据库与临床样本验证,eIF3f 在 HCC 中高表达,且与脂质代谢通路显著富集相关,确定为核心靶点。 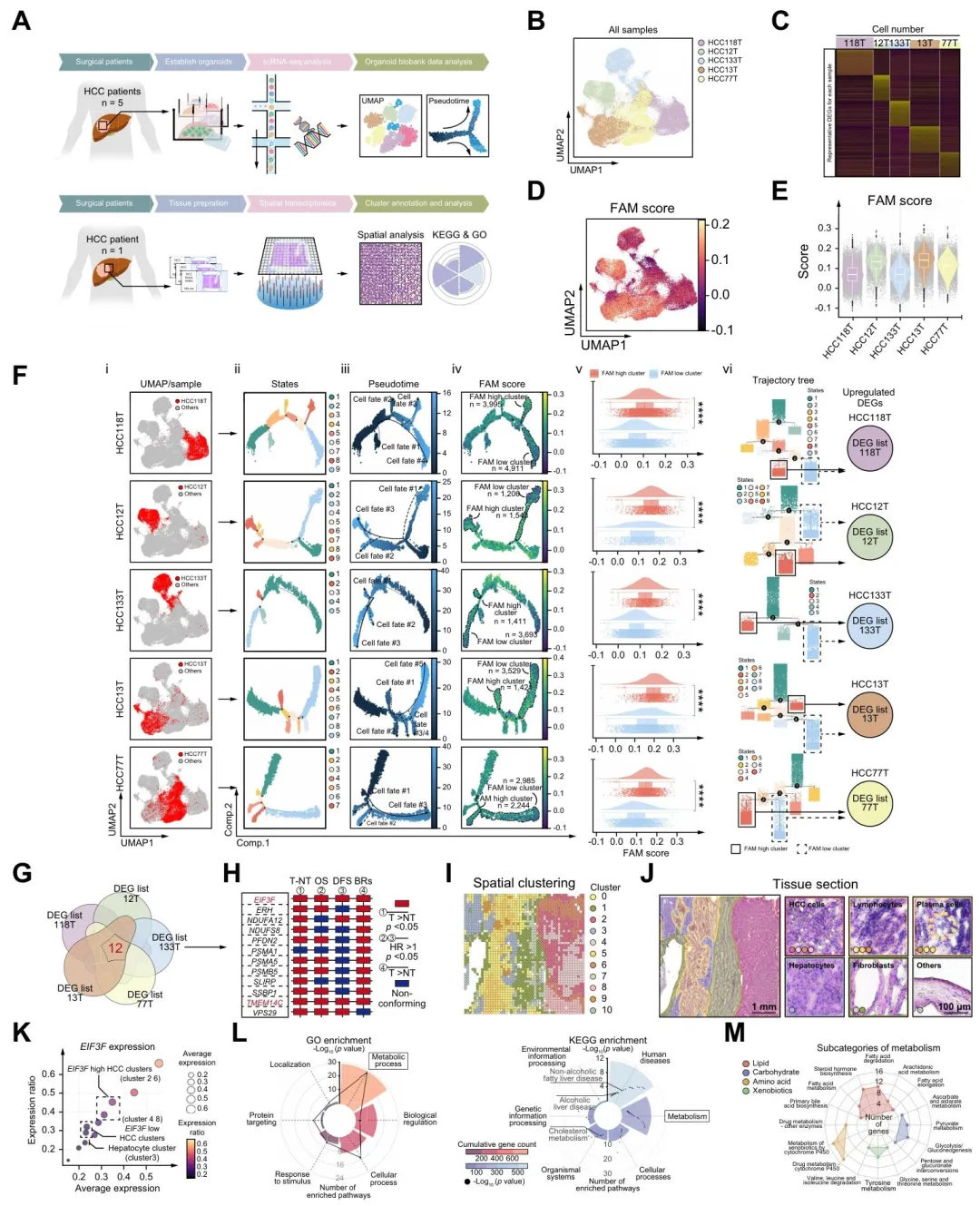
(图1:将类器官的单细胞RNA测序(scRNA-seq)分析与广泛的数据库分析相结合,以探索同时影响肝细胞癌(HCC)中FAM和恶性程度的基因)
2. eIF3f 促进 HCC 体内外恶性表型
(1)体外实验显示,eIF3f 沉默抑制 PDO 增殖、细胞克隆形成及迁移侵袭,过表达则相反; (2)体内 PDOX、裸鼠原位移植瘤及肺转移模型证实,eIF3f 沉默显著降低肿瘤体积、重量及转移灶密度,延长小鼠生存期。 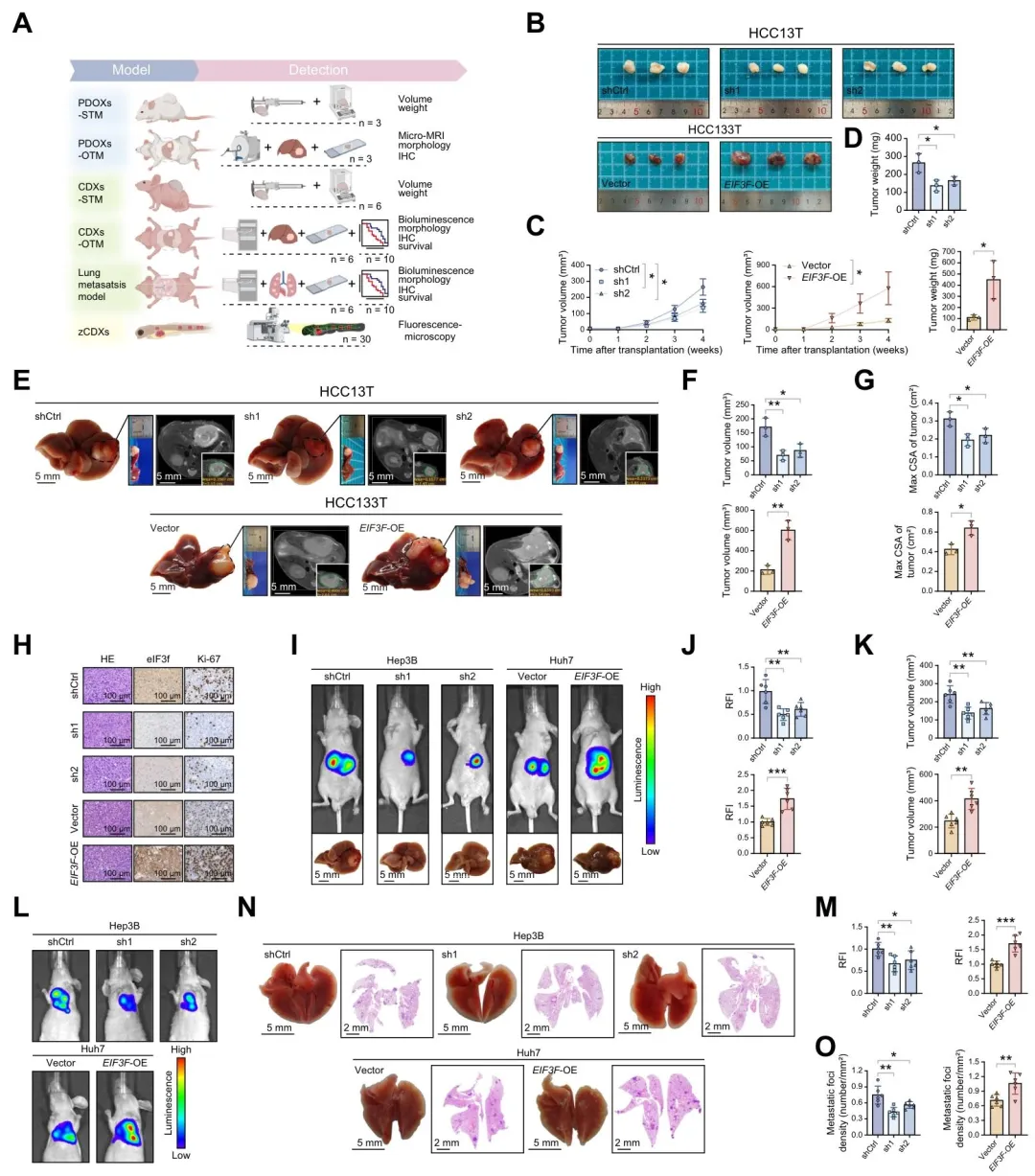
(图2:升高的eIF3f水平在体外和体内均会促进肝癌的恶性程度)
3. eIF3f 调控脂肪酸合成与脂质积累
(1)代谢组与蛋白质组分析显示,eIF3f 过表达组脂质类代谢物显著富集,不饱和脂肪酸合成、脂肪酸生物合成通路激活; (2)13C6 - 葡萄糖示踪实验证实,eIF3f 增强葡萄糖向脂肪酸C16:0、C18:1 等的代谢流; (3)透射电镜与脂质染色显示,eIF3f 过表达增加脂质滴数量,MRI 伪彩成像证实肿瘤内脂质积累增加。 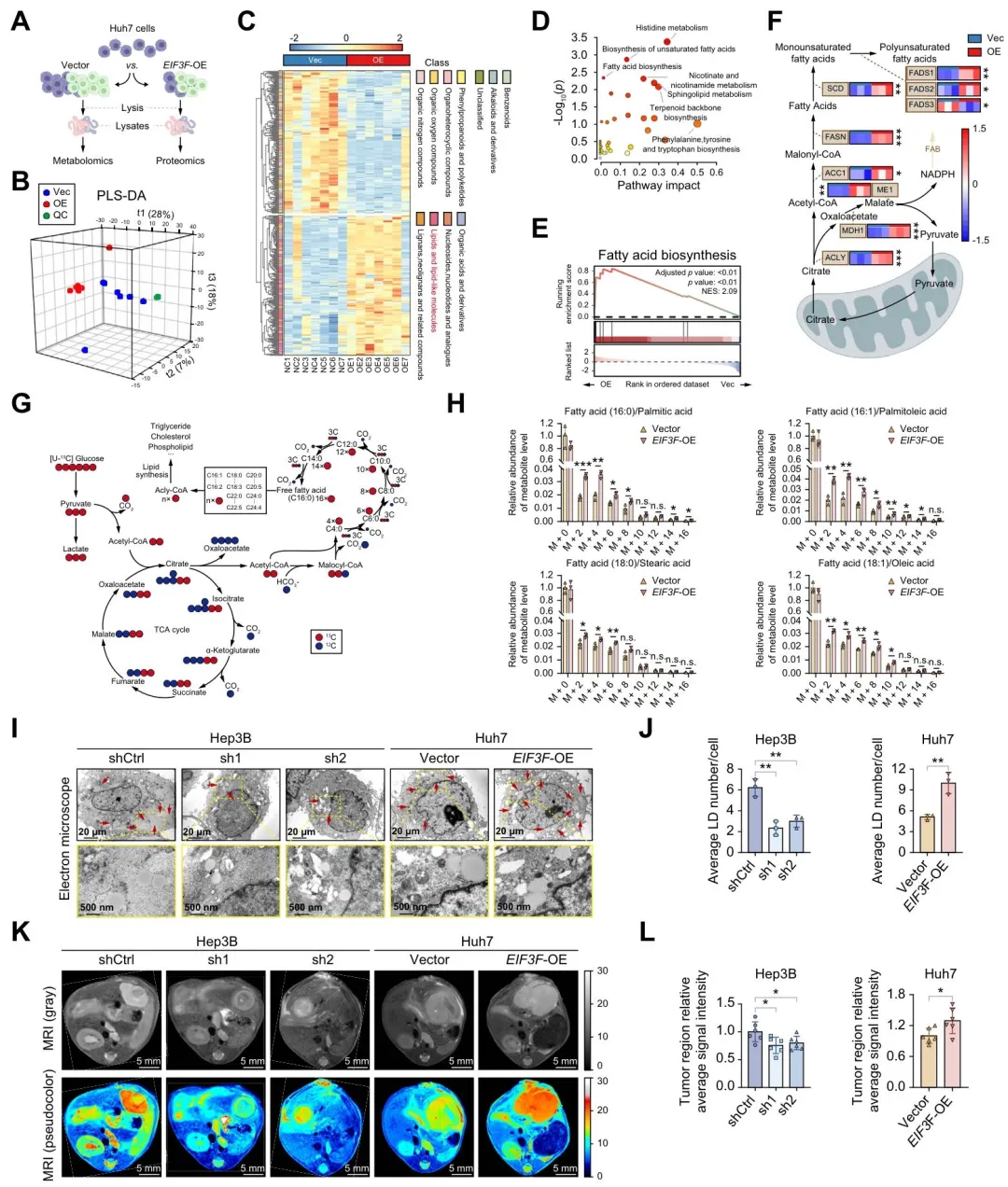
(图3:IF3f增强HC中的FAB和脂质积累)
4. eIF3f 与 ACSL4 的相互作用及调控机制
(1)IP-MS 筛选并验证 ACSL4 为 eIF3f 直接结合蛋白,免疫荧光与 PLA 实验显示二者共定位; (2)截短体与点突变实验确定,eIF3f 的 MitMem 结构域(223-357aa)与 ACSL4 的中央区域(238-474aa)结合,关键位点包括 eIF3f 的 F257/S267 等; 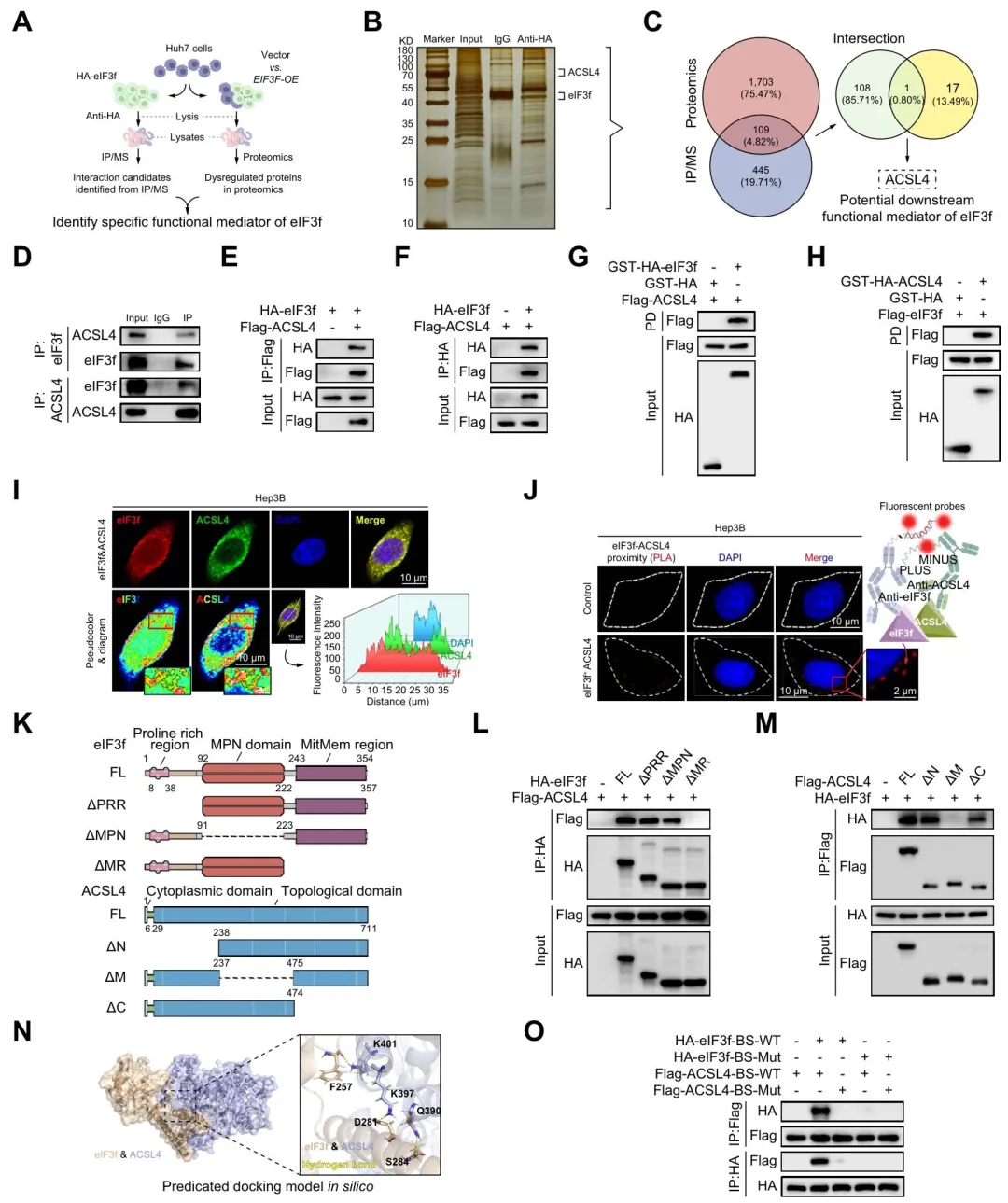
(图4:eIF3f 与 FAB 的关键因子 ACSL4 特异性相互作用)
(3)eIF3f 通过 MPN 结构域介导 ACSL4 K48 位去泛素化,稳定其蛋白水平,关键泛素化位点为 K148 和 K536;NEDD4L 促进 ACSL4 泛素化,可被 eIF3f 逆转。 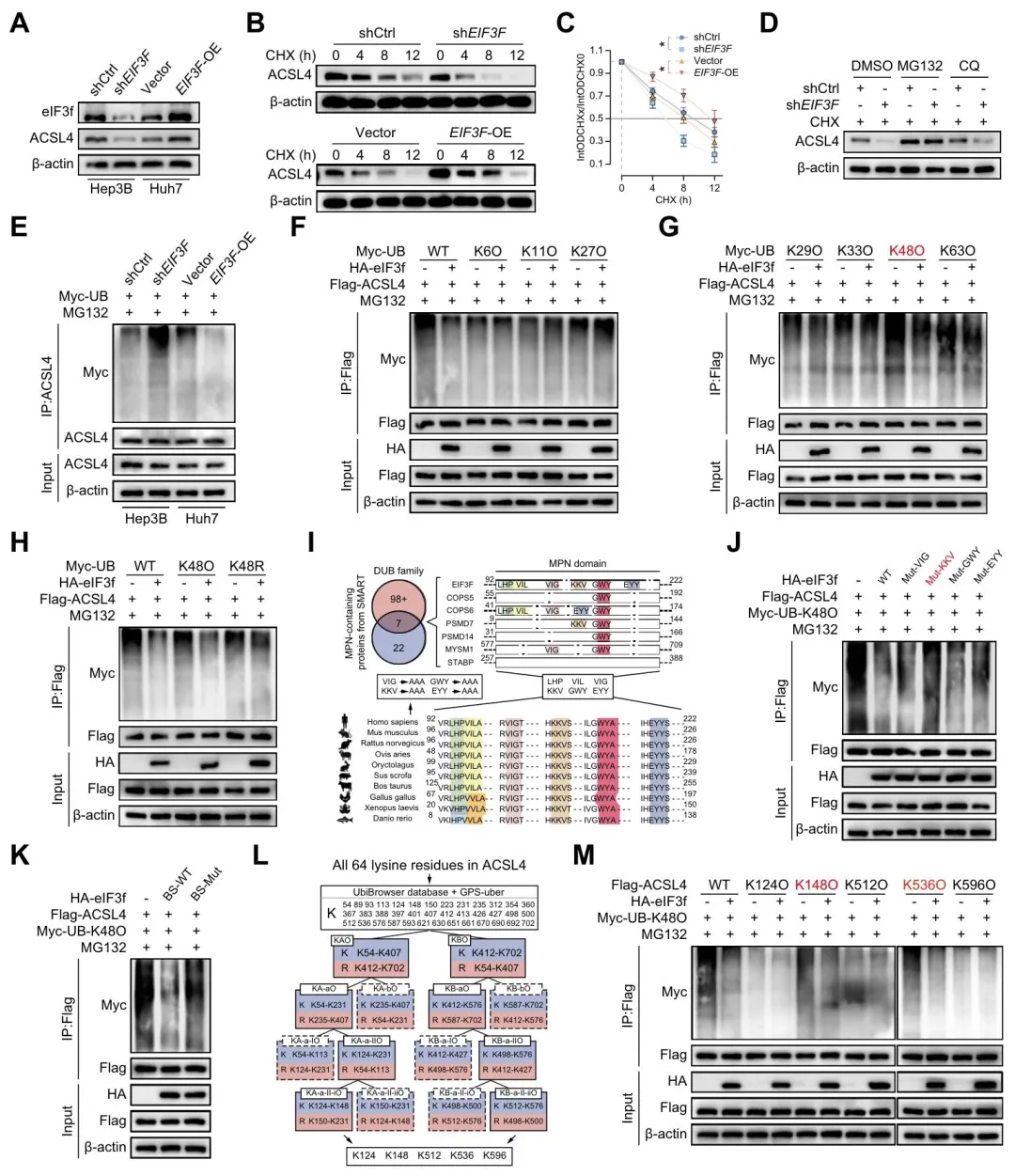
(图5:eIF3f抑制K48连接的泛素介导的ACS蛋白酶体降解)
5. eIF3f 磷酸化修饰的调控作用
(1)磷酸酶处理与 siRNA 筛选显示,SRPK1 介导 eIF3f 磷酸化,增强其与 ACSL4 的相互作用; (2)点突变实验证实 eIF3f Ser266 为关键磷酸化位点,模拟磷酸化突变(S266D)可维持二者结合。 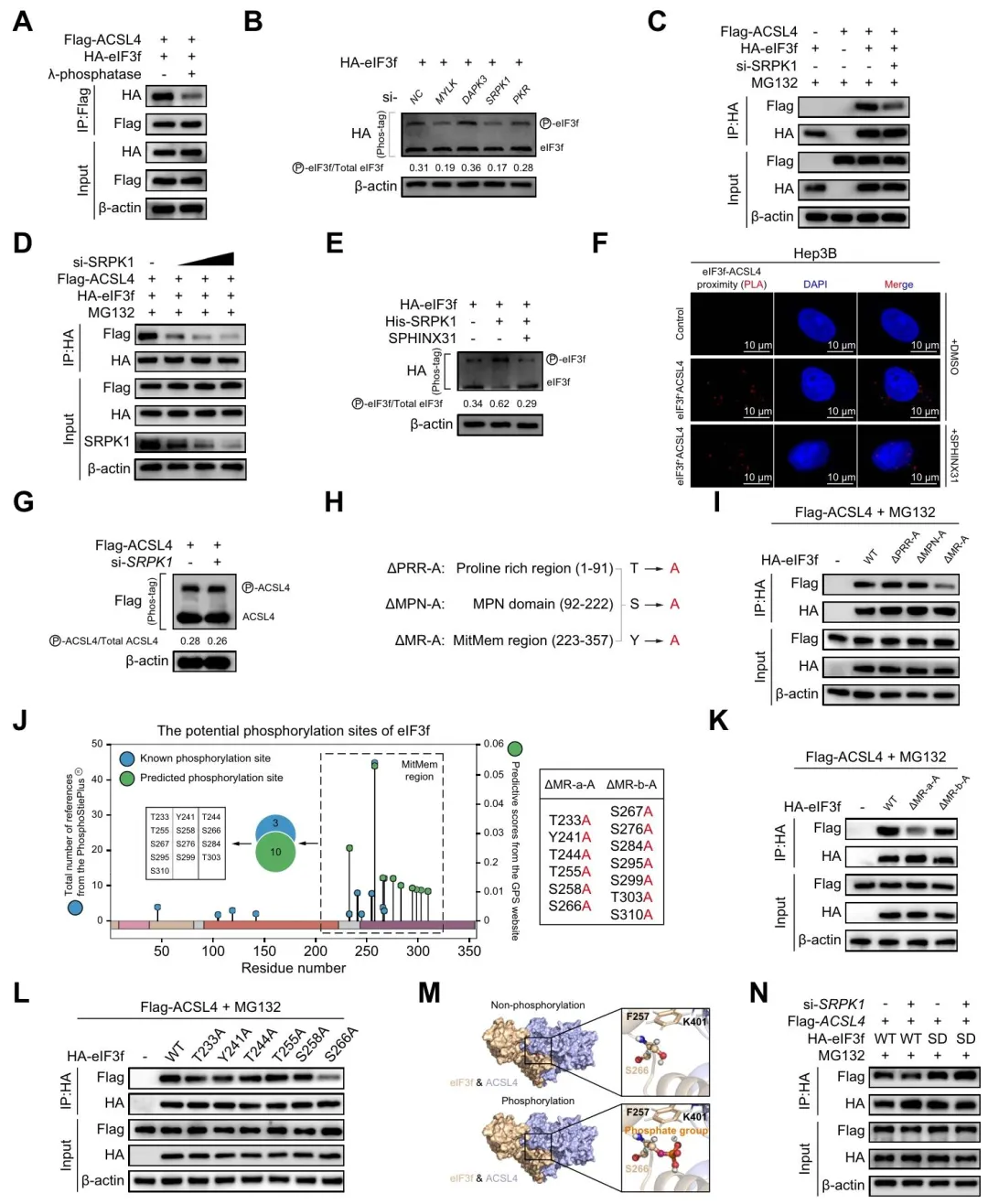
(图6:SRPK1介导的eIF3f中Ser266磷酸化促进其与ACS的相互作用)
6. eIF3f 调控免疫微环境及联合治疗效果
(1)流式与多重免疫组化显示,eIF3f 高表达组 CD8+T 细胞浸润减少,IFN-γ、GZMB 阳性细胞比例降低,临床样本中 eIF3f 与 CD8+T 细胞数量呈负相关; 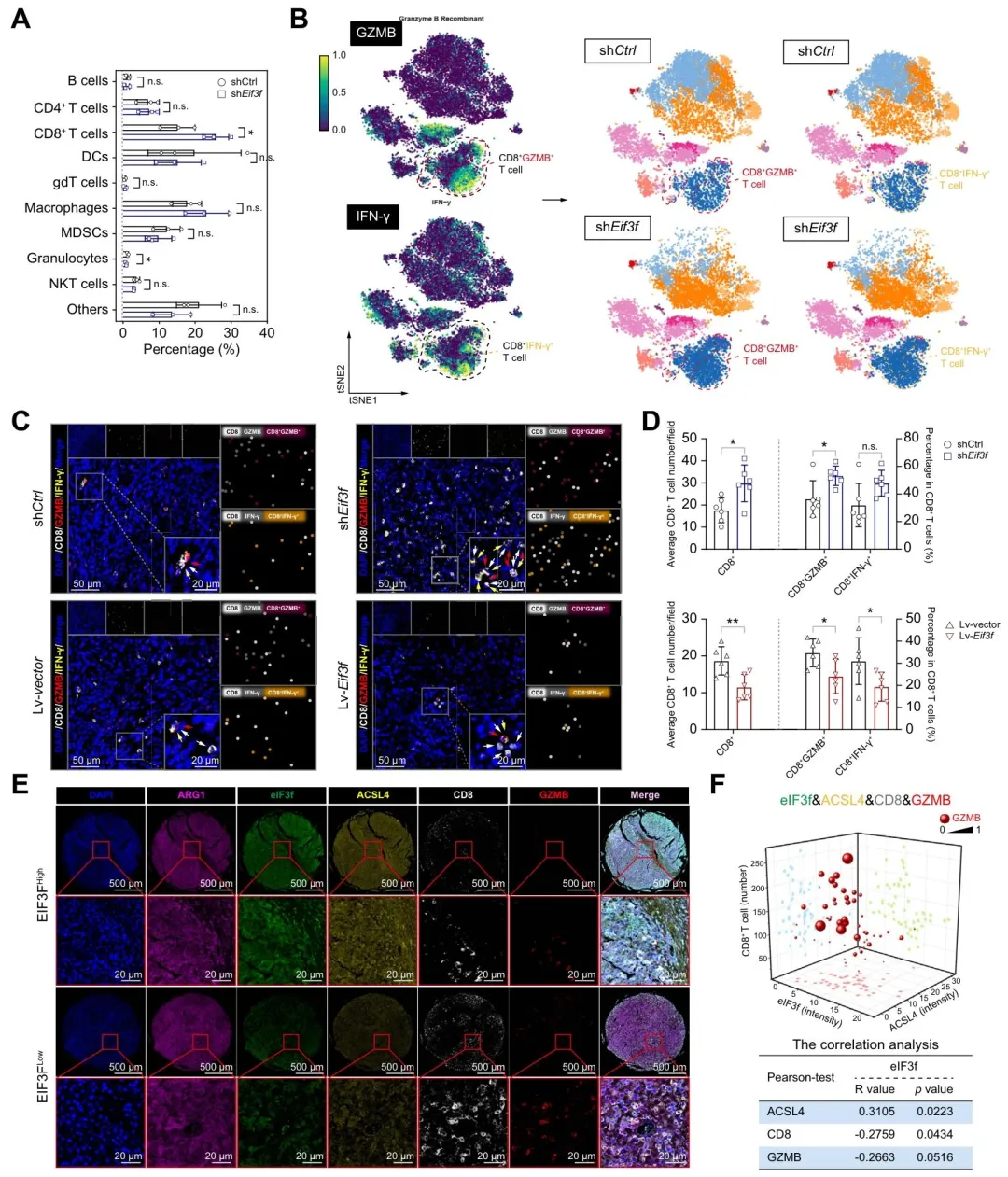
(图7:eIF3f水平升高与肝癌中CD8+T细胞浸润减少相关)
(2)LNP-siEIF3F 体内靶向沉默 eIF3f,可显著增加 CD8+T 细胞浸润,与抗 PD-1 联合使用时,肿瘤体积缩小更显著,小鼠生存期延长。 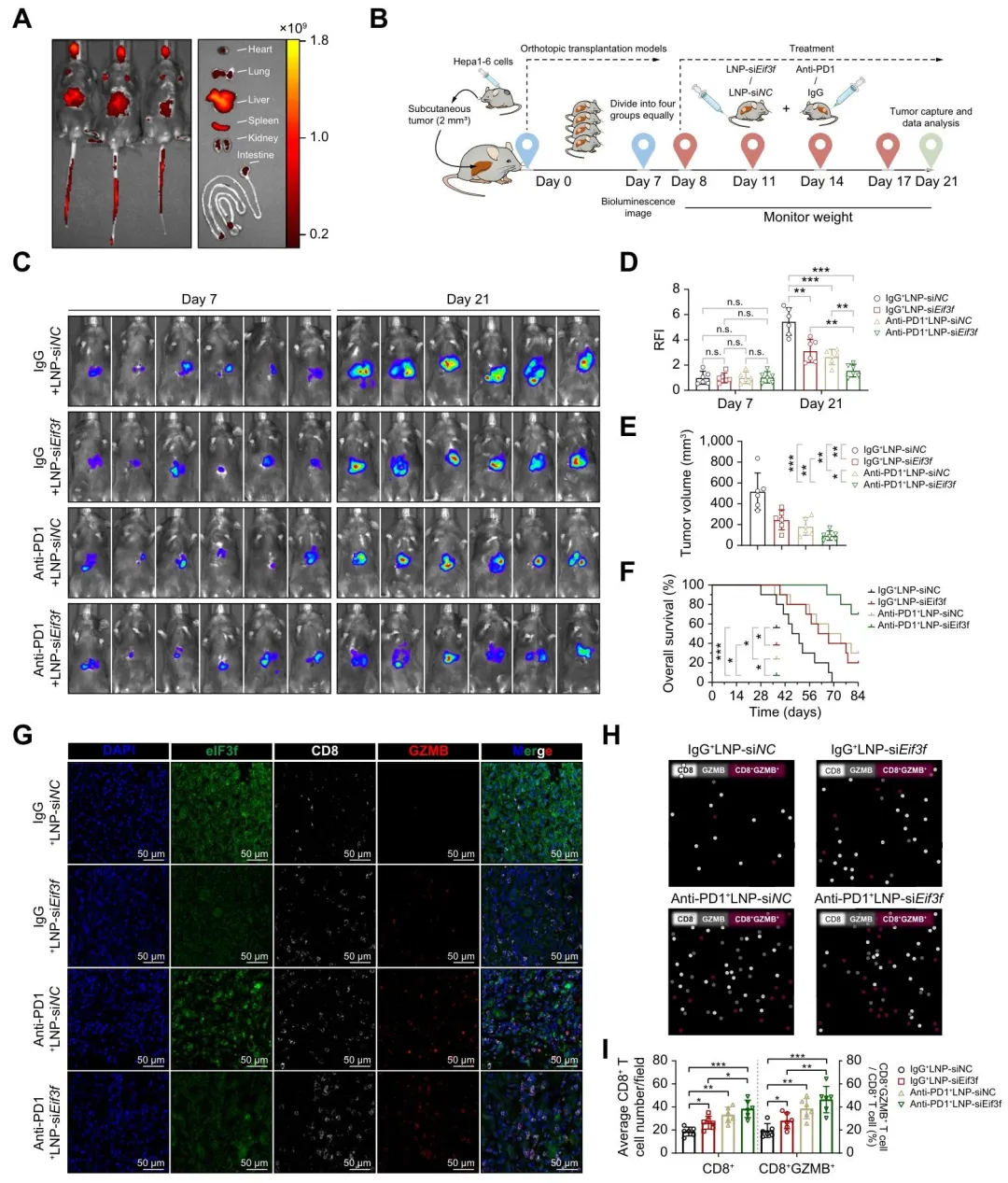
(图8:靶向eIF3f可减轻小鼠的肿瘤负荷并提高抗PD-1的疗效)
研究结果

1. 筛选 FAM 与 HCC 恶性相关核心基因 eIF3f

(图1:将类器官的单细胞RNA测序(scRNA-seq)分析与广泛的数据库分析相结合,以探索同时影响肝细胞癌(HCC)中FAM和恶性程度的基因)
2. eIF3f 促进 HCC 体内外恶性表型

(图2:升高的eIF3f水平在体外和体内均会促进肝癌的恶性程度)
3. eIF3f 调控脂肪酸合成与脂质积累

(图3:IF3f增强HC中的FAB和脂质积累)
4. eIF3f 与 ACSL4 的相互作用及调控机制

(图4:eIF3f 与 FAB 的关键因子 ACSL4 特异性相互作用)

(图5:eIF3f抑制K48连接的泛素介导的ACS蛋白酶体降解)
5. eIF3f 磷酸化修饰的调控作用

(图6:SRPK1介导的eIF3f中Ser266磷酸化促进其与ACS的相互作用)
6. eIF3f 调控免疫微环境及联合治疗效果

(图7:eIF3f水平升高与肝癌中CD8+T细胞浸润减少相关)

(图8:靶向eIF3f可减轻小鼠的肿瘤负荷并提高抗PD-1的疗效)
研究不足与局限性

未来研究改进建议

研究引起的启示

未来方向指引

如何复刻

文章小结

HISTORY
往期推荐

双一区IF15.0TOP!哈佛大学医学院等机构重磅!颠覆传统!生信解码 OI 机制:骨细胞树突缺陷驱动疾病,破骨细胞仅为下游效应!
本文来自网友投稿或网络内容,如有侵犯您的权益请联系我们删除,联系邮箱:wyl860211@qq.com 。
