通过空间代谢组学与转录组学分析,该研究获得一个关键发现:在人类肝细胞癌组织中,调节性T细胞富集的区域呈现独特的代谢特征,表现为谷氨酰胺分解代谢通路高度活跃,而尿素循环活性相对较低,这种代谢失衡导致了局部氨的显著积累。
空间关联分析进一步揭示,Treg的空间分布与高谷氨酰胺分解区域高度重合。重要的是,Treg的富集现象仅在尿素循环活性较低的区域出现,并且在这些区域,Treg的数量(富集程度)与其关键转录因子FOXP3的表达水平呈正相关(详细的空间代谢图谱与共定位分析见图1),首次在组织原位将特定代谢环境与免疫抑制细胞的功能状态联系起来。
Treg对氨诱导凋亡的抗性:细胞水平研究揭示了氨对免疫细胞的选择性调控作用。5mM的氨处理能显著抑制常规CD8⁺和CD4⁺ T细胞的增殖并诱导其凋亡,却不损害甚至能促进调节性T细胞的存活,Treg在高氨环境下的死亡率反而更低。机制上,Treg能通过维持细胞内pH稳定、保护线粒体和溶酶体功能等多种方式抵抗氨的毒性;更重要的是,氨处理后Treg的FOXP3表达水平和免疫抑制功能反而增强。
这一现象在体内小鼠模型中得到了验证:给小鼠喂食高氨饮食,会导致其肿瘤或脾脏中Treg比例显著升高,而CD8⁺/CD4⁺效应T细胞比例下降;使用鸟氨酸等氨清除剂进行处理,则能有效逆转这种免疫失衡(详细的体外选择性杀伤、功能测定及体内干预数据见图2)。
Treg通过尿素循环适应氨环境:为阐明Treg抵抗氨毒性的分子机制,研究发现,在高氨环境中,Treg会特异性上调尿素循环的关键酶——精氨酸琥珀酸裂解酶的表达,从而激活整个尿素循环通路,将有毒的氨转化为无毒的尿素,实现高效的氨解毒。功能验证实验表明,敲低ASL基因会破坏这一解毒过程,导致Treg细胞内氨水平异常积累,并最终引发细胞凋亡显著增加(具体的基因表达、氨水平检测及细胞凋亡数据见图3),证明ASL介导的尿素循环是Treg在肿瘤高氨微环境中存活和发挥功能的关键适应性代谢途径。多胺代谢增强Treg的OXPHOS:该研究揭示了Treg利用氨的另一个关键途径。研究发现,Treg细胞特异性的主调控转录因子FOXP3,能够直接结合并调控下游基因SMS的转录表达。SMS是催化鸟氨酸转化为精胺的关键酶,而鸟氨酸正是尿素循环的中间代谢产物。因此,FOXP3通过驱动SMS表达,将原本用于解毒的尿素循环中间产物,重新定向至精胺合成途径,实现了对氨代谢产物的“废物再利用”(FOXP3与SMS的转录调控关系验证见图4)。研究者利用X射线晶体学等技术,首次确认了精胺分子能够直接结合并激活转录因子PPARγ。这种结合促进了PPARγ下游一系列线粒体电子传递链复合物相关基因的表达,从而显著增强了Treg细胞的氧化磷酸化能力,为其发挥强大的免疫抑制功能提供了充足的能量支持。关键的遗传学实验证明,敲除或突变PPARγ,能显著削弱精胺对Treg线粒体功能和免疫抑制能力的提升作用(精胺-PPARγ互作的结构解析、线粒体功能及PPARγ基因操作验证实验见图5、图6),确立了这条信号轴的功能必需性。
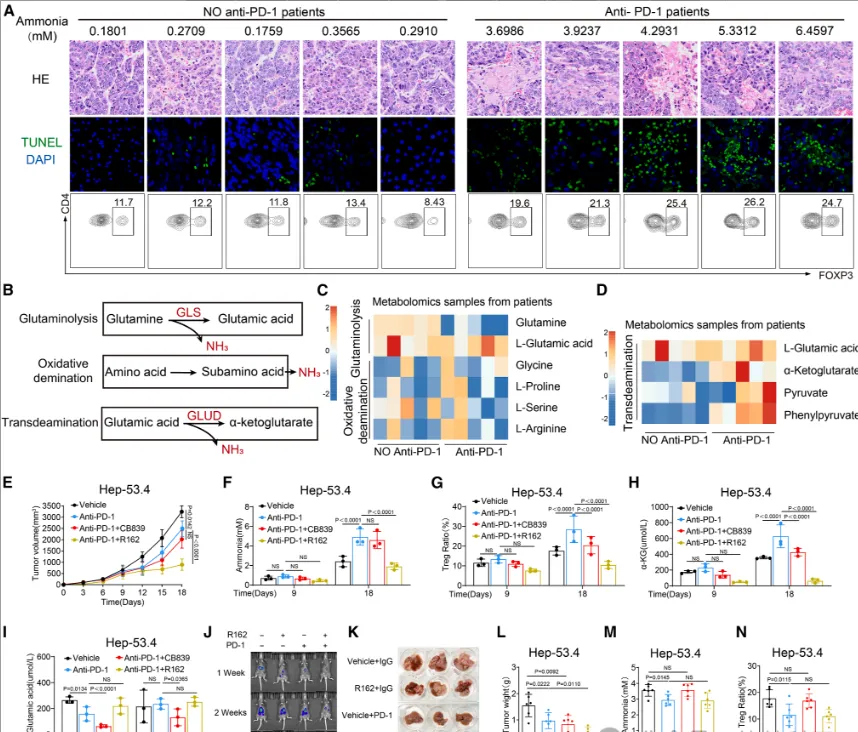
图5. 亚精胺通过 PPARγ 增强调节性T细胞(Treg)OXPHOS 及免疫抑制能力氨促进肿瘤免疫治疗耐药:该研究揭示了免疫治疗自身可能诱发耐药的代谢新机制:抗PD-1治疗会诱导大量肿瘤细胞死亡,这些死亡细胞通过转氨作用释放出大量氨到肿瘤微环境中。释放的氨进一步促进了Treg细胞在肿瘤内的富集与功能增强(机制验证与体内监测数据见图7A-D),形成导致继发性耐药的恶性循环。
基于此机制,研究者提出了克服耐药的新策略:靶向抑制谷氨酰胺分解的关键酶GLUD1。使用GLUD1特异性抑制剂R162,能有效抑制肿瘤细胞的氨产生,降低肿瘤内Treg比例,从而显著增强抗PD-1单药的治疗效果。在小鼠模型中,R162与抗PD-1的联合治疗表现出了强大的协同抗肿瘤活性,能显著抑制肿瘤生长并降低肿瘤局部的氨水平(联合治疗的药效、免疫细胞组成及氨水平数据见图7E-N)。