肿瘤内微生物群近年被证实是影响癌症进展、转移及治疗应答的关键调控因素之一。特定胞内细菌可通过重塑宿主细胞肌动蛋白骨架,降低细胞刚度,使其在血液循环中抵抗剪切力而存活,从而显著增强循环肿瘤细胞的转移潜能。然而,如何高效识别并捕获这些“柔软”且携带细菌的高危循环肿瘤细胞(CTC),仍是液体活检领域的重大技术挑战。
2026年1月8日,南京大学宋玉君教授团队在《Nature Communications》发表研究论文 “A Mechanophenotyping chip for high-throughput detection of metastatic bacteria-infected circulating tumor cells” ,研究团队开发了一种名为LesM的单细胞机械表型筛选微流控芯片,该芯片首次将单细胞机械特性分选与胞内微生物检测相整合,实现了对细菌感染转移性CTC的高效捕获与功能评估,为预测肿瘤远处转移及指导抗生素精准干预提供了革命性的液体活检平台。
一、核心机制:胞内细菌重塑细胞骨架,赋予CTC“柔软”表型
研究团队首先证实,乳腺癌组织来源的特定非致病菌株——松鼠葡萄球菌与动物乳杆菌能够高效侵入MDA-MB-231及MCF-7乳腺癌细胞。细菌入侵通过抑制宿主细胞RhoA-ROCK信号通路,诱导肌动蛋白应力纤维解聚,显著降低细胞杨氏模量,使其表现出增强的可变形性。这一表型变化使被感染细胞能够在流体剪切力下存活,获得更强的血行转移能力。
二、芯片设计:L形陷阱实现力学生物表型分选
LesM芯片的核心结构为L形单细胞捕获陷阱,由“钩形捕获部”与“变形通道部”组成。全芯片集成32条平行通道,共含10,240个L形陷阱,可实现万级单细胞并行捕获与力学分选。
工作原理:
经系统优化,MDA-MB-231细胞的最佳分选条件为:变形通道宽度6 μm、流速5 μL/min、细胞浓度1×10⁶/mL,该条件下感染细胞的挤压效率达41%,显著高于对照组的23.1%。
三、性能验证:高效、特异、适用于全血样本
| |
|---|
| 95.42% |
| 85.34% |
| ROC曲线下面积 0.923(松鼠葡萄球菌)、0.891(动物乳杆菌) |
| 成功从每毫升103个肿瘤细胞中捕获感染CTC,细胞面积及荧光强度均显著高于血细胞 |
LesM无需样本预处理,可直接加载未处理全血,在20分钟内完成从细胞捕获到细菌检测的全流程,展现出优异的临床适用性。
四、体内验证:感染CTC数量与肺转移负荷高度一致
在MDA-MB-231荷瘤小鼠模型中,瘤内注射松鼠葡萄球菌后,外周血感染CTC数量呈时间依赖性递增,并与第30天肺组织转移灶数量显著正相关。LesM检测到的感染CTC荧光强度与肺部细菌定植、组织异常增殖程度高度吻合,证明其可作为血行转移风险的活体预测指标。
五、临床转化潜力:抗生素干预时机评估与患者分层
1. 抗生素干预时机决定疗效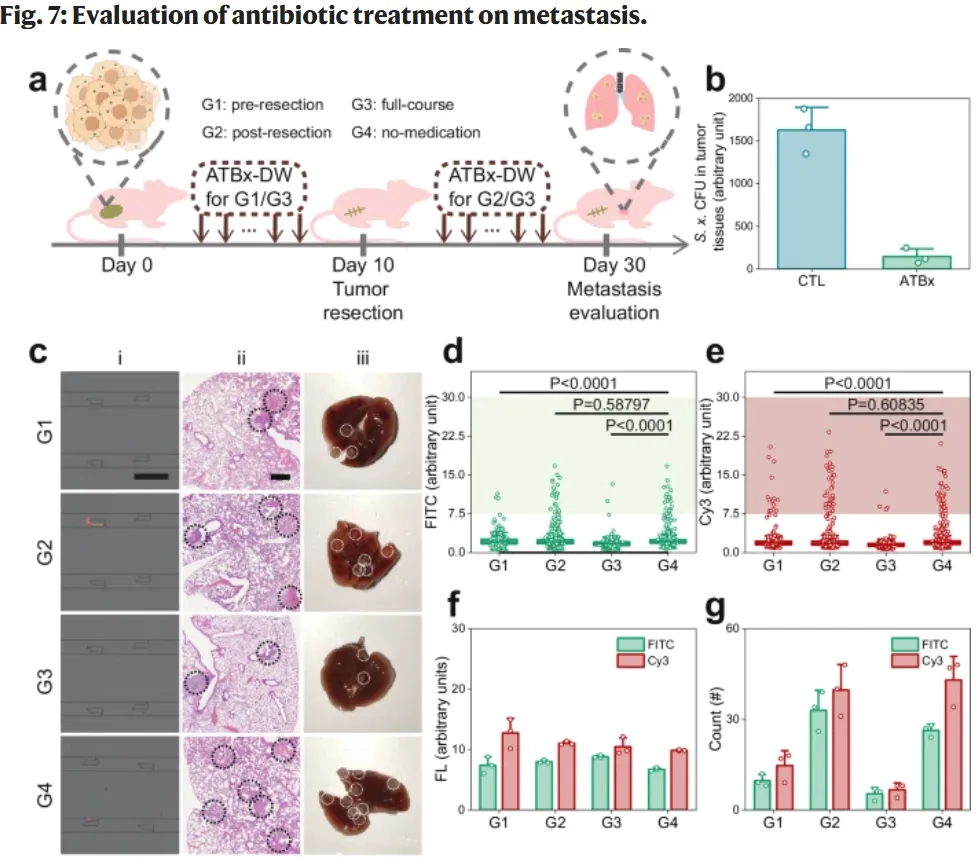 荷瘤小鼠被分为术前、术后、全程、无用药四组。LesM检测显示:
荷瘤小鼠被分为术前、术后、全程、无用药四组。LesM检测显示:
该结果首次在活体层面证明:清除原发灶肿瘤内细菌的关键窗口期在术前,而非术后。
2. 临床样本验证:远处转移预测AUC达0.904
研究纳入69例乳腺癌患者(非转移、淋巴转移、远处转移三组),LesM成功捕获并鉴定出携带胞内细菌的感染CTC。远处转移组患者感染CTC检出率100%,且数量显著高于其他两组。基于感染CTC数量的远处转移预测ROC曲线下面积高达0.904,展现出卓越的临床诊断效能。
六、总结与展望
本研究首次提出“力学生物表型-微生物荷载”双模态CTC分选新范式,主要贡献包括:
机制创新:揭示特定胞内细菌通过RhoA-ROCK通路诱导CTC可变形性增强、转移能力升高的新机制;
技术突破:开发出全球首个整合机械分选+微生物检测的高通量微流控芯片,实现从全血中“无标记捕获-力学筛选-细菌鉴定”一体化;
临床验证:完成从细胞系、动物模型到真实世界患者样本的系统性验证,证实感染CTC可作为乳腺癌远处转移的独立预测标志物,并为抗生素辅助治疗的个体化决策提供全新评估工具。
LesM芯片的问世,标志着肿瘤液体活检从“数量检测”迈向“功能分型”的新阶段。未来,该平台有望拓展至其他实体瘤类型,并进一步整合人工智能图像识别与多组学分析,推动肿瘤精准医学向力学-微生物-分子多维度整合诊断的深度演进。
为助力生物力学研究,笔者也提供可免费试用的细胞刺激系统(拉伸、剪切、压力、电刺激等)和生物力学表征设备(细胞、切片、组织等生物样品以及水凝胶、纤维、微球等材料的力学测试、测试细胞收缩力的牵引力玻片等),并且欢迎致电(或添加)19032235318交流任何生物力学有关的问题!