IF33!南京医科大学一附院王学浩院士“国自然”热点联合拿下双一区TOP刊!
- 2026-05-26 23:14:23


肝细胞癌是全球范围内最常见的肝脏恶性肿瘤,预后通常较差。脂肪酸代谢与HCC的发生发展密切相关,但其精确的分子机制尚不完全清楚。
由南京医科大学第一附属医院王学浩院士团队在《Journal of Hepatology》上发表的题为“eIF3f通过重塑肝细胞癌中的脂肪酸生物合成促进肿瘤恶性进展”的文章,旨在阐明影响HCC脂肪酸代谢的关键分子及其作用机制,以探索新的精准治疗靶点。
文献解读

研究方法
核心分析
模型构建:患者来源HCC类器官模型、细胞系(Hep3B、Huh7等)、多物种动物模型(NCG小鼠、裸鼠、C57BL/6小鼠、斑马鱼)。
组学技术:单细胞RNA测序(scRNA-seq)、空间转录组、代谢组、蛋白质组、免疫沉淀-质谱(IP-MS)。
实验验证
分子生物学实验:免疫共沉淀(Co-IP)、GST pull-down、泛素化实验、免疫荧光、邻近连接分析(PLA)。
功能验证:细胞增殖/迁移/侵袭实验、肿瘤移植模型、脂滴染色、代谢通量分析。
临床验证:患者组织芯片免疫组化、生存分析、脂质纳米颗粒(LNP)递送siRNA体内治疗实验。
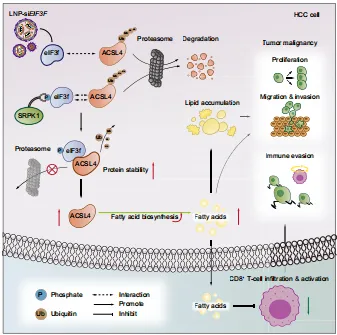
图解摘要

近期前沿热点:虚拟细胞、虚拟敲除🌟
专注于生信分析,包含选题设计方案

文献计量学:方案合理,价格公道👍
主要结果
临床样本中的异常表达
78位ICC患者的组织切片显示,MANF在癌组织中的表达量显著高于癌旁正常组织,就像ICC细胞的“发光标签”,且TNM分期越晚、肿瘤越大,MANF表达越高【图1A-C】。更惊喜的是,ICC患者血清中的MANF水平远高于健康人群,这意味着MANF有望成为一种无创的ICC早期诊断标志物【图1D】。
无论是Sleeping Beauty转座子(SBT)还是硫代乙酰胺(TAA)诱导的ICC小鼠模型,肝脏中MANF的表达都显著升高,伴随ICC标志物CK19和增殖标志物Ki67的同步上调,说明MANF与ICC的发生发展紧密相关【图1H-N】。
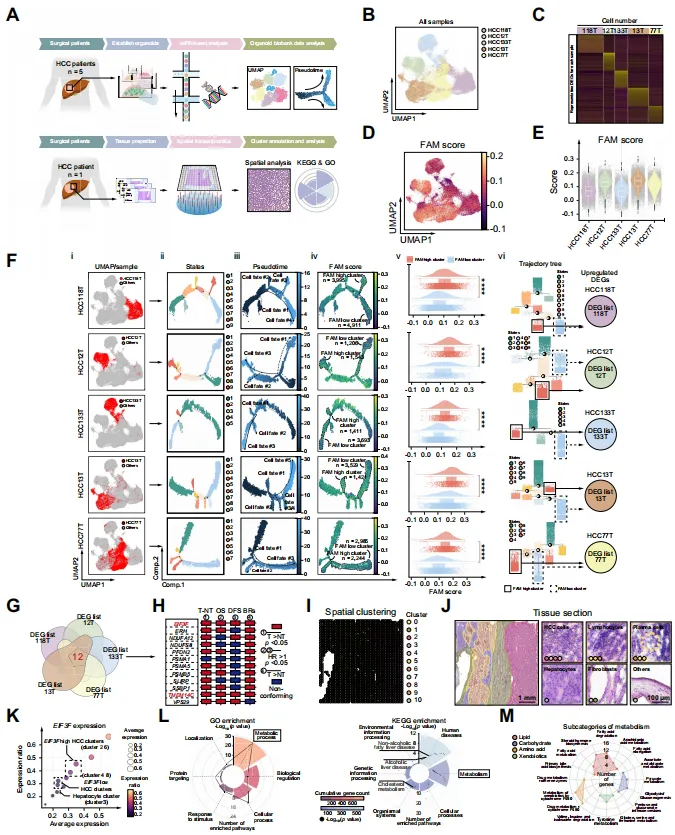
图1.通过将类器官单细胞RNA测序(scRNA-seq)分析与大规模数据库分析相结合,探索同时影响HCC中FAM(脂肪酸代谢)和恶性肿瘤的基因
为验证eIF3f的促癌功能,研究团队在肝癌细胞系和类器官中分别进行敲低和过表达实验:动物实验的结果更具说服力。无论是在免疫缺陷小鼠(NCG鼠、裸鼠)皮下还是原位移植瘤模型中,敲低eIF3f能显著抑制肿瘤生长,而过表达则促进肿瘤生长【图2B-K】。
更重要的是,生存分析显示,敲低eIF3f能延长荷瘤小鼠的生存期,而过表达则缩短生存期。甚至在肺转移模型中,eIF3f也展现出强大的促转移能力【图2L-O】。这些跨越多个物种模型的证据,牢固确立了eIF3f在驱动HCC进展中的核心作用。
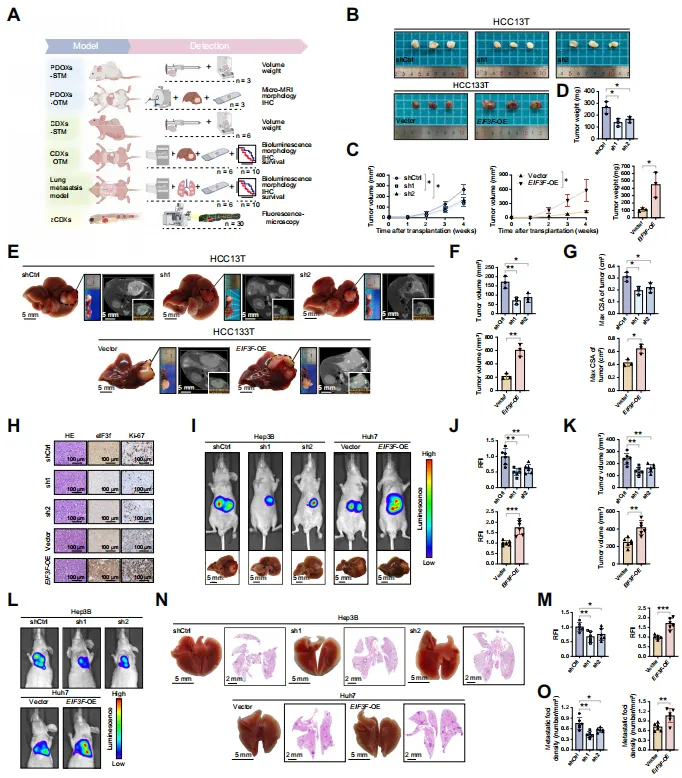
图2.eIF3f水平升高可促进体外和体内HCC恶性转化
eIF3f是如何发挥促癌作用的?研究团队通过整合蛋白质组学和代谢组学分析,找到了突破口。他们发现,过表达eIF3f会导致细胞内脂质和脂样代谢物(特别是脂肪酸)水平显著升高【图3B-C】。通路富集分析明确指出,这些变化最集中体现在“脂肪酸生物合成”通路上【图3D-E】。
进一步的代谢流分析显示,eIF3f过表达的细胞能更高效地将葡萄糖中的碳源整合到新合成的脂肪酸中(如棕榈酸、油酸等)【图3G-H】。细胞内脂肪酸合成增加,最直观的表现就是脂滴堆积。
透射电镜观察清晰地显示,敲低eIF3f后,细胞内的脂滴数量锐减;而过表达eIF3f后,脂滴则大量积聚【图3I-J】。小鼠体内的磁共振成像也证实,eIF3f表达水平与肿瘤内的脂质积累程度正相关【图3K-L】。这些发现将eIF3f与HCC中活跃的脂肪酸生物合成和脂质累积直接挂钩。
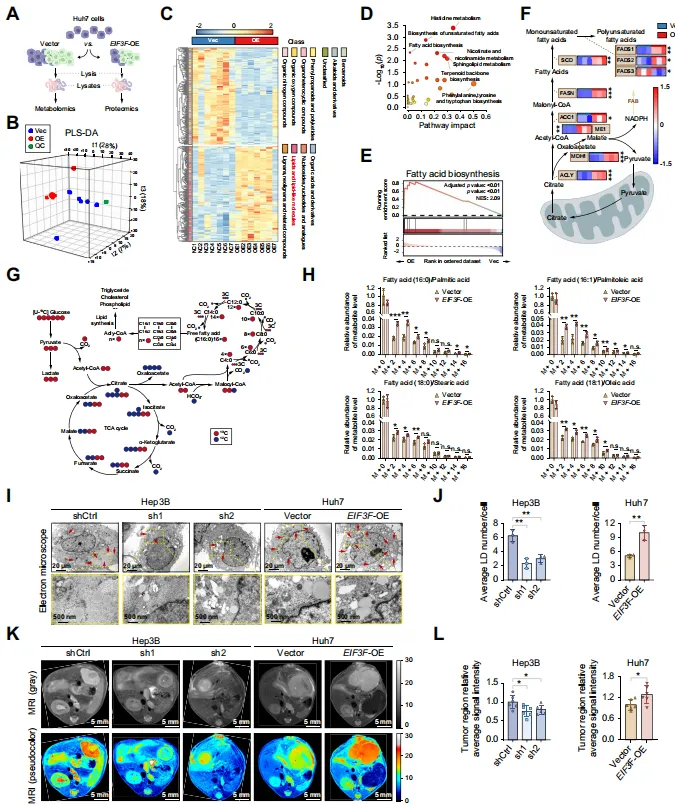
图3.eIF3f增强HCC中FAB及脂质积累
研究深入到分子层面。团队通过免疫沉淀-质谱联用技术,在eIF3f的相互作用蛋白中,筛选出了一个关键靶点——长链脂酰辅酶A合成酶4,即ACSL4【图4B-C】。ACSL4是脂肪酸激活和利用的关键酶,在脂质代谢中扮演重要角色。
实验证实,eIF3f和ACSL4在细胞内存在直接物理相互作用【图4D-J】。他们甚至通过结构模拟和点突变实验,精确定位了两者结合的关键氨基酸位点【图4K-O】。
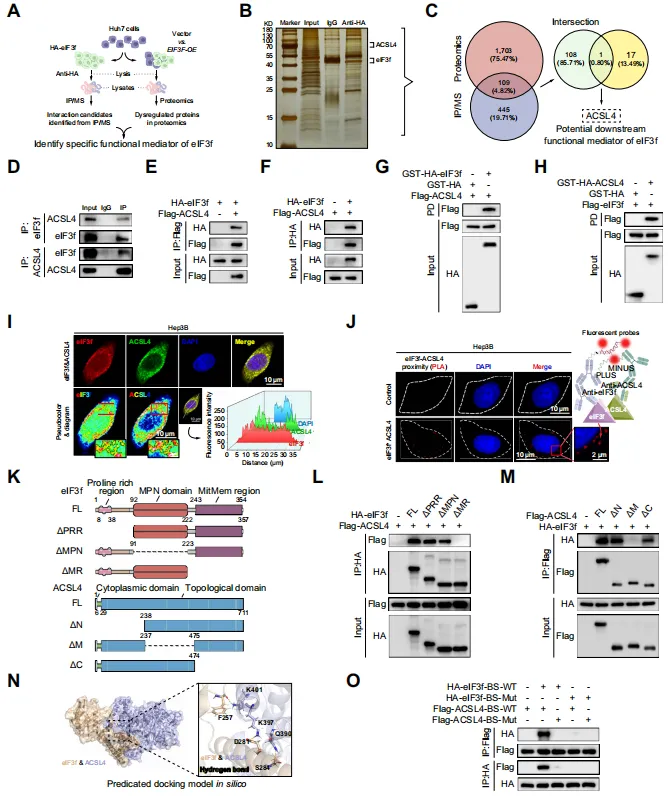
图4.eIF3f特异性与FAB关键因子ACSL4相互作用
最关键的一步来了。团队发现eIF3f作为一个去泛素化酶,能够去除ACSL4蛋白上特定的K48连接型泛素链,从而阻止ACSL4被蛋白酶体降解,稳定了ACSL4蛋白的水平【图5A-H】。
他们进一步鉴定出ACSL4蛋白上的K148和K536是eIF3f去泛素化的关键位点【图5L-M】。简单说,eIF3f就像ACSL4的“稳定器”,通过减少其被标记“销毁”的信号,让更多ACSL4留在细胞里工作。
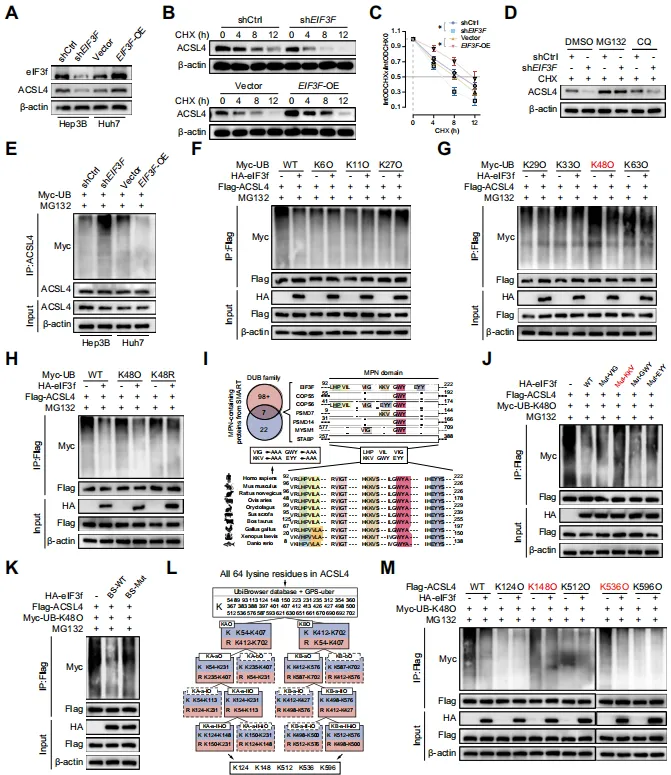
图5.eIF3f抑制K48连接泛素介导的ACSL4蛋白酶体降解
研究团队发现,eIF3f的磷酸化能增强其与ACSL4的相互作用【图6A】。他们筛选出丝氨酸/精氨酸蛋白激酶1是催化这一过程的关键激酶。当SRPK1被抑制时,eIF3f与ACSL4的结合减弱【图6C-F】。
他们最终确定eIF3f蛋白的第266位丝氨酸是该功能的关键磷酸化位点【图6J-N】。这意味着,上游信号可能通过SRPK1磷酸化eIF3f,来“启动”其对ACSL4的稳定和后续的促癌通路。
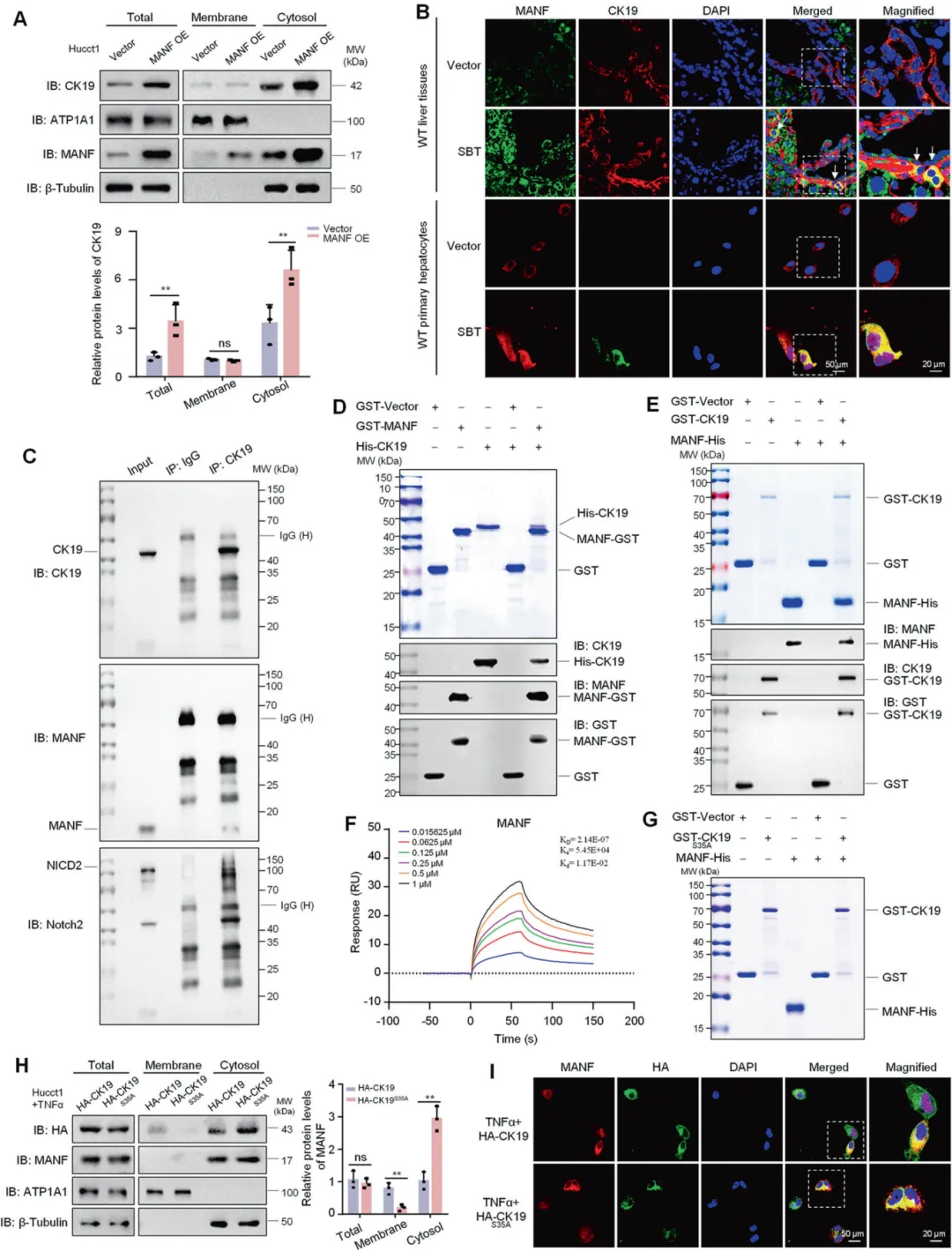
图6.SRPK1介导的eIF3f Ser266磷酸化促进其与ACSL4的相互作用
团队发现,eIF3f敲低不仅能直接抑制肿瘤生长,在免疫健全的小鼠中,其抑瘤效果比在免疫缺陷小鼠中更明显。这提示eIF3f可能影响了肿瘤免疫微环境。
通过高维流式和多重荧光染色,他们发现敲低eIF3f能显著增加肿瘤内CD8+ T细胞的浸润,并增强这些T细胞的活性(产生更多干扰素-γ和颗粒酶B)【图7A-D】。临床样本分析也证实,eIF3f高表达的肿瘤组织中,CD8+T细胞的浸润确实较少【图7E-F】。这表明eIF3f驱动的脂肪酸代谢重编程,创造了一个抑制抗肿瘤免疫的“冷”微环境。
临床样本分析也证实,eIF3f高表达的肿瘤组织中,CD8+T细胞的浸润确实较少【图7E-F】。这表明eIF3f驱动的脂肪酸代谢重编程,创造了一个抑制抗肿瘤免疫的“冷”微环境。
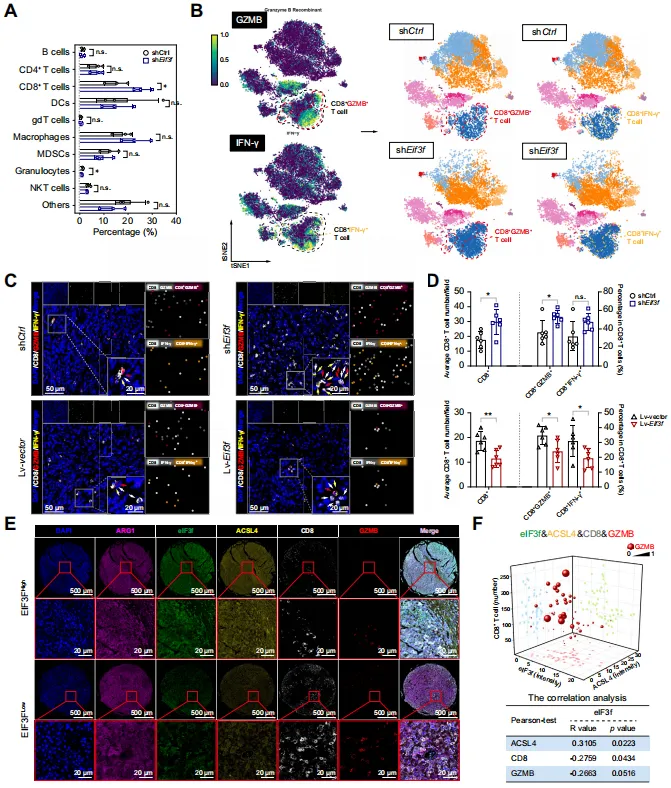
图7.eIF3f水平升高与HCC中CD8+T细胞浸润减少相关
团队提出了一个极具前景的联合治疗策略。他们利用脂质纳米颗粒递送靶向eIF3f的小干扰RNA。
结果显示,单独使用LNP-siEif3f或抗PD-1抗体均有抑瘤效果,而两者联用则产生了显著的协同作用,能更有效地抑制肿瘤生长、延长小鼠生存期,并显著增加肿瘤内活化的CD8+ T细胞【图8C-I】。
这为eIF3f高表达的HCC患者提供了一种潜在的“代谢干预+免疫治疗”组合拳新思路。
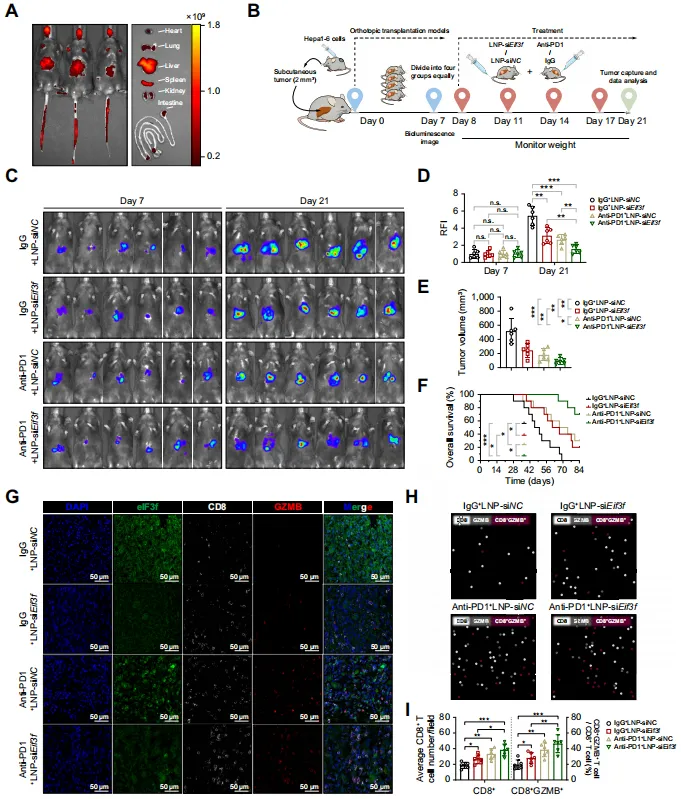
图8.靶向eIF3f可减轻肿瘤负荷并提高抗PD-1疗法在小鼠中的疗效
文章小结
研究系统揭示了eIF3f通过“去泛素化稳定ACSL4→增强脂肪酸合成→抑制CD8+ T细胞浸润”的轴,驱动肝癌恶性进展的完整分子机制。不仅为肝癌代谢重编程的调控网络提供了新视角,更证实eIF3f是极具潜力的肝癌预后标志物和治疗靶点,为肝癌精准治疗尤其是联合免疫治疗提供了全新策略。
如果你也想用“国自然热点+多组学”进行研究,需要生信分析,复现高分思路,那就快来后台联系吧~精彩生信,助力每一个科研梦想!





