科研 | 南京财大:苦瓜多糖通过IRS1/PI3K/Akt-AMPK通路及调节肠道菌群和代谢缓解2型糖尿病(国人佳作)
- 2026-04-29 19:18:07
 点击蓝字“代谢组metabolome”,轻松关注不迷路
点击蓝字“代谢组metabolome”,轻松关注不迷路

生科云网址:https://www.bioincloud.tech/
编译:微科盟草重木雪,编辑:微科盟X、江舜尧。
微科盟原创微文,欢迎转发转载。
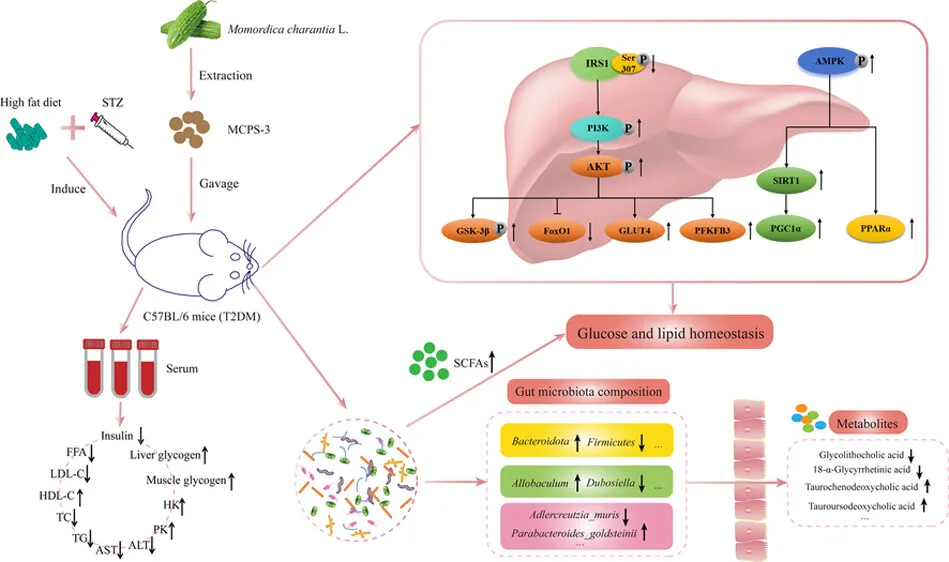
开发有效的2型糖尿病(T2DM)治疗方法仍然是全球卫生领域的一个关键优先事项。本研究探讨了苦瓜多糖MCPS-3在高脂饮食和链脲佐菌素诱导的2型糖尿病小鼠模型中的抗糖尿病潜力及其潜在机制。结果表明,MCPS-3显著降低了血清葡萄糖水平,改善了葡萄糖耐量,增强了胰岛素敏感性,同时增加了糖原储存,提高了肝酶活性。它还减轻了糖尿病引起的胰腺、肝脏和肾脏的损伤,并通过降低甘油三酯和低密度脂蛋白(LDL-C)同时提高高密度脂蛋白(HDL-C)水平来改善血脂状况。机制研究表明,MCPS-3激活了IRS1/PI3K/AKT和AMPK通路,这对葡萄糖和脂质调节至关重要。重要的是,MCPS-3通过增加微生物多样性和改变有害和有益菌的组成来恢复肠道微生物平衡。代谢组学分析进一步确定了46种代谢物的变化,暗示了与类固醇和脂质代谢相关的途径。这些发现强调了MCPS-3抗糖尿病作用的多面性,包括其作为肠道微生物群和代谢途径调节剂的作用,并支持其改善2型糖尿病代谢健康的潜力。
论文ID
实验设计
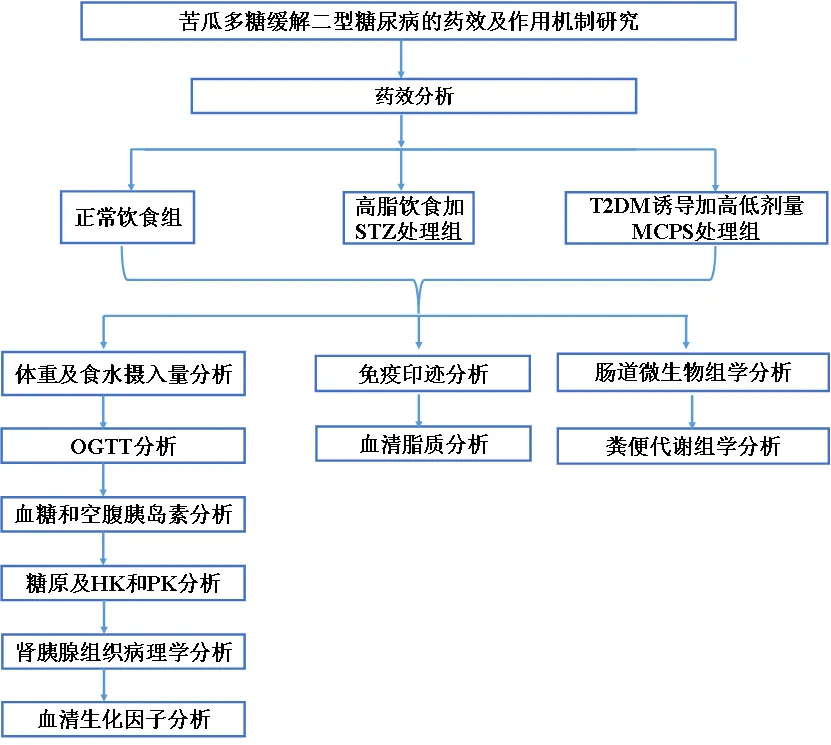
实验结果
1. MCPS-3对糖尿病小鼠体重、饮水和摄食量的影响
如图1B所示,在成功诱导糖尿病后,T2DM组的小鼠体重明显减轻,与糖尿病小鼠的症状一致。相比之下,正常对照(NC)组的小鼠体重逐渐增加。口服MCPS-3 5周后,体重下降在前3周放缓,在第4周和第5周开始增加。5周后,MCPS-3-H和MCPS-3-L组小鼠的体重显著高于T2DM组(P<0.05),但仍低于NC组水平,表明糖尿病状况有所改善。与此同时,2型糖尿病组的食物摄入量在5周后显著增加,这是糖尿病多食症的特征。与T2DM组相比,MCPS-3-L和MCPS-3-H组的小鼠食物摄入量减少(图1C)。“多发性糖尿病”是糖尿病的特征。血糖升高会引起渗透性利尿,增加尿量和脱水,从而刺激口渴。5周后,T2DM组的小鼠饮水量明显多于NC组(P<0.05),证实模型建立成功(图1D)。MCPS-3干预导致耗水量逐渐减少(P<0.05),与食物摄入量的变化平行,表明MCPS-3可以改善糖尿病小鼠的多饮。
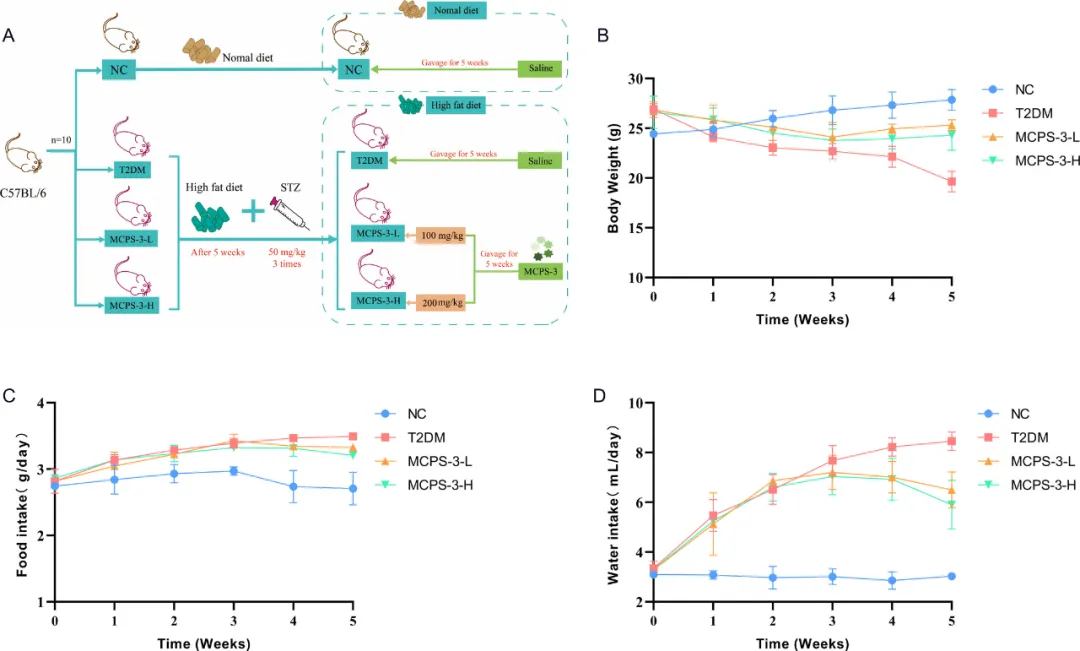
图1 MCPS-3对2型糖尿病小鼠体重、食物摄入量和饮水量的影响。(A)实验设计示意图。(B)体重曲线。(C)食物摄入。(D)摄水量。数据以平均值±标准差(SD)表示。
2. MCPS-3降低糖尿病小鼠的高血糖和胰岛素抵抗
OGTT结果表明,所有小鼠在葡萄糖给药后的葡萄糖水平趋势相似(图2A)。与NC小鼠相比,T2DM小鼠在所有时间点都表现出更高的葡萄糖水平,反映出葡萄糖耐量受损。然而,与T2DM组相比,MCPS-3组的小鼠血糖水平较低,下降速度加快,表明葡萄糖耐量增强。这些发现得到了曲线下面积(AUC)分析的支持,MCPS-3-L和MCPS-3-H组的AUC明显低于T2DM组(图2B,P<0.01)。如图2C所示,NC组小鼠的血糖水平保持在4至5 mmol/L之间。相比之下,T2DM组小鼠的葡萄糖水平显著升高,证实了模型的成功和稳定建立。MCPS-3给药5周后,MCPS-3-L和MCPS-3-H组的小鼠血糖水平显著下降,表明血糖控制有所改善。此外,MCPS-3治疗显著降低了血清胰岛素水平,尤其是MCPS-3-H组(图2D,P<0.05)。这些结果表明,MCPS-3增强了胰岛素敏感性和葡萄糖代谢,从而降低了T2DM小鼠的高血糖症。
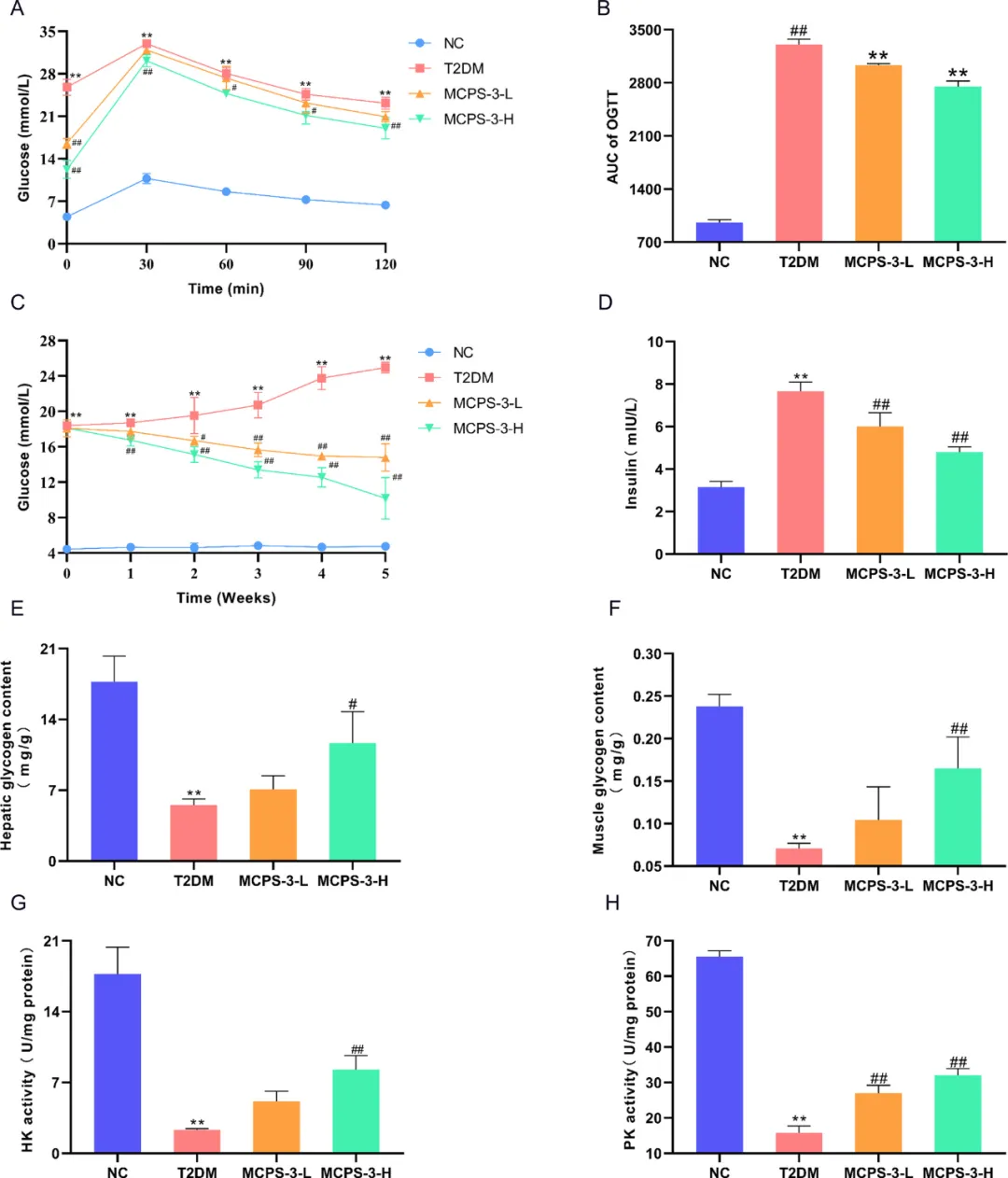
图2 MCPS-3有效改善了T2DM小鼠的葡萄糖代谢紊乱。(A)OGTT。(B)OGTT的AUC。(C)血清葡萄糖水平。(D)空腹血清胰岛素水平。(E)肝糖原含量。(F)肌肉糖原含量。(G)HK活性。(H)PK活性。数据以平均值±标准差(SD)表示。与NC组相比,**P<0.01;与T2DM组相比,##P<0.01。
3. MCPS-3增强糖尿病小鼠的糖酵解和糖原合成
肝脏是胰岛素作用的关键靶点,胰岛素在促进糖原合成的同时抑制糖原分解和糖异生。在2型糖尿病中,胰岛素作用受损导致血糖升高,由于葡萄糖摄取无效导致糖原储存减少,与对照组相比,2型糖尿病小鼠的肝脏和肌肉糖原水平显著降低(图2E,F,P<0.01)。经过5周的MCPS-3处理后,干预组的糖原含量增加,MCPS-3-H组的肝糖原(P<0.05)和肌肉糖原(P<0.01)有显著改善。这表明MCPS-3增强了糖原合成,有助于维持葡萄糖代谢平衡。此外,增加肝脏中关键糖酵解酶如HK和PK的活性可以改善葡萄糖利用和胰岛素抵抗。如图2G、H所示,T2DM小鼠的HK和PK活性降低,反映出葡萄糖代谢受损。MCPS-3显著增强了HK和PK活性,特别是在MCPS-3-H组中(P<0.01),表明MCPS-3减轻了T2DM小鼠的代谢损伤,改善了葡萄糖代谢。
4. MCPS-3改善糖尿病小鼠的病理形态学
在2型糖尿病中,胰腺及其产生胰岛素的β细胞面临需求增加,导致功能和形态变化。本研究通过胰腺指数评估了胰腺健康状况,与对照组相比,T2DM小鼠的胰腺指数显著降低,表明胰岛萎缩(图3A)。五周的MCPS-3治疗显著改善了胰腺指数(P<0.05),在较高剂量下效果更明显(图3B)。组织学分析证实,MCPS-3减轻了胰岛萎缩,改善了细胞形态,特别是在MCPS-3-H组中,证明了其对β细胞的保护作用。糖尿病肾病(DN)是糖尿病的常见并发症,可导致肾功能衰竭。在2型糖尿病小鼠中,肾脏出现空泡、细胞分布不均、边界模糊、核聚集、细胞质减少和肾小球炎症(图2C)。MCPS-3治疗减少了空泡,澄清了细胞边界,减轻了炎症,随着浓度的增加,改善程度也在增加。一致地,T2DM小鼠的肾脏指数显著升高(P<0.01),在MCPS-3治疗5周后显著降低(图2D)。此外,在组织学上观察到肝脏指数降低(P<0.01)和脂质空泡化,增强了MCPS-3的保肝作用(图3E,F)。此外,T2DM小鼠血清丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)水平升高表明肝损伤(图3G,H)。MCPS-3显著降低了这些水平,表明减轻了肝损伤。总体而言,MCPS-3对T2DM小鼠的胰腺、肾脏和肝脏损伤显示出显著的保护作用,表现出剂量依赖性疗效。
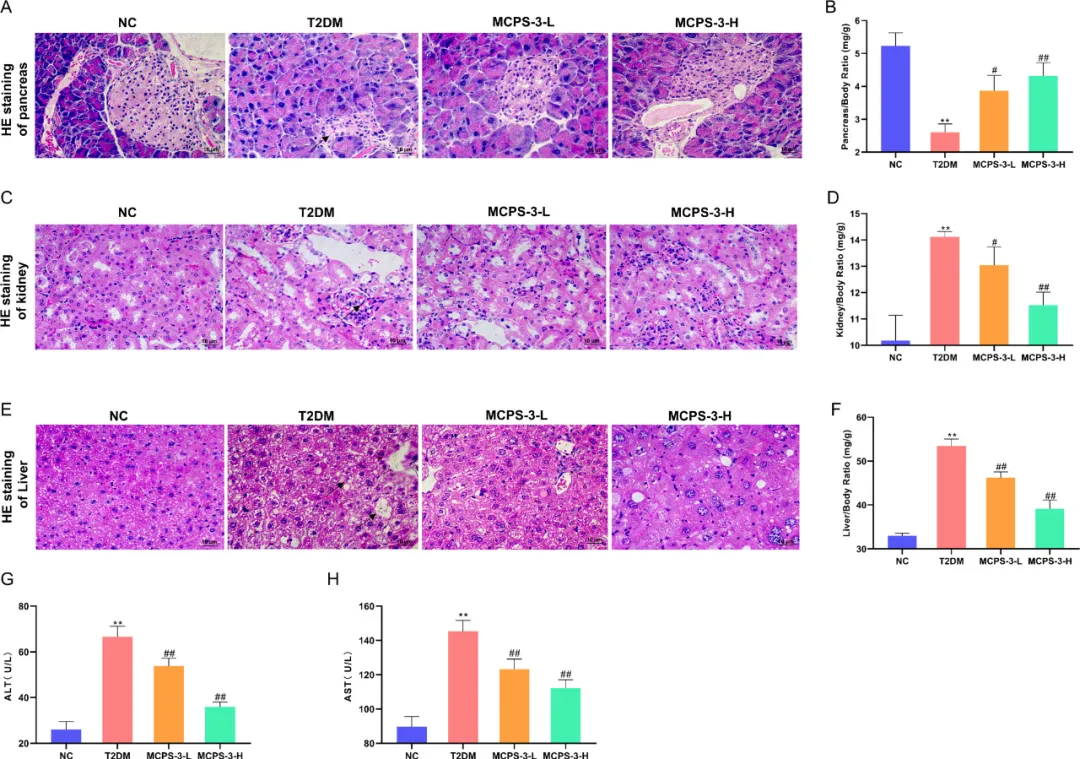
图3 MCPS-3改善了T2DM小鼠的病理形态学。(A)胰腺H&E染色(放大400倍)。(B)胰腺指数。(C)肾H&E染色(放大400倍)。(D)肾脏指数。(E)肝脏H&E染色(放大400倍)。(F)肝脏指数。(G)血清ALT水平。(H)血清AST水平。数据以平均值±标准差(SD)表示。与NC组相比,**P<0.01。与T2DM组相比,##P<0.01。
5. MCPS-3通过调节IRS1/PI3K/AKT信号通路增强糖尿病小鼠的胰岛素信号传导和葡萄糖代谢
IRS1/PI3K/AKT通路对肝细胞中的胰岛素信号传导至关重要,调节葡萄糖和脂质代谢。在胰岛素结合后,IRS1在特定的丝氨酸和酪氨酸残基上发生磷酸化,这决定了它与PI3K的相互作用和随后的AKT激活。在T2DM小鼠中,p-IRS1/IRS1比值升高,p-PI3K/PI3K和p-AKT/AKT比值降低,表明胰岛素信号传导受损,胰岛素抵抗增加(图4A-D)。MCPS-3给药5周后,MCPS-3-H组p-IRS1/IRS1比值显著降低,p-PI3K/PI3K和p-AKT/AKT比值升高。这些发现表明,MCPS-3通过减少IRS1的抑制性磷酸化和促进PI3K和AKT活化来增强胰岛素信号传导,从而缓解胰岛素抵抗并改善葡萄糖代谢。
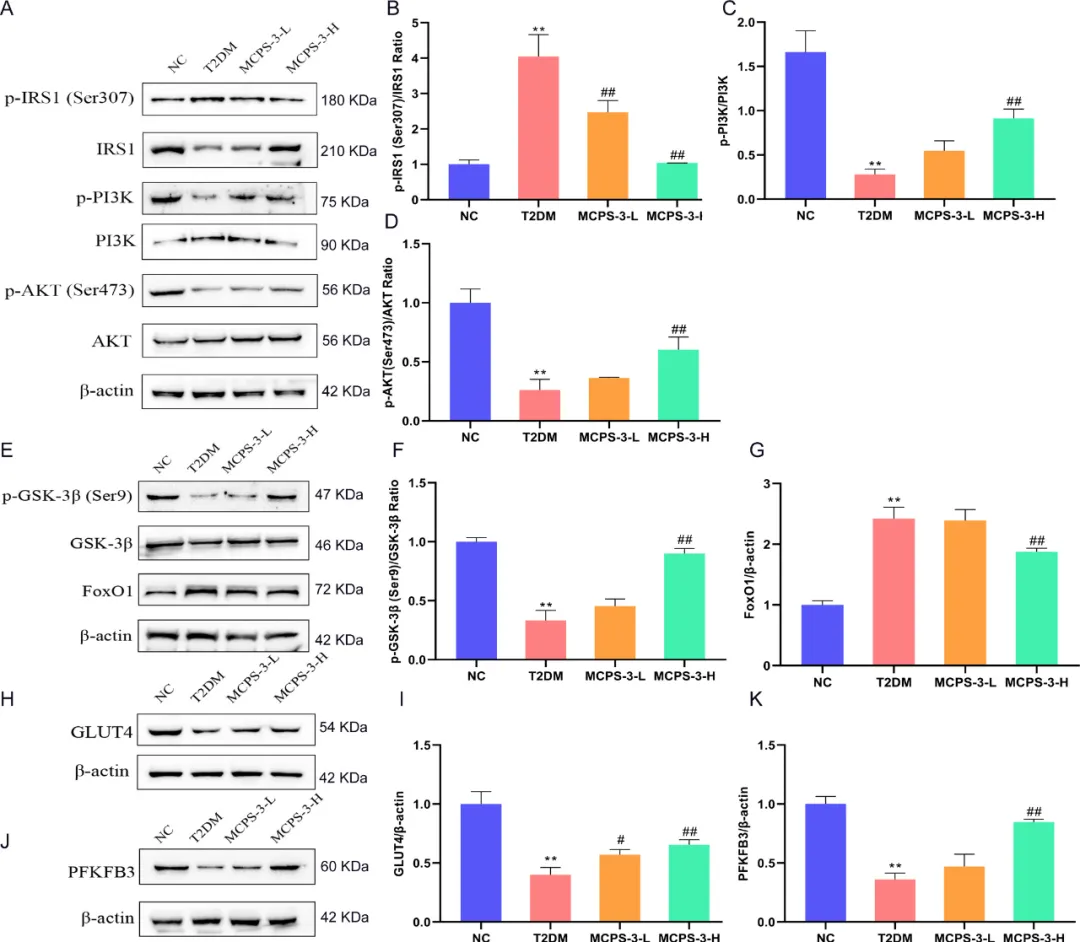
图4 MCPS-3通过IRS1/PI3K/AKT途径增强T2DM小鼠的胰岛素信号传导和葡萄糖代谢。(A)通过蛋白质印迹分析检测p-IRS1/IRS1、p-PI3K/PI3K和p-AKT/AKT的蛋白质表达率。p-IRS1/IRS1(B)、p-PI3K/PI3K(C)和p-AKT/AKT(D)的定量。(E)免疫印迹分析检测p-GSK-3β/GSK-3β的相对蛋白表达率和FoxO1的表达水平。p-GSK-3β/GSK-3β(F)和FOXO1(G)的定量。(H)免疫印迹分析检测GLUT4的相对蛋白表达水平。(I)GLUT4的定量。(J)免疫印迹分析检测PFKFB3的相对蛋白表达水平。(K)PFKFB3的定量。
对IRS1/PI3K/AKT通路下游靶点的进一步研究,如GLUT4、GSK-3β、FoxO1和PFKFB3,揭示了它们在葡萄糖转运和代谢中的关键作用。对糖原合成至关重要的GSK-3β在MCPS-3处理后表现出磷酸化增加,表明糖原储存增强(图4E,F)。FoxO1是糖异生的调节因子,在MCPS-3给药后表达降低,表明糖异生减少,血糖水平降低(图4E,G)。此外,脂肪细胞和肌细胞中的主要葡萄糖转运蛋白GLUT4在T2DM小鼠中的表达显著降低,这是胰岛素抵抗的标志。MCPS-3显著提高了GLUT4水平,增强了葡萄糖转运和代谢效率(图4H,I)。此外,糖酵解和糖异生中的关键酶PFKFB3在MCPS-3处理后其表达显著增强(图4J,K),表明代谢平衡得到改善。
这些结果表明,MCPS-3有效地调节PI3K/AKT信号通路及其下游靶点,抑制糖异生,促进糖原合成,改善整体葡萄糖代谢。本研究强调了MCPS-3在管理与2型糖尿病相关的葡萄糖代谢紊乱方面的治疗潜力,为其作用机制提供了有价值的见解。
6. MCPS-3改善糖尿病小鼠的脂质状况并激活AMPK信号通路
2型糖尿病引起的高血糖通常会导致血脂异常。我们在T2DM小鼠中观察到TG、TC和LDL-C水平升高(图5A-C),表明血脂异常。然而,经过5周的MCPS-3处理后,这些脂质参数明显降低,表明脂质状况有所改善。此外,由于肝损伤,2型糖尿病小鼠的HDL-C水平最初降低,但在MCPS-3给药后升高(图5D)。游离脂肪酸(FFA)的减少,在MCPS-3-H组中尤为明显,进一步表明脂质代谢增强,脂肪积累减少(图5E)。
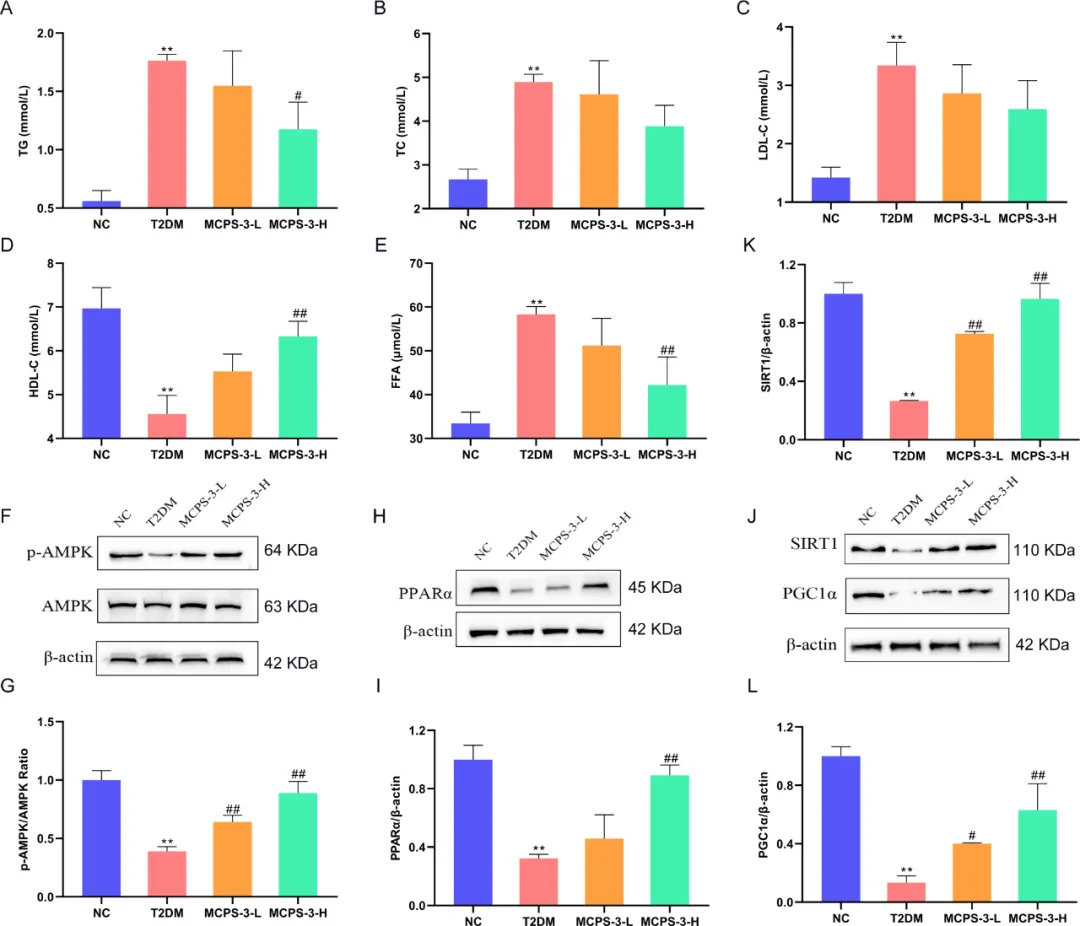
图5 MCPS-3改善了T2DM小鼠的脂质状况并激活了AMPK通路。血清TG(A)、TC(B)、LDL-C(C)、HDL-C(D)和FFA(E)水平。(F)免疫印迹分析检测p-AMPK/AMPK的蛋白表达率。(G)p-AMPK/AMPK的定量。(H)免疫印迹分析检测PPARα的蛋白表达。(I)PPARα的定量。(J)免疫印迹检测SIRT1和PGC1α的蛋白表达。(K)SIRT1的量化。(L)PGC1α的定量。数据以平均值±标准差(SD)表示。与NC组相比,**P<0.01;与T2DM组相比,##P<0.01。
在分子水平上,MCPS-3激活了AMPK信号通路(图5F,G),导致PPARα上调(图5H,I),PPARα是脂肪酸氧化和葡萄糖代谢的关键调节因子。SIRT1和PGC-1α是AMPK信号通路中的关键下游分子,其中SIRT1受AMPK调节,对细胞能量状态敏感,使其能够激活或增强PGC-1α的表达。最近的研究表明,这些蛋白质在脂质和葡萄糖代谢中起着关键作用。因此,饮食MCPS-3激活小鼠肝组织中的AMPK信号通路,导致SIRT1和PGC-1α上调,从而调节葡萄糖和脂质代谢(图5J-L)。
7. MCPS-3调节糖尿病小鼠肠道微生物群组成和多样性
该研究探讨了MCPS-3对2型糖尿病小鼠肠道微生物群的影响,揭示了微生物多样性和组成的显著变化。最初,与正常对照组相比,2型糖尿病小鼠的Shannon指数(衡量微生物多样性的指标)显著降低(P<0.05),表明多样性降低(图6A)。MCPS-3处理五周后,Shannon指数略有改善,但没有统计学意义,表明微生物多样性略有提高。然而,Simpson指数在各组之间没有显著差异,表明MCPS-3对整体多样性的影响有限,但可能是积极的(图6B)。
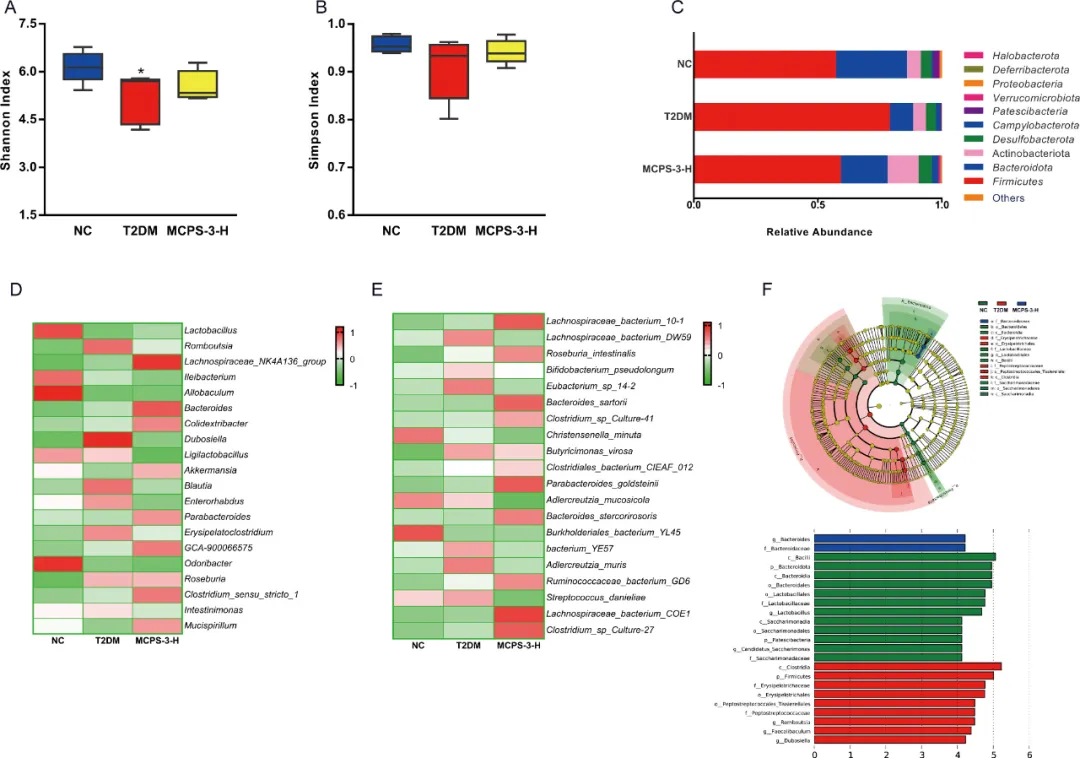
图6 MCPS-3调节T2DM小鼠的肠道微生物群组成和多样性。(A)Shannon指数。(B)Simposn指数。门水平(C)、属水平(D)和种水平(E)肠道微生物群落的相对丰度。(F)肠道微生物群关键属的线性判别分析效应大小(LEfSe)分析。与NC组相比,**P<0.01。
在门水平上,NC、T2DM和MCPS-3-H组的肠道微生物群以厚壁菌门、拟杆菌门、放线菌门和脱硫菌门为主,其中厚壁菌和拟杆菌门最为常见(图6C)。在2型糖尿病小鼠中,由于厚壁菌门升高和拟杆菌门减少,厚壁菌/拟杆菌门(F/B)比值显著增加,这与能量吸收增强有关。MCPS-3通过减少厚壁菌门和增加拟杆菌门丰度扭转了这一趋势,表明微生物平衡得到改善,在调节脂质代谢方面具有潜在作用。在属水平上,2型糖尿病小鼠表现出Allobaculum、Odoribacter和乳杆菌属等有益属的水平降低,而Dubosiella、Romboutsia和Blautia等有害属的水平升高(图6D)。MCPS-3干预后,Dubosiella、Blautia和Romboutsia的丰度显著降低,Lachnospiraceae_NK4A136_group、拟杆菌属和Clostridium_sensus_stricto_1等有益属的数量增加。Romboutsia的减少(通常与葡萄糖代谢受损有关)和短链脂肪酸(SCFA)产生菌Lachnospiraceae_NK4A136_group的富集突显了MCPS-3通过调节肠道微生物群落来改善葡萄糖和脂质代谢的潜力。MCPS-3减少有害细菌和富集有益菌的能力突显了其潜在的治疗作用。此外,物种水平分析显示,与2型糖尿病小鼠相比,MCPS-3-H组中有害菌如Adlercreutzia_muris减少,有益物种如Parabacteroides_goldsteinii和Bacteroides_sartorii增加(图6E)。特别是Parabacteroides_goldsteinii与抗炎和葡萄糖调节特性有关,表明微生物功能发生了积极转变。文献中具有混合相关性的Lachnospiraceae细菌的富集可能反映了环境依赖性的相互作用,值得进一步研究。
如图6F所示,LEfSe分析表明,NC组富含有益菌,如拟杆菌门和拟杆菌属,而T2DM组则富含厚壁菌门和梭菌门。MCPS-3治疗后,有益菌如拟杆菌属和拟杆菌科的增加,这支持了这些分类群在将多糖代谢为SCFA、减轻炎症和调节脂质代谢方面发挥关键作用的观点。总的来说,这些结果强调了MCPS-3以有利于代谢健康的方式重塑肠道微生物群落的能力,这对管理2型糖尿病的葡萄糖和脂质失调具有重要意义。
8. MCPS-3改变糖尿病小鼠粪便代谢产物
代谢组学具有巨大的潜力,可以增强我们对环境暴露如何破坏代谢途径的理解,从而阐明它们在疾病进展中的作用,并揭示影响临床结果的分子机制。该研究采用非靶向代谢组学来研究各组之间的代谢变化,特别关注T2DM及其通过MCPS-3的调节。与NC组相比,T2DM组共有199种代谢物表现出显著的差异表达,其中66种代谢物上调,133种下调,而1714种代谢物保持不变(图7A)。这表明与糖尿病状态相关的代谢紊乱严重。相反,MCPS-3组相对于T2DM组的分析显示,46种代谢物发生了显著变化,其中16种上调,30种下调,1867种代谢物没有变化(图7B)。与代谢应激和炎症相关的代谢产物甘氨石胆酸和18-α-甘草次酸被下调,而具有抗炎和葡萄糖调节特性的胆汁酸牛磺鹅去氧胆酸和牛磺熊去氧胆酸上调(图7C)。牛磺鹅去氧胆酸是胆汁酸的主要成分,因其在抗炎和免疫调节信号传导中的作用而受到认可,这表明其上调可能会增强这些保护途径。此外,在高脂饮食模型中,牛磺熊去氧胆酸的增加与葡萄糖耐量的改善和肥胖的减少有关,这表明MCPS-3有可能积极调节葡萄糖和脂质代谢。与代谢应激相关的甘氨石胆酸和18-α-甘草次酸的下调表明,代谢状态正在向更平衡的方向转变。
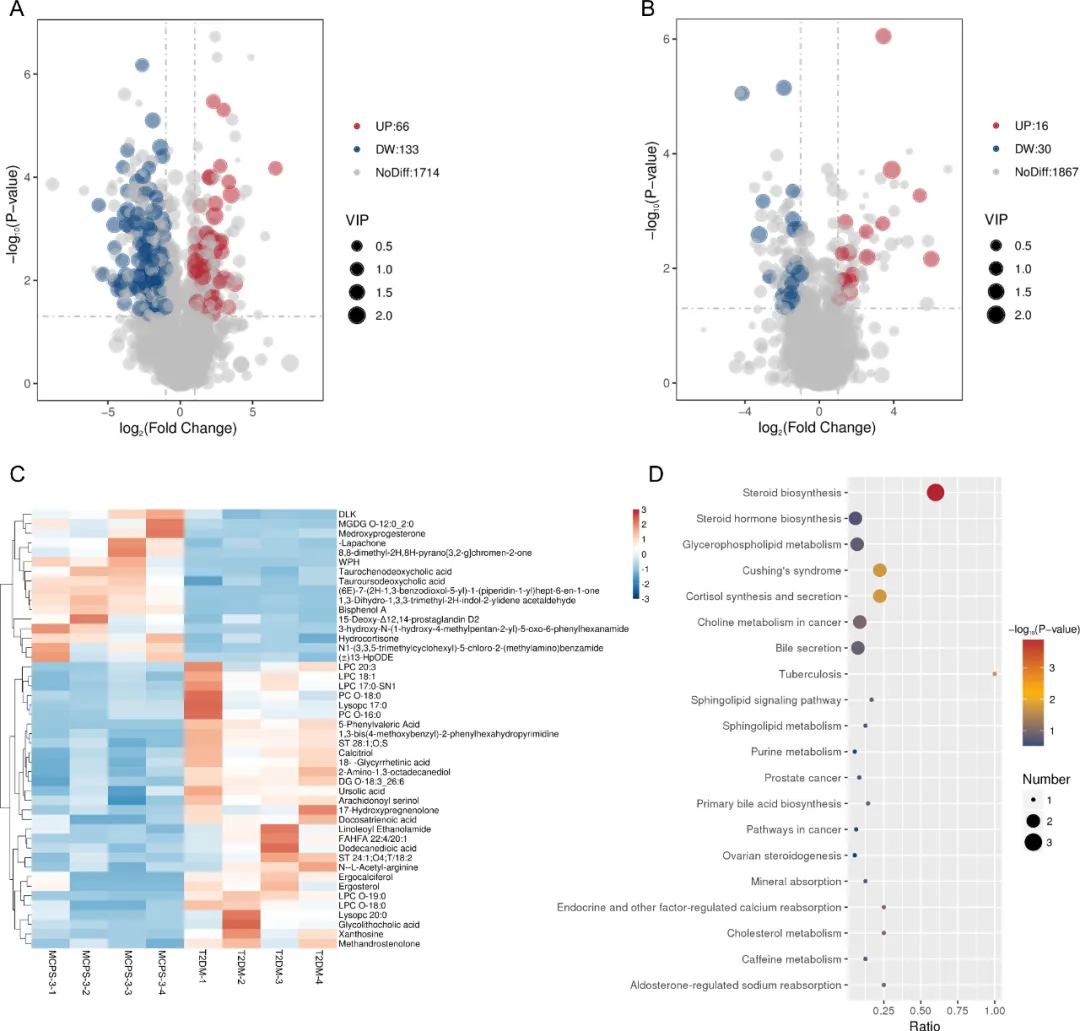
图7 MCPS-3改变了T2DM小鼠的粪便代谢物。血清代谢物的火山图:(A)T2DM组与NC组,(B)MCPS-3组与T2DM组。MCPS-3和T2DM组之间的主要差异代谢物(C)和相应的代谢途径(D)。
KEGG途径富集分析进一步阐明了这些代谢变化,突出了与类固醇生物合成、类固醇激素生物合成和甘油磷脂代谢相关的途径的显著富集(图7D)。此外,与库欣综合征、皮质醇合成和分泌等临床疾病相关的途径以及癌症中的胆碱代谢和胆汁分泌也受到影响。这些发现表明,MCPS-3可能通过调节特定的代谢途径发挥其治疗作用,这些途径对维持代谢稳态和影响疾病病理至关重要。这项综合分析强调了T2DM背后复杂的代谢相互作用以及MCPS-3调节这些途径的潜力。与类固醇和激素生物合成相关的代谢产物的调节表明了改善2型糖尿病代谢失调的潜在机制。同时,观察到的甘油磷脂代谢和胆汁分泌的变化可能反映了恢复脂质稳态和消化过程的尝试。这些见解不仅加深了我们对糖尿病及其治疗相关代谢变化的理解,也为确定新的治疗靶点奠定了基础。需要进一步的研究来阐明这些途径的具体作用,并评估调节这些代谢网络在疾病管理中的临床意义。
结论
总之,MCPS-3通过有效靶向多种途径和肠道微生物群,在缓解小鼠2型糖尿病方面显示出巨大的潜力。MCPS-3激活IRS1/PI3K/Akt和AMPK信号通路,从而改善胰岛素敏感性,增强糖酵解,增加糖原合成。它还改善了高血糖和血脂异常,降低了血糖和血脂水平。此外,MCPS-3通过增加有益细菌和增强微生物多样性来调节肠道微生物群组成,有助于改善代谢健康。粪便代谢物的改变进一步表明了向代谢稳态的转变。这些发现强调了MCPS-3作为靶向2型糖尿病代谢和微生物失调的多方面治疗剂的潜力。尽管如此,这项研究表明MCPS-3在改善2型糖尿病小鼠的葡萄糖代谢、胰岛素敏感性、脂质状况和肠道微生物群组成方面具有很好的治疗效果。然而,由于小鼠和人类生物学之间的差异,在转化这些发现时必须谨慎。未来的研究应侧重于评估MCPS-3在临床前模型中的药代动力学、生物利用度和长期安全性。此外,MCPS-3的治疗效果应通过严格设计的临床试验进行验证,包括不同人群和不同的T2DM分期。此外,探索MCPS-3与已建立的抗糖尿病的联合治疗研究可能会显示协同作用,进一步扩大其临床适用性。这些步骤对于推进MCPS-3作为人类T2DM管理的候选药物至关重要。此外,我们承认,几个关键机制仍有待充分阐明。具体而言,虽然我们已经证明MCPS-3调节肠道微生物群和与改善代谢健康相关的代谢产物,但确切的吸收机制和对IRS1/PI3K/Akt和AMPK等信号通路的直接影响需要进一步研究。未来的研究将侧重于通过评估MCPS-3在体内的吸收效率来解决这些差距,并探索它如何直接和通过微生物代谢物调节这些途径。此外,对MCPS-3的药代动力学、生物利用度和长期安全性的研究对于确认其作为治疗剂的潜力至关重要。这些研究将为MCPS-3的精确作用机制及其在治疗T2DM等代谢性疾病方面的临床应用潜力提供关键见解。
----------微科盟精彩文章----------
科研 | 华南农大&华南理工&马萨诸塞大学:代谢组学和转录组学揭示了余甘子果胶多糖改善结肠炎的作用机制(国人佳作)
科研 | 国家药典委员会&中检院:何首乌多糖通过调节P53/P21通路和氨基酸代谢发挥抗衰老作用(国人佳作)
如果需要原文pdf,请扫描文末二维码



获取此文献原文PDF、申请加入学术群,联系您所添加的任一微科盟组学老师即可,如未添加过微科盟组学老师,请联系微生态老师9,无需重复添加。
请关注下方名片,了解更多代谢组学知识
