IF10.9!南京大学孙洋团队“国自然+共病分析”拿下一区TOP!
- 2026-04-28 10:31:18


强直性脊柱炎(AS)与附着点炎相关性关节炎(ERA)是自身免疫性骨病,以异位骨化和附着点炎为特征,且预后均较差。但目前对这两种疾病的病理机制尚不明确。传统观点聚焦于CD4+Th17细胞的作用,而CD8+T细胞的致病机制仍待阐明。
由南京大学孙洋/陈迪俊团队,联合南京市儿童医院樊志丹/俞海国团队在《Arthritis & Rheumatology》上发表的题为“XCR1阳性常规1型树突状细胞通过IL-17A阳性CD8+T细胞加剧骨关节炎炎症反应”的文章,旨在探究cDC1s和CD8+T细胞在骨生成性关节炎中的相互作用及其致病机制。
文献解读

研究方法
临床样本分析
样本来源:纳入7例寡关节炎(OligoA)和5例ERA患者,采集外周血单核细胞(PBMC)和关节液单核细胞(SFMC),共分析33例标本。
数据分析:细胞聚类、差异基因表达(DEG)分析、细胞间相互作用预测(CellPhoneDB)、RNA velocity和伪时间轨迹分析。
技术手段
单细胞RNA测序(scRNA-seq)和T细胞受体(TCR)测序,解析细胞亚群和克隆多样性。
流式细胞术和多重免疫荧光,验证细胞比例和空间分布。
酶联免疫吸附实验(ELISA)检测细胞因子(如XCL1)水平。
动物模型构建
C2V7模型:将Ⅱ型胶原蛋白与蛋白聚糖versican衍生肽(VG191–115)混合,单次皮下注射诱导BALB/c和DBA/1小鼠出现AS样症状(附着点炎、异位骨化)。
干预实验:使用XCL1中和抗体阻断cDC1的招募,评估对关节炎的缓解效果。
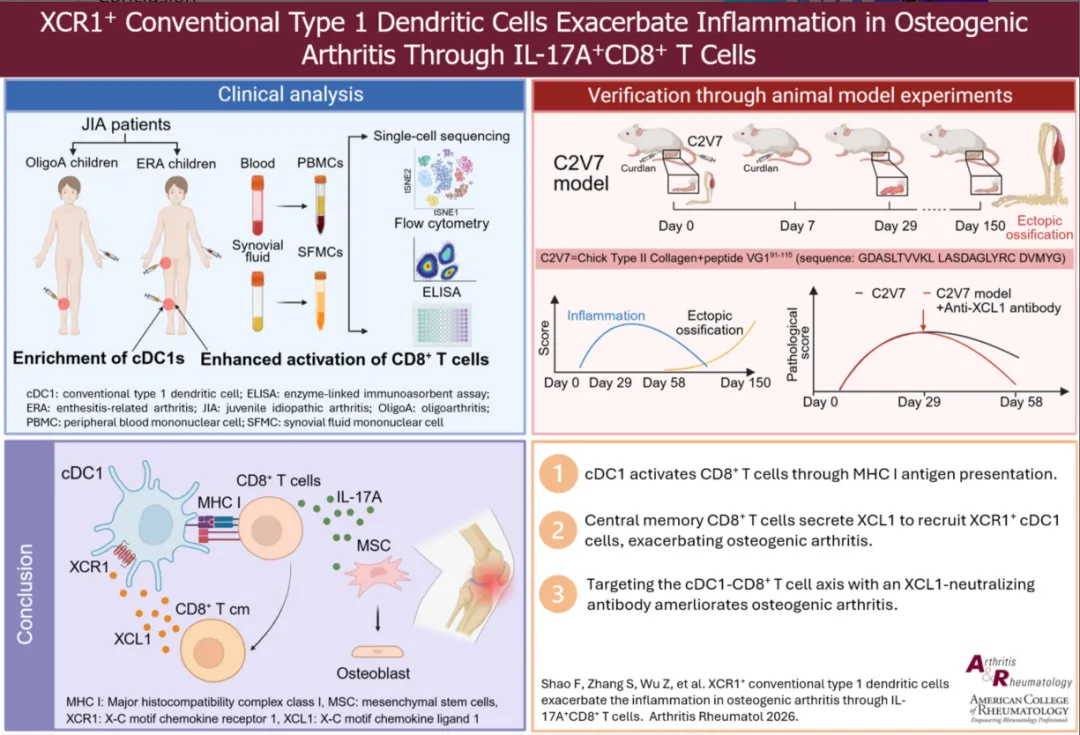
图解摘要

近期前沿热点:虚拟细胞、虚拟敲除🌟
专注于生信分析,包含选题设计方案

文献计量学:方案合理,价格公道👍
主要结果
ERA患者关节液中CD8⁺T细胞高度活化,TCR克隆性显著增强
通过对未治疗的ERA和少关节型JIA患者的外周血和关节液单核细胞进行单细胞测序,团队发现ERA患者关节液中CD8⁺T细胞和中央记忆型CD8⁺T细胞显著富集【图1B】。
TCR测序显示,ERA患者外周与关节液中CD8⁺T细胞存在高度重叠的克隆型,提示存在特异性抗原驱动的免疫应答【图1D, E】。这表明CD8⁺T细胞在ERA发病中起核心作用。
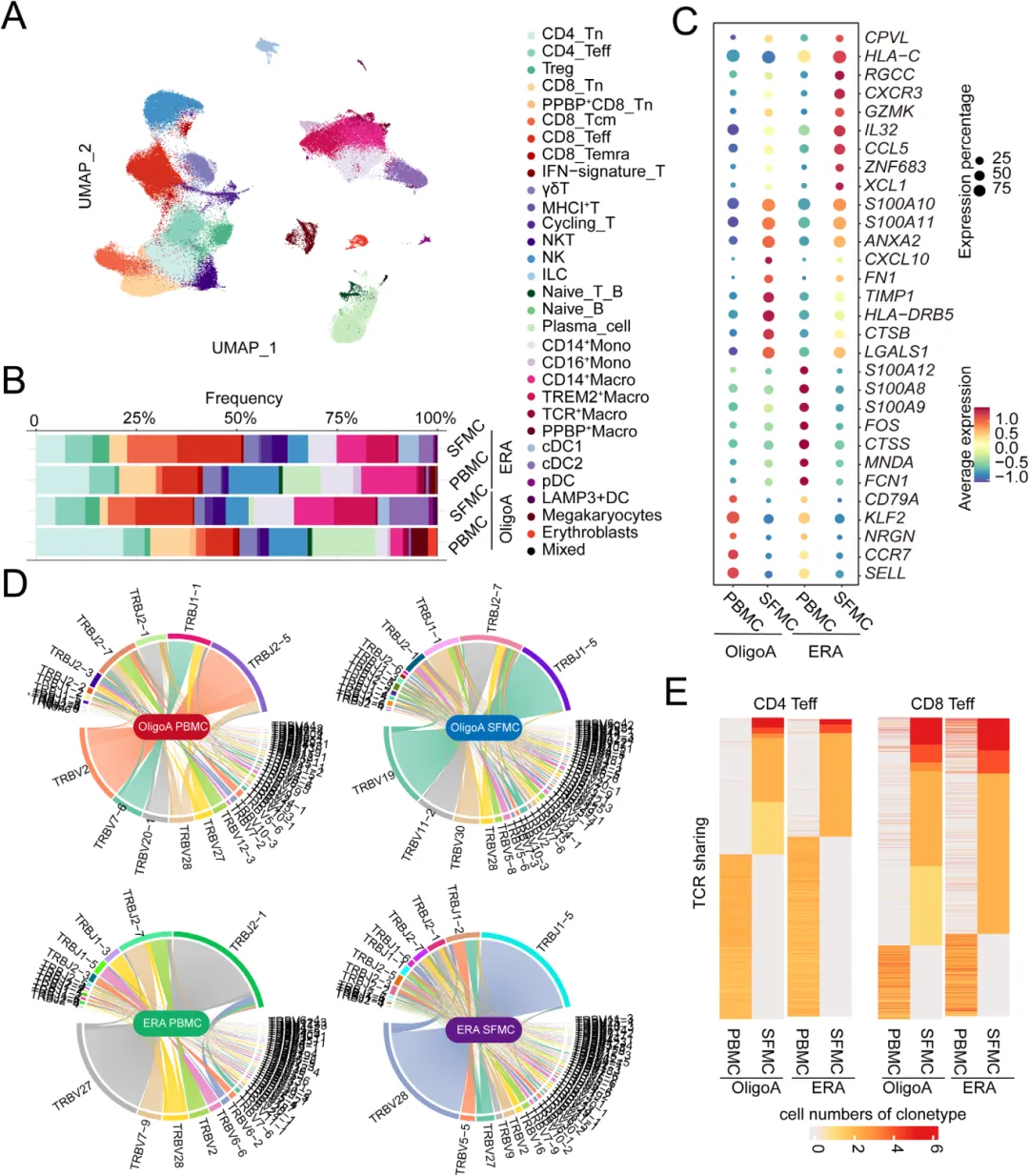
图1.ERA中的滑膜CD8+T细胞表现出增强的活化及克隆性TCR共享
从11,160个树突状细胞中聚类出cDC1、cDC2、pDC和LAMP3⁺DC四类亚群。ERA患者关节液中cDC1比例显著高于OligoA患者【图2C, D】,且流式细胞术进一步证实了这一点【图2E, F】。
转录组分析显示,ERA cDC1高表达MHC I抗原呈递相关基因如HLA-B、TAP1等【图2H】,提示其在抗原交叉呈递中起关键作用。
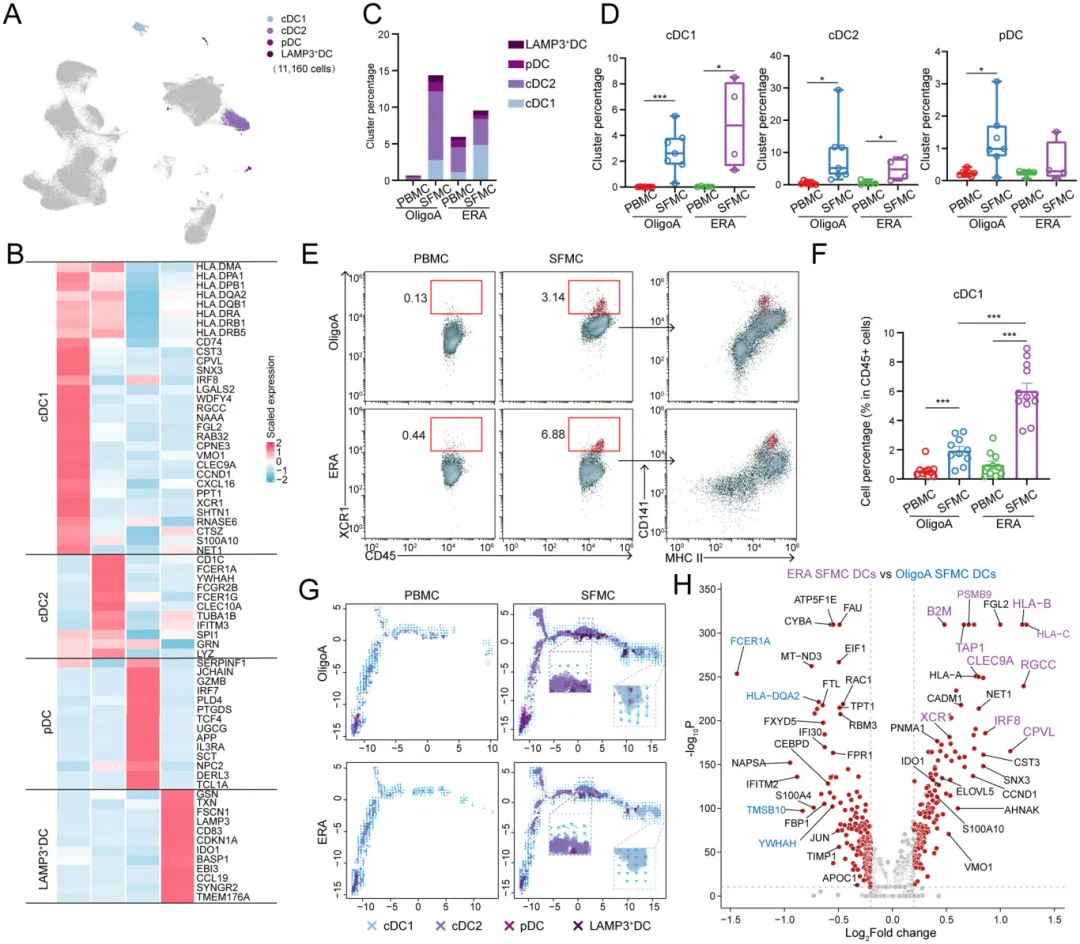
图2.cDC1s在ERA滑液中选择性富集
配体-受体分析显示,cDC1与CD8⁺T细胞之间通过XCL1-XCR1和CXCL16-CXCR6两条通路相互作用【图3C】。
其中,CD8+ Tcm是XCL1的主要来源【图3D, E】,而cDC1则特异性表达其受体XCR1【图3H】。这形成了一个正反馈环路:cDC1通过MHC I激活CD8+T细胞,活化的T细胞分泌XCL1,进而招募更多cDC1到炎症部位,加剧免疫反应。
ELISA证实ERA关节液中XCL1蛋白水平显著升高【图3F】。免疫荧光进一步显示AS患者脊柱韧带中存在XCR1⁺cDC1与B2M共定位【图3I】,说明该轴在人体病变组织中同样活跃。
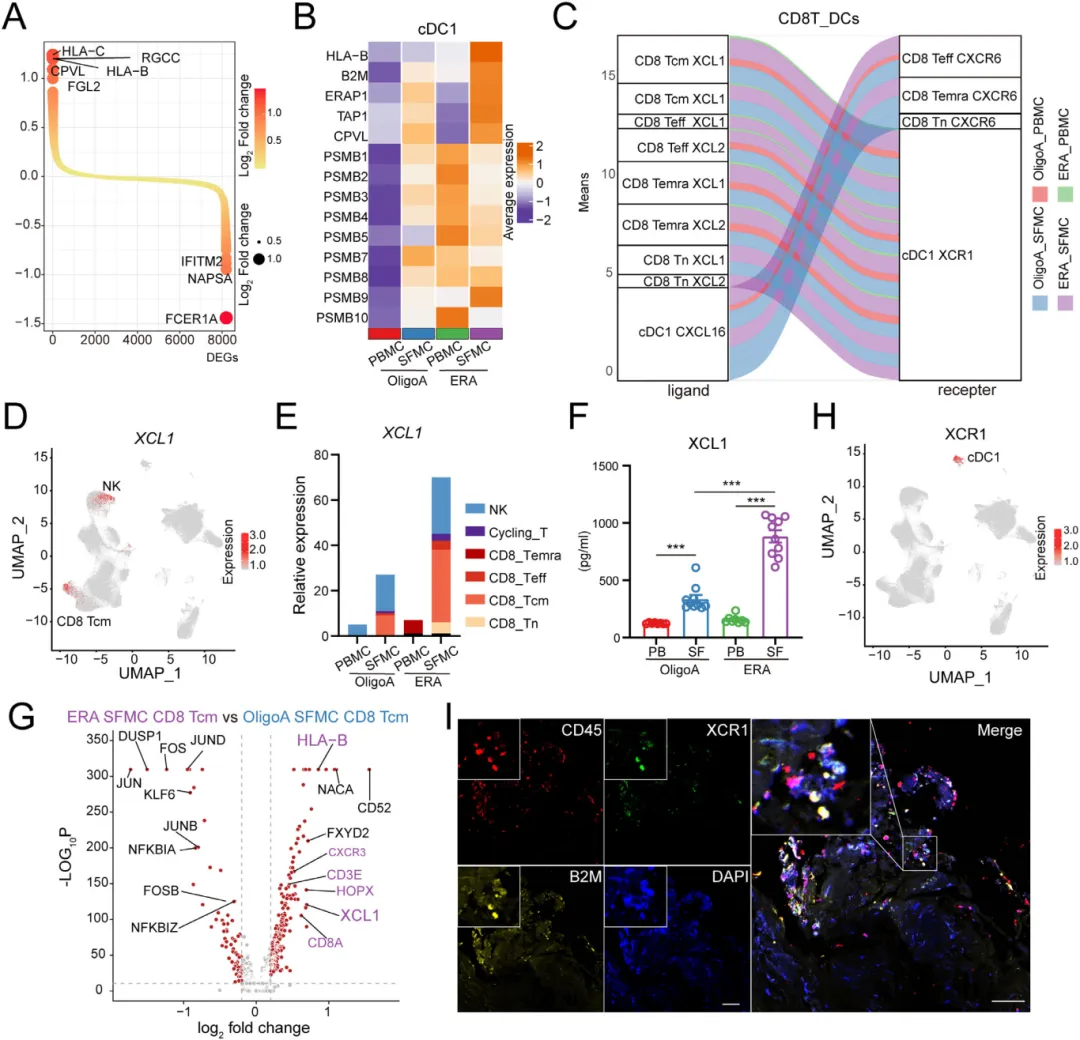
图3.ERA滑液中增强的cDC1-CD8+T细胞相互作用
为突破现有模型局限,团队将II型胶原与多功能蛋白聚糖来源多肽VG191–115联合免疫,建立C2V7模型【图4A】。
模型小鼠在免疫后30天出现足肿胀,60天后病理切片显示明显炎细胞浸润、软骨破坏及异位骨化【图4D–G】,Runx2⁺成骨细胞在附着点区域富集【图4H】,成功模拟了AS的核心病理特征,为机制研究和治疗测试提供了理想工具。
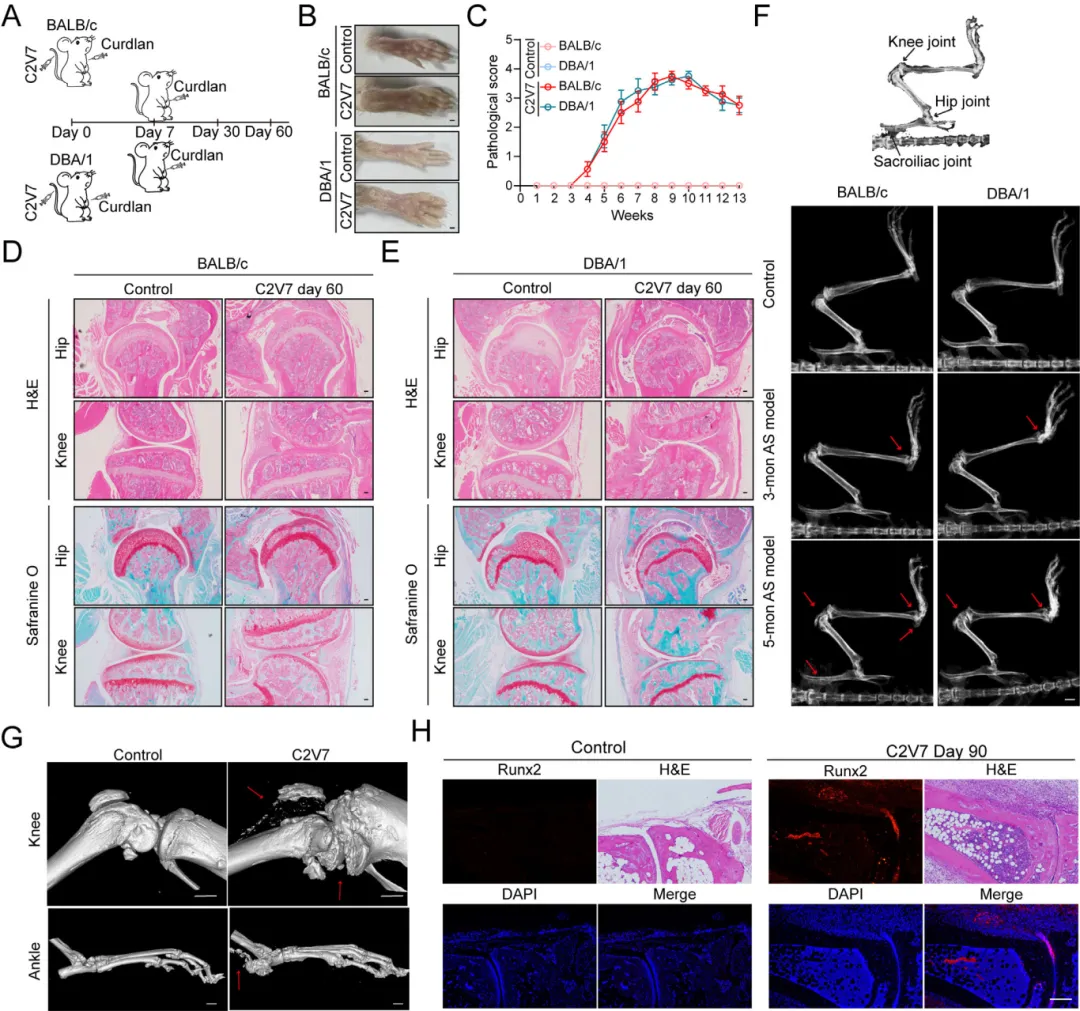
图4.单次接种C2V7可在BALB/c和DBA/1小鼠中诱发类强直性脊柱炎(AS)关节炎
流式细胞术显示,在C2V7模型小鼠发炎的关节组织中CD45⁺免疫细胞和CD3⁺T细胞比例显著升高【图5A–D】。CD8+T细胞数量远超CD4+T细胞,并且其中超过80%的CD8+T细胞分泌致炎因子IL-17A【图5J, K】。
同时,cDC1也在滑膜组织中显著富集【图5L, M】。这表明cDC1和IL-17A+CD8+T细胞共同驱动了该模型中的关节炎症和骨损伤。
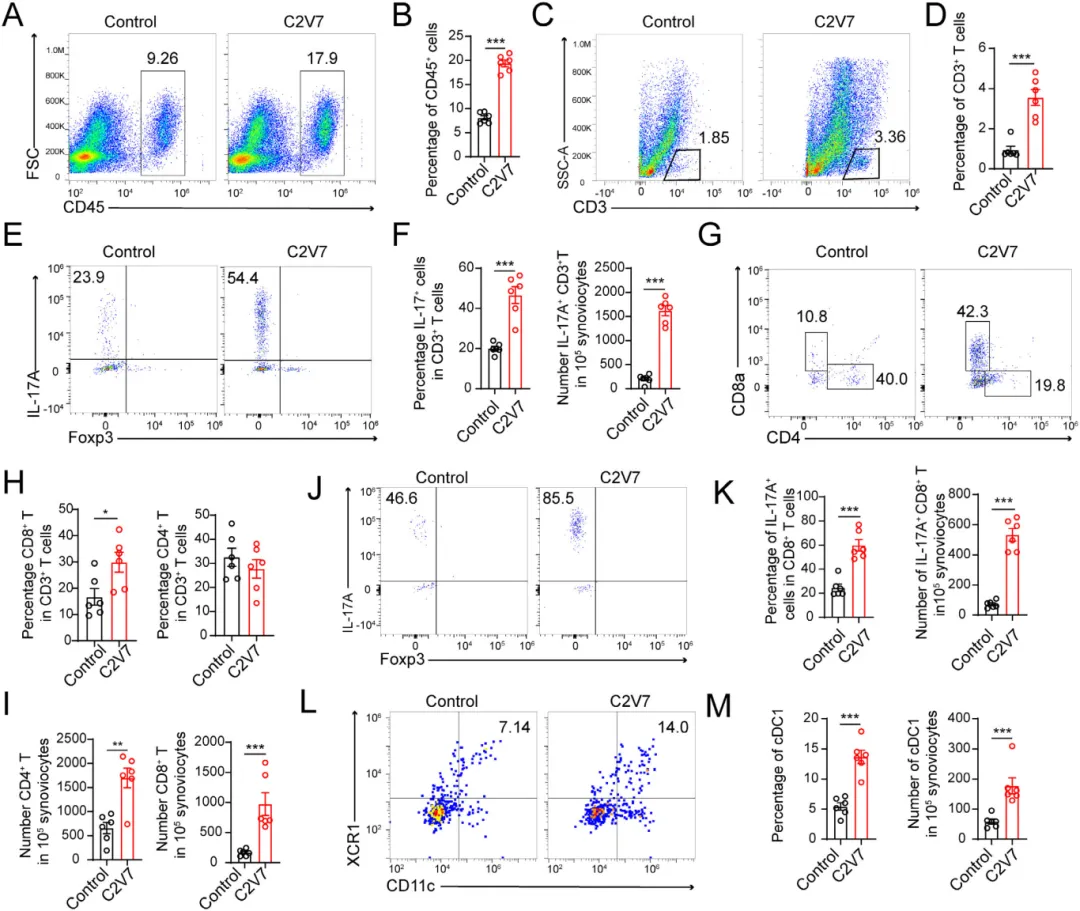
图5.在C2V7模型的炎症关节中,cDC1s和IL-17A+CD8+T细胞聚集
基于上述发现,为验证cDC1-CD8⁺T细胞轴的治疗潜力,研究者在疾病早期使用中和抗体阻断XCL1【图6B】。结果显示,抗体治疗显著减轻了小鼠的足爪肿胀、关节炎症和免疫细胞浸润【图6C, D】,并减少关节中CD45⁺免疫细胞【图6F, G】、cDC1【图6H, I】及IL-17A⁺ T细胞【图6J, K】的浸润。同时,Runx2⁺成骨细胞在附着点区域明显减少,从而抑制了异位骨化【图6L】,证实阻断该轴可有效抑制炎症与骨化。
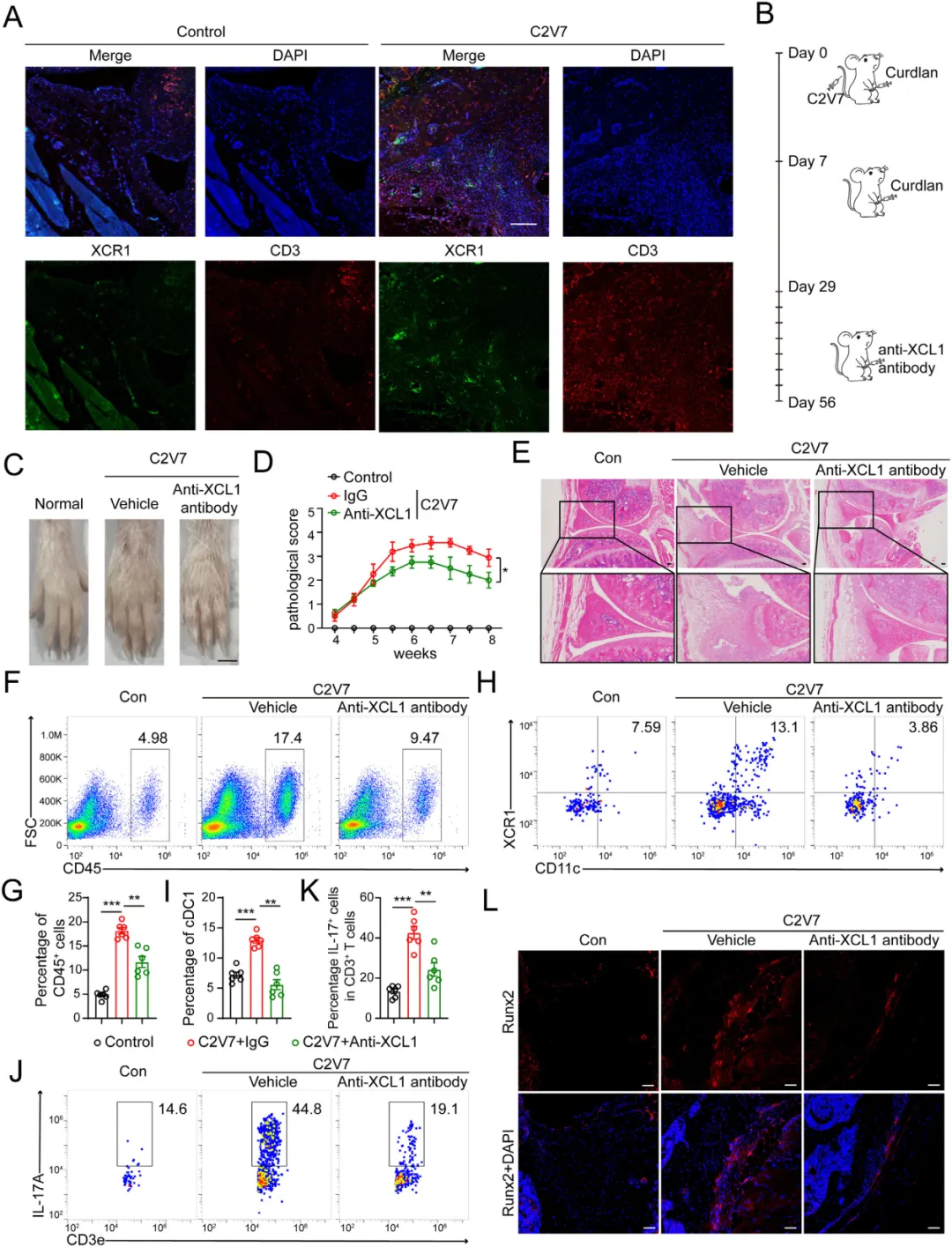
图6.XCL1阻断可减轻C2V7模型中的关节炎症和异位骨化
文章小结
这篇文章通过整合临床样本的高通量数据分析和新型动物模型的机制验证,系统地阐明了一条由cDC1s和CD8+T细胞构成的、以前未被充分认识的免疫致病通路,为理解并治疗一类以异位骨化为特征的关节炎提供了重要的理论依据和潜在的治疗突破口。
如果你也想用“国自然热点+多组学”进行研究,需要生信分析,复现高分思路,那就快来后台联系吧~精彩生信,助力每一个科研梦想!





