南京大学 | 突破骨再生瓶颈!壳强化大孔水凝胶实现干细胞定向成骨与机械保护双效
- 2026-04-17 13:58:42

导读
针对传统水凝胶难以兼顾干细胞存活、定向成骨分化与机械支撑的问题,研究团队通过液 - 液相分离软模板技术与界面超分子自组装,构建壳强化大孔(SP)水凝胶:大孔结构避免细胞增殖接触抑制,刚性蛋白纤维壳提供持续成骨力学信号并抵御机械损伤,软基质具备可调降解性以匹配新组织沉积;通过调控 PEG 与葡聚糖比例、交联剂配比优化结构与降解速率,在兔和猪骨缺损模型中,SP 水凝胶包裹干细胞后实现近完全骨再生,其力学异质性、可控降解性与生物相容性协同作用,解决了传统水凝胶降解与力学信号维持的矛盾,为干细胞辅助骨再生提供了新型生物材料方案。
注:该文章发表于《Nature Communications》,其最新影响因子高达15.7,位于JCR和中科院分区的Q1区。创新设计壳 - 基质力学异质结构,刚性蛋白壳与软基质功能分离;实现时空编程力学信号递送,大孔结构保障细胞增殖空间,刚性壳提供持续成骨 cues,软基质降解速率可调;在兔、猪模型中验证骨再生效果,兼具机械保护与定向分化调控能力,解决传统水凝胶力学 - 降解矛盾,生物相容性优异。
采用液 - 液相分离软模板技术,以 PEG 和葡聚糖为原料调控相分离形成大孔,通过溶菌酶纳米纤维界面自组装构建刚性壳,引入丙烯酰化 RGD 促进细胞粘附;选用含可降解酯键的 PEG-ACLT 与不可降解 PEG-ACA 为交联剂,调控比例实现降解速率可调;通过 AFM 纳米压痕表征力学性能,FESEM 与激光共聚焦荧光显微镜分析结构;体外开展细胞活力、成骨标志物(OCN、Runx2 等)检测与机械损伤保护实验;体内在兔(股骨髁 5mm 缺损)和猪(股骨髁 12mm 缺损)模型中植入干细胞包裹水凝胶,通过 micro-CT、组织学染色评估骨再生效果,同时在大鼠模型中验证生物相容性与降解性。
SP 水凝胶大孔直径约 50μm 适配细胞培养,壳层杨氏模量显著高于基质,降解过程中壳层力学信号维持稳定(42 天仅下降 20%);体外实验显示,SP 水凝胶细胞存活率超 97%,可抵御循环压缩损伤,显著上调成骨标志物表达与 F-actin 聚合;兔模型中,SP-low 组骨缺损近完全修复,BV/TV、骨小梁厚度等指标最优,组织学显示连续皮质骨形成;猪模型中,SP-low-cell 组实现大面积骨缺损修复,再生组织与正常骨结构相似度高;大鼠皮下植入实验表明水凝胶生物相容性良好,仅引发轻微炎症,降解速率与新骨形成同步。
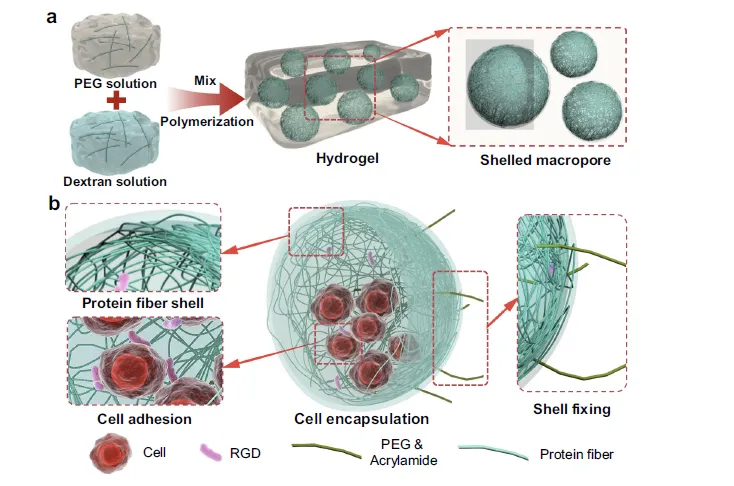
Figure 1:壳强化大孔水凝胶的设计与制备原理
该图清晰展示了壳强化大孔(SP)水凝胶的核心设计逻辑与制备流程,通过分步示意图阐明了材料结构与功能的关联。首先,利用聚乙二醇(PEG)与葡聚糖的液 - 液相分离形成软模板,葡聚糖相形成的纳米液滴为大孔结构提供雏形,PEG 相中的丙烯酰胺等聚合单体通过自由基聚合形成水凝胶基质;同时,预先组装的溶菌酶纳米纤维在相分离界面自组装,形成刚性蛋白纤维壳,且溶菌酶经丙烯酰化修饰实现与水凝胶基质的共价连接,确保壳结构稳定。此外,引入丙烯酰化 RGD 配体以促进细胞粘附,细胞被封装在大孔内并通过 RGD 与孔壁结合。该设计通过 “软基质 + 硬壳” 的力学异质结构,让干细胞主要感知壳层的机械信号而非基质弹性,为后续稳定诱导成骨分化奠定结构基础。

Figure 2:水凝胶的结构表征与 reproducibility 验证
该图通过多维度表征明确了不同类型水凝胶(NN、NP、SP)的结构差异及 SP 水凝胶的制备重现性。前驱体显微图像显示,NP 和 SP 水凝胶因 PEG 与葡聚糖相分离存在纳米液滴,而 NN 水凝胶无此结构,且 SP 水凝胶的纳米液滴直径更均一,荧光标记证实 SP 水凝胶的纳米液滴外围存在溶菌酶纳米纤维形成的壳层。凝胶后光学图像显示 NN 水凝胶透明,NP 和 SP 水凝胶半透明,提示后者存在微米级大孔结构,FESEM 图像进一步证实 NN 水凝胶为微孔结构,NP 和 SP 水凝胶为大孔结构。激光共聚焦荧光显微镜(LCFM)3D 重建结果清晰区分了三类水凝胶的结构特征:NN 水凝胶无明显大孔,NP 水凝胶为无壳大孔,SP 水凝胶为带绿色荧光壳层的大孔,且大孔直径超 50μm 适配细胞培养。此外,对不同批次 SP 水凝胶的壳厚度和孔径测量显示,各批次间无显著差异,证实该水凝胶制备工艺具有良好的重现性。
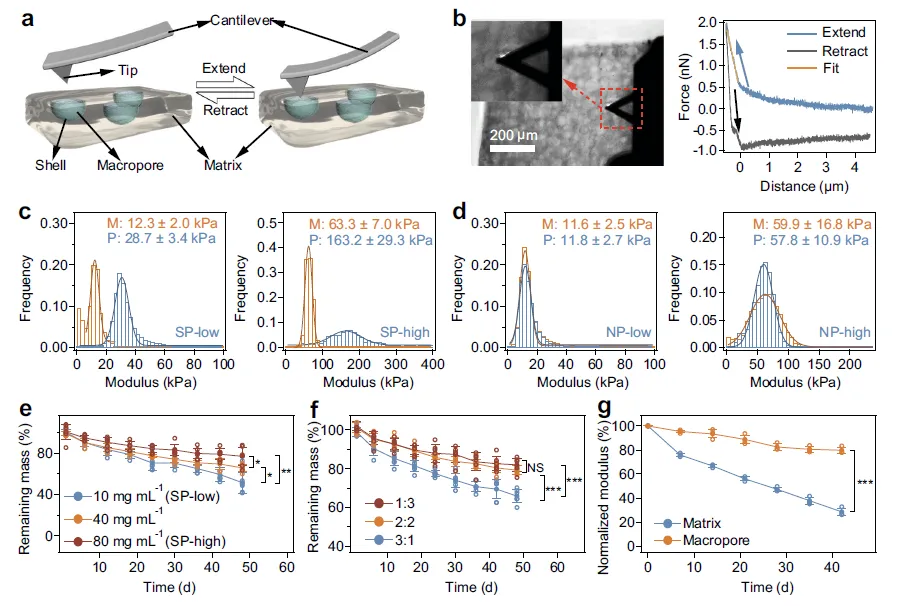
Figure 3:水凝胶的力学异质性与降解特性分析
该图通过 AFM 纳米压痕测试和体外降解实验,揭示了 SP 水凝胶的核心性能优势 —— 力学异质性和可调降解性。AFM 测试示意图及力 - 位移曲线拟合结果显示,SP 水凝胶的壳层(P)杨氏模量显著高于基质(M),SP-low 和 SP-high 水凝胶壳层模量分别约为 28.7±3.4 kPa 和 163.2±29.3 kPa,而 NP 水凝胶的孔与基质无明显刚度差异,证实 SP 水凝胶成功构建了 “壳硬基质软” 的力学异质结构。体外降解实验表明,SP 水凝胶的降解速率可通过 PEG-ACLT 与 PEG-ACA 的浓度和比例调控,PEG-ACLT 占比超 50% 时降解速率显著加快,且 SP-low 水凝胶在 42 天降解过程中,壳层模量仅下降 20%,而基质模量下降超 70%,说明壳层能在基质降解过程中持续提供稳定的机械信号,解决了传统水凝胶降解与力学支撑的矛盾。
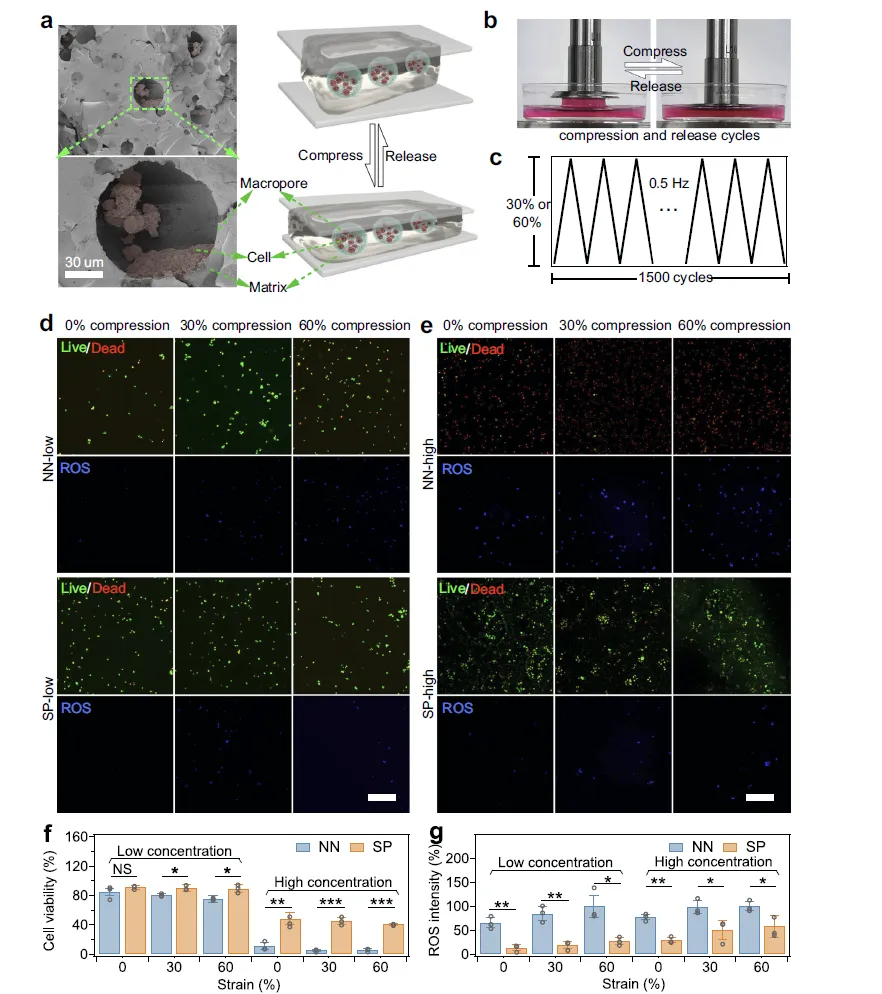
Figure 4:水凝胶对封装细胞的机械损伤保护作用
该图通过细胞封装验证和循环压缩实验,证实了 SP 水凝胶壳层对细胞的机械保护功能。FESEM 图像显示 MC3T3-E1 细胞成功封装在 SP 水凝胶的大孔内,示意图直观呈现了压缩 - 松弛循环中壳层对细胞的保护机制。循环压缩实验(0.5 Hz,30%/60% 应变)后,活 / 死染色和 ROS 染色结果显示,SP 水凝胶封装的细胞存活率显著高于 NN 水凝胶:SP-low 水凝胶在中等和过度压缩下的细胞存活率比 NN-low 高 10% 和 15%,ROS 生成量减少 49% 和 42%;SP-high 水凝胶的细胞存活率更是 NN-high 的 9-7 倍,且随应变增加存活率基本稳定。这一结果表明,SP 水凝胶的刚性壳层能有效抵御动态力学载荷对细胞的损伤,同时不影响细胞增殖,其 ROS 减少源于机械保护而非溶菌酶的抗氧化作用,进一步验证了壳层的结构功能价值。
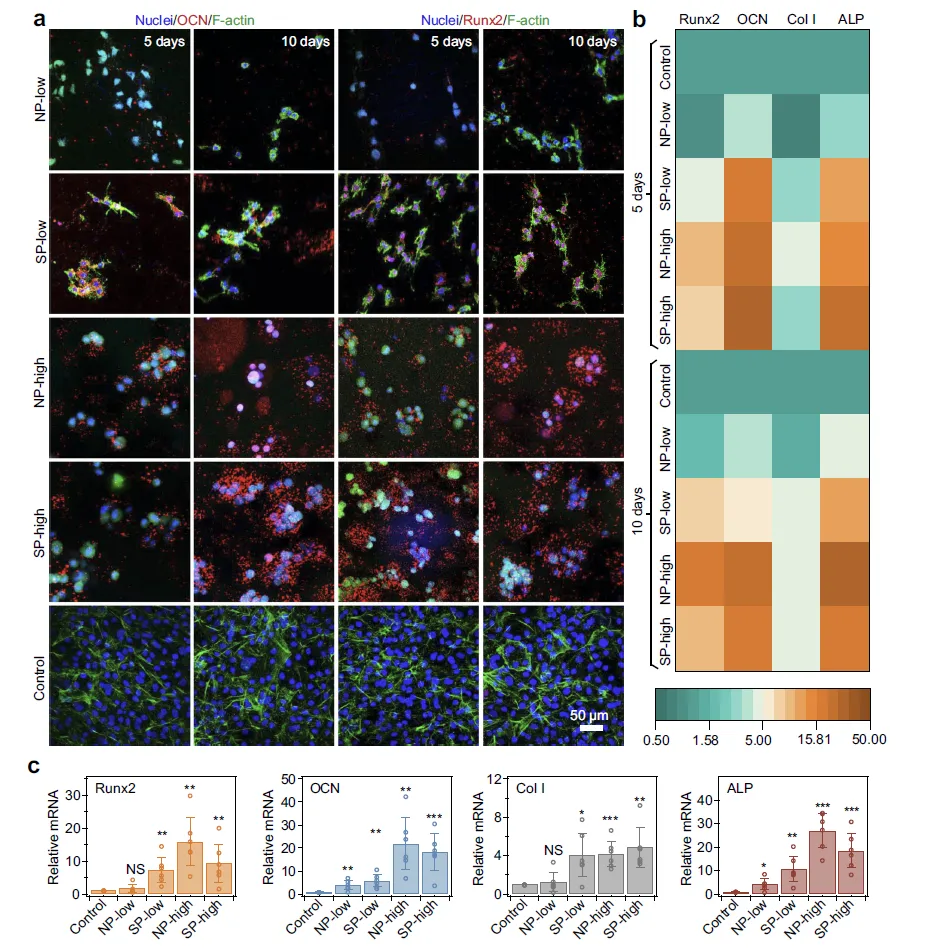
Figure 5:刚性壳层对干细胞成骨分化的调控作用
该图通过免疫染色和 qRT-PCR 实验,明确了 SP 水凝胶壳层提供的持续机械信号对干细胞成骨分化的诱导作用。免疫染色结果显示,培养 5 天和 10 天后,SP-low 水凝胶中 MC3T3-E1 细胞的成骨标志物(OCN、Runx2)显著上调,而 NP-low 水凝胶因缺乏刚性壳层未出现明显成骨分化,NP-high 和 SP-high 水凝胶则因基质高弹性也诱导了成骨标志物表达;同时,SP-low 水凝胶中 F-actin 形成长而致密的纤维且张力显著,而 NP-high 和 SP-high 水凝胶中 F-actin 纤维较短且随时间衰减,提示 SP-low 水凝胶的机械微环境更利于成骨相关信号传导。qRT-PCR 结果进一步量化验证,SP-low、NP-high 和 SP-high 水凝胶中 Runx2、OCN、Col I、ALP 的 mRNA 表达水平均显著高于 NP-low 水凝胶和对照组,证实刚性壳层(或高弹性基质)能通过机械信号调控干细胞成骨分化,且 SP-low 水凝胶更利于干细胞分泌因子扩散,进一步促进骨再生。
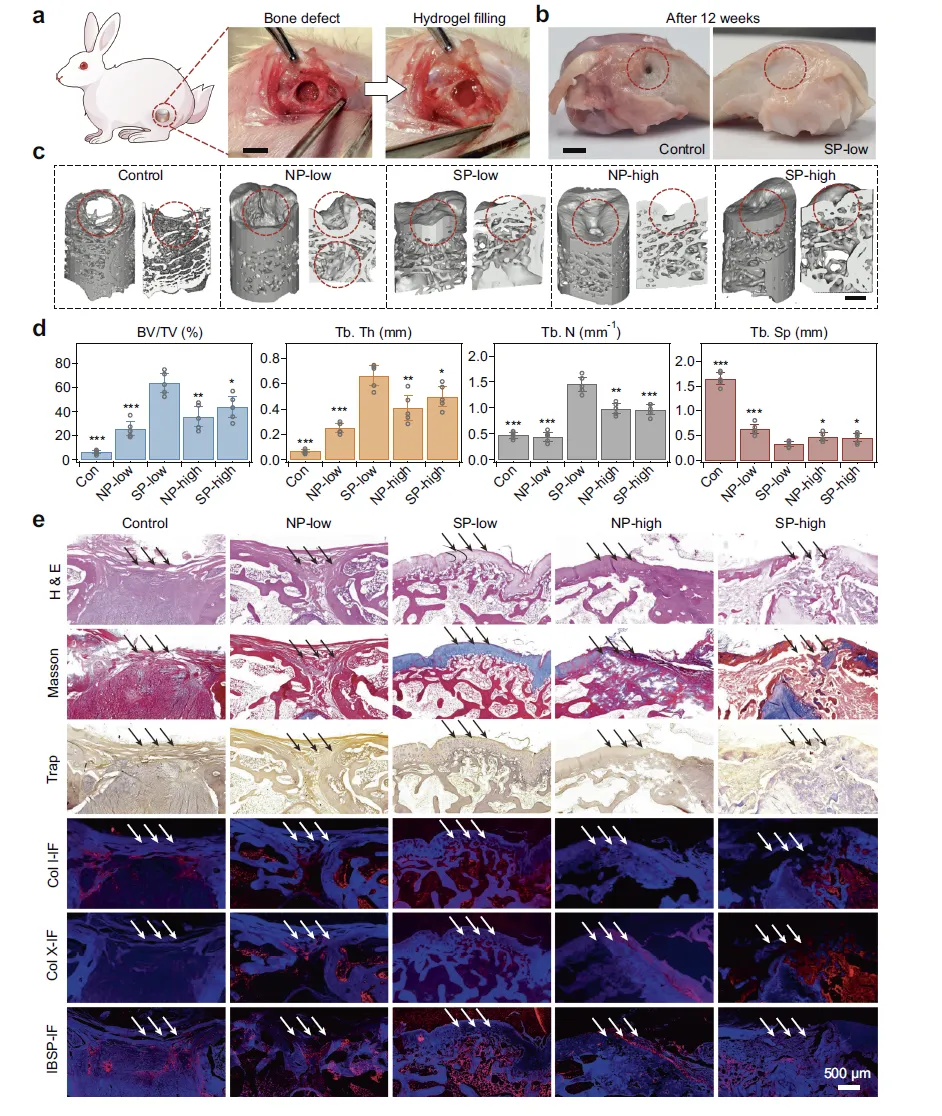
Figure 6:兔模型中 SP 水凝胶的骨再生效果验证
该图通过兔股骨髁骨缺损修复实验,在体内层面证实了 SP 水凝胶辅助干细胞骨再生的优异效能。手术示意图展示了骨缺损(直径 5mm)制备及 rBMSC 封装水凝胶植入流程,12 周后大体观察显示 SP-low 水凝胶组骨缺损区域修复效果显著优于对照组。Micro-CT 成像及定量分析表明,SP-low 水凝胶组骨缺损几乎完全被骨组织填充,形成连续皮质骨,其骨体积 / 总体积(BV/TV)、骨小梁厚度(Tb. Th)、骨小梁数量(Tb. N)均为各组最高,骨小梁分离度(Tb. Sp)最低,而对照组存在明显缺损腔,NP-low、NP-high、SP-high 组修复效果均不及 SP-low 组。组织学染色(H&E、Masson 三色、Trap 染色)显示,SP-low 组再生骨组织均匀连续,皮质骨发育完全,骨吸收不明显;免疫荧光染色(Col I-IF、Col X-IF、IBSP-IF)强度更高,证实该组骨再生质量更优,且无细胞的 SP-low 水凝胶修复效果差,说明骨再生是水凝胶与 BMSCs 协同作用的结果,凸显了壳层与软基质的协同价值。
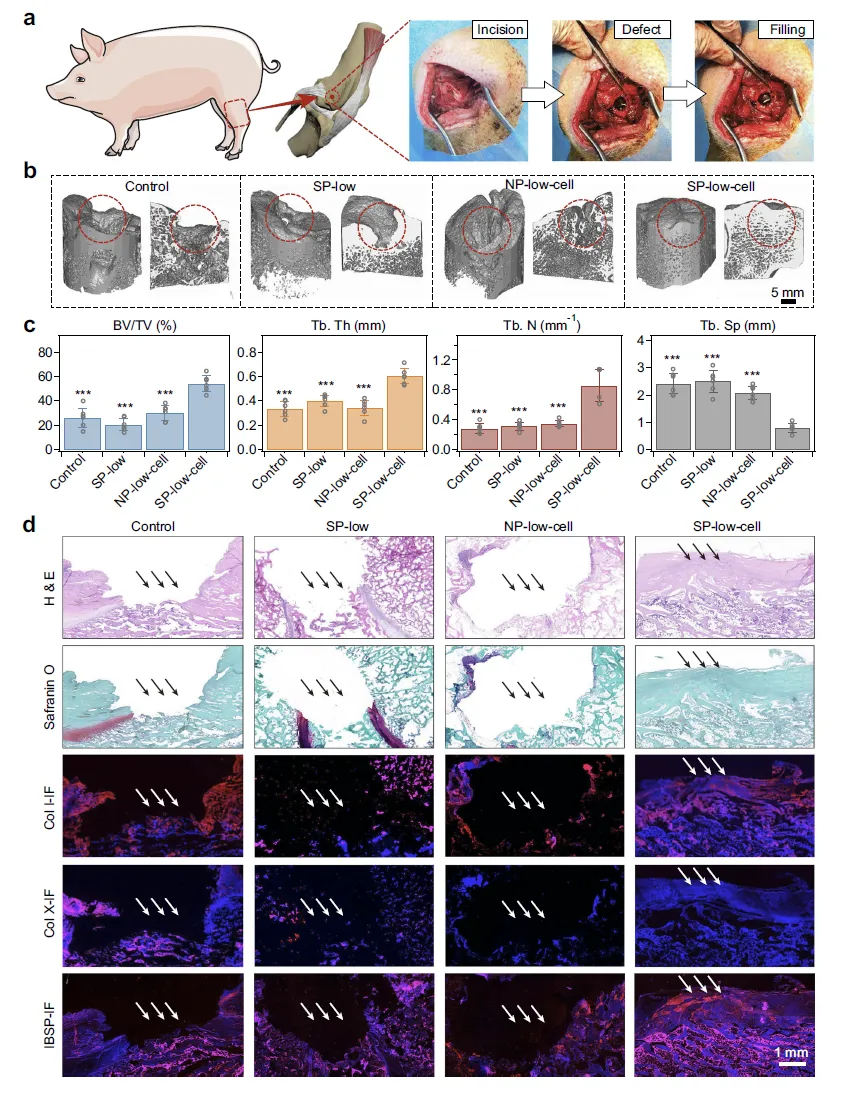
Figure 7:猪模型中 SP 水凝胶的骨再生效果验证
该图在更大动物模型(猪)中进一步验证了 SP 水凝胶的骨再生潜力,解决了大动物骨缺损修复难度更高的问题。手术示意图展示了猪股骨髁更大尺寸骨缺损(直径 12mm)的制备及水凝胶植入流程,12 周后 Micro-CT 成像显示,pBMSC 封装的 SP-low 水凝胶(SP-low-cell 组)能实现骨缺损近完全修复,形成连续皮质骨和骨组织,而对照组、SP-low 组(无细胞)、NP-low-cell 组均存在明显缺损腔。定量分析表明,SP-low-cell 组的 BV/TV、Tb. Th、Tb. N 均为各组最高,Tb. Sp 最低,证实其骨再生效率和质量最优。组织学染色(H&E、Safranin O 染色)及免疫荧光染色(Col I-IF、Col X-IF、IBSP-IF)进一步验证,SP-low-cell 组再生骨组织结构与正常骨相似度高,细胞分布均匀,骨基质成分表达丰富,说明 SP 水凝胶在大动物模型中仍能有效支持干细胞介导的骨再生,为临床转化提供了更有力的证据。
本研究成功开发兼具时空编程力学性能与可调降解性的壳强化大孔水凝胶,其大孔结构、刚性壳层与软基质的协同设计,有效解决了传统水凝胶在干细胞存活、定向成骨与机械支撑间的矛盾。该水凝胶可保护干细胞免受机械损伤,持续提供成骨力学信号,且降解速率与新组织沉积匹配,在兔和猪骨缺损模型中均展现出优异的骨再生效果,生物相容性良好。这一设计为干细胞辅助骨再生提供了新型生物材料平台,推动了骨缺损修复技术的发展,具有重要临床转化潜力。
局限性:未深入探究化学信号与力学信号的协同作用机制,临床转化需进一步优化规模化制备工艺。展望:未来将聚焦信号协同调控,拓展至更大动物模型与临床研究,探索在其他硬组织再生中的应用,推动该类水凝胶的临床转化。
文章来源: Xue B, Xu Z, Li L, et al. Hydrogels with programmed spatiotemporal mechanical cues for stem cell-assisted bone regeneration. Nat Commun. 2025;16(1):3633. Published 2025 Apr 16. doi:10.1038/s41467-025-59016-6
#干细胞#骨再生#水凝胶#力学异质性#壳强化大孔结构#可控降解#生物相容性#骨缺损修复

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究