最新最高转化率!南京工业大学院士组Chem Eng J-合成生物学-通过两阶段生物膜与代谢调控工程化大肠杆菌实现L-缬氨酸连续生产
- 2026-04-17 12:49:54
(点击页面左下角阅读原文,直达文献页面)
一、中文标题
通过两阶段生物膜与代谢调控工程化大肠杆菌实现L-缬氨酸连续生产(Engineering Escherichia coli for continuous L-valine production via two-stage biofflm and metabolic regulation)
二、发表单位及通讯作者
发表单位:南京工业大学生物与制药工程学院、材料化学工程国家重点实验室
通讯作者:Yu Sha、Yong Chen
三、科学问题
如何通过整合生物膜介导的细胞固定化和光遗传学代谢调控,解决L-缬氨酸连续发酵中细胞滞留不足、代谢通量失衡以及生长与生产相矛盾的关键瓶颈问题?
四、发表时间
发表时间:2026年1月
链接:https://doi.org/10.1016/j.cej.2026.173965

五、摘要
L-缬氨酸作为必需氨基酸在饲料和医药等行业至关重要,但其在连续发酵条件下的高效稳定合成鲜有报道。本研究构建了一株具有增强生物膜形成和蓝光激活代谢能力的工程化大肠杆菌,实现了高产和长期发酵。通过研究鞭毛运动相关基因,开发了一种新型氰胺诱导系统驱动fliA表达,在生长阶段加速生物膜形成;在生产阶段,通过光遗传工具pDawn瞬时激活ilvCDE表达,显著提升催化效率。采用两阶段调控策略的最终菌株在50 L生物反应器中连续发酵462小时,L-缬氨酸产量达71.63 g/L,葡萄糖转化率0.57 g/g,生产强度2.05 g/L/h。据我们所知,这是迄今报道的大肠杆菌中最高的葡萄糖-to-L-缬氨酸转化率。本研究建立的系统代谢工程策略为实现L-缬氨酸连续发酵提供了有前景的通用平台。
六、研究背景
作为必需的支链氨基酸,L-缬氨酸在多个行业中扮演着关键角色。由于可持续性和环境效益,微生物发酵已成为L-缬氨酸生产的主要方法。得益于其清晰的遗传背景、快速生长和显著的代谢灵活性,大肠杆菌在众多微生物平台中脱颖而出,被广泛用作L-缬氨酸生物合成的宿主。然而,随着市场对L-缬氨酸需求的增长,将实验室成果转化为稳健的连续生产仍面临挑战,因为传统发酵工艺仍受到细胞滞留不足、产量低、代谢瓶颈以及难以实现高效连续转化等问题的制约。因此,亟需开发新策略来解决这些局限性,实现大肠杆菌连续发酵生产L-缬氨酸。
高效的微生物发酵通常依赖于细胞的大规模聚集,进而形成生物膜。特别是,具有高耐受性的生物膜相比浮游细胞能更好地抵御恶劣环境。此外,借助固定化载体,生物膜可进一步增强发酵的可持续性和连续性。许多研究致力于增强大肠杆菌的生物膜形成。例如,通过过表达fimH基因,大肠杆菌W1688的生物膜量比原始菌株提高了75.9%,在分批发酵中L-苏氨酸产量从10.5 g/L提高到14.1 g/L,在连续发酵中进一步提高到17.5 g/L,生产力显著提升。同样,通过过表达PotD(一种亚精胺/腐胺结合周质蛋白)刺激了大肠杆菌BL21(DE3)的生物膜形成。这些发现强调了生物膜介导的催化对发酵过程的积极影响。
强大的生物膜形成保证了强健和高产的细胞工厂,进而提升了整体过程生产力。同时,代谢工程策略为L-缬氨酸的高效外排带来了巨大希望。通过理性代谢工程和基于转录组分析及计算机模拟基因组规模代谢网络的基因敲除模拟的逐步改进,VAMF菌株过表达ilvBN、ilvCED、ygaZH和lrp基因,在分批培养中从20 g/L葡萄糖生产7.55 g/L L-缬氨酸,产率达0.378 g/g。此外,Hao等人通过优化丙酮酸供应、外排系统和氧化还原平衡,使大肠杆菌菌株能够生产84 g/L L-缬氨酸,产率0.41 g/g,生产力2.33 g/L/h。Zhang等人设计了自我进化工程和代谢工程策略,通过高葡萄糖适应性培养系统筛选优良表型,发现大肠杆菌从非生产菌转变为能够产生高达6.62 g/L的L-缬氨酸生产菌。这些研究取得了相当进展,但大多数策略受限于分批处理的局限性,尚未为长期稳定的L-缬氨酸生产提供可持续的解决方案。此外,值得注意的是,细胞生长与L-缬氨酸生物合成之间存在权衡。当这种平衡被打破时,丙酮酸分配转向核心代谢途径,过度强调产物合成可能导致生物量不足,降低生产力和产率。因此,开发一种能够巧妙操控生物膜形成和代谢调控的高效方法,将有助于L-缬氨酸连续发酵的可行性和稳定性。
七、研究结果
结果1、鞭毛运动基因对大肠杆菌生物膜形成的影响
为探究鞭毛运动相关基因对大肠杆菌生物膜形成的作用,研究选取了motA、motB、fliA、flgM、flgN、flgK和flgL等基因进行遗传操作。通过质粒过表达构建了相关基因的过表达菌株,同时利用CRISPR-Cas9系统构建了fliA、flgN、flgK和flgL的敲除菌株。结晶紫染色半定量分析表明,+fliA和+flgK+L菌株的生物膜形成较起始菌株E. coli 045分别显著提高了41.14%和39.87%,而敲除菌株则呈现相反趋势。
透射电镜分析显示,与E. coli 045相比,+fliA和+flgK+L菌株的鞭毛数量明显增加,其中+flgK+L菌株不仅表现出更多鞭毛,鞭毛长度也显著延长,证实fliA和flgK+L在鞭毛表型中发挥重要调控作用。游动和群集运动实验表明,motA+B、fliA和flgK+L的过表达显著增强了细胞运动性,而其他基因影响甚微。菌落形态分析显示,过表达菌株的菌落直径更大、表面图案更复杂、厚度更明显。
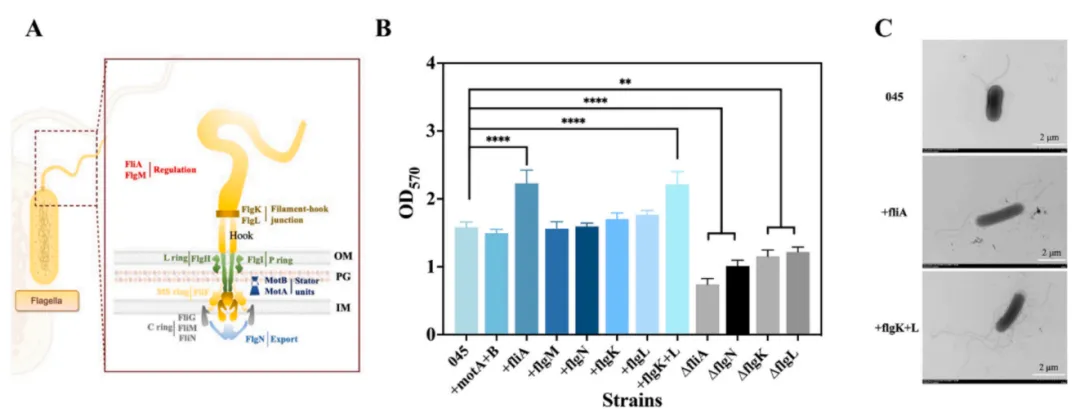
图1 鞭毛相关基因
结果2、新型氰胺诱导表达系统的构建及其增强生物膜形成
基于鞭毛运动相关基因对生物膜形成的积极影响,研究构建了一种新型氰胺诱导表达系统,以进一步增强生物膜发育,同时在生长阶段降低杂菌污染风险。虽然氰胺具有一定细胞毒性,但10 mM氰胺对细胞生长影响最小,且对主要污染源蜡样芽孢杆菌具有显著的抑制效果。
为实现氰胺诱导表达系统,研究对酿酒酵母来源的DDI2和DDI3启动子进行密码子优化以适配大肠杆菌。令人惊讶的是,两个DDI启动子均表现出温度不依赖性诱导,这对大肠杆菌的恒温发酵十分有利。以Ptrc-eGFP菌株为对照,荧光强度分析表明DDI3启动子在10 mM氰胺下诱导效率最高。qRT-PCR定量分析证实,DDI3启动子在选定诱导条件下有效驱动了fliA、flgK和flgL的转录。
值得注意的是,DDI3启动子的引入不仅增加了鞭毛数量,还延长了鞭毛长度。菌株PDDI3-fliA和PDDI3-flgK+L的生物膜形成分别提高了54.7%和68.8%。SEM和CLSM图像显示,通过过表达fliA和flgK+L介导的鞭毛运动增强了细胞聚集,形成了更致密、更有结构的生物膜。
在游离细胞发酵中,E. coli 045、PDDI3-fliA和PDDI3-flgK+L的L-缬氨酸产量分别为84.42 g/L、87.35 g/L和65.64 g/L。PDDI3-fliA的生产速率(2.56 g/L/h)和葡萄糖转化率(0.46 g/g)也略高于E. coli 045(2.23 g/L/h和0.42 g/g)和PDDI3-flgK+L(1.97 g/L/h和0.32 g/g)。然而,在固定化连续发酵中,PDDI3-fliA未能维持游离细胞发酵中的协同特性,表明仅调控鞭毛相关基因和增强生物膜形成不足以解决连续发酵系统中L-缬氨酸产量下降的问题。
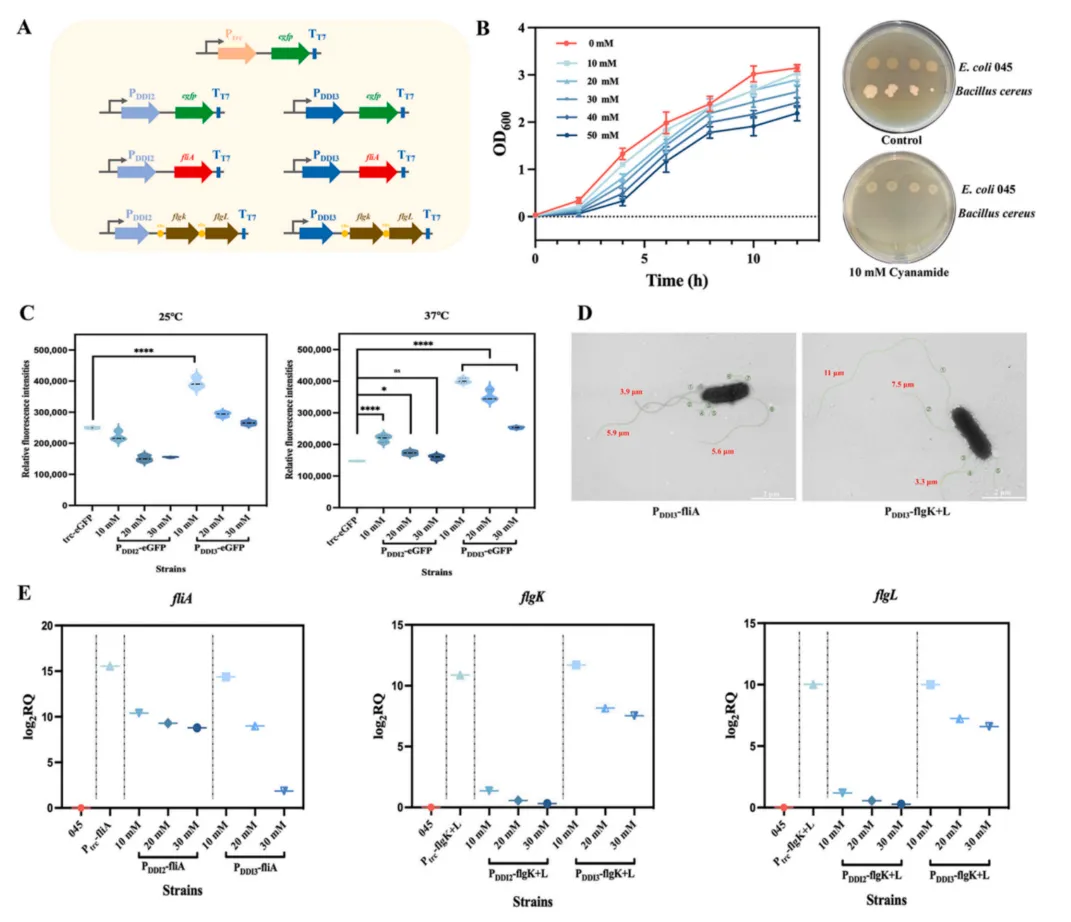
图2 评估系统
结果3、蓝光激活的光遗传调控L-缬氨酸代谢及两阶段调控策略在连续发酵中的应用
除在生长阶段构建氰胺诱导表达系统促进生物膜形成外,研究还通过蓝光激活进一步调控L-缬氨酸代谢通量。以ilvE为报告基因,筛选了组成型启动子PBS76、厌氧启动子Pdih和蓝光诱导型光遗传质粒pDawn。尽管原始两阶段发酵过程包括好氧生长阶段和随后的厌氧催化阶段,但研究发现蓝光诱导的pDawn质粒实现了最高的ilvE表达。值得注意的是,虽然trc启动子具有高诱导表达特性,但ilvE的表达明显低于pDawn。在蓝光诱导下,L-缬氨酸代谢途径关键基因ilvC、ilvD、ilvE、ilvH和ilvI的表达显著增强,有力验证了光遗传调控在L-缬氨酸代谢途径中的可行性。
在低于900 lx的光强下,pDawn-ilvCDE与E. coli 045生长趋势相似,而pDawn-ilvIH出现生长抑制,可能归因于ilvIH过表达引起的代谢失衡或辅因子耗竭。在给定光强下,生物膜形成差异表明300 lx和600 lx的影响可忽略,而在900 lx时抑制作用显著,尤其是pDawn-ilvIH菌株。因此,成功构建了调控L-缬氨酸生物合成途径关键代谢基因的蓝光诱导系统。
在各测试基因中,ilvCDE被发现最为有效,被选用于增强L-缬氨酸生产。游离细胞发酵实验中,在36小时,E. coli 045、pDawn-ilvCDE和pDawn-ilvIH的L-缬氨酸产量分别达到85.12 g/L、90.87 g/L和48.52 g/L。其中,pDawn-ilvCDE的平均生产速率和葡萄糖转化率分别为2.41 g/L/h和0.44 g/g,高于E. coli 045和pDawn-ilvIH。出乎意料的是,pDawn-ilvIH表现出明显的L-缬氨酸产量和细胞生长下降,即使延迟蓝光诱导4小时也未能改善。
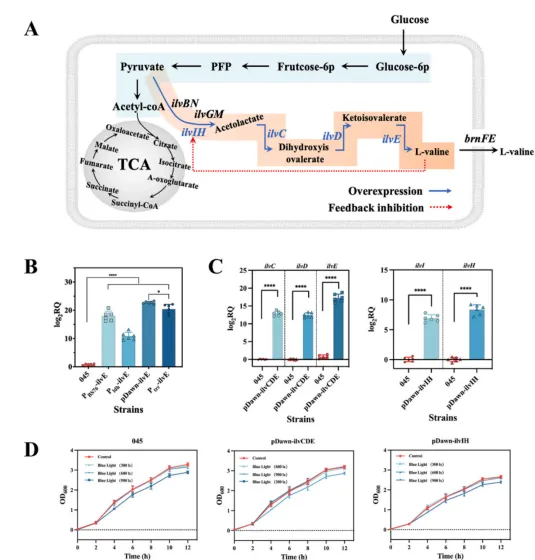
图3 系统构建
结果4、两阶段调控策略在连续发酵中的整合应用
基于上述研究,将生长阶段的氰胺诱导生物膜形成系统与生产阶段的蓝光激活代谢调控系统整合,构建了双调控菌株PDDI3-fliA+pDawn-ilvCDE。在50 L生物反应器中,以棉纤维为固定化载体,采用两阶段发酵策略:生长阶段添加10 mM氰胺诱导fliA表达促进生物膜形成,生产阶段开启蓝光(600 lx)激活ilvCDE表达增强L-缬氨酸合成。
该菌株在连续发酵中表现出卓越性能,稳定运行462小时,L-缬氨酸产量达71.63 g/L,葡萄糖转化率0.57 g/g,生产强度2.05 g/L/h。与对照菌株相比,PDDI3-fliA+pDawn-ilvCDE的L-缬氨酸产量提高了13.92%,转化率提高了约15%。这是迄今报道的大肠杆菌中最高的葡萄糖-to-L-缬氨酸转化率。
进一步分析表明,两阶段调控策略成功解耦了细胞生长与产物合成之间的矛盾:生长阶段通过氰胺诱导fliA表达增强生物膜形成,促进细胞聚集和固定化,为后续连续发酵奠定基础;生产阶段通过蓝光瞬时激活ilvCDE表达,在不影响细胞活性的前提下显著提升代谢通量。这种时空分离的调控模式有效避免了代谢负担对细胞生长的负面影响,实现了高产与稳定的统一。
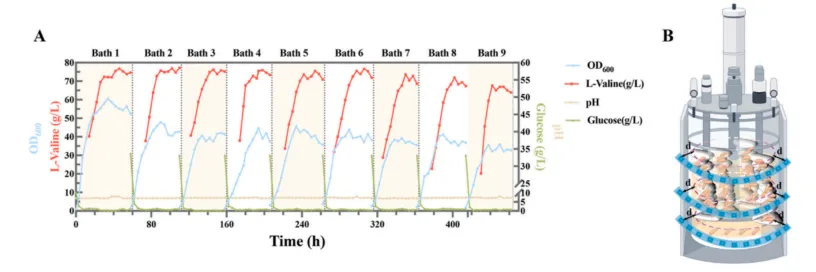
图4 两阶段连续发酵
八、讨论
本研究通过整合生物膜工程和光遗传学代谢调控,成功开发了一种两阶段连续发酵策略用于高效生产L-缬氨酸。研究发现fliA介导的鞭毛功能和运动性影响大肠杆菌045的生物膜形成。在10 mM氰胺诱导下,菌株PDDI3-fliA在生长阶段的生物膜形成提高了54.7%。值得注意的是,通过光遗传调控瞬时激活代谢通量中的ilvCDE显著提高了生产阶段的催化效率,使L-缬氨酸产量提高13.92%。最终,双调控菌株PDDI3-fliA+pDawn-ilvCDE在50 L生物反应器中连续发酵462小时表现出持续性能,实现葡萄糖-to-L-缬氨酸转化率0.57 g/g和生产强度2.05 g/L/h,创下迄今报道的最高转化率记录。
本研究的创新点在于:首次将氰胺诱导系统应用于大肠杆菌生物膜工程,实现生长阶段的可控生物膜形成;首次将光遗传学调控引入L-缬氨酸代谢途径,实现生产阶段代谢通量的精准瞬时激活;通过两阶段时空分离调控,成功解耦细胞生长与产物合成的矛盾。这些发现为将微生物生长与产物合成相耦合提供了宝贵的见解和实用策略,为更高效的生物制造铺平了道路。该策略具有良好的通用性,可望扩展到其他代谢产物的连续发酵生产。
