中科大刘扬中、南京师范大学刘红科ACS Nano!!开发肿瘤内点击化学工厂,协同诱导新型细胞死亡通路
- 2026-05-17 14:59:44
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

近日,中国科学技术大学刘扬中教授团队与南京师范大学刘红科教授团队合作,在《ACS Nano》期刊上发表了一项创新研究成果。该研究针对肿瘤治疗中的选择性诱导细胞死亡难题,开发了一种基于铜触发生物正交反应的“肿瘤内点击化学工厂”策略。这一方法能够在肿瘤细胞内原位合成细胞毒性物质,特异性诱导二硫化物死亡和铜死亡两种新型程序性死亡通路,为精准癌症治疗提供了新思路。二硫化物死亡是近期发现的细胞死亡机制,其关键调控蛋白SLC7A11在多种癌细胞中高表达,使得肿瘤细胞在代谢应激状态下更易发生二硫化物应激。然而,如何在肿瘤组织中特异性激活这一死亡通路一直面临挑战,本研究通过精巧的生物正交设计成功解决了这一难题。
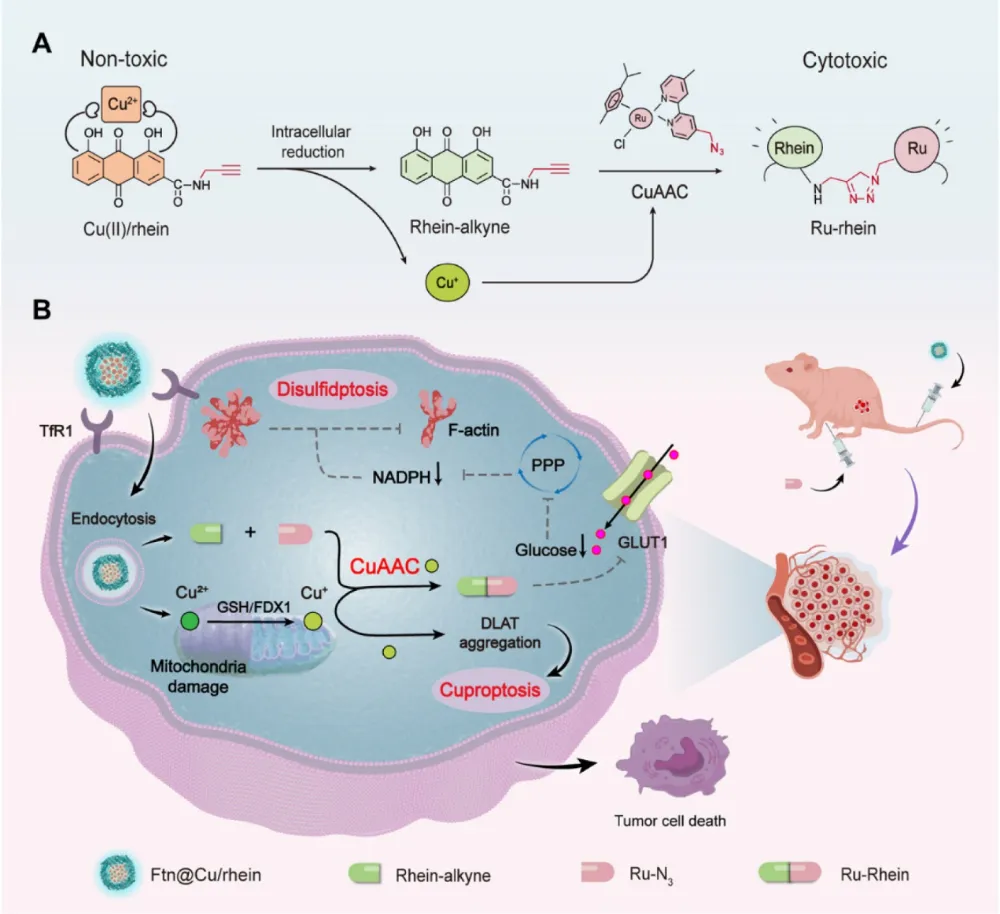
研究团队设计了一种双前药系统,其中一种前药是叠氮修饰的钌配合物(Ru–N₃),另一种是炔烃偶联的大黄酸衍生物与铜形成的配位复合物(Cu/rhein)。为提高肿瘤靶向性,研究人员将Cu/rhein包载于具有天然肿瘤靶向能力的铁蛋白纳米笼中。当这两种前药同时递送至肿瘤区域后,细胞内环境将Cu(II)还原为具有催化活性的Cu(I),进而启动铜催化的叠氮-炔烃环加成反应。这一生物正交反应在肿瘤细胞内原位生成细胞毒性产物Ru-rhein加合物,而正常细胞由于前药浓度较低,几乎不受影响。这种靶向激活策略有效避免了传统化疗药物的全身毒性问题,通过空间控制实现了治疗效应的局部化,显著提高了治疗的安全性指标。
生成的Ru-rhein通过下调葡萄糖转运蛋白1(GLUT1)的表达,降低肿瘤细胞内的葡萄糖摄取和NADPH水平,破坏氧化还原稳态,导致二硫键异常积累,从而诱发二硫化物死亡。同时,铜配合物释放的铜离子在细胞内蓄积,通过与三羧酸循环中的脂酰化线粒体酶结合,诱导线粒体功能障碍,引发铜死亡。这两种死亡通路产生协同效应,在体外和荷瘤小鼠模型中均显示出显著的抗肿瘤效果。该研究不仅验证了生物正交化学在活体层面的可行性,还为利用肿瘤特异性代谢弱点开发精准疗法开辟了新途径,有望推动基于新型细胞死亡通路的肿瘤治疗策略向临床转化。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
