今天给大家分享南京医科大学的重磅文章,一个意外的发现,让研究人员找到了人类原肠干细胞构建的钥匙!所以做实验时还是要细心观察各种现象!
打破多能干细胞培养的“纯种”魔咒
多能干细胞 (PSCs) 是再生医学的基石。但现有的培养体系存在一个根本性局限:它们只能稳定维持单一类型的细胞。这就像一个只有工程师,没有产品经理和设计师的公司,无法协同工作。
胚胎发育的真相恰恰相反。原肠胚时期,外胚层、中胚层、内胚层以及胚外组织细胞紧密互作,通过复杂的信号网络,精确引导组织塑形和器官发生。
传统的PSC培养,人为切断了这种细胞间的天然“社交网络”。结果就是,当这些“社交孤立”的干细胞被诱导分化或移植体内时,往往形成无序、混乱的畸胎瘤,而非结构化的组织。
如何在一个培养皿中,捕获并稳定维持一个包含多谱系、能够相互对话、并具备有序自组织潜能的细胞群体?这成为干细胞领域亟待攻克的关键瓶颈。
为了攻克这一难题,2025年,南京医科大学沙家豪教授、袁艳教授、张浩博后与德克萨斯大学西南医学中心吴军教授团队在顶级期刊《Cell Research》上发表了最新研究成果。

DOI/链接:https://doi.org/10.1038/s41422-025-01146-z
核心速递
一分钟速读: 研究团队通过特定的筛选,建立了一种全新的、可长期稳定传代的“人类原肠干细胞”(hGaSCs)体系。该体系颠覆性地在一个培养皿中同时包含了外胚层、中胚层、内胚层、羊膜和原始生殖细胞等多种谱系。更重要的是,hGaSCs在体内移植后能自组织形成有序的胚胎样结构和早期器官,而非混乱的畸胎瘤,为再生医学和发育生物学提供了前所未有的研究平台。
“细胞大杂烩”的有序共生:GK10培养基如何锁定原肠发育关键窗口?
传统PSC培养追求的是“纯净”,而这项研究反其道而行之,目标是创造一个稳定的“细胞生态系统”。
实验设计:从PGCLC分化中意外“截胡”
研究的起点颇具巧思。团队注意到,在人类原始生殖细胞样细胞 (hPGCLCs) 的诱导过程中,会出现一个短暂的、混合了多种细胞类型的过渡状态。
他们敏锐地抓住这个分化的“十字路口”。通过对hPGCLC诱导第2天的细胞进行单细胞测序分析,发现这群细胞的转录组特征与真实人类CS7阶段(原肠期)的原条上胚层细胞高度相似。
接下来是关键一步:如何将这个稍纵即逝的“混合状态”稳定下来?团队通过大规模的小分子和生长因子筛选,最终锁定了一个包含Forskolin、hSCF和Rolipram的极简组合,命名为GK10培养基。
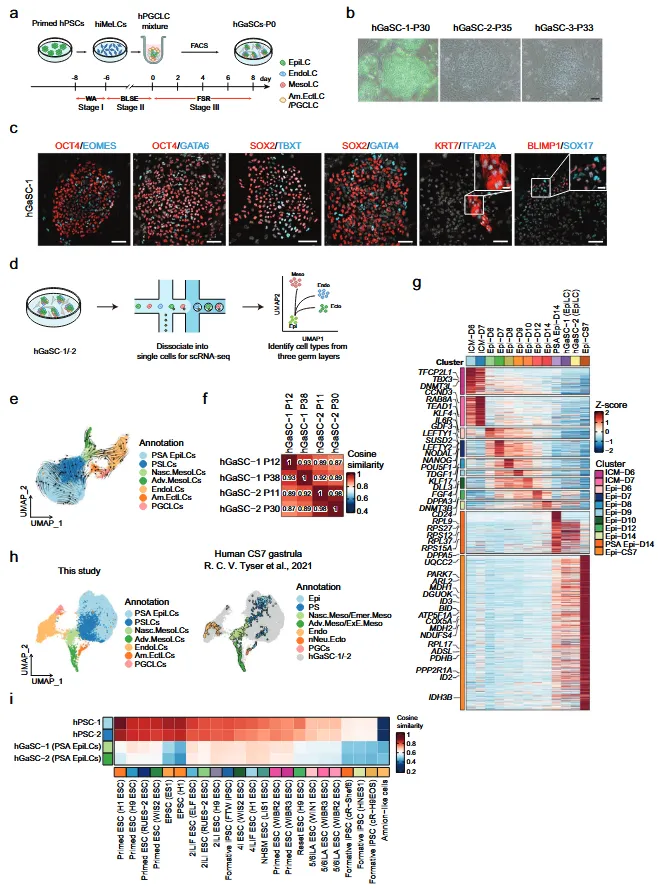
Figure 1. Establishment of stable hGaSCs.
机制拆解:一个能“生”也能“养”的细胞群落
在GK10培养基中,这群细胞成功实现了长期稳定传代(超过30代),并被正式命名为人类原肠干细胞(hGaSCs)。
1. 稳定的异质性: 免疫荧光染色证实,hGaSCs并非单一细胞类型。它是一个稳定的“嵌合体”,包含了OCT4+的上胚层样细胞 (EpiLCs)、GATA4+的内胚层样细胞、TBXT+的中胚层样细胞、GATA3+的羊膜外胚层样细胞以及SOX17+/BLIMP1+的原始生殖细胞样细胞。
2. EpiLCs是“发动机”: 谁是这个多种细胞群落的“维生核心”?单细胞克隆实验给出了答案。单个分离出的EpiLC可以重新建立起包含所有谱系的完整hGaSC克隆。而其他谱系的细胞,如内胚层样细胞,则不具备这种克隆再生能力。这说明,EpiLCs是hGaSC体系自我更新和维持多谱系平衡的驱动源。
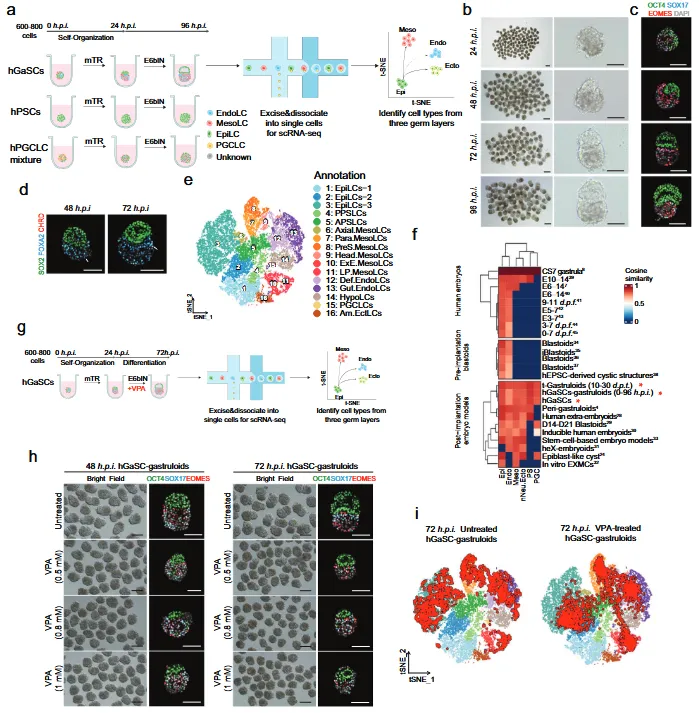
Figure 2. Structure, morphology, and transcriptional characterization of hGaSC-gastruloids.
颠覆性验证:从畸胎瘤到有序器官发生
hGaSCs最惊人的能力,在于其强大的体内自组织潜能。
当研究人员将传统的hPSCs移植到免疫缺陷小鼠的睾丸曲细精管时,形成的是典型的、结构混乱的畸胎瘤。
然而,当他们移植hGaSCs时,结果截然不同。hGaSCs没有形成畸胎瘤,而是在10-20天内自组织形成模拟人类CS7阶段原肠胚的高度有序结构,研究者将其命名为t-Gastruloids。
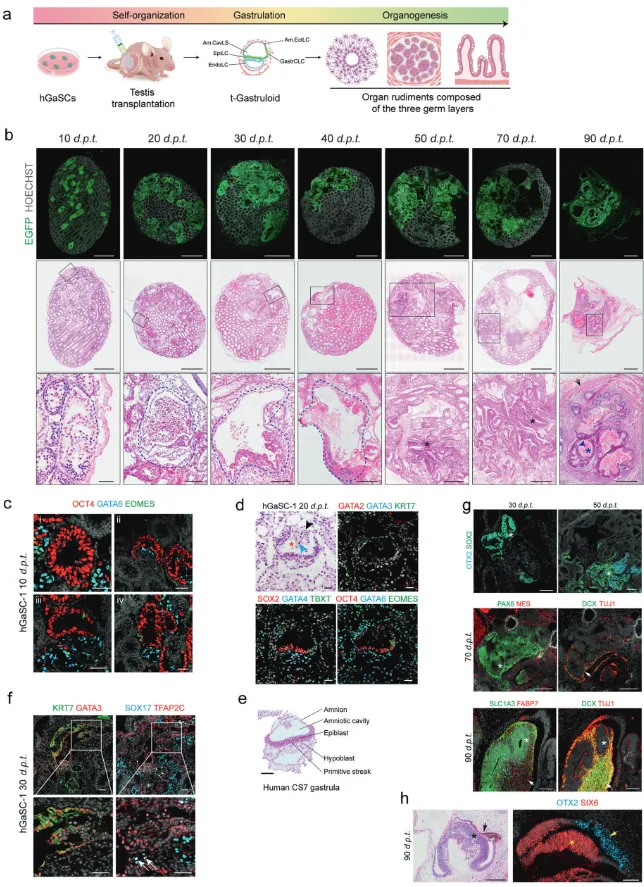
Figure 3. Morphological and transcriptional characterization of t-Gastruloids formation from hGaSCs transplanted testes.
随着时间推移 (70-90天),这些t-Gastruloids进一步发育,形成了包括神经上皮、肠上皮、软骨样组织,甚至分化出了具备视杯结构的早期眼部雏形。单细胞测序数据证实了这种有序、分步的发育轨迹,与人类胚胎发育进程高度吻合。这首次证明,一个预先建立的多谱系干细胞“微生态”,是实现体内有序组织再生的关键。
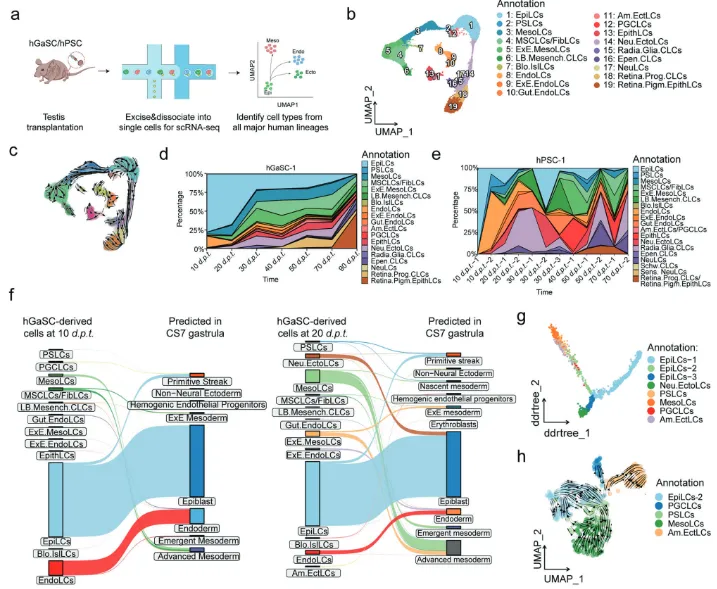
Figure 4. Single-cell visualization of the ordered gastrulation pattern of hGaSCs in the testis.
逻辑导图
hPSCs -> 诱导分化至hPGCLCs-d2 (原肠期过渡态) -> GK10培养基 (Forskolin+hSCF+Rolipram) 筛选 -> 捕获并稳定培养hGaSCs (多谱系共存) -> 体内移植 -> 自组织形成t-Gastruloids -> 绕开畸胎瘤,实现有序的早期器官发生
主笔点评:从“细胞纯化”到“生态构建”的范式转移
本质洞察: 这项工作在底层逻辑上,挑战了干细胞领域长期以来对“细胞纯度”的执念。它揭示了,实现高级别的自组织和器官发生,关键可能不在于起始细胞有多“纯”,而在于起始细胞群落的“生态多样性”和谱系是否完备。hGaSCs的成功,本质是从细胞培养的“纯种农业”思维,转向了“模拟生态系统”的构建。
局限与挑战: hGaSCs虽然实现了有序发育,但目前仍无法形成完整的胚胎体轴和“管中管”结构,距离完整胚胎模型或功能性器官还有很长距离。此外,其体外培养依赖于MEF饲养层,如何实现化学成分明确的无饲养层培养,是走向标准化的关键一步。
灵魂发问: hGaSCs在睾丸微环境中展现了惊人的有序发育能力,远超体外3D培养。这是否意味着,当前所有类器官或胚胎模型研究,都过度忽视了“物理微环境”(如曲细精管的空间限制和机械力)和“生化微环境”(如支持细胞分泌的复杂因子)的决定性作用?我们距离在体外复刻这种“终极”培养环境,还有多远?
尾语
你认为未来再生医学的方向,是继续优化单一谱系的分化方案,还是转向构建更复杂的“细胞生态系统”?在评论区留下你的思考。欢迎关注、点赞和在看。
明星科学家

教授简介:https://sklrm.njmu.edu.cn/1922/list.htm

教授简介:https://labs.utsouthwestern.edu/wu-jun-lab/people

教授简介:https://sklrm.njmu.edu.cn/yy_18865/list.htm