南京大学医学院附属鼓楼医院心血管内科徐标教授团队长期致力于心肌梗死(MI)后微循环障碍的机制与干预研究,取得了一系列原创性成果。近期,研究团队报道了不饱和脂肪酸Maresin 1(MaR1)在治疗心肌缺血再灌注损伤中发挥显著的保护效应。然而,MaR1基于其循环内易降解、驻留时间短的特点,既往的心肌注射方式并不适用于常规临床途径。为此,研究团队与南京工业大学团队合作,利用微流体策略构建一种偶联心脏靶向肽的脂质体载体,使得药物MaR1可以精准地到达心脏缺血局部,在心肌梗死后微血管阻塞的治疗领域取得重要突破。该研究成果于2026年1月发表于国际化工与工程领域期刊Chemical Engineering Journal (IF=13.2)。该研究首次构建了一种基于心脏靶向肽修饰的MaR1脂质体纳米药物(nano-MaR1),通过调控巨噬细胞极化和抑制单核细胞-血小板聚集,为MVO的治疗提供了全新的纳米干预策略。

心肌梗死(MI)后即使成功实现血运重建,仍约有50%的患者发生微血管阻塞(MVO),这一现象与炎症风暴、微血栓形成密切相关,是目前临床预后不良的独立危险因素。MaR1作为一类促炎症消退介质,具有抗炎、促修复的潜力,但其临床应用受限于体内不稳定、代谢迅速等瓶颈。针对上述挑战,本研究从药物递送系统创新出发,系统性解决了MaR1的稳定性与靶向性问题:
研究亮点:
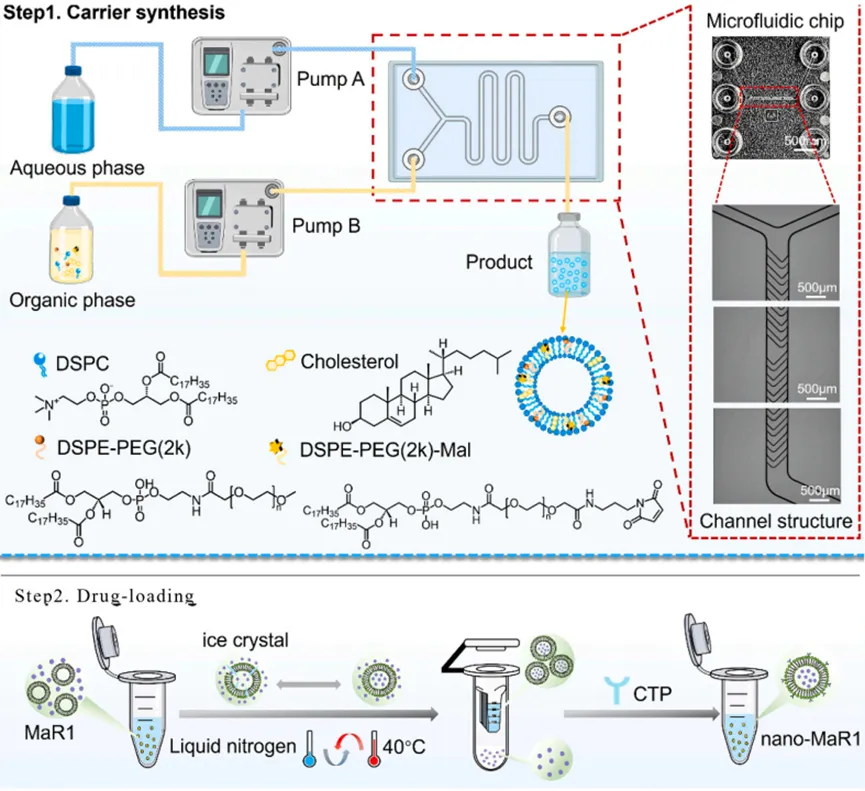
01构建微流控平台精准制备靶向脂质体团队采用微流控混合芯片,通过可控的纳米沉淀结合反复冻融法,成功制备了粒径均一、包封率高、稳定性强的MaR1脂质体,并进一步偶联心脏靶向肽(CTP),构建了具备心肌靶向能力的nano-MaR1。该制备方法具有良好可重复性与规模化潜力。
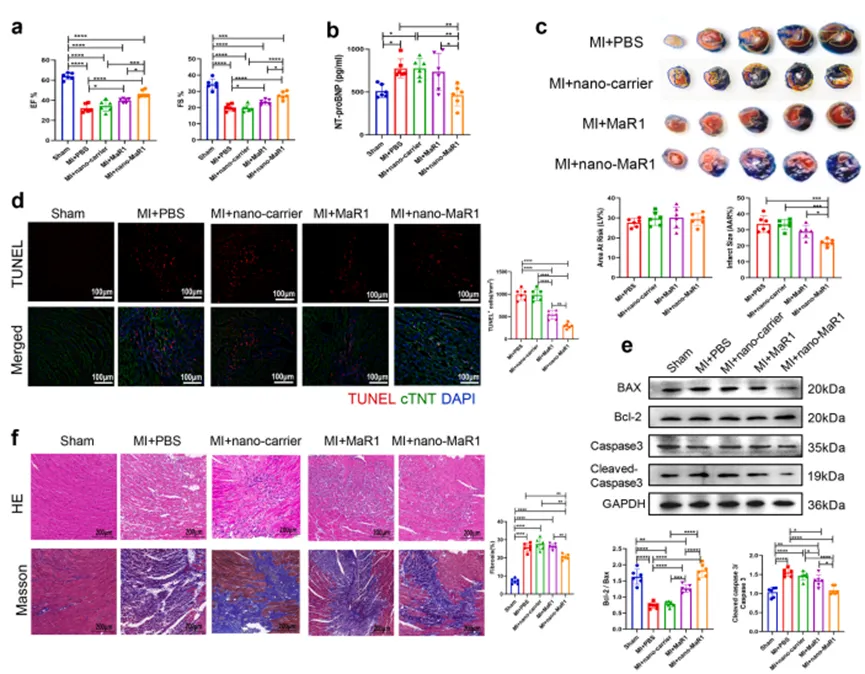
02揭示靶向递送系统的心脏保护效应在心肌缺血再灌注小鼠模型中,nano-MaR1静脉注射后12小时内即在心肌组织中显著富集,有效缩小梗死面积、抑制心肌细胞凋亡和纤维化,并改善心功能。其疗效显著优于游离MaR1,证实了靶向递送系统在提升MaR1生物利用度中的关键作用。
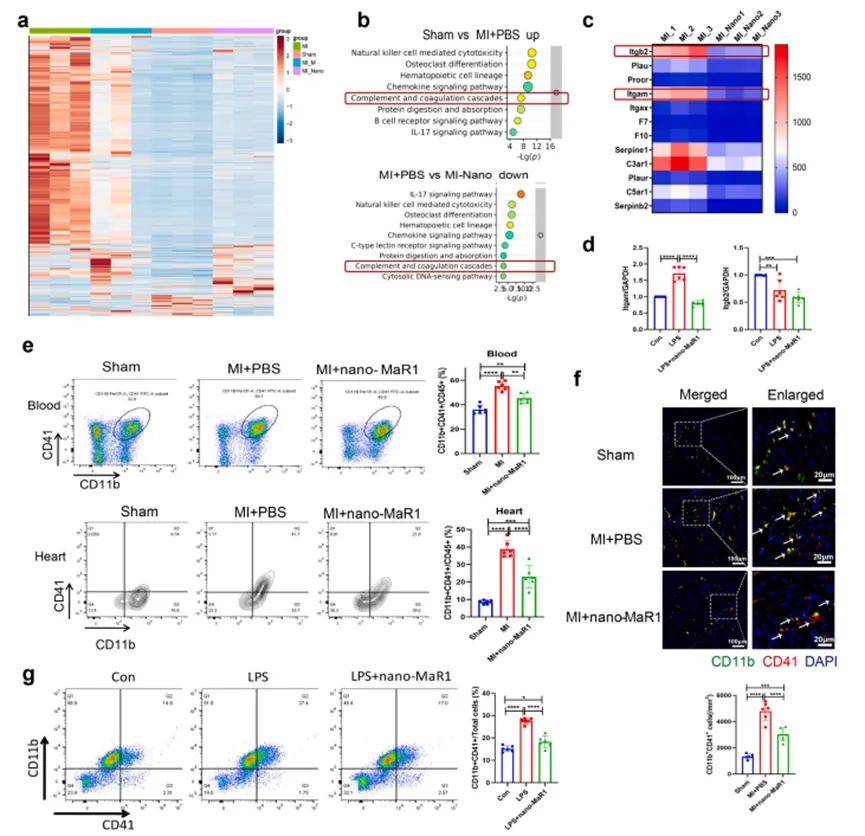
03阐明通过CD11b调控MVO的关键机制研究进一步揭示,nano-MaR1通过下调CD11b表达,抑制单核-血小板聚集(MPAs),减少微血栓形成,同时促进巨噬细胞向M2型极化,减轻局部炎症与氧化应激。CD11b中和抗体实验证实,该分子是nano-MaR1发挥抗MVO作用的核心靶点。
04验证长期疗效与生物安全性在28天观察期内,nano-MaR1持续改善左心室重构,且未引起溶血反应、肝肾功能损伤或主要脏器病理改变,展现出良好的体内安全性和临床应用潜力。
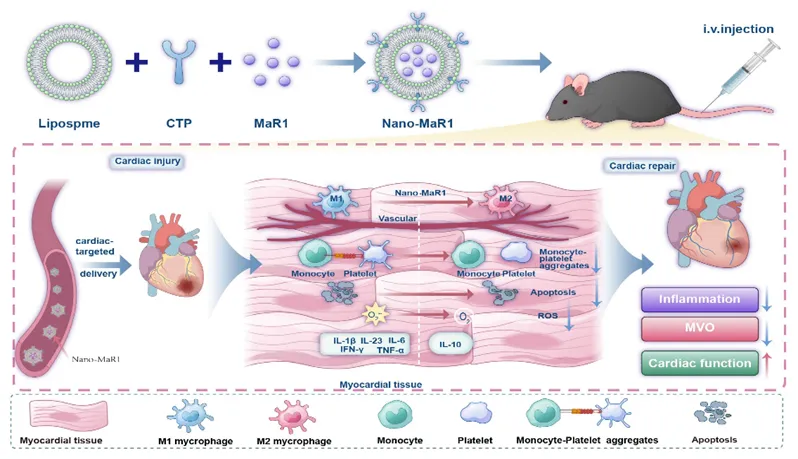
本研究首次将MaR1与心脏靶向脂质体递送系统结合,成功突破了MaR1稳定性差、靶向性弱的瓶颈,系统阐明了其通过CD11b调控单核-血小板互作、抑制MVO的分子机制。nano-MaR1作为一种兼具抗炎、促修复、靶向递送三重优势的新型纳米药物,不仅为心肌梗死后微循环障碍的治疗提供了新策略,也为脂质介质类药物的临床转化开辟了新路径。
南京大学医学院附属鼓楼医院心血管内科孙璇副研究员、徐标教授和南京工业大学余子夷教授为本文的通讯作者,南京大学医学院附属鼓楼医院心血管内科赵亚伟博士和南京工业大学张静教授为本文的第一作者。本研究工作得到了国家重点研发计划和国家自然科学基金等项目的资助。
编辑丨王静
审核丨孙璇
终审丨康丽娜