南京医科大学郭兴、刘妍、陈盼盼Neuron!!突破性研究发现:靶向PGAM5可延缓多种渐冻症亚型进展
- 2026-05-08 14:10:14
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

肌萎缩性侧索硬化(ALS)是一种致命的神经退行性疾病,主要特征为运动神经元的进行性退化,导致肌肉萎缩、瘫痪和呼吸衰竭。该疾病在遗传和临床上具有高度异质性,约10%的病例为家族性(fALS),与SOD1、TARDBP、FUS等40多个基因突变相关,而大多数病例为散发性(sALS),可能与衰老、环境因素及细胞应激共同作用有关。尽管近年来在ALS的遗传机制研究方面取得进展,但由于疾病亚型多样,共同致病通路不明确,目前尚无有效治疗方法。线粒体整合应激反应(mtISR)作为连接线粒体功能障碍与细胞适应性反应的核心途径,在维持线粒体稳态中发挥关键作用,但其异常激活的调控机制在疾病背景下尚不清晰。2026年3月11日,南京医科大学郭兴、刘妍和陈盼盼团队在《Neuron》期刊发表研究,通过CRISPR-Cas9筛选发现磷酸甘油酸变位酶5(PGAM5)是ALS多种亚型的共性致病枢纽,为开发广谱疗法提供了新方向。
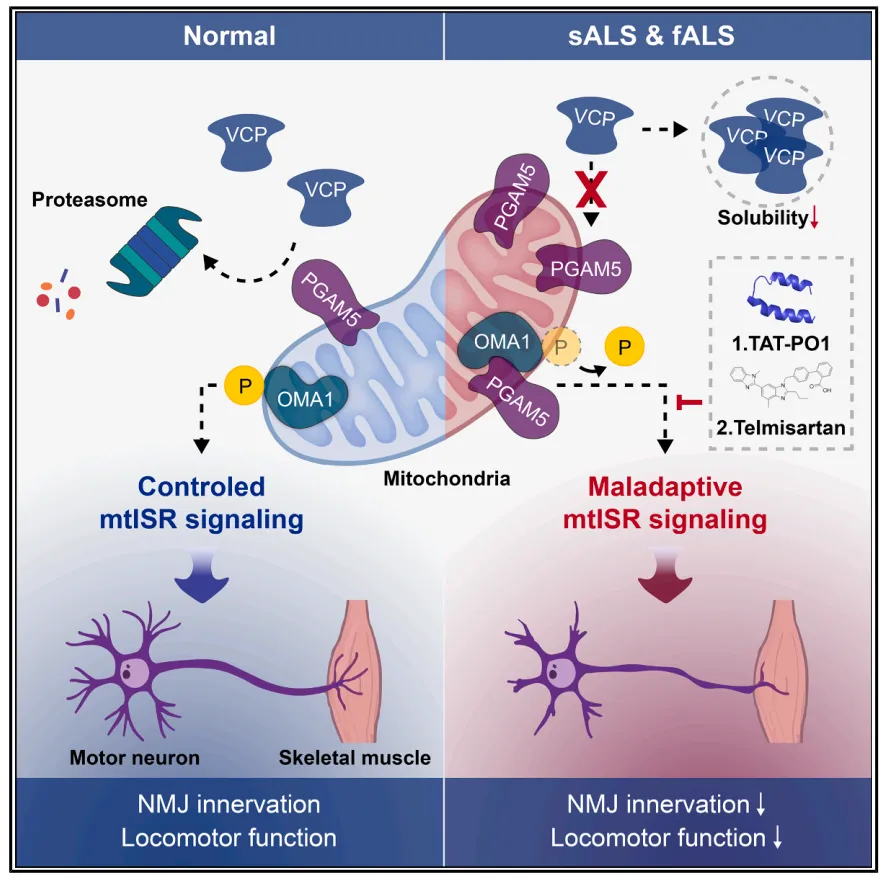
该研究首次通过全基因组筛选将PGAM5确定为ALS发病机制中的关键介质。PGAM5是一种线粒体蛋白,在散发性ALS患者脊髓、家族性ALS模型及小鼠模型中均呈现持续高表达。机制上,PGAM5通过金属肽酶OMA1在Ser223和Ser237位点的去磷酸化被激活,进而驱动mtISR信号通路。这一过程涉及OMA1切割DELE1蛋白,激活HRI激酶,导致eIF2α磷酸化并诱导转录因子ATF4表达,最终引发线粒体应激反应的异常持续。研究发现,PGAM5是含缬蛋白(VCP)的底物,其异常活化会破坏神经肌肉接头功能,加速运动神经元退化和运动缺陷。通过选择性抑制剂TAT-PO1干扰PGAM5-OMA1相互作用,或使用替米沙坦进行药理学抑制,可有效阻断mtISR的过度激活,显著改善ALS模型中的病理表型。这种干预方式不同于传统的eIF2B激活策略,通过重塑mtISR输出,展现出跨亚型的治疗潜力。
该研究的创新点在于揭示了PGAM5-mtISR轴作为ALS亚型间趋同致病通路的核心地位,并验证了其作为药物靶点的可行性。在多种ALS模型(包括散发性和家族性)中,靶向PGAM5均能延缓疾病进展,且作用机制独立于特定基因突变,为开发广谱疗法奠定了理论基础。通讯作者郭兴教授指出,这一发现不仅深化了对ALS异质性背后共同机制的理解,还可能推广至其他线粒体相关神经退行性疾病的研究中。未来工作将聚焦于优化PGAM5抑制剂的特异性与安全性,推动临床转化。本研究由南京医科大学团队完成,郑志隆、杨王菊、陈震等为共同第一作者,成果以开放获取形式发表,为ALS治疗策略提供了新的科学依据。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
