南京大学医学院附属南京鼓楼医院丨SLC6A19 介导色氨酸摄取调控 NAD+/SIRT1 通路抑制肾细胞癌转移的机制研究
- 2026-05-10 22:16:24

前言
本研究基于肾细胞癌转移机制不明且氨基酸代谢重编程参与其转移的背景,先通过 TCGA 数据库和临床样本筛选出与肾癌转移、预后相关的 SLC6A19,验证其在肾癌组织 / 细胞中低表达;再通过体外细胞实验和体内动物模型证实 SLC6A19 过表达可抑制肾癌增殖、迁移侵袭及 EMT 过程;随后通过缺色氨酸培养基、代谢组学、基因敲低实验明确 SLC6A19 依赖色氨酸转运促进 NAD + 从头合成;进一步结合蛋白乙酰化检测、ChIP-qPCR 等验证 NAD + 激活 SIRT1 介导 H3K27 去乙酰化,抑制 NF-κB p65 转录从而阻断 EMT;最后通过生信预测、过表达及双荧光素酶报告实验证实 KLF4 失活是 SLC6A19 低表达的关键原因。研究证实 SLC6A19 是肾癌新型转移抑制基因,KLF4-SLC6A19-NAD+/SIRT1-p65 轴为肾癌转移提供新的治疗靶点。
研究要点解析
研究方法
首先通过生物信息学分析和临床样本验证 SLC6A19 在肾癌中的表达特征及与临床病理特征、预后的关联;其次通过体外细胞功能实验和体内动物模型明确 SLC6A19 对肾癌增殖、转移及 EMT 的抑制作用;接着通过色氨酸耗竭、代谢组学、关键酶敲低实验探究 SLC6A19 依赖色氨酸转运调控 NAD + 从头合成的核心机制;然后结合去乙酰化酶敲低、ChIP-qPCR 等实验阐明 NAD+/SIRT1-H3K27ac-NF-κB p65 轴调控 EMT 的下游分子机制;最后通过生信预测、转录因子过表达、双荧光素酶报告及 ChIP-qPCR 实验明确肾癌中 SLC6A19 低表达的上游调控因素 KLF4;综合上述实验揭示肾癌转移的新型分子通路,为临床治疗提供靶点。
研究结果
SLC6A19 在肾癌组织 / 细胞中显著低表达,其低表达与肾癌高 T 分期、高组织学分级、远处转移相关,高表达则预示患者更好的预后;体外过表达 SLC6A19 可显著抑制肾癌细胞的迁移、侵袭及 EMT 过程,体内可减少肾癌皮下瘤体积 / 重量并抑制肺转移;SLC6A19 的抑癌作用依赖其色氨酸转运功能,耗竭培养基中色氨酸则其抑癌作用消失,且 SLC6A19 过表达可促进肾癌细胞内 NAD + 从头合成,敲低 NAD + 合成关键酶 NMNAT1 会阻断其抑癌作用;SLC6A19 通过 NAD + 激活 SIRT1,介导组蛋白 H3K27 去乙酰化,减少 H3K27ac 在 NF-κB p65 启动子区的富集,抑制 p65 转录及下游 EMT 相关分子表达,敲低 SIRT1 则 SLC6A19 的抑癌作用被阻断;生信预测并验证 KLF4 是 SLC6A19 的上游转录激活因子,KLF4 在肾癌中低表达,其失活是 SLC6A19 低表达的关键原因,且 KLF4 高表达与肾癌患者更好的预后相关。
研究结论
本研究首次证实 SLC6A19 是肾细胞癌的新型转移抑制基因,其在肾癌中因转录因子 KLF4 失活而低表达,且 SLC6A19 通过转运色氨酸促进 NAD + 从头合成,激活 SIRT1 介导的 H3K27 去乙酰化,抑制 NF-κB p65 转录从而阻断 EMT 过程,揭示了 KLF4-SLC6A19-NAD+/SIRT1-p65 这一连接代谢重编程与表观遗传调控的肾癌转移新通路,为肾癌治疗提供了潜在靶点。同时研究也存在局限性,未直接定量色氨酸 - NAD + 从头合成通路中的关键中间代谢物,也未明确该通路与 NAD + 其他合成途径的协同关系,且 SIRT1 在肾癌中调控的下游分子网络尚未完全解析,未来需通过靶向代谢组学、同位素示踪及高通量测序等技术进一步完善机制研究。
图文结果解读
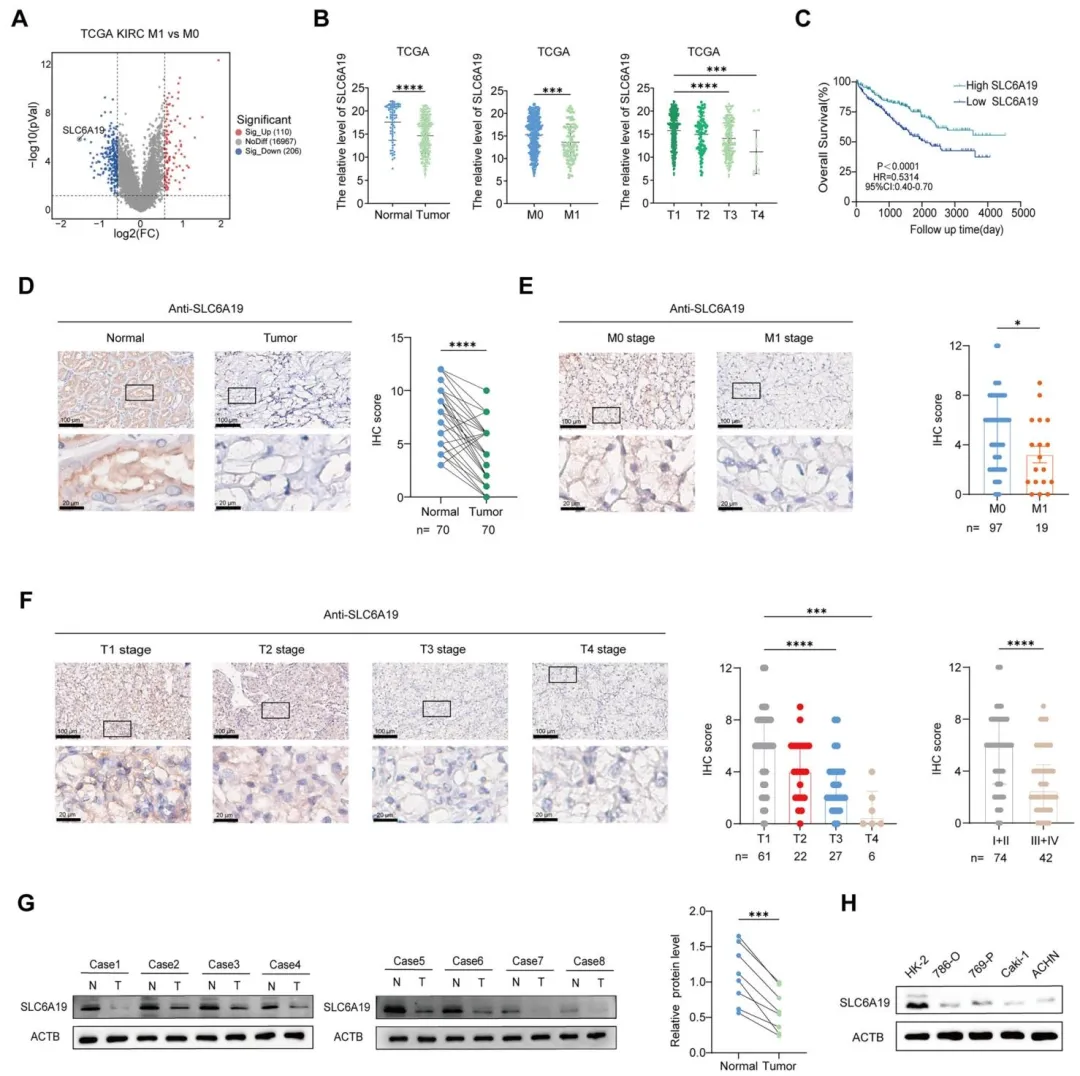
Fig1:通过 TCGA 数据库和临床样本从转录组、蛋白水平验证 SLC6A19 在肾癌组织 / 细胞中低表达,且其低表达与肾癌高 T 分期、远处转移相关,高表达与患者良好预后相关,明确 SLC6A19 是肾癌潜在的抑癌基因。
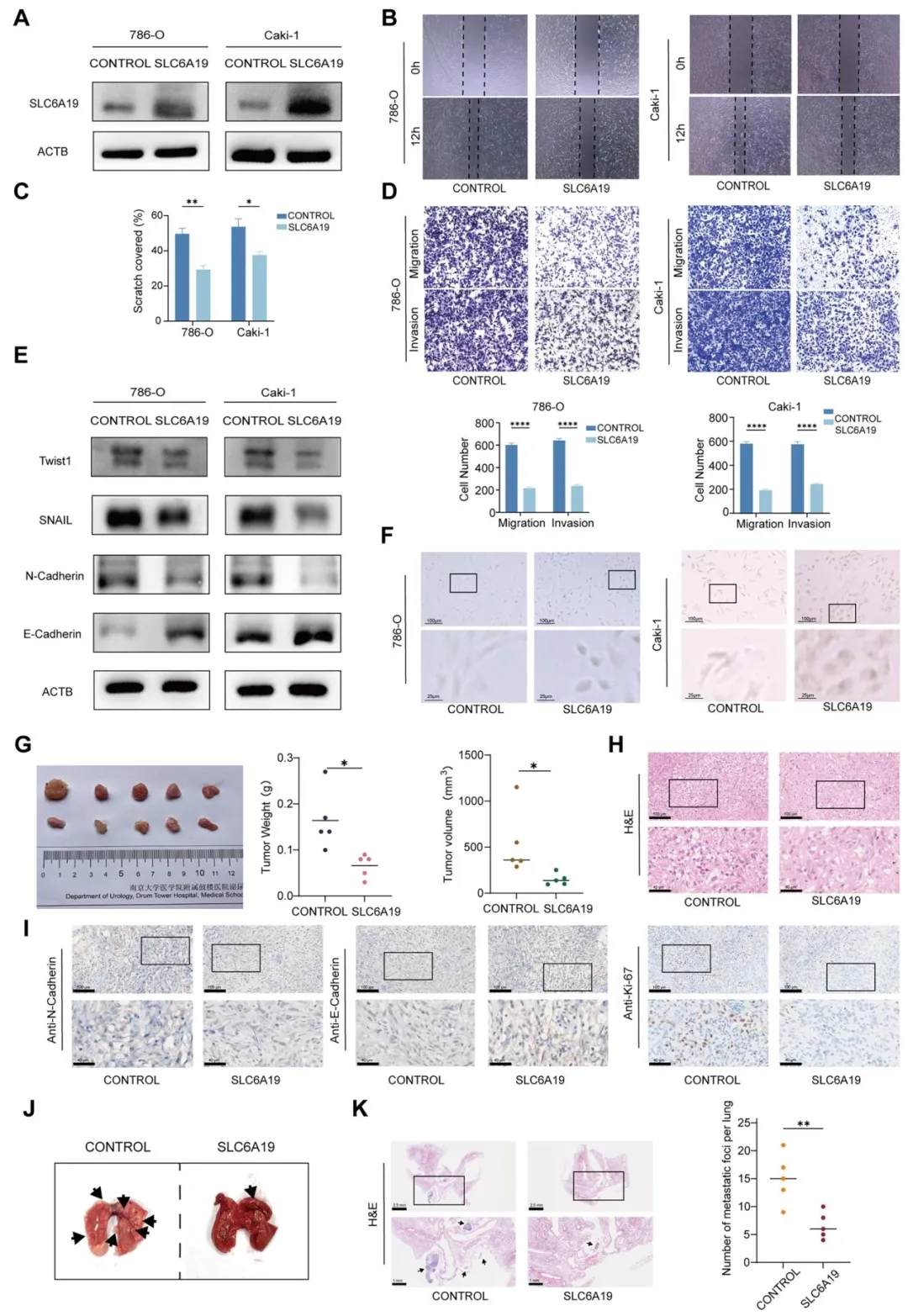
Fig2:通过体外细胞过表达实验验证 SLC6A19 抑制肾癌细胞迁移、侵袭及 EMT 过程,通过体内皮下成瘤和肺转移模型证实 SLC6A19 在体内可抑制肾癌生长和远处转移,明确 SLC6A19 对肾癌进展的体内外抑制作用。
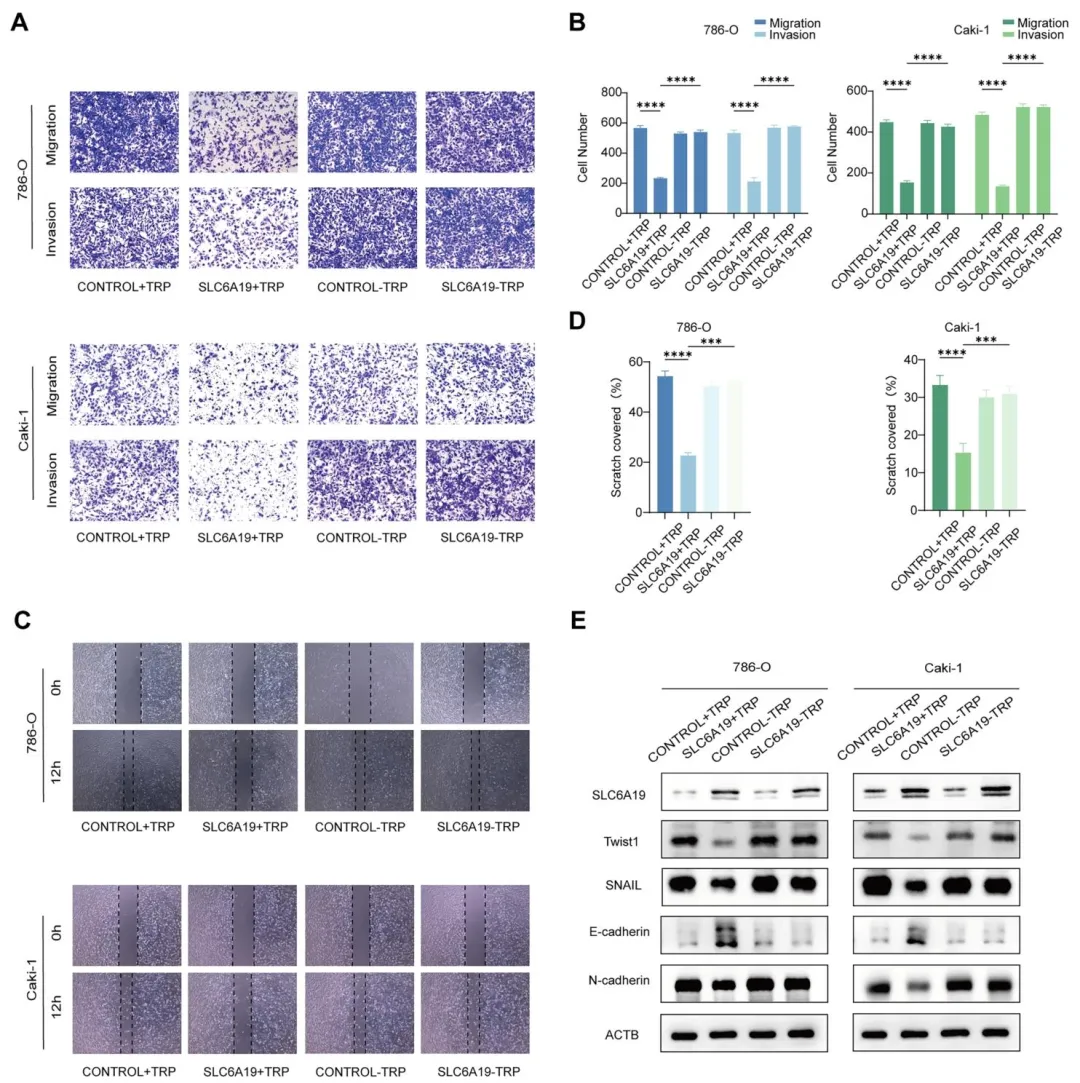
Fig3:通过耗竭培养基中的色氨酸,证实 SLC6A19 对肾癌转移的抑制作用依赖其色氨酸转运功能,色氨酸缺失则其无法调控 EMT 相关分子及肾癌细胞的迁移侵袭能力。
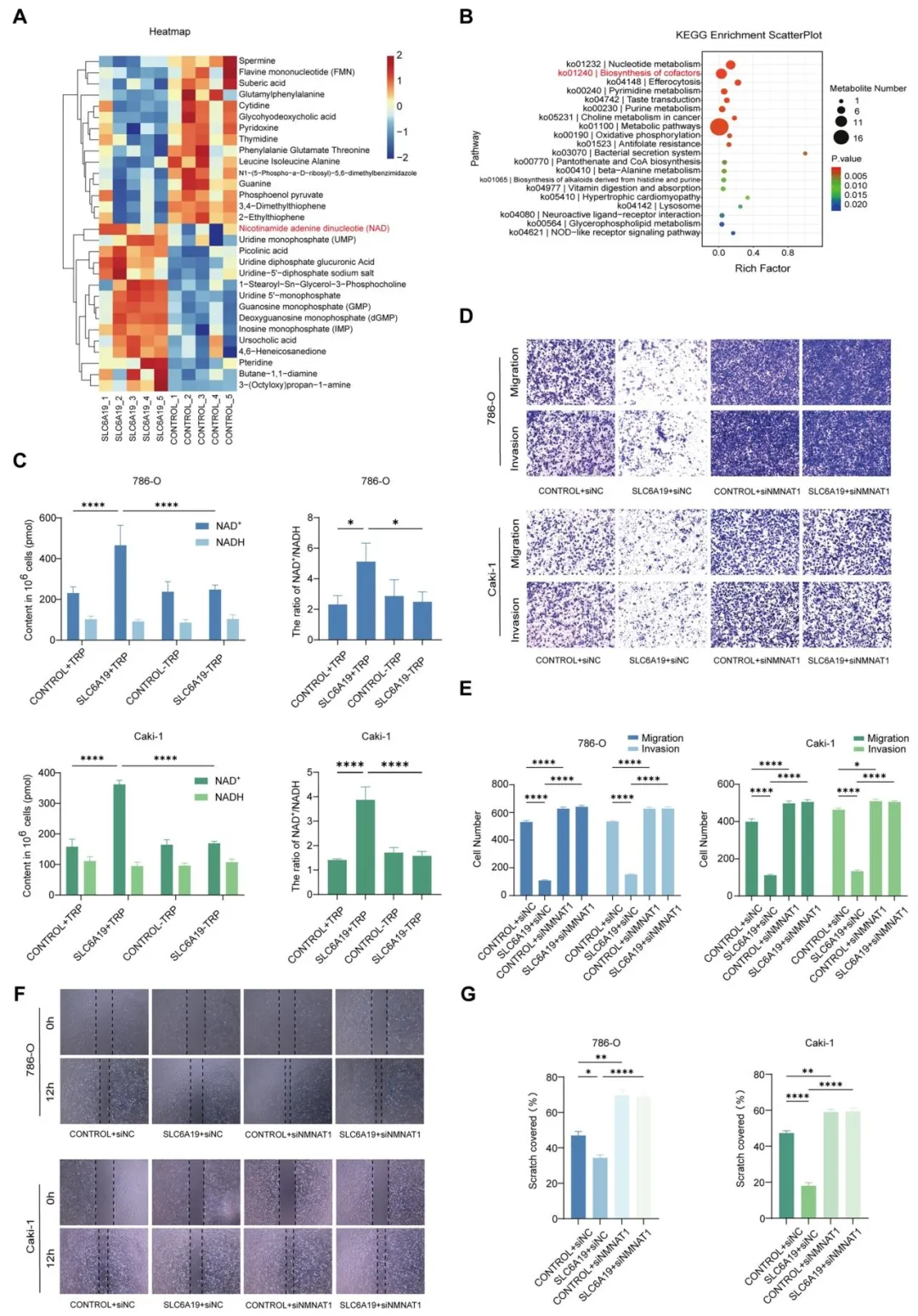
Fig4:通过代谢组学证实 SLC6A19 过表达可升高肾癌细胞内 NAD + 水平,且该过程依赖色氨酸,敲低 NAD + 从头合成关键酶 NMNAT1 会阻断 SLC6A19 的抑癌作用,明确 SLC6A19 通过介导色氨酸转运促进 NAD + 从头合成抑制肾癌转移。
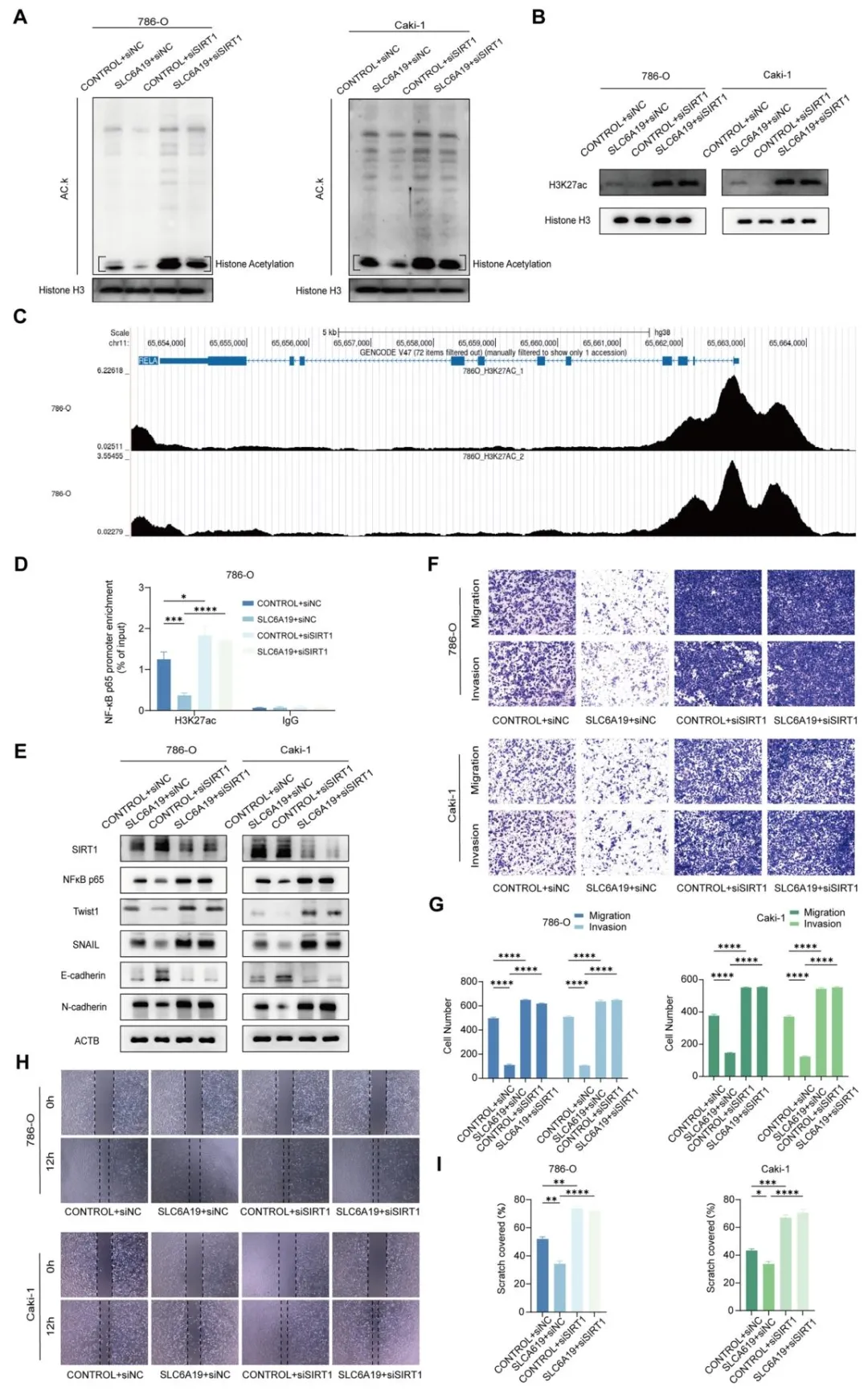
Fig5:证实 SLC6A19 通过 NAD + 激活 SIRT1 介导组蛋白 H3K27 去乙酰化,减少 H3K27ac 在 NF-κB p65 启动子区的结合,抑制 p65 转录及下游 EMT 过程,敲低 SIRT1 会逆转 SLC6A19 的抑癌作用,阐明 SLC6A19 下游调控 EMT 的分子机制。
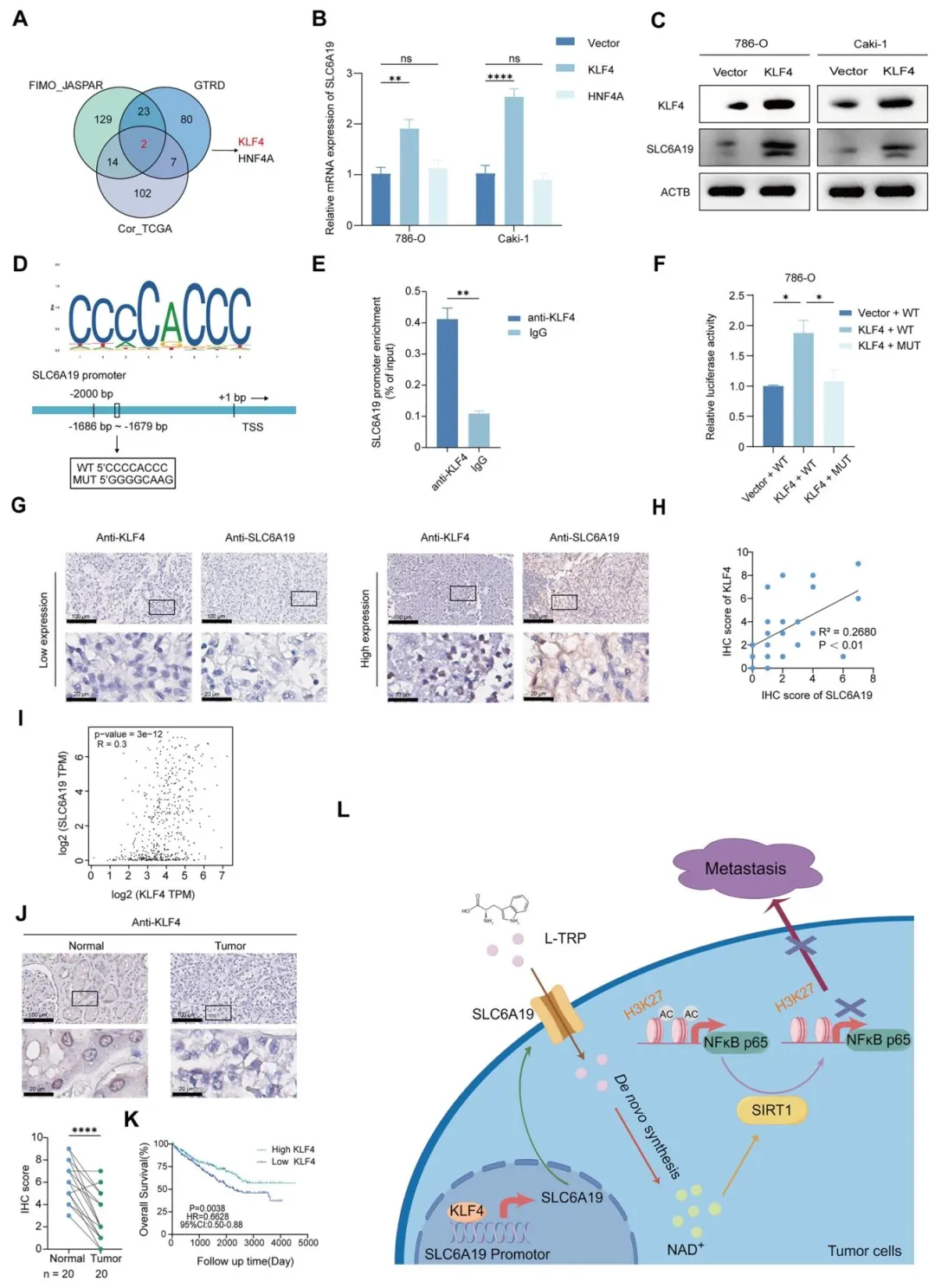
Fig6:通过生信预测、转录因子过表达、ChIP-qPCR 和双荧光素酶报告实验,证实 KLF4 是 SLC6A19 的上游转录激活因子,可直接结合其启动子区促进其转录,且 KLF4 在肾癌中低表达、与 SLC6A19 表达正相关并与患者良好预后相关,明确肾癌中 SLC6A19 低表达的关键原因,最后总结出 SLC6A19 抑制肾癌转移的完整分子机制。
参考文献:Chen Z, Duan R, Chen Z, Tang X, Yang W, Yin H, Chen Y, Cao Y, Guo H, Ding M, Ji C. SLC6A19-mediated tryptophan uptake suppresses renal cell carcinoma metastasis via activating NAD+-dependent deacetylase SIRT1. Oncogenesis. 2025 Nov 7;14(1):38. doi: 10.1038/s41389-025-00580-3. PMID: 41203631; PMCID: PMC12595055.
本文中使用的图片来源Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究