南京医科大学第一附属医院丨2 型糖尿病相关射血分数保留心衰新机制:脂肪细胞胞外囊泡线粒体货物介导心肌细胞功能障碍
- 2026-05-08 05:36:36
文献学习
为探究 2 型糖尿病(T2D)相关射血分数保留心衰(HFpEF)的发病机制并寻找治疗靶点,研究先对 T2D-HFpEF 患者皮下脂肪组织行单核 RNA 测序,发现存在线粒体氧化应激的应激富集脂肪细胞亚群 AD3,且患者循环中脂肪细胞来源胞外囊泡(AdEVs)升高,其线粒体货物氧化修饰增强;随后构建脂毒性脂肪细胞模型,证实脂毒性可诱导脂肪细胞释放富含氧化修饰线粒体成分的 AdEVs;再将该 AdEVs 作用于人心肌细胞,发现其引发心肌细胞活性氧升高、线粒体功能障碍及凋亡,且患者来源 AdEVs 可复现该损伤;最后通过药物干预证实,抑制 EV 生成或清除线粒体活性氧可缓解上述损伤,最终证实 AdEVs 中氧化修饰的线粒体货物是连接脂肪应激与心肌细胞功能障碍的关键,且 AdEV 释放和线粒体活性氧为潜在治疗靶点。

研究背景
射血分数保留心衰(HFpEF)在 2 型糖尿病(T2D)患者中发病率高,现有治疗多为对症治疗且无法延缓疾病进展,脂肪组织通过胞外囊泡(EVs)参与器官间通讯,但其释放的 EVs 中线粒体蛋白的氧化修饰及对 HFpEF 心肌细胞的影响尚不明确,而线粒体功能障碍是糖尿病 HFpEF 的重要特征,应激细胞或通过 EVs 排出受损线粒体成分,T2D 脂肪细胞是否通过该方式向心脏传递代谢毒性仍未知。
研究方案
先对 T2D-HFpEF 患者和非糖尿病对照的皮下脂肪组织做单核 RNA 测序,鉴定脂肪细胞亚群及分子特征,同时检测患者循环 AdEVs 的线粒体货物氧化修饰及与临床指标的关联;再构建 3T3-L1 脂肪细胞脂毒性模型,分离 AdEVs 并分析其成分;随后将脂毒性及患者来源 AdEVs 作用于 AC16 心肌细胞和人诱导多能干细胞来源心肌细胞(hiPSC-CMs),检测心肌细胞线粒体功能、活性氧及凋亡等指标;最后采用 GW4869 抑制 EV 生成、Mito-TEMPO 清除线粒体活性氧,验证干预该通路对心肌细胞损伤的缓解作用。
研究结果
T2D-HFpEF 患者脂肪组织中存在高表达线粒体氧化应激和囊泡分泌通路的 AD3 脂肪细胞亚群,循环中 FABP4+AdEVs 升高且线粒体货物氧化修饰增强,其水平与血浆蛋白羰基、NT-proBNP 及 E/e' 比值正相关;脂毒性脂肪细胞释放的 AdEVs 富含氧化修饰线粒体成分,该 AdEVs 可使心肌细胞活性氧升高、线粒体膜电位耗散、线粒体网络碎裂、氧耗和 ATP 生成减少,激活内源性凋亡并上调心衰标志物;患者来源 AdEVs 可加剧心肌细胞线粒体功能障碍和凋亡;抑制 EV 生成或清除线粒体活性氧可显著缓解 AdEVs 诱导的心肌细胞损伤,且 hiPSC-CMs 模型验证了该脂肪 - 心脏 EV 轴的作用及干预价值。
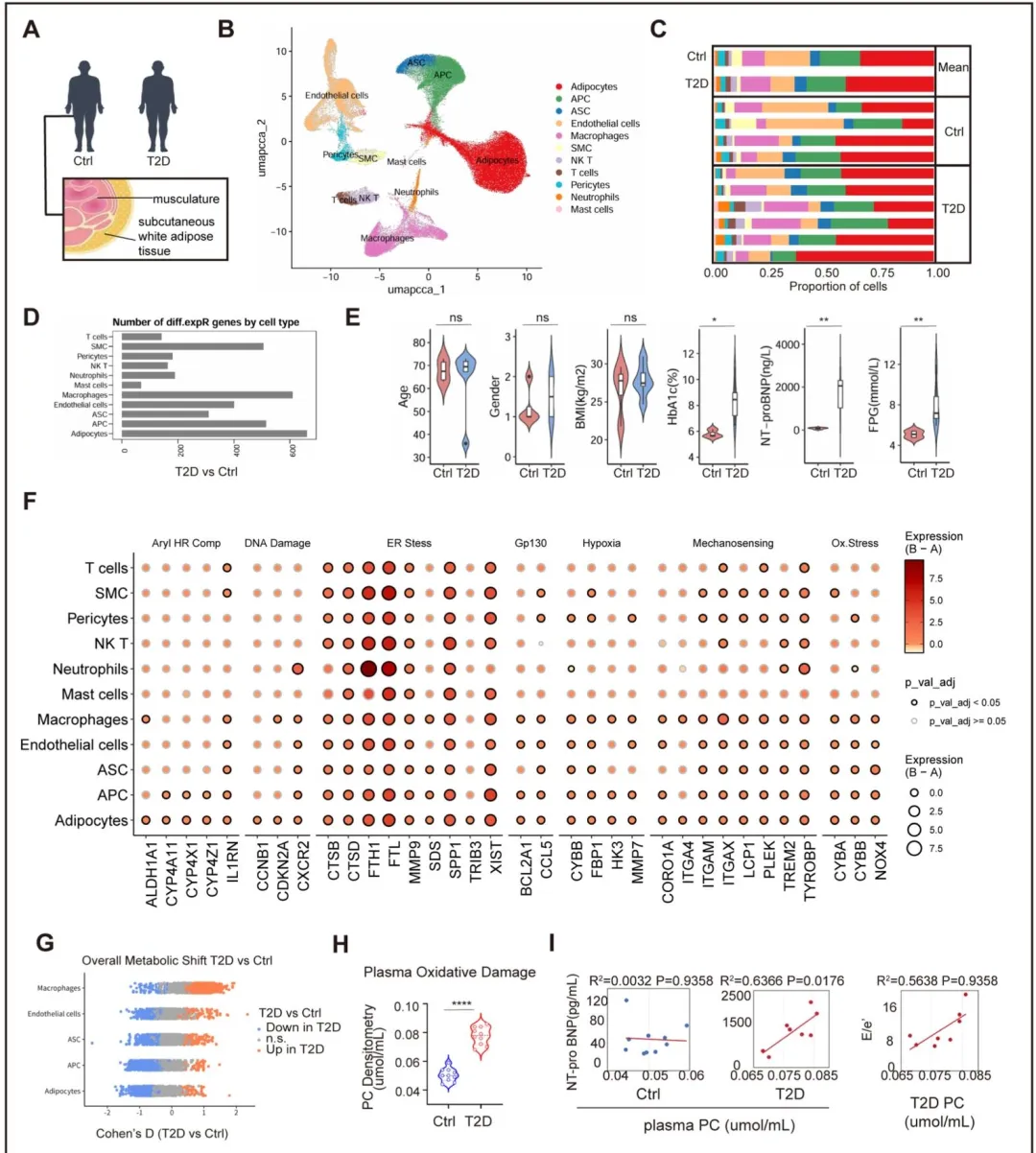
Fig1:通过人脂肪组织单核 RNA 测序绘制细胞图谱,发现 T2D-HFpEF 患者脂肪细胞存在显著的代谢应激,氧化应激和线粒体应激相关基因富集,且患者血浆蛋白羰基水平升高,与 HFpEF 严重程度指标正相关,证实 T2D-HFpEF 存在脂肪组织代谢应激和全身促氧化环境。
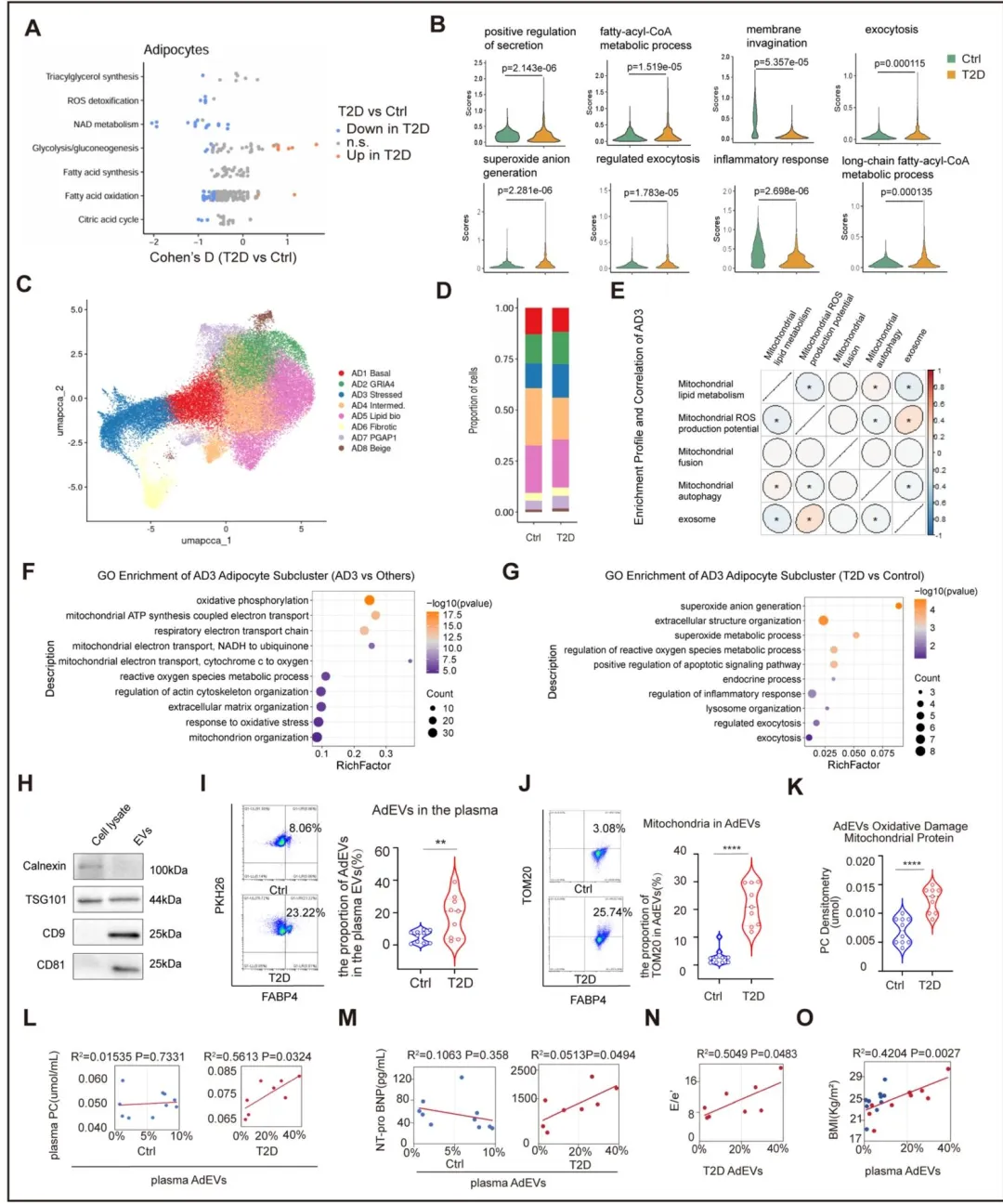
Fig2:证实 T2D-HFpEF 脂肪细胞发生代谢重编程,EV 分泌和超氧阴离子生成通路激活,鉴定出应激富集的 AD3 脂肪细胞亚群;同时验证患者循环 AdEVs 中线粒体蛋白 TOM20 富集且氧化修饰增强,AdEVs 水平与全身氧化应激、心脏负荷临床指标正相关,建立脂肪细胞应激与循环致病性 AdEVs 的关联。
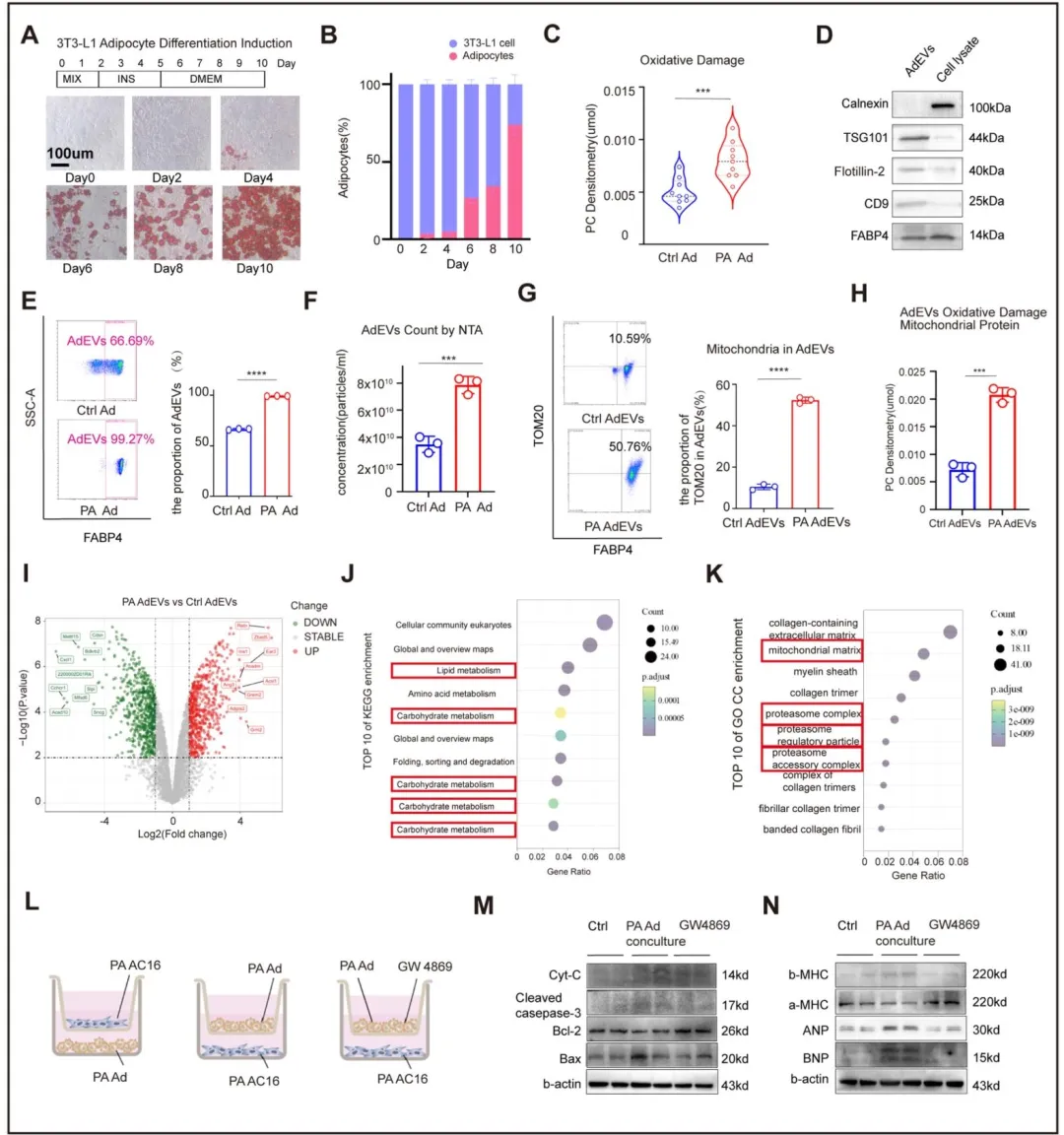
Fig3:证实棕榈酸诱导的脂毒性脂肪细胞会升高细胞内氧化损伤、增加 AdEVs 释放,且 AdEVs 中线粒体成分富集并发生氧化修饰;通过 Transwell 共培养模型发现,脂毒性脂肪细胞可诱导心肌细胞凋亡和病理性重构,而抑制 EV 分泌可逆转该效应,证实 AdEVs 介导了脂毒性脂肪细胞对心肌细胞的损伤。
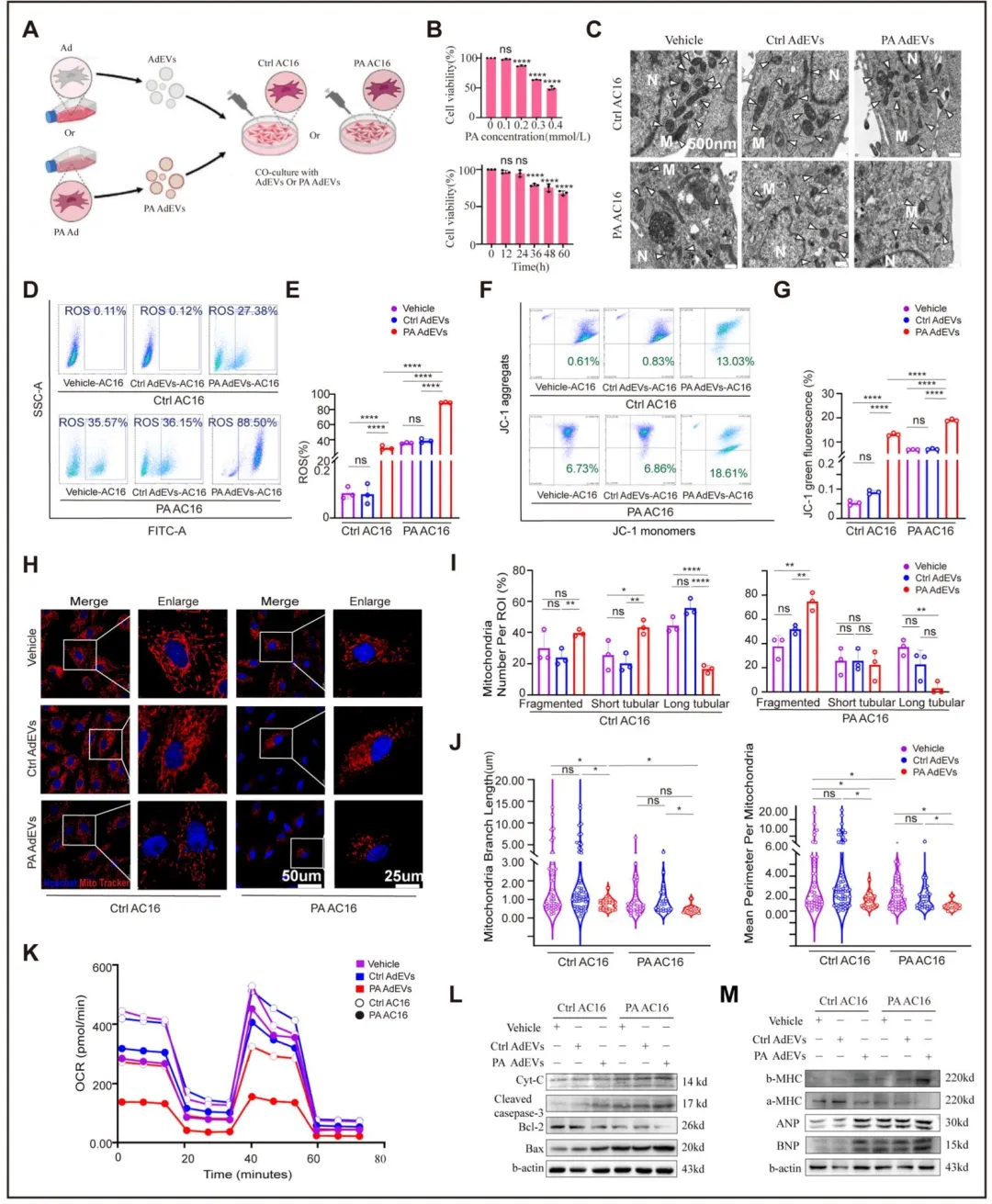
Fig4:证实脂毒性脂肪细胞来源 AdEVs 可导致心肌细胞活性氧蓄积、线粒体膜电位丢失、线粒体网络碎裂,线粒体呼吸功能受损,同时激活心肌细胞内源性凋亡通路并上调心衰标志物,明确该 AdEVs 可直接引发心肌细胞线粒体功能障碍和病理性重构。
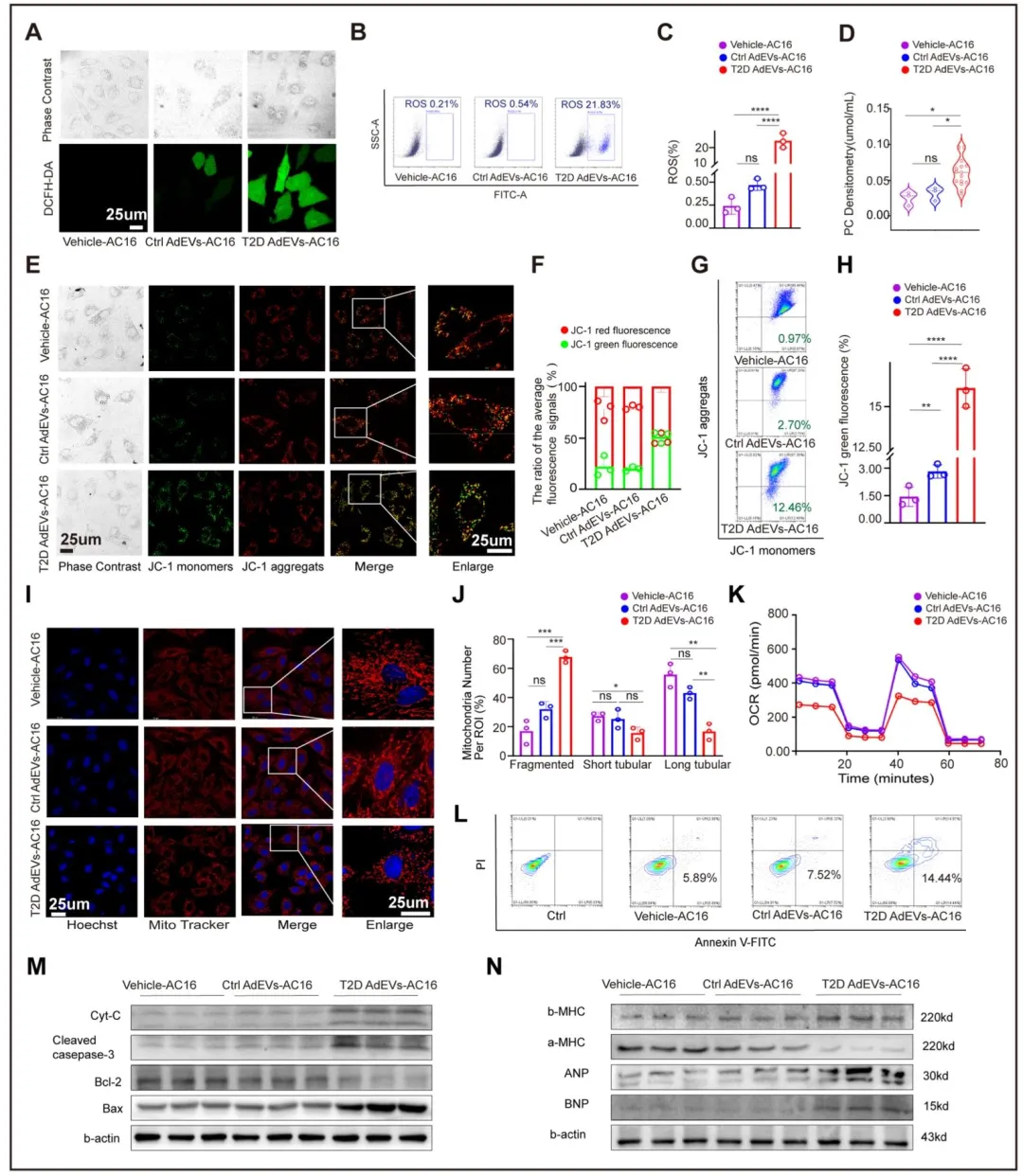
Fig5:证实 T2D-HFpEF 患者来源 AdEVs 可加剧心肌细胞的氧化应激、线粒体功能障碍和线粒体碎片化,导致心肌细胞呼吸功能进一步受损、凋亡增加,且显著上调心衰标志物,验证了患者来源 AdEVs 对心肌细胞的致病性,体现临床相关性。
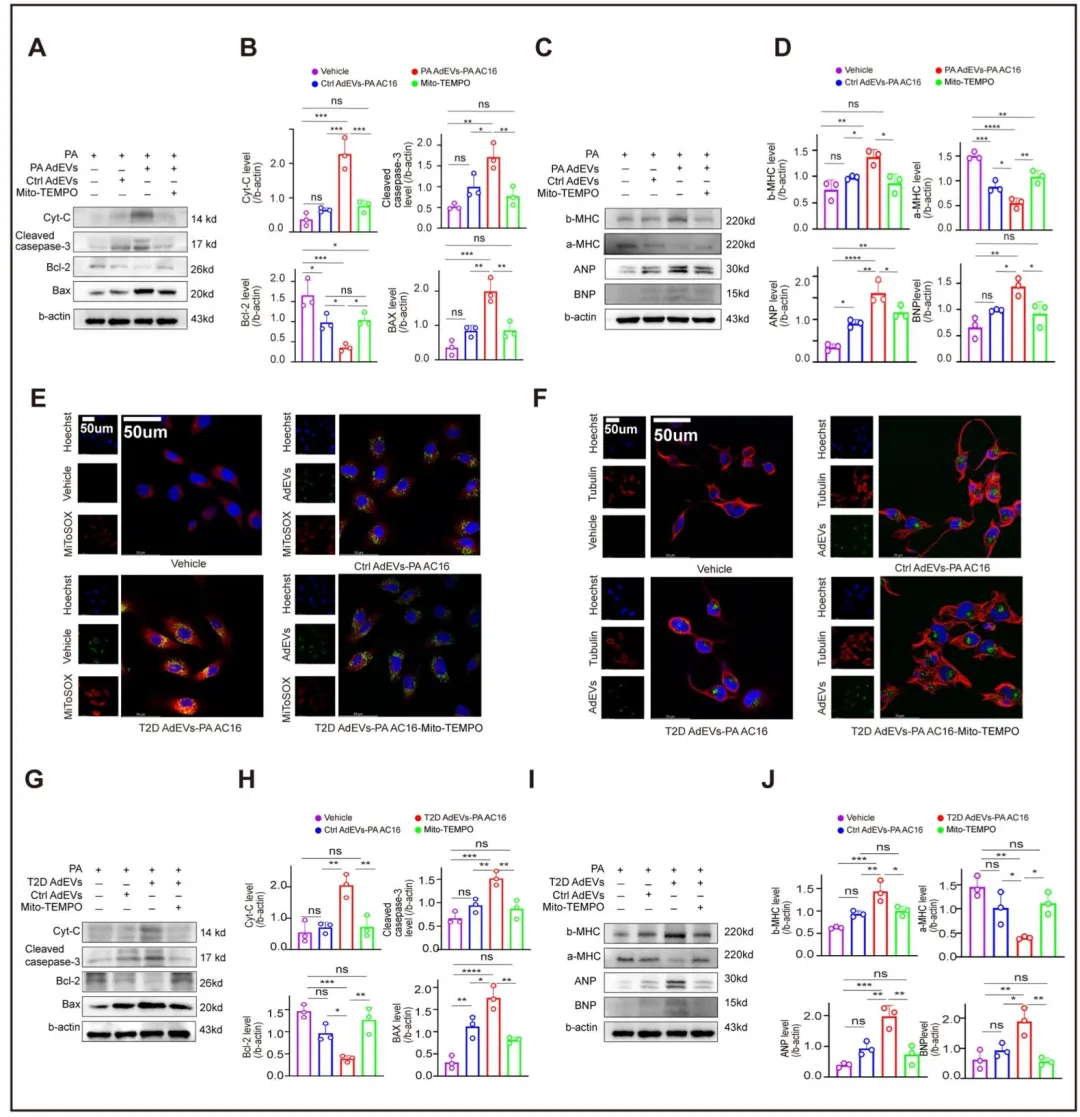
Fig6:证实线粒体活性氧清除剂 Mito-TEMPO 可显著抑制 AdEVs 诱导的心肌细胞活性氧生成,缓解细胞骨架和线粒体结构损伤,下调促凋亡蛋白和心衰标志物,证实线粒体活性氧是 AdEVs 诱导心肌细胞损伤的关键介质。
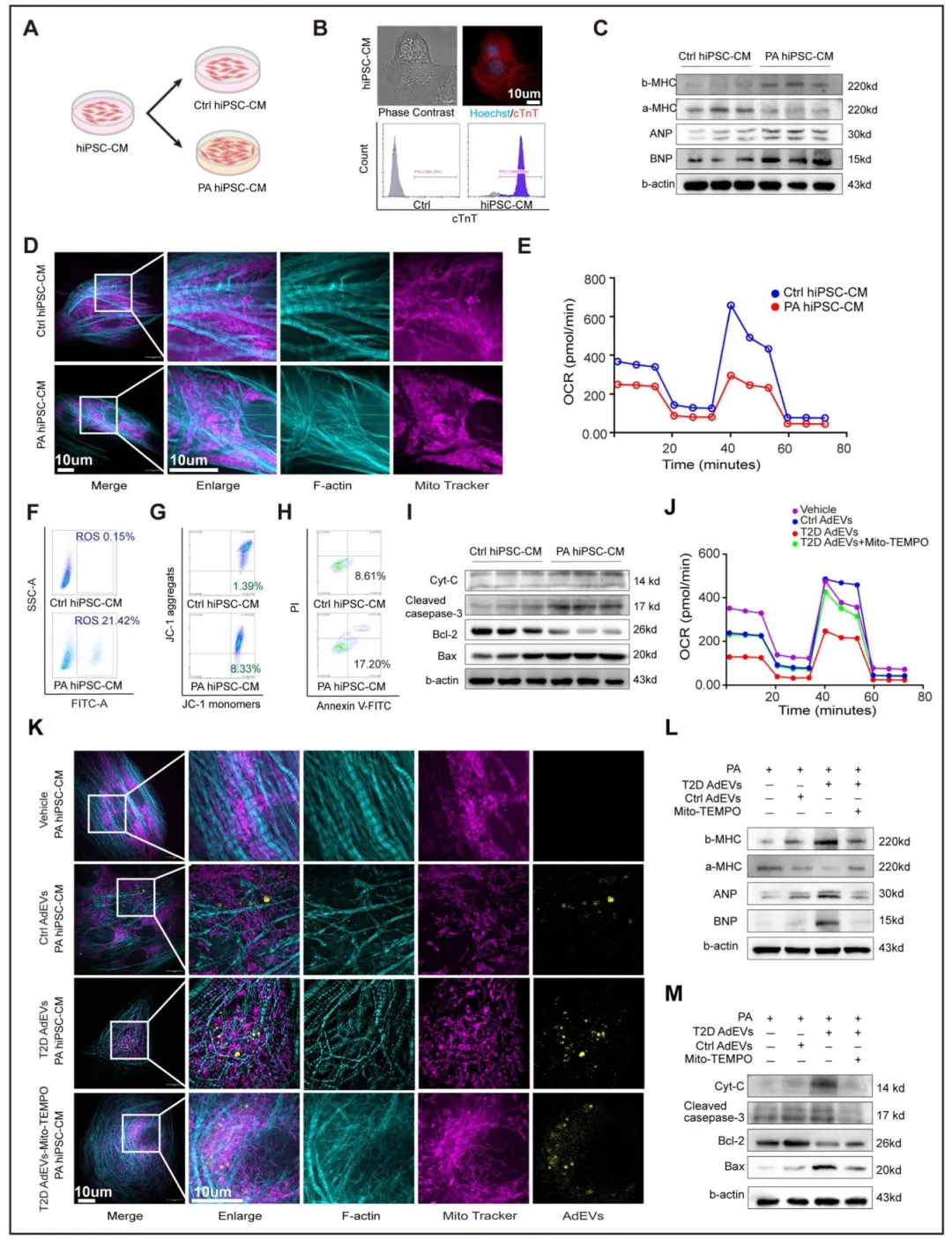
Fig7:在 hiPSC-CMs 模型中证实,棕榈酸可诱导心肌细胞线粒体功能障碍、氧化应激和凋亡,而 T2D 患者来源 AdEVs 会加剧该损伤,Mito-TEMPO 可恢复线粒体形态和生物能功能,在人源心肌细胞模型中验证了脂肪 - 心脏 EV 轴的作用及线粒体活性氧干预的治疗潜力。
研究结论
本研究揭示了 T2D 相关 HFpEF 中脂肪 - 心脏通讯的新机制,即应激脂肪细胞释放富含氧化修饰线粒体货物的 AdEVs,该囊泡作为介质将脂肪组织的代谢应激传递至心肌细胞,引发心肌细胞线粒体功能障碍和凋亡,这一发现拓展了对 HFpEF 多器官发病机制的认知,也与现有糖尿病心肌病中线粒体功能障碍的研究相印证,且临床样本和两种心肌细胞模型均验证了该机制的可靠性,同时证实抑制 AdEV 释放或清除线粒体活性氧可缓解心肌损伤,提示这两个靶点具有治疗 T2D-HFpEF 的潜力,还推测该机制可能适用于肥胖相关 HFpEF、非酒精性脂肪肝等其他代谢性心肌病。但研究存在局限性,一是人类队列样本量小、单中心且局限于冠脉搭桥手术患者,研究结果的普适性有限,相关关联仅为探索性;二是使用小鼠 3T3-L1 脂肪细胞而非原代人脂肪细胞,未对比物种间 AdEV 货物差异,也未明确氧化修饰线粒体蛋白中具体的致病成分;三是未系统收集患者内脏 / 心外膜脂肪相关数据,无法分析脂肪库特异性的影响,且 EV 鉴定未纳入经典阴性标志物,难以完全排除非 EV 结构污染,未来需开展大样本队列、原代人细胞及体内模型研究以验证机制并推进转化。
本文中使用的图片来源Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究