细胞表面糖基化构成动态分子界面,调控细胞间通讯、免疫监视、病原识别和肿瘤进展。糖链的结构复杂性——包括分支模式、连接方式和末端修饰——编码了精确的调控信号。然而,在活体系统中以相当的时间和空间精度操控特定糖链仍极具挑战。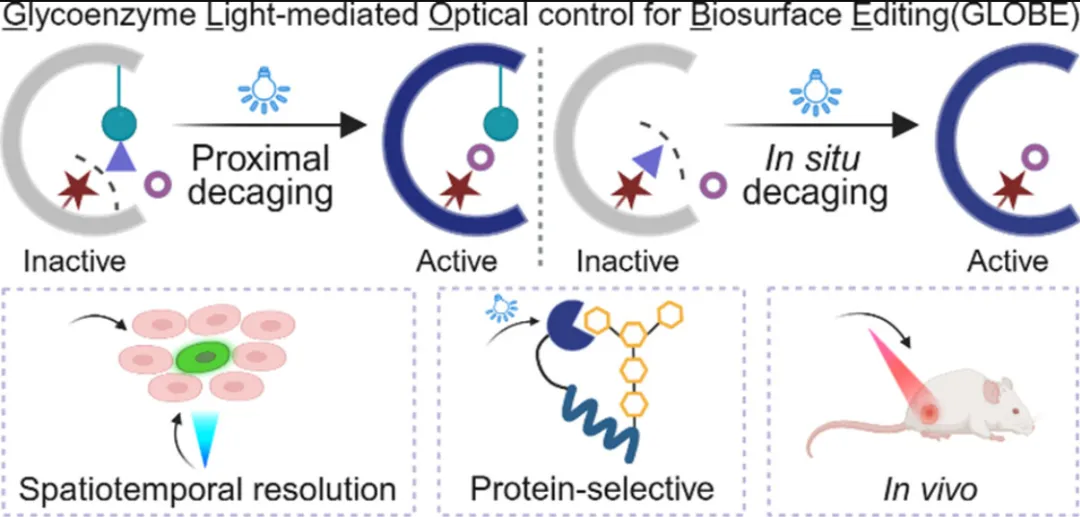
功能性地编辑完整细胞表面的聚糖依赖于糖酶,其反应性、底物特异性和区域选择性是小分子试剂无法比拟的。现有策略如配体靶向糖基化编辑(抗体-唾液酸酶偶联物、纳米抗体-O-GlcNAc转移酶等)可实现蛋白选择性编辑,但依赖组成型活性酶,难以将编辑限制在特定细胞、微结构域或时间窗口。作为互补方向,利用金属离子、MOFs或PEG化预抑制糖酶已开始应对这一挑战,但兼具亚细胞定位和按需激活糖酶活性的通用平台仍属空白。
遗传密码扩展结合非天然氨基酸已成为活体系统中非侵入性、位点特异性调控蛋白质活性的强大策略。光敏UAAs可在催化位点安装光学开关,实现快速、非侵入性、空间限定的酶激活。尽管已有工作开创了O-GlcNAc转移酶的光学调控,但该方法需对内源性酶进行分子生物学操作,扰乱了天然环境,且尚未实现细胞表面直接的蛋白选择性糖基化编辑。
创新突破:GLOBE平台——光控糖酶实现活细胞表面糖基化精准编辑
图1 | 光控糖酶平台GLOBE工作原理。通过遗传编码将光敏非天然氨基酸定点插入目标糖酶的催化位点附近,光解保护基团后恢复酶活性,实现细胞表面糖基化的时空精准编辑。
本研究提出了GLOBE平台,通过将光敏UAA与外源糖酶整合,实现对细胞表面糖基化的精准时空控制。通过在催化中心附近安装光可移除的笼闭基团,GLOBE能够以微米级分辨率实现糖酶的非侵入性、实时激活。该策略支持近端和原位脱笼设计,可扩展至多种糖酶类别,并在活细胞上实现唾液酸化和半乳糖基化的局部重塑。GLOBE为以空前精度解析特定糖链动态功能提供了分子级可编程工具包。
图2 | (A)GAO活性位点结构;(B)GAO近端突变体表达的Western blot分析;(C)GAO-Y405ONBY的LC-MS鉴定;(D)不同光照条件下GAO与GAOM的Amplex Red活性分析;(E)A549细胞经GAOM处理并光照不同时间后的FTZ染色共聚焦图像;(F)不同光照时间后GAOM的LC-MS分析;(G)经GAOM处理并光照后A549细胞的一步法肼基-AF488染色;(H)GAOM活性位点的分子动力学模拟结构。
选择半乳糖氧化酶(EC 1.1.3.9)作为近端笼闭的模型酶。基于GAO晶体结构,选取15个参与底物结合、铜配位、硫醚形成或结构容许的近邻位点进行ONBY安装。优化表达和纯化后,Y405ONBY突变体(GAOM)表现出理想的光调控:MS确认预期分子量;光照前酶活性被强效笼闭;365 nm光照后活性恢复,5分钟内恢复约80%,30分钟内完全恢复。在A549细胞中,醛基生成在光照1分钟内即可检测,5分钟内几乎完全脱笼。分子动力学模拟显示,野生型GAO中底物羟基距催化Cu(II)约1.86 Å,而GAOM中增至约9.66 Å,阻止了有效氧化。
图3 | (A)RgGH33结构与ONBY安装位点;(B)RgGH33突变体表达与活性分析;(C)RgGH33M及不同光照条件下的活性;(D)细胞表面唾液酸酶活性的共聚焦验证。
将GLOBE拓展至糖基水解酶。选择肺炎链球菌唾液酸酶和Ruminococcus gnarus的分子内转唾液酸酶催化域(RgGH33)作为候选。SpNA变体均未表现出UV依赖性激活,而RgGH33-Y355ONBY(RgGH33M)成功实现光调控。RgGH33M在光照后活性恢复,可有效去除细胞表面唾液酸,并随后与凝集素SNA染色证实。
图4 | (A)GAOM-apt的制备流程;(B)GAOM-Tz/Apt-TCO偶联反应的SDS-PAGE分析;(C)不同光照条件下GAO、GAOM和GAOM-apt的Amplex Red活性;(D)共培养MCF-7和HepG2细胞经GAOM-apt处理后的共聚焦图像。
将GAOM与MUC1靶向适配体偶联,实现蛋白选择性糖基化编辑。在共培养的MCF-7(MUC1高表达)和HepG2(MUC1低表达)细胞中,光照后仅MCF-7细胞表面检测到绿色荧光信号,证实GAOM-apt实现了MUC1蛋白选择性的糖基化修饰。
图5 | (A)光触发单细胞糖基化编辑示意图;(B)选定区域光照后A549细胞的共聚焦图像;(C)选定单细胞光照后的三维成像;(D)三维重建图像。
利用共聚焦显微镜的ROI扫描功能,对选定区域内细胞进行光照。结果显示仅光照区域细胞呈现荧光信号,未光照区域无信号。进一步对单个细胞进行定点光照,三维成像证实信号定位于光照细胞膜表面。GLOBE实现了微米级、单细胞水平的糖酶光激活。
图5 | (E)光触发细胞-细胞耦合示意图;(F)光照依赖性Jurkat与MCF-7细胞耦合的共聚焦图像;(G)光触发T细胞-4T1细胞耦合增强细胞毒性与细胞因子分泌示意图;(H-I)不同条件下T细胞分泌TNF-α和IFN-γ的ELISA分析。
在免疫-癌症体系中,Jurkat T细胞功能化表面肼基,与GAOM处理的MCF-7细胞共孵育。光照后,GAOM在癌细胞表面生成醛基,驱动与T细胞的生物正交偶联。仅当双方携带互补化学基团且暴露于光照时,才观察到紧密的T细胞/MCF-7接触。小鼠脾脏T细胞修饰肼基后与光激活的4T1细胞共孵育,TNF-α和IFN-γ分泌水平显著升高,表明GLOBE介导的强制邻近可功能性地编程免疫行为。
图5 | (J)体外受精模型中卵母细胞光触发糖基化标记;(K)受精后2小时高分辨率成像。
在体外受精模型中,卵母细胞在授精后0、2、5小时分别进行GAOM光激活。GLOBE标记显示受精过程中ZP糖基化信号逐渐增加。受精后2小时高分辨率成像捕捉到多个精子在不同焦平面与卵母细胞相互作用,位于透明带内或更深处的精子表面半乳糖可视化信号减弱,提示空间依赖的可及性和/或动态糖基化重塑。
图6 | (A)正交光响应级联示意图;(B)A549细胞依次经RgGH33M和GAOM处理并光照后的共聚焦图像。
RgGH33M去除末端唾液酸后生成LacNAc,增加GAOM氧化底物。细胞先经RgGH33M处理并光照,再经GAOM处理并光照,荧光信号显著强于GAOM单独处理。正交光响应级联证明多个工程化糖酶可通过层级激活实现模块化、时空可控的糖基化编辑。
图7 | (A)UCNP辅助光激活示意图;(B)不同处理组肿瘤组织的共聚焦成像;(C)荧光强度定量分析。
为解决UV光组织穿透深度限制,制备NaYF4:Yb,Tm上转换纳米颗粒,在980 nm近红外激发下发射365 nm UV光。4T1荷瘤小鼠瘤内注射UCNP与GAOM混合物后,近红外照射显著增强肿瘤部位荧光信号,对照组无信号。GLOBE首次实现了活体水平的光控糖基化编辑。
本研究开发了GLOBE平台,通过将光敏非天然氨基酸定点引入糖酶,实现对细胞表面糖基化的时空精准调控。
核心创新点:
近端笼闭策略:通过在催化位点附近引入光敏UAA,实现酶活性的可逆抑制与光控恢复,保留天然活性位点微环境;
蛋白选择性编辑:适配体偶联实现混合细胞群中MUC1高表达细胞的特异性糖基化修饰;
单细胞水平光控:微米级空间分辨率,可对选定区域甚至单个细胞进行定点激活;
多功能拓展:成功应用于GAO、RgGH33两种糖酶,支持正交级联反应;
生物学场景验证:在免疫细胞-肿瘤细胞相互作用、体外受精模型中揭示动态糖基化变化;
体内应用:UCNP辅助近红外激活,首次实现活体肿瘤模型的糖基化光控编辑。
研究意义:
GLOBE为解析特定糖链在细胞通讯、免疫调控、发育等过程中的动态功能提供了分子级可编程工具包,突破了传统组成型活性酶或静态染色方法无法揭示的瞬时、时空可控糖基化动态。
题目:A Photoactivatable Glycoenzyme Platform for Spatiotemporally Controlled, Protein-Selective, and In Vivo Glycan Editing
作者:Xiaocui Zheng, Wanqing Wei, Changjiang Wang, Yingdan Du, Jing Yang, Yao Zhou, Ying Liu, Yong Liang, Lijun Ding, Ran Xie
通讯作者:
单位:南京大学
期刊:Journal of the American Chemical Society
DOI:10.1021/jacs.5c21919
(本文仅作学术分享,解读内容仅供参考)