Neuron︱南京医科大学卢应梅/韩峰团队揭示内侧缰核介导焦虑情绪的发生的新机制
- 2026-04-16 08:30:07

撰文︱郑志伟
审阅︱卢应梅,韩峰
责编︱王思珍
焦虑症(anxiety disorders)是一类以过度且持续的焦虑、恐惧及情绪调节异常为主要特征的精神疾病。焦虑症患者通常需要长期甚至按需服药,但现有的药物——基于GABA受体激动机制的苯二氮䓬类药物,存在临床局限性。这类药物虽然起效快,但因其作用靶点广泛分布于全脑,导致其在发挥抗焦虑作用的同时,不可避免地激活运动控制区与认知相关脑区的受体,从而引发共济失调、嗜睡和记忆力下降等剂量依赖性副作用。更为严峻的是,长期使用会诱发受体下调,导致患者产生耐受性和药物依赖,停药后出现强烈的戒断反应。由此,阐明焦虑障碍发生的新病理机制,鉴定并验证具有高成药性的新靶点,开发具备“疗效与副作用解偶联”特征的新型先导化合物,是满足临床需求的当务之急。

一、意外发现神经元亚群放电模式的转换
研究人员首先通过动物实验模拟了一种特定情境下的焦虑状态,并利用c-Fos染色与光纤钙信号记录技术,实时监测内侧缰核腹侧区域一群特殊的乙酰胆碱能神经元(vMHbChAT)的活动。结果发现,当焦虑状态出现时,这群神经元被显著激活,提示它们与焦虑情绪的产生密切相关。
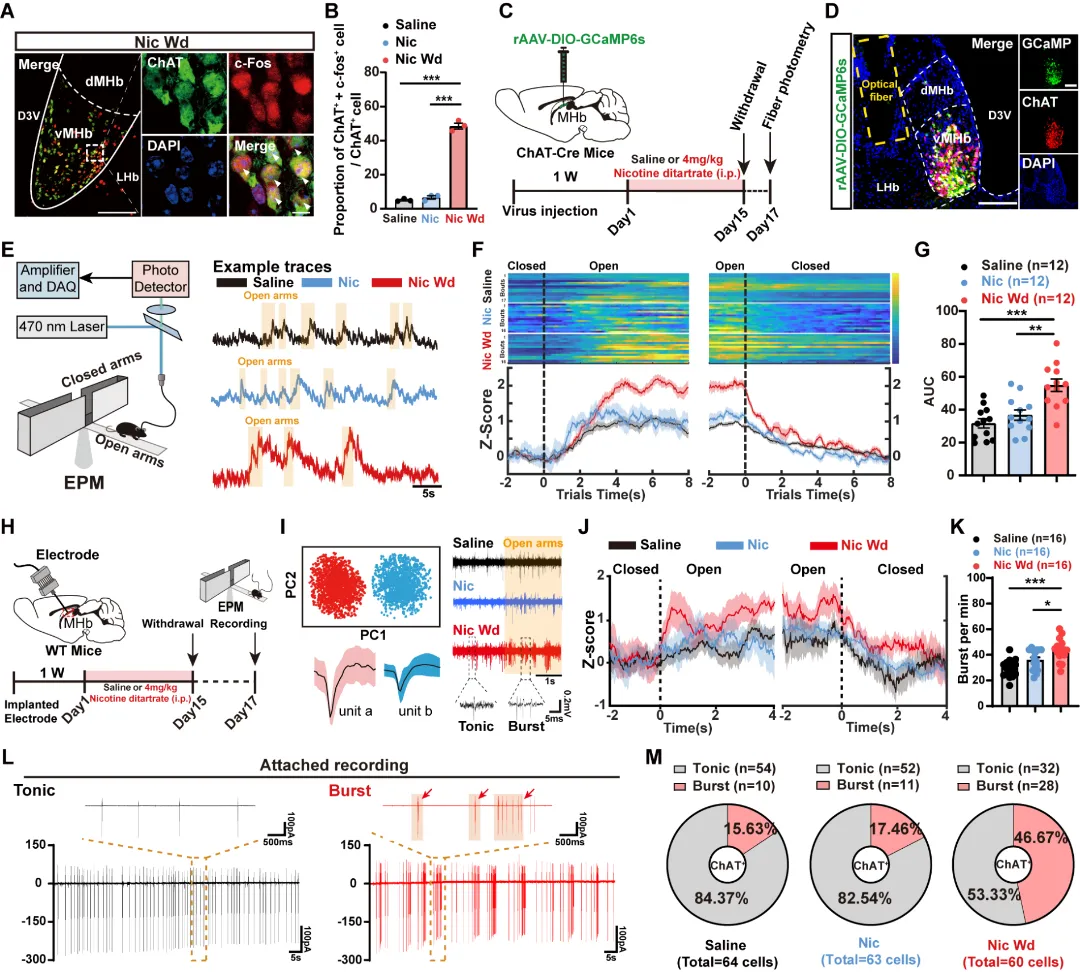
图1. 焦虑状态诱导vMHbChAT神经元簇状放电增加
二、解析簇状放电直接驱动焦虑产生的新规律
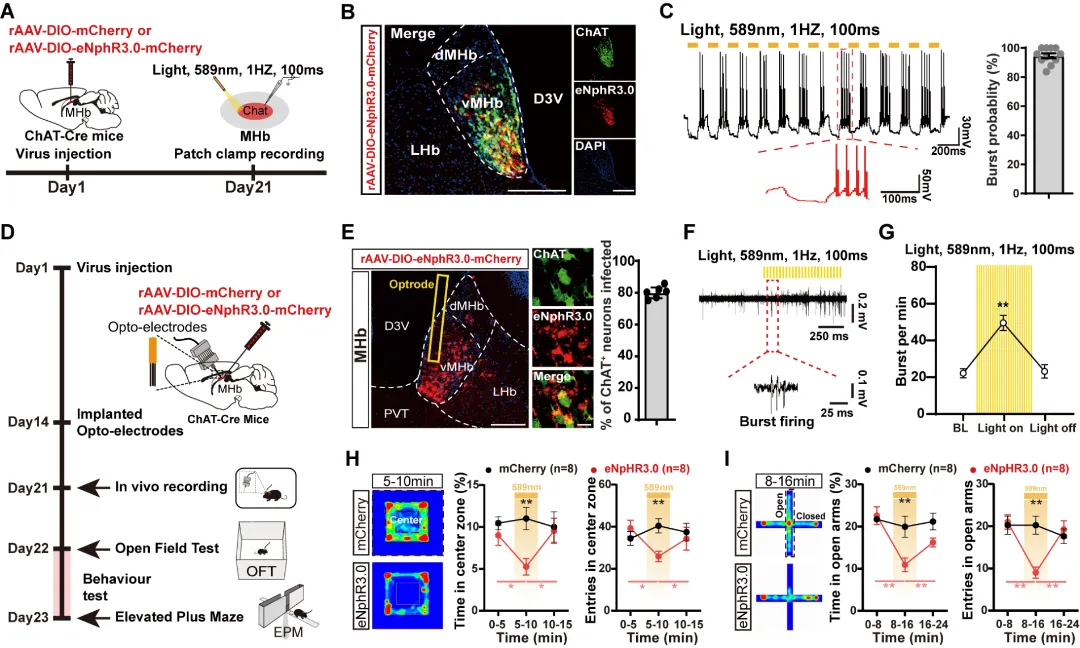
图2. 光遗传诱导vMHbChAT神经元burst放电引发焦虑样行为
三、电生理层面阐明T型钙通道Cav3.1的重要功能
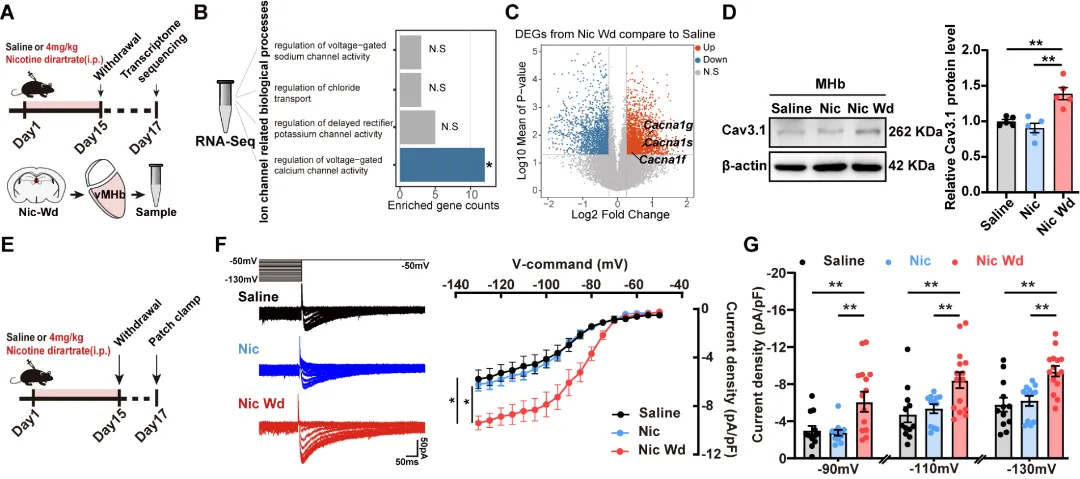
图3. 焦虑状态下vMHbChAT神经元中Cav3.1表达增加
四、分子层面发现RNA结合蛋白Pum1为潜在调控靶标
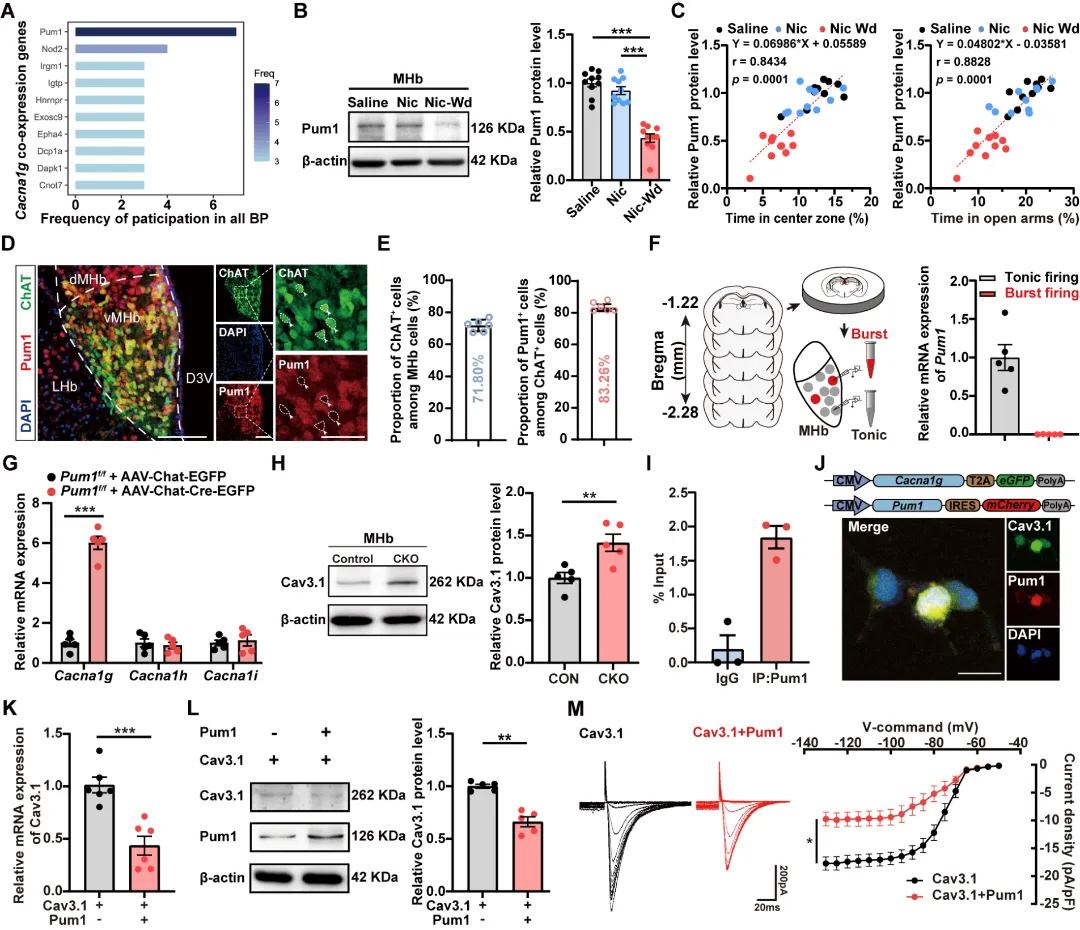
图4. Pum1通过结合并促进Cav3.1 mRNA降解,从而抑制其表达
五、Pum1分子“救援”可挽救焦虑状态
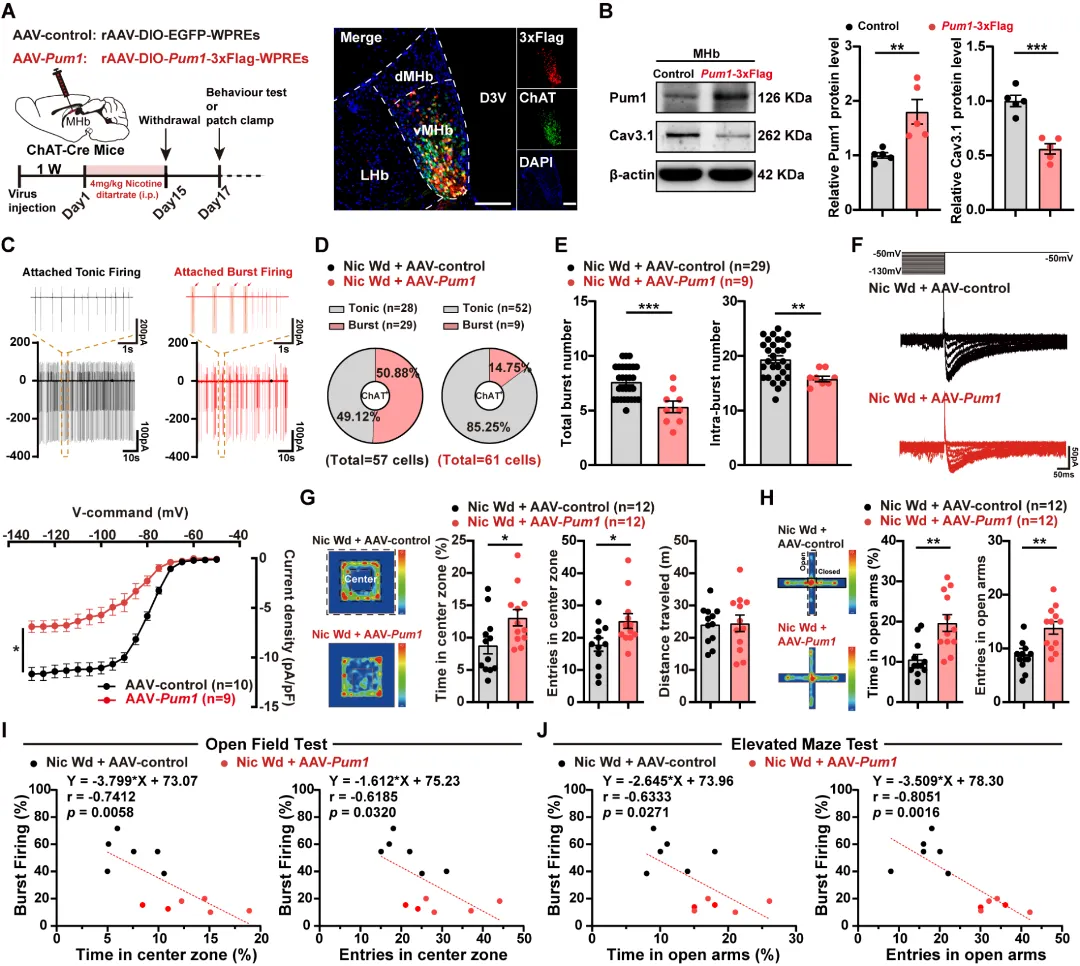
图5. vMHbChAT神经元特异性过表达Pum1挽救焦虑样行为
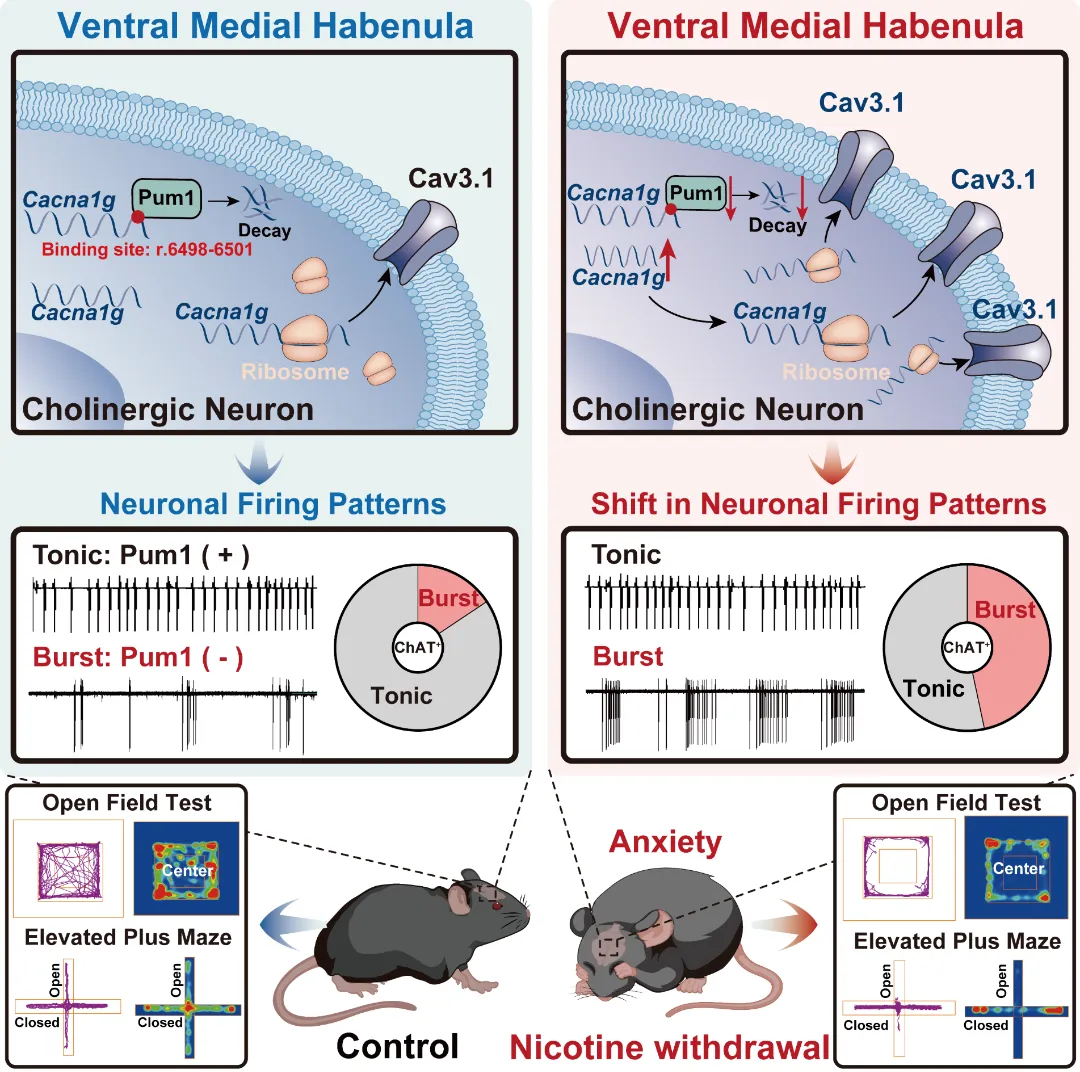
图6. 文章总结图
本研究将焦虑的病理机制锚定于“神经元放电模式”这一更基础的神经动力学层面,并首次揭示了Pum1–Cav3.1分子轴在其中的核心调控作用。这一原创发现不仅突破了传统“神经递质失衡”理论的局限,更为抗焦虑创新药物的研发开辟了全新的靶标体系——从“化学信号调节”走向“电生理节律修复”。未来,以Cav3.1通道和Pum1蛋白为代表的新型靶点,有望催生具备“高效、低毒、非依赖”特征的新一代抗焦虑药物,为临床患者提供更安全有效的治疗选择,同时为我国在精神神经类药物领域的“First-in-class”原始创新提供重要的靶标储备。
原文链接:https://www.cell.com/neuron/fulltext/S0896-6273(26)00126-1
本研究的通讯作者为南京医科大学基础医学院卢应梅教授、药学院韩峰教授和美国芝加哥大学徐宇君教授;南京医科大学基础医学院博士研究生郑志伟、博士后闵鹏翔和博士研究生罗艺灵为该研究的共同第一作者。该项目得到国家自然科学基金重点项目、国家自然科学基金国际(地区)合作研究项目和国家重点研发计划“科技创新2030—重大项目”等项目资助。
转载须知:“逻辑神经科学”特邀稿件,且作者授权发布;本内容著作权归作者和“逻辑神经科学”共同所有;欢迎个人转发分享,未经授权禁止转载,违者必究。

“逻辑神经科学”微信群:文献学习


