前言
动物乳腺生物反应器是利用哺乳动物特异性乳蛋白基因启动子,指导外源目的基因在乳腺中高效特异性表达,通过乳腺分泌作用获得重组蛋白的技术。1987年,首次成功制备转基因小鼠乳腺生物反应器并提取出具有生物活性的人体组织型纤溶酶原激活剂(tPA),开创里程碑。2006年,美国GTC公司开发的山羊乳腺生物反应器生产重组人抗凝血酶III(ATryn)成为首个被欧洲药监局EMA和美国FDA批准上市的转基因动物产品。2010年,荷兰Pharming公司通过转基因兔乳腺生物反应器制备的Ruconest单克隆抗体药物也获批上市。该技术具有独特优势,在生命科学和生物医药领域应用潜力巨大。
1 动物乳腺生物反应器的原理
利用分子生物学方法将特异性乳蛋白基因启动子与目的基因连接,构建乳腺特异性表达载体,通过转基因技术导入动物早期胚胎或受精卵,制备整合目的基因的转基因动物。雌性哺乳动物分娩后乳腺持续分泌乳汁,乳蛋白基因调控序列驱动外源基因在乳腺靶向高效表达。通过遗传育种技术选择性杂交繁育高表达纯合子转基因动物,建立优质种系,从乳汁中源源不断获取外源性重组蛋白。
2 动物乳腺生物反应器的特点
2.1 表达产量高
乳腺作为高度分化的专门化腺体,可高效合成蛋白质,外源蛋白表达可达1 g·L⁻¹,具有工业化生产潜力。
2.2 易于分离纯化
乳汁蛋白成分种类相对较少,重组蛋白通过去除酪蛋白沉淀乳清、层析等常规程序即可纯化,操作简单;生产过程不产生有毒物质,无环境污染。
2.3 周期短、成本低
转基因动物易扩大种群进行大规模繁殖;新药研发周期从传统10~15年缩短至约5年,降低开发成本,适合罕见病特效药物生产。
2.4 生物活性高和安全性高
乳腺作为成熟"分子工厂",能对蛋白质进行高效翻译后加工修饰,重组蛋白折叠成功能性构象,与天然蛋白高度相似;乳腺作为外分泌器官,乳汁不进入体内循环,生物安全性高,对动物本身危害小。
3 乳腺生物反应器的目标动物选择
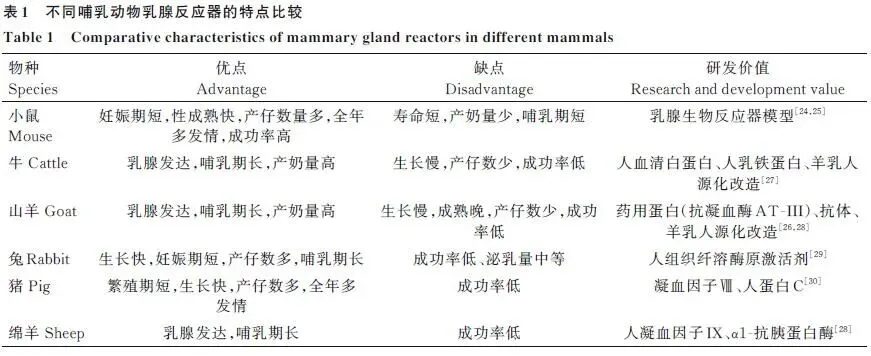
小鼠:繁殖周期短、产仔数多、全年多发情、成功率高,常用于初期模型和载体验证试验;缺点为寿命短、产奶量少、哺乳期短。牛:乳腺发达、哺乳期长、产奶量高;缺点为生长慢、产仔数少、成功率低;用于人血清白蛋白、人乳铁蛋白、羊乳人源化改造。山羊:乳腺发达、哺乳期长、产奶量高;缺点为生长慢、成熟晚、产仔数少、成功率低;用于药用蛋白(抗凝血酶AT-III)、抗体、羊乳人源化改造。兔:生长快、妊娠期短、产仔数多、哺乳期长;缺点为成功率低、泌乳量中等;用于人组织纤溶酶原激活剂。猪:繁殖期短、生长快、产仔数多、全年多发情;缺点为成功率低;用于凝血因子VIII、人蛋白C。绵羊:乳腺发达、哺乳期长;缺点为成功率低;用于人凝血因子IX、α1-抗胰蛋白酶。
4 动物乳腺生物反应器的应用进展
4.1 改善乳品质
通过基因工程技术去除致敏原基因(如BLG、酪蛋白),增加功能营养蛋白基因,实现动物乳"人源化"改造。敲除致敏原:TALEN技术敲除牛BLG基因;CRISPR/Cas技术敲除水牛BLG基因;Red同源重组系统敲除牛β-酪蛋白基因;CRISPR/Cas9生产BLG敲除山羊;CRISPR/Cas9制备β-酪蛋白敲除奶山羊。增加功能营养蛋白:基因打靶在山羊BLG基因座导入人乳铁蛋白基因(细胞水平验证);CRISPR/Cas9在猪α-s1酪蛋白基因座定点插入人乳铁蛋白基因,乳铁蛋白持续高表达,乳汁具抗菌活性;CRISPR/Cas9在猪白蛋白基因座定点插入重组人血清白蛋白基因,可种系遗传;CRISPR/Cas9介导人乳铁蛋白基因敲入牛β-酪蛋白基因座,通过抑制DNA MMR基因和过表达DSB修复基因提高敲入效率。
4.2 生产(重组)医药蛋白
主要类别:蛋白酶和多肽两大类,包括人凝血因子、抗凝血酶III、溶菌酶、人蛋白C、超氧化物歧化酶(SOD)、人纤溶酶原激活物等。代表性成果:1997年绵羊乳腺生物反应器生产人凝血因子,奠定初始基础;2006年山羊ATryn成为全球首个获批上市的转基因动物重组医药蛋白。人重组凝血因子VIII转基因小鼠,表达水平最高2.81 mg·mL⁻¹;重组人溶菌酶转基因山羊,浓度224 μg·mL⁻¹(接近人初乳226 μg·mL⁻¹),具良好体外抗菌活性。转基因猪和小鼠乳腺特异性表达人蛋白C,表达水平分别为380 μg·mL⁻¹和28 ng·mL⁻¹;山羊β-酪蛋白/CMV杂合启动子构建SOD1/SOD3乳腺特异性表达载体,重组人SOD1表达88.81 mg·L⁻¹、SOD3表达267.82 mg·L⁻¹,酶活力1432 U·mL⁻¹;山羊乳腺生物反应器表达重组人纤溶酶原激活物(rhPA),表达水平78.32 μg·mL⁻¹,体外溶栓活性是瑞替普酶的13.3倍,可稳定遗传。
4.3 制作抗体
转基因山羊整合全人源抗Her2单克隆抗体(胎儿水平鉴定);体细胞核移植制备转基因克隆山羊整合抗人黑色素瘤/CD28双抗(胎儿水平鉴定);转基因小鼠乳腺高度表达功能性小鼠-人嵌合抗体chHAb18,表达水平1.1~7.4 mg·mL⁻¹,与肝癌细胞特异高效结合,亲和力为亲本鼠源抗体的68%。转基因小鼠表达重组人抗PD-1抗体最高水平达80.52 mg·L⁻¹;表达抗HBV单克隆抗体转基因小鼠,乳腺表达水平17.8 mg·mL⁻¹。
4.4 合成基因工程疫苗
TALEN基因打靶将口蹄疫病毒(FMDV)、猪瘟病毒(CSFV)重组病毒结构蛋白基因(rVP1和rE2)整合至山羊BLG基因第二外显子,乳汁表达rVP1 1.02 mg·mL⁻¹、rE2 1.46 mg·mL⁻¹,免疫小鼠可检测特异性抗体。表达冠状病毒通用表位噬菌体外壳蛋白嵌合病毒样颗粒的转基因小鼠,纯化后病毒嵌合颗粒可诱导特异性抗体反应和中和活性。
4.5 其它方面的应用
富含褪黑素乳品:CRISPR/Cas9与显微注射结合开发绵羊乳腺生物反应器,34只转基因羊在乳腺上皮细胞高水平表达褪黑激素。表达人FGF2:CRISPR/Cas9与体细胞核移植技术,牛β-酪蛋白基因座表达人成纤维细胞生长因子2。改善乳脂肪酸组成:β-酪蛋白位点基因打靶人ω-3多不饱和脂肪酸脱氢酶(hfat-1)的奶山羊,获得59株定点整合细胞系,打靶效率74.29%。表达人GCSF:转基因山羊乳腺表达人粒细胞集落刺激因子,泌乳期表达浓度360 μg·mL⁻¹,与商业规模相当。导管灌注递送:水牛β-酪蛋白启动子指导人γ-干扰素在小鼠乳腺高效表达,绕过生殖细胞基因整合,避免相关风险。
5 动物乳腺生物反应器面临的挑战与前景展望
现存挑战 小型动物(小鼠、兔)泌乳量低、寿命短,难以满足产业化需求;大型动物(牛、羊、猪)制备技术难度高、效率低、周期长;"非预期效应":外源基因整合受"位置效应"和"剂量效应"制约;目标蛋白翻译后修饰加工和分离纯化导致与天然活性蛋白存在差异;蛋白产品对人体健康可能存在安全隐患。
发展前景技术革新:CRISPR/Cas9等基因编辑技术使外源蛋白基因靶向敲入天然蛋白基因座特定位点,避免"位置效应",自动获得天然乳蛋白所有调控序列,提高表达能力,产物更接近天然状态。市场需求:我国人口大国对生物医药蛋白、功能营养蛋白、人源化乳品需求量大,既是挑战也是机遇。产业化基础:已有美国GTC Biotherapeutics、荷兰Pharming、英国Piramal Pharma Limited等大型制药公司产品上市。技术趋势:基因定点靶向编辑技术结合体细胞核移植克隆技术为核心平台,是未来生产乳腺生物反应器的关键和必然趋势。
小结:动物乳腺生物反应器具有产量高、易提纯、成本低、生物活性和安全性高等独特优势,在改善乳品质、生产医药蛋白、制作抗体、合成基因工程疫苗等方面前景广阔。需加大技术创新和研发投入,建立更成熟、高效、可靠、安全的技术体系,为人类健康带来更大福祉。
关键词:乳腺生物反应器;蛋白表达产物;重组医药蛋白;基因编辑