南京医科大学附属口腔医院正畸科:腭裂修复新靶点?解密OGT如何“糖基化”修饰MEIS2,调控腭骨发育
- 2026-04-10 05:37:34
南京医科大学附属口腔医院正畸科:腭裂修复新靶点?解密OGT如何“糖基化”修饰MEIS2,调控腭骨发育
研究导读:本文由南京医科大学附属口腔医院正畸科于《International Journal of Oral Science》(IF:12.2)发表,本研究共同揭示了MEIS2 O-GlcNAc修饰在腭骨发育中的重要作用,并为理解腭部发育调控网络建立了新的理论框架。该发现可能为未来腭裂的诊断与预防提供新途径。 
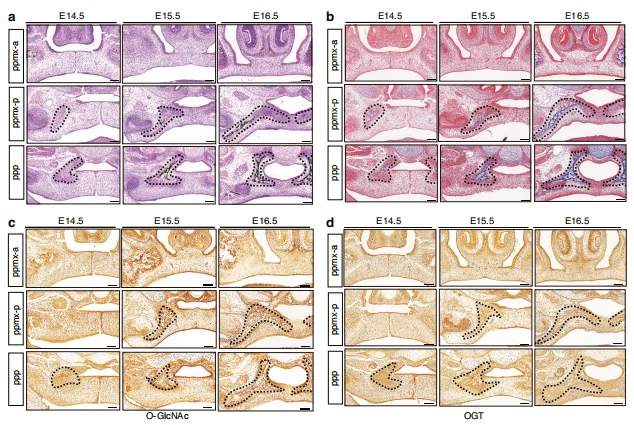
图1:OGT 和O-GlcNAc修饰在腭部发育中起关键作用。(a)VonKossa染色与(b)Masson三色染色显示E14.5至E16.5冠状切面结果,黑色虚线标示腭骨区域。(c、d)E14.5至E16.5冠状切面 OGT 及整体O-GlcNAc修饰的代表性免疫组化染色结果。比例尺:100 μm 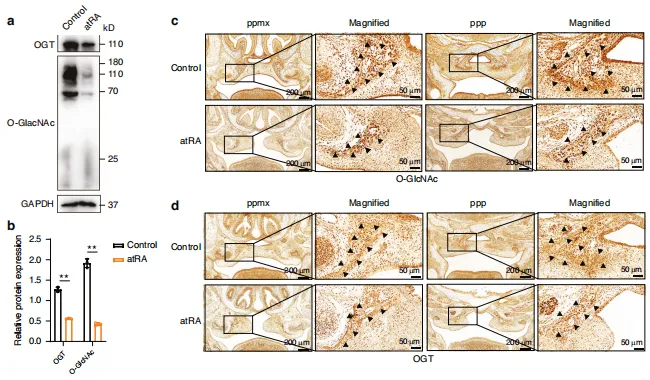
图2:atRA诱导小鼠中O-糖基化修饰的下调及其在腭部发育调控中的作用。a 对照组小鼠与atRA小鼠腭部托架组织中 OGT 及O-糖基化表达的蛋白质印迹分析。b (a)中相对蛋白水平的半定量数据。c E15.5胚胎冠状切片中整体O-糖基化修饰的代表性免疫组化染色结果。d E15.5胚胎冠状切片中 OGT 的代表性免疫组化染色结果。n=3次生物学独立实验。ppmx上颌骨腭突,ppp腭突腭突 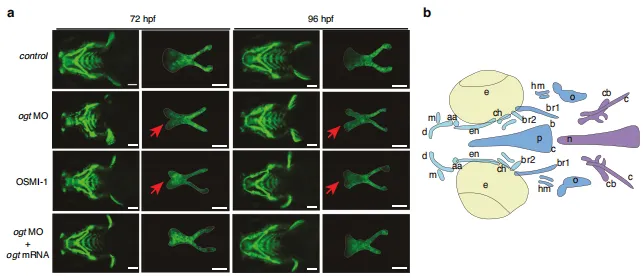
图3:斑马鱼中O-GlcNAc糖基化缺失导致的腭裂与蝶骨旁骨形成障碍。a Tg(sox10:eGFP)转基因斑马鱼幼体腹侧荧光代表性视图。腭部骨骼经解剖后平铺固定,前部朝上。白色实线表示筛骨腭。比例尺:100 μm 。b 9日龄斑马鱼幼体骨结构腹侧(上方)视图示意图。aa:关节角;br1:鳃弓肋1;en:翼外肌;m:上颌骨;n:脊索;o:鳃盖;p:蝶骨旁;br2:鳃弓肋2;c:镫骨;cb:角鳃骨5;ch:角软骨;d:下颌骨;hm:下颌骨下部;v:椎骨;bop:基枕关节突 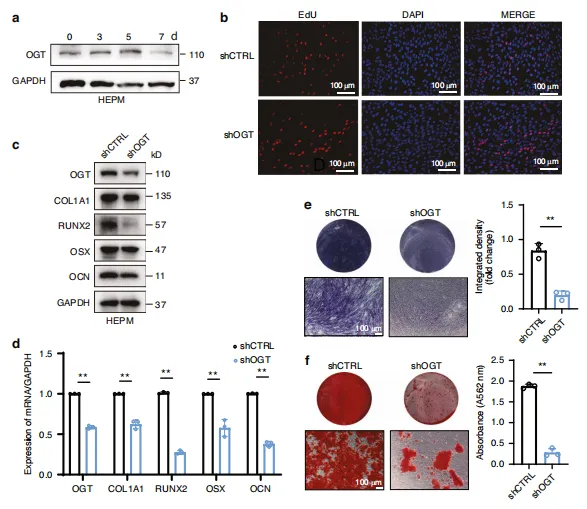
图4:OGT 敲低对 HEPM 细胞体外成骨分化过程的负面影响。a 成骨分化过程中 OGT 蛋白水平的蛋白质印迹分析。b shCtrl与shOGT HEPM 细胞的代表性Edu染色图像。shCtrl短发夹对照(对照慢病毒),shOGT短发夹 OGT(OGT 慢病毒)。c 经指定处理的 HEPM 细胞中成骨标志物(COL1A1、RUNX2、 OSX 和氰酸盐)的表达及蛋白质水平,通过蛋白质印迹法评估。d 经指定处理的 HEPM 细胞中成骨基因(COL1A1、RUNX2、 OSX 和氰酸盐)的表达及mRNA水平,通过实时定量PCR评估。e、f 经指定处理的 HEPM 细胞中碱性磷酸酶(ALP)和抗逆转录酶(ARS)染色结果。 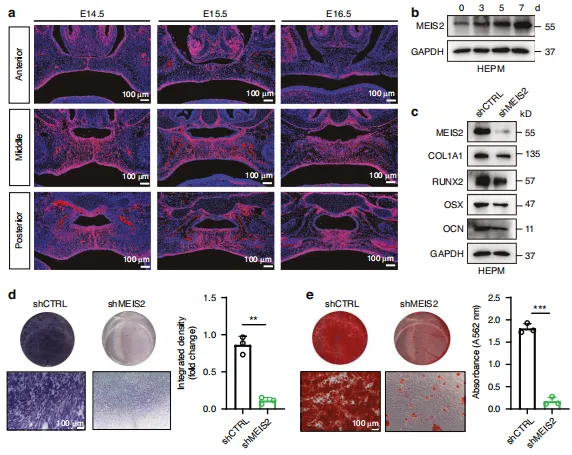
图5:MEIS2对腭骨形成至关重要。a 对E14.5至E16.5冠状切片中MEIS2的免疫荧光染色。b 骨形成分化过程中MEIS2蛋白水平的蛋白质印迹分析。c 骨形成标志物(COL1A1、RUNX2、 OSX 和氰酸盐)的表达及按指定处理的 HEPM 细胞蛋白水平,通过蛋白质印迹法评估。d、e 按指定处理的 HEPM 细胞的碱性磷酸酶(ALP)和抗原识别序列(ARS)染色。n = 3次生物学独立实验。 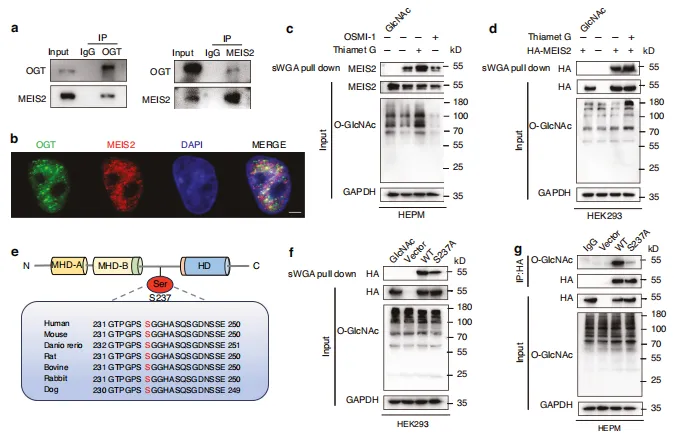
图6:OGT 介导的MEIS2 Ser237位点O-GlcNAc修饰。a 共免疫沉淀实验证实了 HEPM 细胞中 OGT 与MEIS2的相互作用。b 采用代表性免疫荧光染色法检测 HEPM 细胞内亚细胞 OGT(绿色)与MEIS2(红色)的定位。比例尺:5 μm 。c、d 通过sWGA下拉实验观察HEK293细胞中外源性MEIS2及 HEPM 细胞内源性MEIS2表达。细胞收获前经30 μΜ TMG 或 OSMI -1处理12小时。e MEIS2跨物种蛋白质序列比对。f HEK293细胞中sWGA下拉实验结果。转染HA-MEIS2(野生型或S237A突变体)质粒的细胞。g 对HA-WT或HA-S237A突变体转染HEK293细胞中 WCL 及免疫沉淀物进行免疫印迹分析。 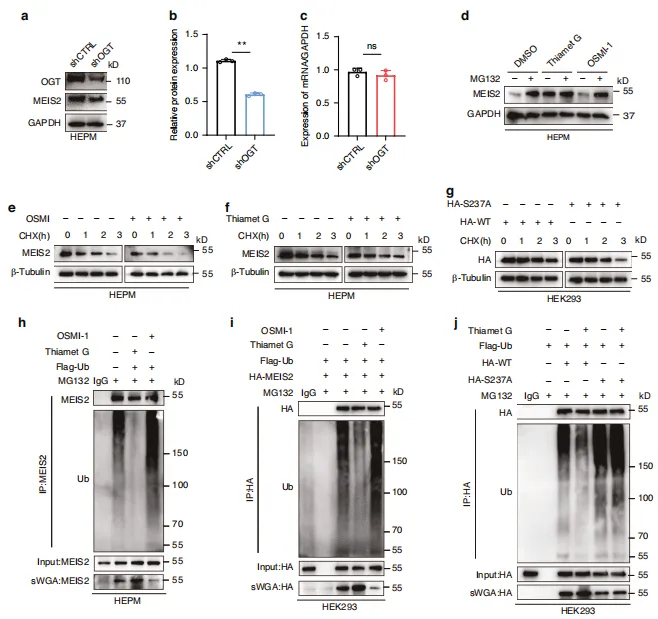
图7:通过抑制泛素化作用实现MEIS2的O-GlcNAc修饰稳定化。a、b shCtrl和shOGT HEPM 细胞中MEIS2蛋白水平的Western印迹(WB)及半定量分析。shOGT是short hairpin OGT(OGT 慢病毒)的缩写。c shCtrl和shOGT HEPM 细胞中MEIS2 mRNA水平的qRT-PCR结果。d HEPM 细胞在经DMSO、30 μmol/L Thiamet G或30 μmol/L OSMI -1处理12小时后,接受10 μmol/L MG132处理8小时。通过WB观察MEIS2表达。e、f HEPM 细胞中MEIS2的半衰期分析。经250 μmol/L CHX 处理指定时间后,通过免疫印迹(IB)观察细胞中MEIS2水平。细胞分别接受DMSO、30 μmol/L OSMI -1或30 μmol/L Thiamet G处理。g HEK293细胞中HA-MEIS2的半衰期分析。经250 μmol/L CHX 处理指定时间后,通过IB观察HEK293细胞中HA-MEIS2水平。转染HA-MEIS2(野生型或S237A)质粒的细胞。h、i 细胞接受DMSO、30 μmol/L Thiamet G或30 μmol/L OSMI -1处理12小时后,通过抗MEIS2或抗HA抗体免疫沉淀观察内源性(h)或外源性(i)MEIS2泛素化。j 细胞转染HA-WT或HA-S237A质粒并经30 μmol/L Thiamet G处理12小时后收集,通过免疫沉淀法检测MEIS2泛素化水平。 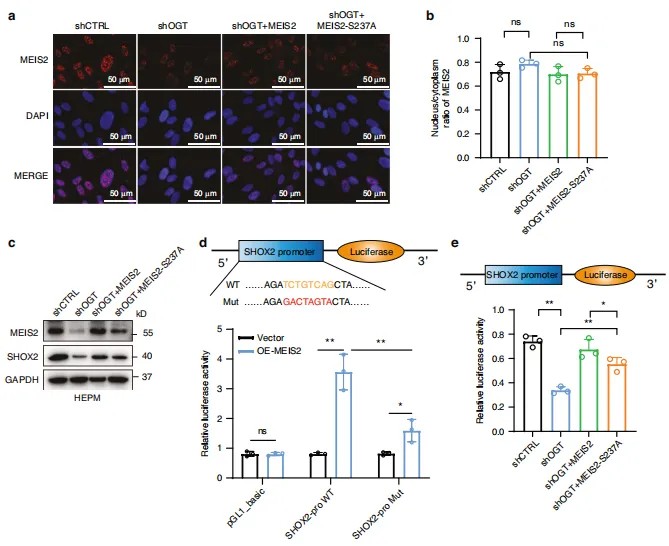
图8:MEIS2 O-GlcNAc化对SHOX2表达的调控。 HEPM 细胞经 OGT shRNA慢病毒载体转染以诱导内源性 OGT 敲低,随后感染表达MEIS2(野生型或S237A突变体)的质粒。a 上述处理条件下 HEPM 细胞中MEIS2的代表性免疫荧光染色结果。b 采用抗MEIS2抗体对核质组分进行免疫共沉淀(IB),并定量分析MEIS2在核质中的比例分布。n=3次生物学独立实验。c 上述处理条件下 HEPM 细胞中SHOX2与MEIS2蛋白水平的蛋白质印迹(WB)分析。d 双荧光素酶报告基因实验显示MEIS2过表达对 HEPM 细胞中SHOX2启动子相对活性的影响。n=3次生物学独立实验。e 通过双荧光素酶报告基因实验测定SHOX2启动子荧光素酶报告构建体的活性。n=3次生物学独立实验。 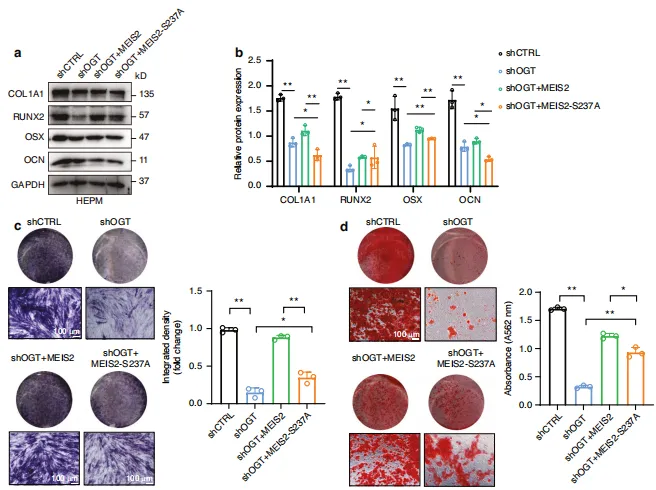
图9:MEIS2的O-GlcNAc修饰在体外促进腭部成骨发育。 HEPM 细胞通过转染 OGT shRNA慢病毒载体诱导内源性 OGT 基因敲低,随后感染表达MEIS2(野生型或S237A突变体)的质粒。a、b 采用蛋白质印迹法及半定量分析检测 HEPM 细胞中成骨分化标志蛋白的表达水平(处理方法同上)。c、d 对指定处理的 HEPM 细胞进行碱性磷酸酶(ALP)和抗原识别序列(ARS)染色。 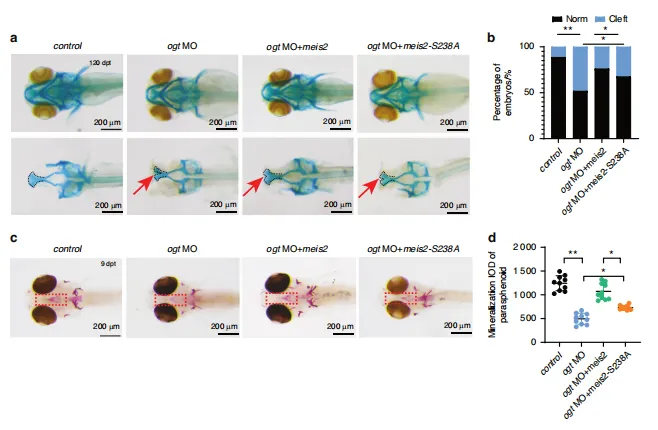
图10:MEIS2的O-糖基化修饰在体内促进腭部成骨发育。a 120小时受精后斑马鱼幼体经阿尔新蓝染色图像。黑色虚线表示筛骨腭部。b 对斑马鱼胚胎腭裂发生率进行定量分析。n=3次生物学独立实验。c 9日龄斑马鱼幼体ARS染色图像。d 对(c)图中蝶骨旁骨矿化 IOD 进行半定量分析。n=10。 
#牙周炎#口腔科#口腔科医生#口腔科科研#牙周病科#口腔医院 源于Zhongyin Zhang的论文《OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development》(2025年),因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。 医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI 
科研信息合集 高分文献解析 国自然立项 展博课题申报 医学硕博论文解析 消化领域科研分享 呼吸领域科研分享 国自然设计思路 皮肤科科研分享

图文结果解读










研究结论
总之,本研究证实 OGT 介导的OGlcNAc化通过抑制MEIS2泛素化来稳定其结构,从而调控腭部发育过程中的成骨分化。Ser237被鉴定为MEIS2的关键O-GlcNAc化位点。这些发现为腭裂的分子诊断提供了新见解,并提出 OGT -MEIS2轴可作为潜在治疗靶点。

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究
本文来自网友投稿或网络内容,如有侵犯您的权益请联系我们删除,联系邮箱:wyl860211@qq.com 。
