2026年南京大学医学院方雷团队和南京鼓楼医院李森团队发表名为“Plasma Proteomic Profiling Identifies a Six-Protein Panel for Grading and Predicting Intervertebral Disc Degeneration”文章,通过病例对照研究,用 SomaScan 技术对比 Ⅱ、Ⅴ 级 IDD 患者血浆,筛选出 COL6α3 等 6 个差异显著蛋白;经 50 例患者酶联免疫吸附试验(ELISA )验证后构建六蛋白组合模型,AUC 达 0.8700,为 IDD 早期诊断提供了无创、快速的血浆生物标志物,由云准实验室提供SomaScan检测服务。
热烈祝贺南京大学医学院方雷团队和南京鼓楼医院李森团队发表重要研究成果,感谢您对云准实验室的信任与支持,云准作为国内首家SOMAscan授权实验室,必将以专业的实验水平,优异的实验数据为您的研究助力。
椎间盘退变(IDD)是全球范围内高发的慢性骨骼肌肉疾病,可引发顽固性腰背痛、肢体功能障碍等问题,累及各年龄阶层且在中老年群体中尤为突出,严重降低患者生活质量,也给全球医疗体系带来沉重负担。目前 IDD 的病理机制尚未被完全阐明,临床评估病情依赖医师主观判读,存在操作难度大、评价结果不客观的问题,且缺乏能实现早期诊断、动态监测的无创手段。血浆因成分稳定、易采集,是理想的无创生物标志物来源,已在多种肿瘤的早诊和预后评估中广泛应用,而 SomaScan 适配体技术的发展,为 IDD 血浆蛋白标志物的筛选提供了技术支撑。
筛选队列:20例IDD患者,按Pfirrmann分级分为Ⅱ级(n=10)和Ⅴ级(n=10),用于 SomaScan蛋白质组学分析,筛选差异表达蛋白。
验证队列:50例IDD患者,同样分为Ⅱ级(n=25)和Ⅴ级(n=25),用于ELISA验证候选蛋白,并构建和评估预测模型。
图1.IDD生物标志物筛选流程示意图
不同椎间盘退变分级患者的血浆临床特征
本研究依据 Pfirrmann 分级系统,对不同退变程度的IDD患者的血浆临床特征进行了分析,本研究纳入的 Ⅱ 级退变病例均符合髓核部分纤维化但椎间盘高度维持正常的标准,而 Ⅴ 级退变病例则严格符合髓核信号丢失伴随椎间隙塌陷的终末期特征(图 2A)。MMP3、MMP13、ADAMTS4 和 ADAMTS7 的活性升高会通过分解胶原和聚集蛋白聚糖,破坏椎间盘结构与功能,进而促进椎间盘退变进展,这些标志物也可作为该疾病的潜在生物标志物。作者得到了 MMP3、MMP13、MMP3、MMP13、ADAMTS4 和 ADAMTS7 的蛋白印迹结果(图 2D),并以 β- 肌动蛋白的相对蛋白表达量为参照完成了定量分析(图 2E),这进一步验证了本研究中样本分级的可靠性。
图2.不同椎间盘退变(IDD)分级患者的临床特征
利用 SomaScan 技术鉴定与椎间盘退变分级相关的血浆蛋白
本研究借助高通量 SomaScan 蛋白质组学技术平台,对 20 例IDD患者的血浆样本开展了全面的蛋白质组学分析,其中包含 10 例 Ⅱ 级退变患者和 10 例 Ⅴ 级退变患者。通过主成分分析(PCA)对血浆蛋白质组学数据进行整体评估,结果显示样本的组内重复性良好,组间差异则具有统计学显著性(图 3A)。研究筛选出 208 种在样本中呈现出统计学显著且一致性差异表达的蛋白,107 种蛋白显著上调、101 种蛋白显著下调,呈现出明确的表达差异模式,同时绘制火山图和热图将该表达差异可视化,并重点标注出了一组上调最为显著的蛋白(图 3B、C)。在GO和KEGG的通路注释分析中发现,发现这些差异蛋白显著富集于与人类免疫系统及细胞外基质(ECM)组装相关的通路。在GO功能注释分析中,上调蛋白主要富集于细胞外基质免疫调控及免疫应答激活相关通路(图 3D)。这一研究结果在GO、REACTOME 通路分析中也得到进一步验证,结果显示这些蛋白在补体激活和固有免疫应答相关通路中显著富集,包括补体与凝血级联反应通路(hsa04610),这表明椎间盘退变晚期与免疫微环境的活跃改变密切相关(图 3E)。与此同时作者开展了 REACTOME 通路富集分析(图 3G),明确了此类蛋白在相关生物通路中的富集特点。
图3.利用SomaScan检测法鉴定血浆中IDD分级相关蛋白
蛋白质组学分析中差异表达血浆蛋白的定量检测
研究中作者注意到,随着椎间盘退变程度的加重,一组差异表达蛋白质呈现出显著的聚类特征,且变化倍数较大,该聚类包含COL6α3、REG1β、ATF5、CAP1、MAGEA4和LILRB3等蛋白质。接着对差异表达蛋白进行了定量分析,结果显示:ATF5(图 4A)、CAP1(图 4B)、REG1β(图 4E)和 LILRB3(图 4F)在 Ⅱ 级与 Ⅴ 级退变组间存在显著表达差异(p值<0.05);MAGEA4(图 4C)和 COL6α3(图 4D)的表达差异更为显著(p值<0.01)。值得注意的是,ATF5 可调控线粒体应激反应,CAP1 参与细胞应激适应,REG1β 可调节与应激颗粒形成相关的蛋白磷酸酶活性,LILRB3 影响免疫微环境调控,MAGEA4 在 DNA 损伤应答及肿瘤发生中起关键作用,而 COL6α3 则有助于维持ECM的稳定性。这些差异表达蛋白共同在细胞外基质重塑、应激反应调控及免疫动态平衡中发挥关键作用,凸显了它们在IDD进展中的重要性。其中,COL6α3 作为细胞外基质的重要组成成分,其表达水平变化尤为显著(p值 = 0.0053),这可能与椎间盘退变过程中发生的结构损伤直接相关。此外,MAGEA4和 LILRB3等免疫相关蛋白的差异表达,进一步证实了免疫调控在椎间盘退变中的关键作用。
图4.蛋白质组学分析中差异表达蛋白定量研究
更大规模IDD患者队列中差异表达血浆蛋白的ELISA验证
随后作者在更大规模的血浆样本队列中通过ELISA对这些蛋白进行了验证,该队列共包含 50 例患者的样本。验证结果证实,这六种蛋白在上述两个退变分级组间呈现出稳定且显著的表达差异,柱状图展示了这六种蛋白的表达差异情况,分别为 ATF5(图 5A)、CAP1(图 5B)、MAGEA4(图 5C)、COL6α3(图 5D)、REG1β(图 5E)和 LILRB3(图 5F)。具体而言,应激调控因子ATF5在 Ⅴ 级组中的表达水平(2.495 ± 0.8256 ng/mL)较 Ⅱ 级组(1.502 ± 0.5074 ng/mL)显著升高,差异具有高度统计学意义。细胞骨架调控蛋白CAP1的表达量也由 Ⅱ 级组的 3.236 ± 1.229 ng/mL 升高至 Ⅴ 级组的 5.754 ± 4.114 ng/mL。最为显著的是,ECM核心成分COL6α3在 Ⅴ 级组中的浓度(23.73 ± 4.591 ng/mL)显著高于 Ⅱ 级组(19.40 ± 2.800 ng/mL)。免疫调控分子LILRB3由 Ⅱ 级组的 10.00 ± 1.621 ng/mL 升高至 Ⅴ 级组的 11.25 ± 0.8256 ng/mL,呈显著上升趋势;而肿瘤相关抗原MAGEA4同样表现出大幅升高,由 Ⅱ 级组的 2.825 ± 0.7773 ng/mL 上升至 Ⅴ 级组的 6.236 ± 5.889 ng/mL。此外,组织修复相关蛋白 REG1β 在 Ⅴ 级退变组中的浓度(90.06 ± 31.34 ng/mL)较 Ⅱ 级退变组(69.59 ± 12.01 ng/mL)显著升高。这些结果通过 ELISA 实验验证了本研究前期蛋白质组学结果的可靠性,同时揭示了上述分子在IDD进程中的动态变化,这为构建基于外周血生物标志物的退变分级诊断体系提供了实验依据。值得注意的是,MAGEA4表现出最大的表达倍数变化(2.2 倍),COL6α3稳定的差异表达特征凸显了其作为临床诊断标志物的潜力。
图5.ELISA 验证结果展示在更大规模IDD患者队列中存在差异蛋白表达
基于 ROC 分析的候选血浆蛋白对IDD进展的预测效能
通过ROC 曲线分析,作者系统评估了候选蛋白对IDD发生发展的预测效能,具体结果如下:在单一蛋白预测模型中,所有生物标志物均表现出良好的预测能力,其中ATF5预测效果最优(AUC = 0.8672),其次为 MAGEA4(AUC = 0.8243)和 COL6α3(AUC = 0.7840);REG1β(AUC = 0.7512)、CAP1(AUC = 0.7288)及 LILRB3(AUC = 0.7120)亦表现出中等预测价值(图 6A)。基于在提升诊断效能的同时兼顾临床可行性这一原则,作者采用二元 logistic 回归构建了多蛋白联合预测模型。在模型构建过程中综合考虑了三个关键因素:(1) 验证队列中差异具有统计学意义;(2) 血浆蛋白浓度的可检测性;(3) 临床应用的便捷性。最终构建的六蛋白联合模型(REG1β、COL6α3、ATF5、CAP1、MAGEA4、LILRB3)表现出最优的预测效能(AUC = 0.8700)(图 6B);而精简后的五蛋白联合模型(REG1β、COL6α3、ATF5、MAGEA4、LILRB3,AUC = 0.7989)在保持较高预测准确度的同时,具备更好的临床实用性。另一组五蛋白联合模型(REG1β、COL6α3、CAP1、MAGEA4、LILRB3)的预测准确度略低(AUC = 0.7700)(图 6C)。随着纳入蛋白数量的减少,模型的预测效能呈梯度下降趋势:四蛋白联合模型(REG1β、COL6α3、MAGEA4、LILRB3,AUC = 0.7011)和三蛋白联合模型(REG1β、COL6α3、MAGEA4,AUC = 0.6978)的预测能力均显著降低(图 6D)。同时,本研究结合大样本患者队列的 ELISA 验证蛋白浓度结果与 ROC 预测分析得到的最佳临界值,制定了相应诊断标准:COL6α3:≥22.73 ng/mL;MAGEA4:≥3.9 ng/mL;REG1β:≥87.5 ng/mL;ATF5:≥1.67 ng/mL;LILRB3:≥10.12 ng/mL;CAP1:≥3.838 ng/mL。本研究中采用所有血浆蛋白的浓度绘制 ROC 曲线以进行预测分析,为评估模型的预测效果并提升其稳定性,运用了机器学习中常用的五折交叉验证法,该方法可保证模型具备良好的可靠性。经交叉验证的严格评估,结果表明该模型具有稳健的预测性能,可有效、准确地反映椎间盘退变的进程。上述结果证实了单个生物标志物的诊断价值,更为重要的是,通过多指标联合分析可显著提高预测准确度,这为IDD 临床诊断模型的构建提供了重要依据。
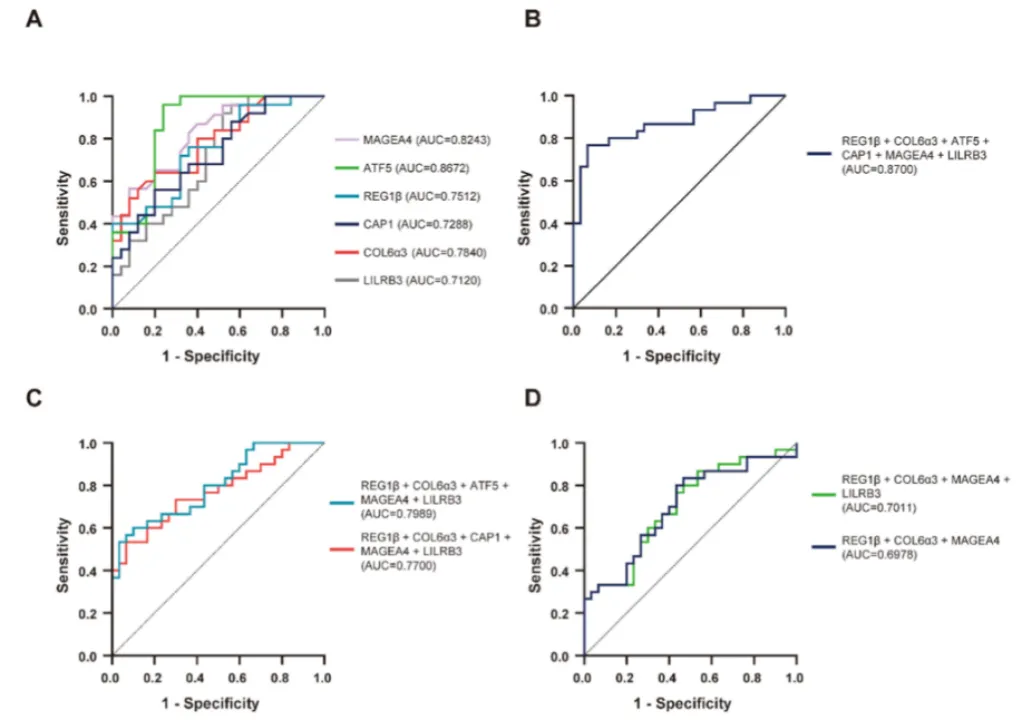
图6.基于ROC分析候选血浆蛋白及其组合对IDD进展预测效能
本研究基于 SomaScan 高通量血浆蛋白质组学技术,对比分析了 Ⅱ 级和 Ⅴ 级IDD患者的血浆样本,鉴定出 208 个差异表达蛋白,其中 Ⅴ 级患者中 107 个蛋白上调、101 个蛋白下调,且差异蛋白显著富集于免疫调控和ECM重塑相关通路。研究筛选出 COL6α3、REG1β、ATF5、CAP1、MAGEA4、LILRB3 这 6 个差异倍数最高的蛋白作为核心候选生物标志物,并在 50 例大样本队列中通过 ELISA 验证,证实其在不同退变分级中存在稳定且显著的表达差异。进一步经 ROC 曲线分析构建预测模型,发现六蛋白联合模型预测效能最优(AUC=0.8700),同时结合 ELISA 浓度数据与 ROC 最佳临界值制定了对应的诊断标准;五折交叉验证则证实该模型具备稳健的预测性能,可准确反映 IDD 进展程度。此外研究还揭示了这 6 个蛋白参与 IDD 进程中的 ECM 重构、应激反应与免疫微环境调控,为疾病发病机制提供了新的分子视角。该研究建立的无创血浆蛋白标志物组合,可弥补传统 MRI Pfirrmann 分级主观化的不足,为 IDD 的早期筛查、退变分级诊断及个性化治疗提供了重要的实验依据与新方法,同时也为 IDD 的靶向治疗挖掘了潜在分子靶点。
云准医药科技(上海)有限公司是一家专注于提供单细胞多组学、空间多组学和SomaScan蛋白质组学科研服务的公司。
围绕疾病生物学研究、药物研发、新型诊断技术开发等生物医学领域和公共卫生等全民健康领域,云准实验室已经与众多客户产生合作。
合作方向涉及肿瘤、免疫、慢病、罕见病等诸多方向以及公共卫生等全民健康领域。涉及疾病机理机制研究和分子分型、生物标记物发现、药物新靶点发现、药物机理机制研究、临床前和临床研究以及临床检测等细分领域。
一直以来,质量意识和技术创新都是云准实验室的立身之本。
未来,云准将以创新为驱动,继续对产品进行深度整合与开发,推动慢病诊疗、罕见病研究、肿瘤免疫治疗、病理诊断技术以及药物研发领域的突破性发展,必将为这些领域带来革命性变化。
单细胞+空间多组学技术服务
单细胞原位空间蛋白组表型分析服务 | 空间转录组整体解决方案服务 | PhenoImager多色荧光免疫成像技术服务 | 单细胞多组学解决方案 | 流式细胞分选技术服务 | 激光显微切割服务
显微成像扫片服务
活细胞成像及玻片扫描服务 | Marianas LightSheet 成像技术服务 | CTLS 组织透明化成像服务
基因测序服务
全外显子测序服务 | MassARRAY 核酸质谱基因分型检测 | 肿瘤分子诊断服务
高通量蛋白组学服务
SomaScan新一代高通量蛋白组学检测服务 | Krex自身抗体检测方案
全代谢组检测服务
非靶向代谢检测服务 | 全靶向代谢检测服务 | 靶向代谢检测服务
云准医药科技(上海)有限公司
地址:上海市徐汇区桂平路333号5号楼7楼
电话:021-64157928
邮箱:marketing@accuramed.com
云准医药科技(广州)有限公司
地址:广州市海珠区广州国际生物岛,百济神州创新中心5楼510-511
电话:020-22066070
雲準生物科技有限公司
地址:香港新界香港科技园二期9W1楼CCC13室
电话:852 5933 6081