2025国自然立项图谱:南京医科大学附属无锡人民医院,从乳酸化到胞外诱捕网,机制研究的精度卡在哪一层?
- 2026-04-16 02:23:54
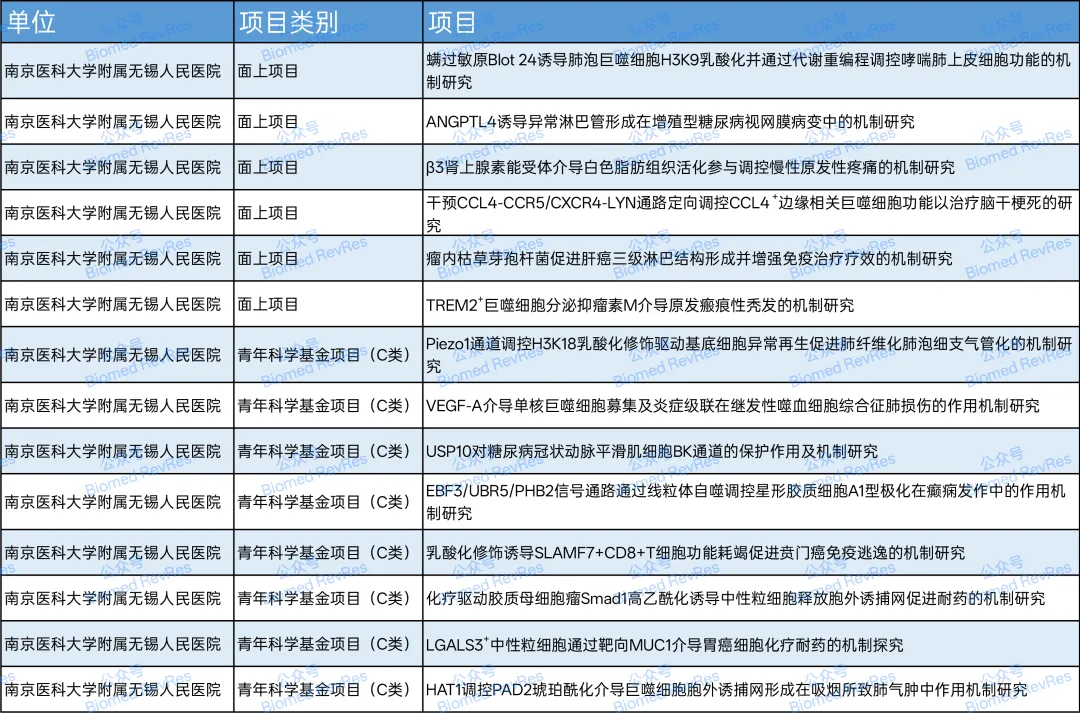
整理到无锡人民医院14项的立项信息,面上6项、青年C类8项。疾病谱拉一下:哮喘、糖尿病视网膜病变、慢性疼痛、脑干梗死、肝癌、瘢痕性秃发、肺纤维化、噬血细胞综合征、糖尿病冠脉病变、癫痫、贲门癌、胶质母细胞瘤、胃癌、肺气肿——跨度可以感受一下。
乳酸化修饰冒出来三次,哮喘一次、肺纤维化一次、贲门癌一次,三个病八竿子打不着,修饰位点也不一样。胞外诱捕网也出来两次,一次在胶质母细胞瘤的化疗耐药里,一次在吸烟肺气肿里,两边不约而同地把问题往上游推——不是问"ETs有没有用",而是问"谁在调控ETs的形成",而且都落到了翻译后修饰上。再就是好几个项目写靶点的方式变了,不写"巨噬细胞",写"CCL4⁺边缘相关巨噬细胞";不写"中性粒细胞",写"LGALS3⁺中性粒细胞"——没有单细胞测序,这些亚群根本分不出来。
南京医科大学附属无锡人民医院2025年国自然立项项目清单
南京医科大学附属无锡人民医院2025年国自然立项核心科研思路拆解表
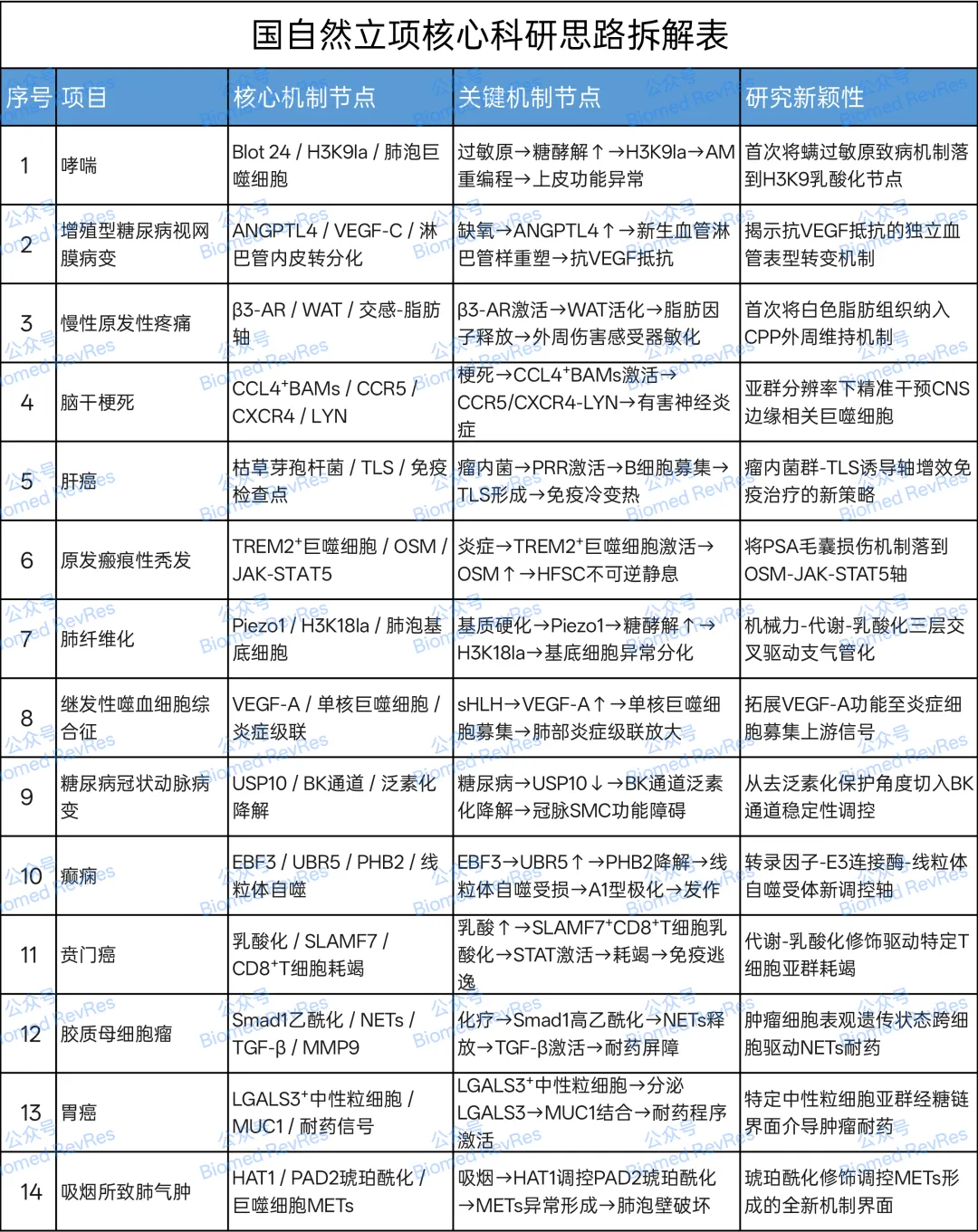
一、乳酸化修饰的三个战场:从哮喘巨噬细胞到纤维化基底细胞,再到贲门癌T细胞耗竭
乳酸化这个方向,2019年那篇Nature[1]之后发了很多文章,多到现在看到"乳酸化"三个字我会先停一下——先看它到底说了什么,是真的在问修饰怎么决定细胞命运,还是只是报告了"这里也有乳酸化"。后者占多数。无锡这三个项目属于前者,各自切的细胞、位点、疾病都不一样,但都在问同一件事:代谢状态变了,表观遗传程序怎么跟着变。
第一个战场:螨过敏原Blo t 24-H3K9乳酸化-哮喘肺上皮细胞功能。 热带无爪螨(Blomia tropicalis)在热带亚热带是仅次于尘螨的主要致敏螨种,过敏原组分有过系统鉴定[2]。Blo t 24是其中近年命名的一个,UQCRB家族,线粒体呼吸链复合物III的亚基。说白了,这个过敏原是线粒体蛋白。这个事实本身就值得停一下想想:线粒体蛋白怎么变成过敏原的,致敏机制跟蛋白酶类过敏原肯定不是一条路——后者靠破坏上皮屏障,Blo t 24走的是激活固有免疫受体、启动IgE应答。研究的切入点在肺泡巨噬细胞(AM)的H3K9乳酸化(H3K9la):过敏原暴露推高糖酵解,乳酸积累,H3K9la升高,AM的基因表达程序被改写,对气道上皮的调控跟着变。以前做哮喘研究,AM那边问的是分泌了什么细胞因子;现在这个项目问的是AM通过哪个修饰事件改变了自身的调控能力。这两个问法能找到的靶点,精度差很远。
第二个战场:Piezo1-H3K18乳酸化-肺纤维化肺泡支气管化。 肺泡支气管化(bronchiolization)——肺纤维化进展到某个阶段,肺泡上皮开始被支气管样上皮替换,基底细胞的再生方向跑偏了。Piezo1在肺部疾病里的机械力感知有过报道[3],这不是新鲜事。新的地方在后面:Piezo1激活之后,钙信号怎么一路影响到组蛋白修饰,再影响到基底细胞往哪个方向分化。具体说,钙信号进来,代谢状态变,糖酵解通量上去,H3K18乳酸化(H3K18la)水平跟着升,基底细胞的分化程序在表观遗传层面被重新写了一遍,支气管化相关基因开了。机械力、代谢、修饰、分化方向,四件事能不能串成一条链,是这个项目要验证的核心。能串上,这条链就是一个可以被干预的靶点序列;串不上,就得重新找断点在哪里。
第三个战场:乳酸化修饰-SLAMF7⁺CD8⁺T细胞耗竭-贲门癌免疫逃逸。 贲门癌(胃食管结合部腺癌)肿瘤微环境中的高乳酸状态是Warburg效应的直接产物。SLAMF7(信号淋巴细胞激活分子家族成员7)是一个在CD8⁺T细胞耗竭研究中受到关注的免疫受体,其信号通路通过激活STAT1和STAT3,诱导多个耗竭相关基因的表达,驱动T细胞逐渐丧失效应功能[4]。这项研究的假说是:肿瘤微环境中积累的乳酸,通过乳酸化修饰影响SLAMF7⁺CD8⁺T细胞的关键功能蛋白,在表观遗传层面加速其走向耗竭状态,构成贲门癌免疫逃逸的一个上游代谢-修饰驱动机制。这个切入点把"肿瘤代谢如何压制免疫细胞"这个宏观问题,落到了一个具体的修饰事件和特定T细胞亚群上。
三个战场放在一起,有一个值得注意的结构性差异:H3K9la和H3K18la的修饰位点不同,功能效应可能有所分化——近年研究显示,H3K9la和H3K18la在CD8⁺T细胞激活后均显著积累,但在不同细胞类型和疾病背景下的调控方向并不完全一致[5]。乳酸化的靶细胞从巨噬细胞到上皮细胞再到T细胞,跨越了固有免疫、上皮稳态和适应性免疫三个层面。这说明乳酸化修饰的生物学意义远不止于某一类细胞或某一类疾病,而是一个在不同细胞类型和疾病背景下均有独立干预价值的代谢-表观遗传界面。
二、ANGPTL4-淋巴管样重塑:把增殖型糖尿病视网膜病变的抗VEGF抵抗落到了血管表型转变的分子解释层
增殖型糖尿病视网膜病变(PDR)的抗VEGF治疗,临床上存在相当比例的应答不佳患者——这个现象提示PDR的血管病理不是只有VEGF一条驱动轴在工作。ANGPTL4(血管生成素样蛋白4)在缺氧条件下由视网膜细胞高度诱导表达,在PDR患者玻璃体液中的浓度显著升高,且在抗VEGF治疗后浓度不受影响——这一点直接说明ANGPTL4代表了一条独立于VEGF的病理通路[6]。
最新研究发现,ANGPTL4在PDR中诱导的血管重塑并非经典的血管新生模式,而是一种异常淋巴管样重塑:视网膜新生血管获得了淋巴管内皮细胞的分子标志物和功能特性,同时玻璃体液中VEGF-C水平也显著升高[7]。这个发现的临床意义相当直接:如果部分PDR患者的新生血管已经发生了淋巴管样转变,那么这类血管对抗VEGF的敏感性就可能与典型血管新生不同,这为抗VEGF抵抗提供了一个此前缺失的分子解释。ANGPTL4通过什么受体信号、在哪个细胞类型中触发了淋巴管内皮转分化程序,是这项研究要系统回答的核心机制问题。如果这条轴能被明确,ANGPTL4就不只是"VEGF之外的血管因子",而是PDR血管病理中一个具有独立干预价值的靶点,为抗VEGF抵抗患者提供新的治疗策略。
三、β3肾上腺素能受体-白色脂肪组织:把慢性原发性疼痛的外周机制推进到了脂肪-神经轴的新界面
慢性原发性疼痛(CPP)的发生机制长期以来被主要归因于中枢敏化,但外周机制的贡献——尤其是非神经组织如何参与痛觉维持——是近年来疼痛研究的新兴方向。白色脂肪组织(WAT)密集分布着交感和感觉神经末梢,WAT脂肪分解产生的信号可以直接激活局部感觉传入神经,形成WAT与中枢神经系统之间的神经回路[8]。
β3肾上腺素能受体(β3-AR)是WAT上表达最丰富的肾上腺素能受体亚型,其激活驱动脂肪分解、产热和局部炎症信号的释放。这项研究的核心假说是:β3-AR介导的WAT活化——包括脂肪分解产物的释放、脂肪因子谱的改变、局部免疫细胞的募集——通过影响周围神经的微环境,参与调控慢性原发性疼痛的维持。这个假说把疼痛研究的视野从"神经-神经"的经典框架,拓展到了"脂肪-神经"这个在CPP语境里几乎没有被系统研究过的界面。β3-AR在WAT中具体通过哪条信号路径影响伤害感受器的敏感性,是这项研究需要在分子层面精确回答的问题——如果这条轴能被验证,WAT的代谢状态和交感张力就成为CPP干预的一个全新外周靶点。
四、CCL4⁺边缘相关巨噬细胞-CCL4-CCR5/CXCR4-LYN:把脑干梗死的治疗靶点推进到了特定巨噬细胞亚群的精准调控层
脑干梗死的神经炎症干预,面临一个根本困境:大脑的炎症反应中,促炎和抗炎功能往往由不同的细胞亚群承担,笼统抑制炎症可能同时损害有利于修复的免疫功能。CCL4⁺边缘相关巨噬细胞(BAMs)是单细胞测序研究揭示的一类特定CNS巨噬细胞亚群,定居于脑膜、脉络丛和血管周围间隙,是大脑与外周免疫系统之间的界面细胞。在缺血性卒中后,BAMs的功能状态发生显著改变,不同亚群在神经保护和神经损伤中的作用方向截然不同,其动态转录变化为靶向干预提供了理论依据[9]。
这项研究的机制链落在CCL4-CCR5/CXCR4-LYN通路上。CCL4作为趋化因子,通过CCR5和CXCR4双受体信号调控巨噬细胞的迁移和功能状态;LYN是一个非受体酪氨酸激酶,在免疫细胞的激活阈值调控中有关键作用,也是CCR5/CXCR4下游信号的重要整合节点。干预这条通路轴,目标是在不影响有益免疫功能的前提下,通过精准调控CCL4⁺BAMs这一特定亚群,减轻脑干梗死后的有害神经炎症。这个精度——不是"抑制炎症",而是"定向调控特定巨噬细胞亚群的特定信号轴"——是这项研究区别于一般神经炎症研究的核心所在,也是单细胞测序技术进入机制研究之后,选题精度所能达到的新层次。
五、瘤内枯草芽孢杆菌-三级淋巴结构:把肝癌免疫治疗增效的策略推进到了瘤内菌群-TLS诱导的新轴
肝癌免疫治疗的获益率仍然有限,核心障碍是相当比例的肝癌处于免疫"冷"状态——T细胞浸润不足,缺乏有效的局部抗肿瘤免疫应答。三级淋巴结构(TLS)是在肿瘤微环境中形成的异位淋巴组织,其存在与肝癌患者更好的预后和免疫治疗获益密切相关,是将"冷"肿瘤转变为"热"肿瘤的重要机制[10]。
瘤内细菌对肿瘤免疫微环境的调控,是近年来肿瘤生物学的重要新方向——在胰腺癌中已有研究证实,瘤内微生物组的多样性和组成能够通过重塑局部免疫应答影响患者预后[11]。基于这一发现,瘤内特定细菌能否通过激活免疫信号、募集B细胞和T细胞前体来诱导TLS形成,是本研究要在肝癌中系统验证的核心假说。枯草芽孢杆菌作为一种革兰氏阳性菌,其对模式识别受体的激活和对先天免疫信号的诱导,使其具备促进TLS形成的潜在能力。这项研究的核心假说是:瘤内枯草芽孢杆菌通过激活特定免疫信号,诱导肝癌微环境中TLS的形成,从而增强免疫检查点抑制剂的治疗效果。枯草芽孢杆菌通过什么分子机制驱动TLS形成——是通过改变趋化因子谱募集B细胞和T细胞前体,还是通过激活树突状细胞启动局部免疫组织化——这些问题的答案,决定了这条轴能否成为肝癌免疫治疗增效的可操作靶点。把"瘤内菌群"和"TLS诱导"两个当前肿瘤免疫领域最活跃的方向连接在同一个实验框架内,在肝癌这个具体适应症里是一个相当新颖的切入点。
六、TREM2⁺巨噬细胞-抑瘤素M:把原发瘢痕性秃发的发病机制落到了皮肤巨噬细胞亚群-毛囊干细胞静息轴
原发瘢痕性秃发(PSA)以毛囊永久性破坏为特征,炎症细胞浸润毛囊周围是其核心病理,但"哪种炎症细胞通过什么分子机制导致了毛囊干细胞的不可逆损伤",一直缺乏精确的机制解释。
TREM2⁺真皮巨噬细胞是皮肤免疫微环境中一个功能高度特化的亚群。发表于Cell Stem Cell的研究系统揭示了这一亚群的核心功能:TREM2⁺真皮巨噬细胞通过分泌抑瘤素M(Oncostatin M,OSM),激活毛囊干细胞(HFSC)上的JAK-STAT5信号,维持HFSC的静息状态,抑制毛发生长周期的启动[12]。这一机制在正常毛发周期调控中有生理意义,但在PSA的炎症微环境中,TREM2⁺巨噬细胞的异常激活和OSM的过度分泌,可能将HFSC的静息状态推向不可逆的功能丧失,最终导致毛囊的永久性破坏。
这项研究把OSM-JAK-STAT5轴引入PSA的发病机制框架,是一个在机制精度上明显超越"炎症导致毛囊损伤"这一描述性结论的切入点。TREM2⁺巨噬细胞在PSA局部如何被激活、OSM的分泌量与HFSC损伤程度之间的定量关系,以及干预这条轴能否在动物模型中阻止毛囊的不可逆破坏——这三个问题的系统回答,将为PSA提供一个此前缺失的分子靶点,也为JAK抑制剂等已有药物在PSA中的应用提供新的机制依据。
七、胞外诱捕网的两种调控逻辑:Smad1高乙酰化驱动中性粒细胞NETs,HAT1-PAD2琥珀酰化调控巨噬细胞METs
胞外诱捕网(ETs)最初在中性粒细胞中被描述,作为抗感染的防御机制,但在肿瘤和慢性肺病的语境里,它的角色要复杂得多——既可以是肿瘤耐药的促进者,也可以是慢性炎症的放大器。这两项研究分别切入了ETs在两个完全不同场景里的上游调控机制,一个聚焦于中性粒细胞NETs,一个聚焦于巨噬细胞METs(macrophage extracellular traps),共同指向"ETs的形成如何被翻译后修饰精确调控"这个问题。
化疗驱动胶质母细胞瘤Smad1高乙酰化-NETs-耐药。 胶质母细胞瘤(GBM)的化疗耐药是临床治疗的核心障碍。Smad1在GBM中与p53和p300形成竞争性复合物,导致p53乙酰化水平下降而Smad1乙酰化水平升高,这一竞争性乙酰化事件通过削弱p53的促凋亡功能,促进了肿瘤生长和化疗抵抗[13]。与此同时,化疗本身可以诱导肿瘤微环境中的中性粒细胞释放NETs——NETs通过整合素αvβ1捕获潜伏TGF-β、经基质金属蛋白酶9激活后,为肿瘤细胞提供耐药保护[14]。这项研究的核心假说是:化疗驱动的GBM细胞Smad1高乙酰化,是否能够通过改变肿瘤微环境中的信号输出,进而诱导中性粒细胞释放NETs,由此为GBM细胞构建耐药屏障——这个跨细胞调控回路的存在,正是本研究要系统验证的问题。
HAT1-PAD2琥珀酰化-巨噬细胞METs-吸烟肺气肿。 吸烟暴露与肺部PAD2的表达升高之间存在直接关联——吸烟者支气管肺泡灌洗液中PAD2水平显著升高,胞外PAD2的积累与局部炎症反应密切相关[15]。PAD2(肽酰精氨酸脱亚胺酶2)催化蛋白质精氨酸残基的瓜氨酸化,是METs形成的关键酶,METs的形成机制与NETs类似,均需要PAD酶的参与[16]。这项研究的新颖之处,在于提出了HAT1(组蛋白乙酰转移酶1)可能作为琥珀酰转移酶调控PAD2琥珀酰化状态这一假说——HAT1具有对非组蛋白底物的琥珀酰化催化能力已有报道,但其是否直接靶向PAD2,正是本研究要验证的核心问题。琥珀酰化是通过琥珀酸修饰赖氨酸残基的翻译后修饰,近年来被发现在代谢-炎症调控中有重要作用。吸烟暴露通过影响HAT1对PAD2的琥珀酰化修饰状态,调控PAD2的酶活性和稳定性,进而影响肺泡巨噬细胞METs的形成,驱动肺气肿的慢性炎症进程——这条HAT1-PAD2-METs轴,把吸烟暴露的代谢效应、翻译后修饰调控和巨噬细胞的ETs形成串联在了一起,在COPD/肺气肿的机制研究中是一个相当新颖的分子界面。
两项研究放在一起,有一个共同的方法论逻辑值得指出:它们都不是在问"ETs有没有作用"——这个问题在各自领域已经有了基本答案——而是在问"ETs的形成被哪个翻译后修饰事件所调控,以及这个修饰事件是否构成一个可以被精确干预的上游节点"。这个问题的精度,决定了研究结论能否为后续干预策略提供真正可操作的靶点。
八、USP10-BK通道与EBF3/UBR5/PHB2-线粒体自噬:翻译后修饰调控细胞命运的两个独立节点
这两项研究一个在糖尿病冠脉,一个在癫痫,疾病场景完全不同,但都把干预精度推到了翻译后修饰调控细胞功能的层面,而且都选择了一个此前在各自疾病语境里几乎没有被系统研究过的分子界面。
USP10对糖尿病冠状动脉平滑肌细胞BK通道的保护。 糖尿病冠脉功能障碍不只是粥样硬化斑块的问题,更根本的是冠状动脉平滑肌细胞(SMC)本身的功能改变。BK通道(大电导钙激活钾通道)是冠状动脉SMC中调控血管张力的核心离子通道,其在糖尿病状态下的功能受损——蛋白水平下降和开放概率降低——是糖尿病冠脉微循环障碍的重要分子基础。在糖尿病冠脉疾病中,E3泛素连接酶介导的BK通道蛋白泛素化降解,是通道蛋白水平下调的关键机制[17]。USP10(泛素特异性蛋白酶10)是一个去泛素化酶,通过去除靶蛋白上的泛素链来拮抗蛋白酶体降解,维持靶蛋白的稳定性。这项研究的核心假说是:USP10通过去泛素化修饰稳定BK通道蛋白,在糖尿病冠脉SMC中发挥保护功能;糖尿病状态下USP10活性的下调,导致BK通道蛋白的加速降解,是冠脉功能障碍的一个可干预上游节点。这个思路绕开了"直接激活BK通道"的传统路径,从通道蛋白稳定性的泛素化调控切入,提供了一个更上游的干预逻辑。
EBF3/UBR5/PHB2信号通路通过线粒体自噬调控星形胶质细胞A1型极化在癫痫发作中的作用。 A1型极化的星形胶质细胞具有强烈的促炎和神经毒性功能,在癫痫发作后大量出现,是维持癫痫发作易感性和加剧神经元损伤的重要细胞机制,而星形胶质细胞线粒体功能障碍与A1型极化之间的关联,已有初步研究积累[18]。这项研究构建了一条精细的调控轴:EBF3是一个转录因子,参与神经细胞的分化和应激响应;UBR5是一个E3泛素连接酶,通过靶向底物蛋白的泛素化降解调控细胞功能;PHB2(Prohibitin 2)是线粒体内膜上的支架蛋白,已被确认为线粒体自噬的关键受体,通过与LC3直接结合介导受损线粒体的选择性清除[19]。研究假说是:EBF3通过转录调控UBR5的表达,UBR5通过泛素化修饰影响PHB2的稳定性,PHB2水平的改变导致线粒体自噬功能失调,进而驱动星形胶质细胞向A1型极化,促进癫痫发作。从转录因子到E3连接酶到线粒体自噬受体,这条调控链在癫痫的星形胶质细胞研究中是一个相当新颖的分子框架,把"线粒体质量控制"和"神经炎症细胞极化"两个此前平行推进的研究方向,整合进了同一条可以被逐步验证的机制轴。
九、VEGF-A单核巨噬细胞募集与LGALS3⁺中性粒细胞-MUC1:免疫细胞在炎症失控和肿瘤耐药中的两种异常动员模式
VEGF-A介导单核巨噬细胞募集及炎症级联在继发性噬血细胞综合征肺损伤中的作用。 继发性噬血细胞综合征(sHLH)是一种以失控性免疫激活和多器官损伤为特征的危及生命的综合征,其核心病理是单核细胞和巨噬细胞的过度激活与扩增,肺损伤是其最严重的并发症之一。sHLH中单核细胞对IFN-γ信号的超敏反应[20],是驱动炎症级联持续放大的关键机制。这项研究把VEGF-A的功能从"血管因子"拓展到了"炎症细胞募集信号":在sHLH状态下,高水平的VEGF-A不只是血管渗漏的被动反映,而是通过募集单核巨噬细胞浸润肺组织,主动参与肺部炎症级联的启动和放大——这一募集功能是否构成sHLH肺损伤的关键上游节点,正是本研究要系统验证的问题。
LGALS3⁺中性粒细胞通过靶向MUC1介导胃癌细胞化疗耐药。 LGALS3(半乳糖凝集素-3)在胃癌中的高表达与化疗耐药和不良预后有已知关联,其抗凋亡效应通过多条信号通路实现,包括抑制线粒体凋亡通路和激活AKT/GSK-3β信号[21]。这项研究的新颖之处,在于把LGALS3的作用场景从肿瘤细胞本身,转移到了LGALS3⁺中性粒细胞这一特定免疫细胞亚群上。中性粒细胞在肿瘤微环境中的作用具有高度的亚群依赖性,LGALS3⁺中性粒细胞亚群对肿瘤细胞耐药的促进作用,是一个此前几乎没有被系统研究过的方向。MUC1(黏蛋白1)是胃癌细胞上高度表达的糖蛋白,在肿瘤细胞的凋亡抵抗和信号传导中有重要作用,半乳糖凝集素-3与MUC1之间存在糖链介导的相互作用[22]。这项研究的假说是:LGALS3⁺中性粒细胞通过分泌LGALS3,与胃癌细胞表面的MUC1发生相互作用,激活胃癌细胞的耐药信号程序——这是一个从特定中性粒细胞亚群,经由配体-受体界面,到肿瘤细胞耐药的跨细胞调控机制,在胃癌耐药研究中是一个相当新颖的切入点。
写在最后
乳酸化修饰出现了三次,修饰位点、靶细胞和疾病场景各不相同——这不是选题跟风,而是这个修饰方式本身的生物学覆盖面确实很宽。从2019年的Nature原始论文[1]到现在,乳酸化研究的扩张速度相当快,但大多数研究还停留在"哪些细胞里有乳酸化"这个描述层面,真正把特定位点的乳酸化修饰与具体疾病的细胞命运决定连接起来的研究,仍然相当有限。
胞外诱捕网的两个项目,切入点都在修饰调控层面,而不是在"ETs有没有作用"这个已经有答案的问题上打转。Smad1高乙酰化-NETs这条轴,把肿瘤细胞内的表观遗传状态和肿瘤微环境中免疫细胞的行为接在了一起,是一个跨细胞的调控回路;HAT1-PAD2琥珀酰化-METs这条轴,把一个此前在RA研究中被关注的修饰酶(PAD2)和一个新型翻译后修饰(琥珀酰化)组合在了肺气肿这个新场景里。两者的共同特点,是把"如何调控ETs的形成"这个问题,从细胞生物学层面推进到了修饰化学的精度。
还有一点值得注意:有两个项目同时涉及特定细胞亚群的精准识别——CCL4⁺BAMs和LGALS3⁺中性粒细胞,都是单细胞测序技术进入疾病机制研究之后才能被精确定义的亚群。这个选题逻辑的转变,说明课题组在设计研究假说时,已经不再把"巨噬细胞"或"中性粒细胞"作为均质的效应细胞群体来处理,而是在亚群分辨率下去问"哪个亚群,通过什么分子机制,在疾病进程中起关键作用"——这个精度的差别,是近五年来整个免疫学研究范式转变的一个缩影。
参考文献
[1] Zhang D, Tang Z, Huang H, et al. Metabolic regulation of gene expression by histone lactylation. Nature. 2019;574(7779):575-580. doi:10.1038/s41586-019-1678-1
[2] Santos da Silva E, Asam C, Lackner P, et al. Allergens of Blomia tropicalis: An Overview of Recombinant Molecules. Int Arch Allergy Immunol. 2017;172(4):203-214. doi:10.1159/000464325
[3] Fang XZ, Li M, Wang YX, et al. Mechanosensitive ion channel Piezo1 mediates mechanical ventilation-exacerbated ARDS-associated pulmonary fibrosis. J Adv Res. 2023;53:175-186. doi:10.1016/j.jare.2022.12.006
[4] O'Connell P, Hyslop S, Blake MK, Godbehere S, Amalfitano A, Aldhamen YA. SLAMF7 Signaling Reprograms T Cells toward Exhaustion in the Tumor Microenvironment. J Immunol. 2021;206(1):193-205. doi:10.4049/jimmunol.2000300
[5] Raychaudhuri D, Singh P, Chakraborty B, et al. Histone lactylation drives CD8+ T cell metabolism and function. Nat Immunol. 2024;25(11):2140-2151. doi:10.1038/s41590-024-01985-9
[6] Lu Q, Zou W, Chen B, Zou C, Zhao M, Zheng Z. ANGPTL-4 correlates with vascular endothelial growth factor in patients with proliferative diabetic retinopathy. Graefes Arch Clin Exp Ophthalmol. 2016;254(7):1281-1288. doi:10.1007/s00417-015-3187-8
[7] Li Z, Guan L, Mu T, et al. ANGPTL4 Induces Aberrant Lymphatic-Like Remodeling in Proliferative Diabetic Retinopathy. Diabetes. Published online March 10, 2026. doi:10.2337/db25-0445
[8] Garretson JT, Szymanski LA, Schwartz GJ, Xue B, Ryu V, Bartness TJ. Lipolysis sensation by white fat afferent nerves triggers brown fat thermogenesis. Mol Metab. 2016;5(8):626-634. Published 2016 Jun 30. doi:10.1016/j.molmet.2016.06.013
[9] Yu N, Zhao Y, Wang P, Zhang F, Wen C, Wang S. Changes in border-associated macrophages after stroke: Single-cell sequencing analysis. Neural Regen Res. 2026;21(1):346-356. doi:10.4103/NRR.NRR-D-24-01092
[10] Liu L, Wang Y, Ban J, et al. Intratumoral Tertiary Lymphoid Structures in Hepatocellular Carcinoma: Current Evidence and Future Directions - a Narrative Review. J Hepatocell Carcinoma. 2026;13:595363. Published 2026 Mar 21. doi:10.2147/JHC.S595363
[11] Riquelme E, Zhang Y, Zhang L, et al. Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes. Cell. 2019;178(4):795-806.e12. doi:10.1016/j.cell.2019.07.008
[12] Wang ECE, Dai Z, Ferrante AW, Drake CG, Christiano AM. A Subset of TREM2+ Dermal Macrophages Secretes Oncostatin M to Maintain Hair Follicle Stem Cell Quiescence and Inhibit Hair Growth. Cell Stem Cell. 2019;24(4):654-669.e6. doi:10.1016/j.stem.2019.01.011
[13] Gong L, Xu D, Ni K, et al. Smad1 Promotes Tumorigenicity and Chemoresistance of Glioblastoma by Sequestering p300 From p53. Adv Sci (Weinh). 2025;12(4):e2402258. doi:10.1002/advs.202402258
[14] Mousset A, Lecorgne E, Bourget I, et al. Neutrophil extracellular traps formed during chemotherapy confer treatment resistance via TGF-β activation. Cancer Cell. 2023;41(4):757-775.e10. doi:10.1016/j.ccell.2023.03.008
[15] Damgaard D, Friberg Bruun Nielsen M, Quisgaard Gaunsbaek M, Palarasah Y, Svane-Knudsen V, Nielsen CH. Smoking is associated with increased levels of extracellular peptidylarginine deiminase 2 (PAD2) in the lungs. Clin Exp Rheumatol. 2015;33(3):405-408.
[16] Bashar SJ, Holmes CL, Shelef MA. Macrophage extracellular traps require peptidylarginine deiminase 2 and 4 and are a source of citrullinated antigens bound by rheumatoid arthritis autoantibodies. Front Immunol. 2024;15:1167362. Published 2024 Feb 27. doi:10.3389/fimmu.2024.1167362
[17] Yi F, Wang H, Chai Q, et al. Regulation of large conductance Ca2+-activated K+ (BK) channel β1 subunit expression by muscle RING finger protein 1 in diabetic vessels. J Biol Chem. 2014;289(15):10853-10864. doi:10.1074/jbc.M113.520940
[18] Su Y, Tang M, Wang M. Mitochondrial Dysfunction of Astrocytes Mediates Lipid Accumulation in Temporal Lobe Epilepsy. Aging Dis. 2024;15(3):1289-1295. Published 2024 May 7. doi:10.14336/AD.2023.0624
[19] Wei Y, Chiang WC, Sumpter R Jr, Mishra P, Levine B. Prohibitin 2 Is an Inner Mitochondrial Membrane Mitophagy Receptor. Cell. 2017;168(1-2):224-238.e10. doi:10.1016/j.cell.2016.11.042
[20] Canna SW, Marsh RA. Pediatric hemophagocytic lymphohistiocytosis. Blood. 2020;135(16):1332-1343. doi:10.1182/blood.2019000936
[21] Stojanovic B, Jovanovic I, Dimitrijevic Stojanovic M, et al. Galectins as Master Regulators of Gastric Cancer Progression. Cells. 2025;14(14):1090. Published 2025 Jul 16. doi:10.3390/cells14141090
[22] Radziejewska I. Galectin-3 and Epithelial MUC1 Mucin-Interactions Supporting Cancer Development. Cancers (Basel). 2023;15(10):2680. Published 2023 May 9. doi:10.3390/cancers15102680
-推荐阅读-
决胜2026!更新至4194项!2025国自然获批名单(Plus版) + 2024近万项名单
关于国自然申请,最后这一步还是想提醒一句:形式审查 【提供 2026年度形式审查明细表 下载】
2026年国自然面上/青C模板有调整:关于“AI说明那一项”,我补充说明一下 【提供 2026年面上/青C 申请书模版 下载】
