IF12.7!前天新篇!南京农业大学用“多组学”拿下双一区TOP!揭示毛螺菌科调控乳脂PUFA比例!
- 2026-04-20 12:25:10





牛奶中ω-6/ω-3多不饱和脂肪酸比例过高是影响乳制品营养品质的关键问题,而瘤胃微生物的生物氢化是决定该比例的核心环节。
南京农业大学团队通过对95头荷斯坦奶牛的多组学分析,通过分离培养验证,B. hungatei偏好代谢α-亚麻酸,而Eubacterium_I偏好代谢亚油酸,揭示了底物特异性生物氢化的机制基础。该研究为通过微生物干预优化牛奶脂肪酸组成提供了理论依据。
📢如果你也想用“多组学”发文的话,关注西瓜生信,联系我们带你进一步了解~


文章标题:整合宏转录组学鉴定毛螺菌科为调控瘤胃生物氢化及牛奶ω-6/ω-3 PUFA比例的关键菌群
发表期刊:Microbiome
发表时间:2026年4月13日
影响因子:IF12.7/Q1

研究背景

牛奶是全世界广泛消费的营养食品,但其常规产品中ω-3 PUFA含量低,本研究通过整合宏转录组学、扩增子测序和靶向代谢组学,系统解析了瘤胃微生物调控牛奶ω-6/ω-3 PUFA比例的机制。

研究方法

本研究选取95头泌乳中期的荷斯坦奶牛,采集瘤胃液、血液和牛奶样本,测定脂肪酸组成及瘤胃发酵参数。通过线性混合模型估计“微生物性”,即瘤胃微生物对表型的贡献度。分离培养B. hungatei和Eubacterium_I菌株,进行体外脂肪酸代谢验证和全基因组测序。

你也想挑战前沿生信研究方向?你也想拥有同款高分数据库,却苦于不知从何入手?别再观望了,赶紧联系西瓜生信团队!我们提供全方位专业支持,从数据分析到思路设计,助你轻松搞定科研难题!

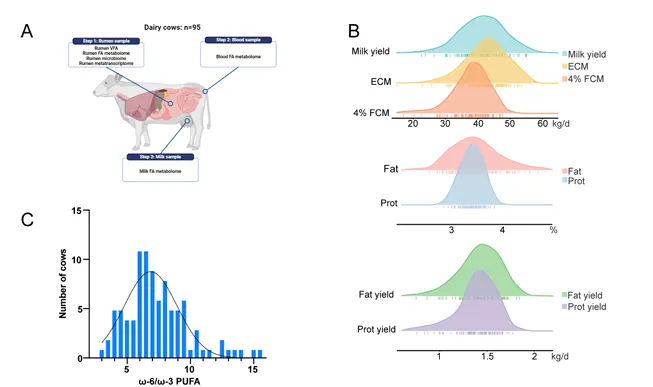
瘤胃细菌群落解释牛奶ω-6/ω-3 PUFA比例41%的变异
95头奶牛的牛奶ω-6/ω-3 PUFA比例范围为2.87至15.16,群体均值为7.18,个体间变异显著。线性混合模型分析显示,瘤胃细菌群落组成解释了41.02%的表型方差,远高于此前报道的甲烷排放和乳蛋白产量(图1)。
这表明瘤胃微生物是调控牛奶脂肪酸组成的关键因素,为后续微生物靶向干预提供了理论依据。
HFR与LFR奶牛瘤胃、血液和牛奶中的脂肪酸差异代谢物
基于GC-MS/MS的靶向代谢组学分析显示,HFR与LFR组在瘤胃、血清和牛奶中均存在显著的脂肪酸差异。LFR组瘤胃中总SFA和PUFA浓度较低,但ALA和花生四烯酸比例更高;HFR组则富含LA及其异构体,ω-6/ω-3比例更高(图2)。
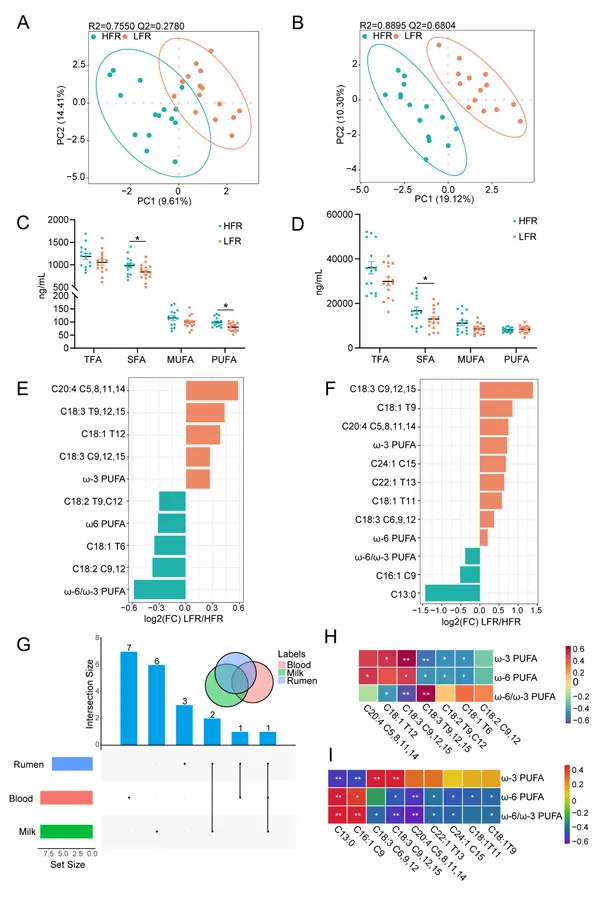
图2.HFR与LFR奶牛瘤胃和血液脂肪酸组成的差异
三组学联合分析发现,ALA在瘤胃、血清和牛奶中均差异显著,LA在瘤胃和牛奶中差异显著。相关性分析表明,瘤胃中C18:3 T9,12,15与牛奶ω-3 PUFA含量正相关,而C18:2 C9,12与牛奶ω-6/ω-3比例正相关。
HFR与LFR奶牛瘤胃微生物群落的差异
PCoA分析显示HFR与LFR组细菌群落显著分离,而真菌也有差异,但产甲烷古菌和原生动物无显著差异。HFR组细菌Shannon多样性更高,LFR组原生动物多样性更高(图3)。
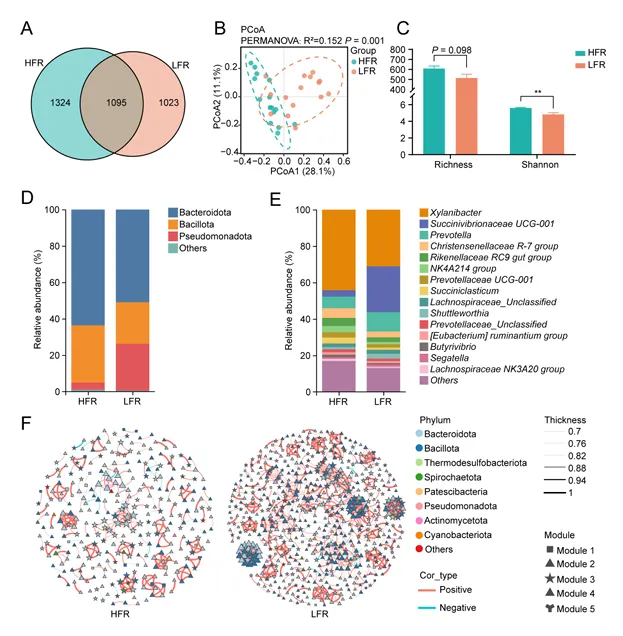
图3.HFR与LFR奶牛瘤胃微生物组差异
在属水平,LFR组富集了Succinivibronaceae UCG-001、Prevotella等,HFR组则富集了Xylanibacter、Christensenellaceae R-7 group、Butyrivibrio、Lachnospiraceae NK3A20 group等。WGCNA网络分析显示,LFR组网络复杂度远高于HFR组,且模块2与牛奶LA及ω-6/ω-3比例正相关。
宏转录组揭示Lachnospiraceae为活性PUFA代谢核心菌群
宏转录组测序显示,活性微生物中细菌占93.04%,真核生物占4.89%,古菌占1.38%。在Lachnospiraceae家族中,HFR组富集了Butyrivibrio、Eubacterium_G等属,LFR组富集了Blautia、Eubacterium_I、Copromonas等属(图4)。
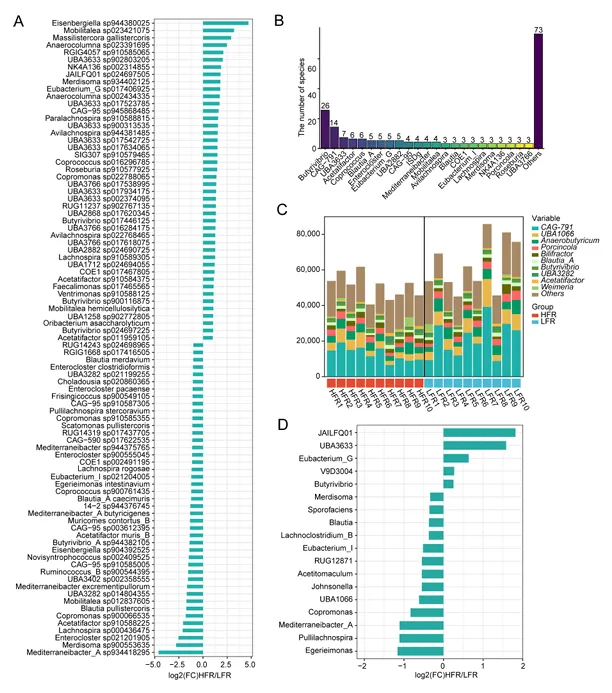
图4.转录水平活性微生物谱
差异物种分析发现198个Lachnospiraceae物种在两组间丰度差异显著,包括26个Butyrivibrio物种、14个CAG-791物种、5个Eubacterium_G物种和3个Eubacterium_I物种。相关性分析显示,瘤胃ALA浓度与Johnsonella、Blautia、Eubacterium_I正相关,而LA浓度与Butyrivibrio、Acetitomaculum正相关。
异构酶基因的微生物来源与表达差异
功能注释发现,HFR组中大多数异构酶基因的表达水平显著高于LFR组。这些异构酶基因主要来源于Lachnospiraceae、Anaerovoracaceae和Oscillospiraceae等(图5)。
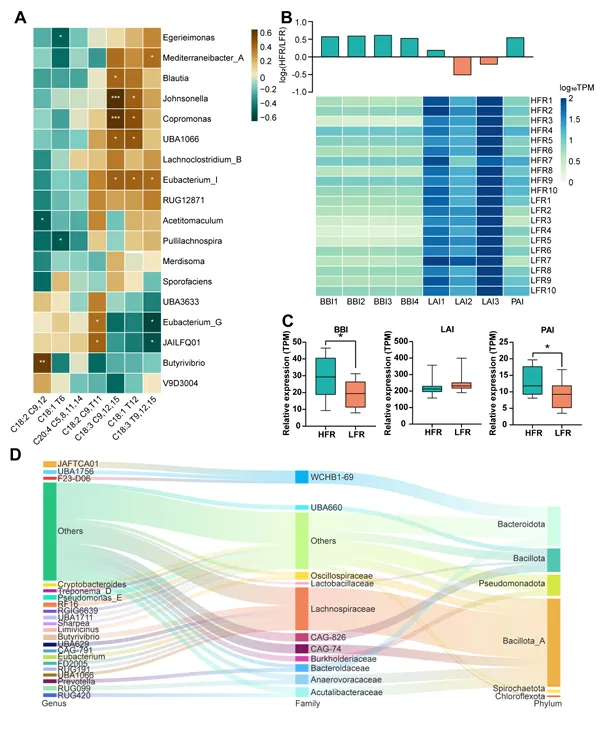
图5.异构酶通路的转录水平分布
BBI和PAI基因丰度与瘤胃中C18:1 T12、C18:1 T11负相关,与C20:5正相关。这一结果表明,HFR组中增强的异构酶表达可能促进了LA的积累和后续转化,从而导致更高的ω-6/ω-3比例。
HFR与LFR组瘤胃微生物功能与PUFA代谢通路的差异模型
整合相关性分析构建了差异代谢模型:在HFR表型中,Eubacterium_G、Limivicinus和Butyrivibrio等菌属相对活跃,伴随BBI水平升高,与瘤胃中LA和C18:1 T6积累相关,最终导致牛奶ω-6/ω-3比例升高(图6)。
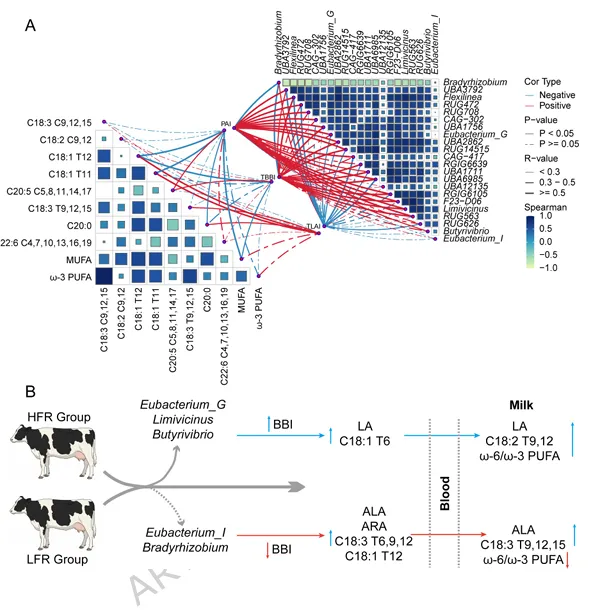
图6.HFR与LFR奶牛瘤胃微生物功能与FA代谢模式的差异
相反,LFR组以Eubacterium_I和Bradyrhizobium为主导,BBI水平降低,与ALA、ARA和C18:3 T9,12,15的代谢通量改变相关,对应更低的牛奶ω-6/ω-3比例。

本研究首次整合宏转录组学与代谢组学,系统揭示了瘤胃微生物调控牛奶ω-6/ω-3 PUFA比例的机制。毛螺菌科被鉴定为核心功能菌群,其中Butyrivibrio偏好代谢ALA,Eubacterium偏好代谢LA,这种底物特异性分工决定了不同PUFA在瘤胃中的代谢命运,进而影响牛奶脂肪酸组成。
研究还发现,瘤胃微生物解释了该表型41%的变异,远高于其他生产性状。分离菌株的功能验证为未来开发益生菌或靶向调控策略提供了直接证据。该研究为通过调节瘤胃微生态改善乳制品营养品质奠定了理论与技术基础。
📢如果你也想用“多组学”进行发文,思路复现,那就快来联系我们吧~

有需要的朋友联系~

IF30.9!南京大学&南京医科大学联手用“国自然”荣登《Cell》子刊!竟发现父亲运动可通过精子miRNA提升后代耐力!

